1. 서 론
최근 환경문제가 심각하게 대두됨에 따라 전 세계적으로 에너지 소비 절감 및 탄소배출 감축을 위해 다양한 노력을 하고 있으며 제지산업에서도 에너지 소비 절감을 위해 다양한 시도가 진행되고 있다. 이러한 시도중의 하나로 nanofibrillated cellulose(NFC), nano crystalline cellulose(NCC), cellulose whisker 및 microfibrillated cellulose(MFC) 등 셀룰로오스계 미세 결정소재가 초지 중에 첨가 되었을 때 강력한 지력 증강 효과를 입증한 바 있다.1-4) Gonzalez 등2)은 TEMPO 산화 전처리 후 고압의 균질기(homogenizer)를 처리하여 NFC를 제조하였으며 NFC를 첨가하여 초지한 종이의 물성을 측정하였다. 그 결과 NFC를 첨가한 종이의 인장강도와 파열강도가 증가하였으며 NFC 첨가량이 증가할수록 인장강도와 파열강도도 점점 증가한다고 보고하였다. Ryu5)는 그라인더(grinder)를 이용한 기계적 처리에 의해 NFC를 제조하였으며 NFC와 펄프의 비율을 다르게 조절하여 만든 NFC mat의 인장특성을 평가하였다. 인장 측정기를 통해 인장응력을 평가해본 결과, 건조한 매트에서 NFC의 비율이 높아질수록 인장파괴응력이 점차 증가하였으며 젖은 매트의 경우에 NFC의 비율이 70%일 때 인장파괴응력이 최대값을 나타낸다고 보고하였다. 현재 대부분은 MFC는 균질기(homogeneizer), 그라인더(grinder) 등 강력한 기계적 동력에 의해 제조하고 있으나 제조 동력비가 지나치게 높은 단점이 있다. 또한 수율이 낮고 대량 생산이 어려워 산업화 단계에 진입하기 위해서는 많은 노력이 필요하다.6)
효소는 생물이 생성한 생체촉매로, 무기촉매와는 달리 기질에 대한 특이성이 있고 상온상압 및 중성 pH에서도 생화학반응을 원활히 촉진할 수 있다. 효소는 반응종류에 따라 분류할 수 있는데 그 중 목재 가수분해 효소에 해당되는 것이 cellulase이다. Cellulase는 cellulose를 가수분해하는 효소의 총칭으로 한정된 범위의 pH와 적정온도에서만 작용하는 특성이 있다. Cellulase는 cellulose 사슬의 β-1,4-D-glucoside 결합을 가수분해하며 분해특성에 따라 크게 3가지로 나눌 수 있다. 먼저 endo-glucanase는 cellulose chain을 무작위로 절단하여 oligosaccharide를 생성하는 효소로 비결정영역에 주로 작용한다. 가용성의 carboxyl methyl cellulose를 기질로 사용하기 때문에 CMCase라고도 한다. 두 번째는 cellobiohydrolase 혹은 exo-glucanase라고 부르며 cellulose chain의 말단부를 공격하여 oligosaccharide를 cellobiose로 분해한다. Avicel 등의 결정성 셀룰로오스에도 작용하기 때문에 avicelase라고도 한다. 생성된 cellobiose는 β-glucosidase에 의해 단당류인 glucose로 최종 분해된다. 이처럼 cellulose를 분해하기 위해서는 한 가지 효소가 작용하는 것이 아니라 3가지의 효소가 함께 작용한다. 이러한 cellulase의 특성을 이용하여 MFC 제조 시에 효소 전처리를 적용할 수 있다.7-13) Henriksson 등12)은 endo-glucanase를 전처리과정에서 사용하여 MFC를 제조하였으며 그 결과 효소 처리를 했을 때 화학적 처리를 했을 때 보다 중합도가 적게 감소했으며 섬유의 형태는 길이가 약간 감소하였으나 세포벽의 파괴도 많이 발생하여 높은 장폭비(aspect ratio)를 가진 MFC를 제조할 수 있다고 보고하였다.
따라서 본 연구에서는 MFC 제조를 위한 전처리 방법 중 하나인 enzyme 처리를 적용하기 위해 선별된 endo-glucanase의 pH와 온도에 따른 최적 활성조건을 탐색하고 이를 펄프에 적용하여 고해 특성을 평가해보고자 하였다.
2. 재료 및 방법
2.1 공시재료
2.1.1 기질
본 실험에서 효소 활성 측정을 위한 기질로 1%의 carboxymethyl cellulose(CMC, Sigma, Germany) 용액을 사용하였다. CMC는 Endo형 cellulase에 기질로 작용하는 특성이 있다.
2.1.2 효소
본 연구에서는 상업적인 용도로 사용되고 있는 3종류의 endo형 glucanase를 사용하였으며 그 특성은 Table 1에 나타냈다. Endo-B는 섬유, 세탁 등의 용도로 사용되는 상업용 효소로 분말로 되어 있어 저장 안정성이 뛰어나지만 액체상에서는 안정화되지 않는다. Endo-L은 액상의 효소로 가격이 비싸고 pH 범위가 좁은 단점이 있다. Enod-N은 효소 활성이 가장 낮으며 pH와 온도 범위가 좁아 특정 조건에서만 최적의 활성을 나타내는 것이 단점이다.14)
2.1.3 DNS 시약 제조
효소처리에 의해 생성된 환원당을 정량하기 위하여 DNS법을 사용하였다. 이때 환원당을 염색하기 위해 사용되는 DNS 시약의 제조방법은 먼저 3,5-dinitrosalicylic acid(DNS, Lancaster, England) 10.6 g과 가성소다 19.8 g을 증류수 1385.6 mL에 녹여서 총 1,416 mL를 만든 다음 potassium sodium tartrate(Wako, Japan) 306 g을 서서히 투입한다. 그런 다음 phenol(Wako, Japan) 8.44 mL와 sodium metabisulfate(Duksan, Korea) 8.3 g를 투입한 후 충분히 교반하여 DNS 시약을 제조하였다.14)
2.2 실험방법
2.2.1 표준검량선
환원당을 측정하기 위해 먼저 표준검량선을 측정하였다. 먼저 dextrose(Difco, USA)의 순도를 향상시키기 위하여 95% ethanol에 2시간동안 침전시킨 후 여과와 건조를 하여 dextrose를 재결정시켰다.15) 증류수에 용해시킨 dextrose 용액 1 mL와 DNS 시약 2 mL를 혼합하여 100℃ 물에서 10분간 반응시켰다. 냉수로 방랭하여 반응을 종료 시킨 후 UV/VIS spectrophotometer (Optizen 3220UV, Korea)를 이용하여 575 nm 파장에서 흡광도를 측정하였다.16)
2.2.2 농도에 따른 효소 활성 측정
기질 0.5 mL에 희석한 효소액 0.5 mL을 혼합하여 40℃물에서 10분간 진탕하였다. 기질과 효소 혼합액 1 mL에 DNS 시약 2 mL를 혼합하여 100℃ 물에서 10분간 반응하여 효소를 실활성시킨 후 냉수로 방랭하였다. 반응이 종료된 시료를 UV/VIS spectrophotometer를 이용하여 575 nm 파장에서 흡광도를 측정하였다.
2.2.3 pH와 온도 변화에 따른 효소 활성 측정
기질에 0.1% 가성소다와 0.1% 초산 수용액을 사용하여 pH 5 ∼ 9로 조절하였다. pH를 조절한 기질과 효소 혼합액을 25, 30, 40, 50, 60 및 70℃의 온도에 10분간 진탕하였으며 상기와 같은 방법으로 효소활성을 측정하였다.
3. 결과 및 고찰
3.1 표준검량선
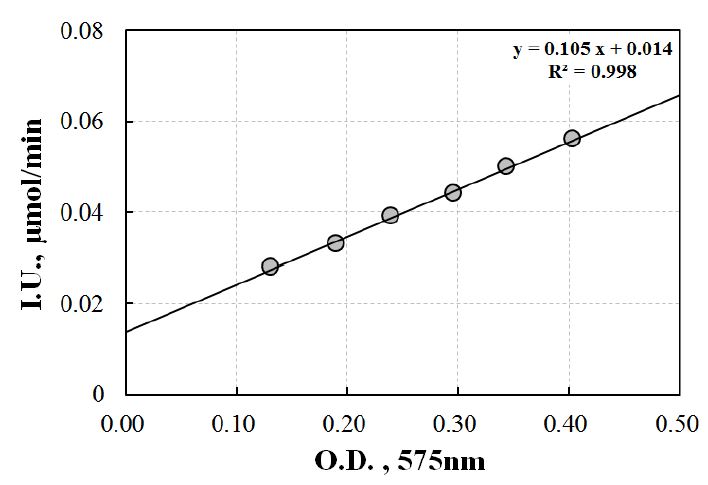
Dextrose를 농도별로 희석하여 흡광도(O.D., optical density)를 측정하고 이를 국제 효소활성단위인 I.U. (International unit)로 환산하여 Fig. 1에 나타내었다. 1 I.U.란 정해진 조건에서 1분간 기질 1 µmol의 변화를 활성화시키는 효소량으로 1 µmol/min과 같이 나타낸다.17) 본 연구의 표준검량선을 통해 나타난 dextrose의 검량선을 I.U.로 환산한 식은 y=0.105x+ 0.014이며 정확도(R2)는 0.998이다. 이 계산식으로 흡광도를 환산하면 흡광도 0.3는 약 0.046 I.U.에 해당되고 흡광도 0.5는 약 0.067 I.U.에 해당된다.
3.2 효소 활성
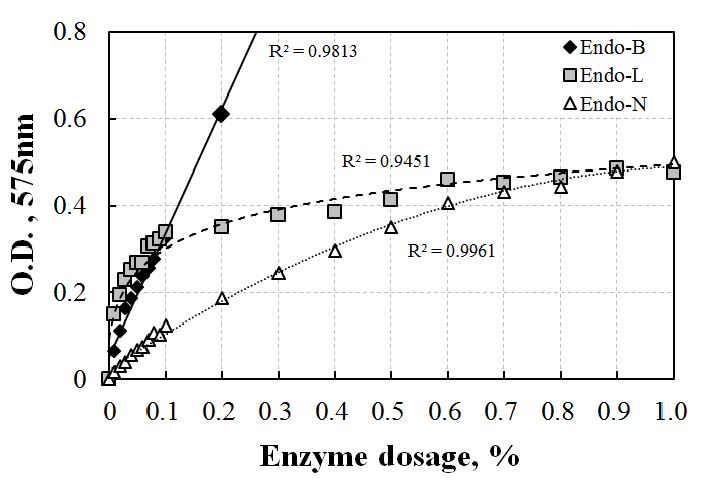
기질에 효소 처리 시 중성의 pH, 온도 40℃, 진탕시간 10분으로 고정하고 3종류 효소의 투입량에 따른 활성을 비교한 결과를 Fig. 2에 나타내었다. Endo-N은 3종류의 효소 중 가장 낮은 활성을 보였으며 0.1% 이하의 투입량에서는 Endo-B와 Endo-L의 효소활성은 거의 비슷하게 나타났다. 하지만 0.1% 이상에서 Endo-B는 활성이 가장 급격하게 증가하였으며 Endo-L은 활성의 증가폭이 감소하였다. 이는 같은 투입량의 효소를 같은 조건에서 처리했을 때 Endo-B가 가장 많은 양의 기질을 가수분해할 수 있기 때문이며 따라서 3종류의 효소 중 가장 활성이 뛰어난 것으로 판단된다. 이후의 실험은 정밀도가 높은 0.1-0.6 사이의 흡광도에서 같은 흡광도를 나타내는 각각의 효소 투입량을 사용하여17) pH와 온도에 따른 활성을 실험하였으며 이때의 효소 투입량은 Endo-B와 Endo-L이 0.1%이고 Endo-N은 0.5%로 선별하였다.
3.3 온도와 pH에 따른 효소 활성
기질의 pH가 pH 5부터 pH 9의 조건에서 진탕 온도를 25℃, 30℃, 40℃, 50℃, 60℃ 및 70℃로 변화시켜 각 효소의 활성을 측정한 결과를 Table 2에 나타냈다. pH에 상관없이 3종류의 효소가 대체로 50 ∼ 60℃에서 활성이 가장 좋게 나타났다. 특히 Endo-B의 경우 60℃에서 활성이 가장 높으며 50℃와 70℃에서도 60℃에서와 비슷한 활성을 보였다. Endo-L의 경우 50℃에서 가장 높은 활성이 나타났고 Endo-N의 경우 70℃에서 가장 높은 활성이 나타났다. 이 결과는 Kim 등18)의 연구결과와 일치하는 것으로 효소액의 온도가 최대 활성온도보다 낮을 경우 효소가 낮은 활동성을 가지게 되어 기질과 원활하게 결합할 수 없고 최대 활성온도보다 높을 경우 효소가 열에 의해 변성되어 활성이 제대로 일어나지 않기 때문인 것으로 판단된다. 그런 이유로 효소를 적용할 때는 효소가 기질과 가장 원활하게 결합 할 수 있는 최적의 온도에서 처리해야한다.
Table 2.
Enzyme activity(O.D.) with pH and temperature
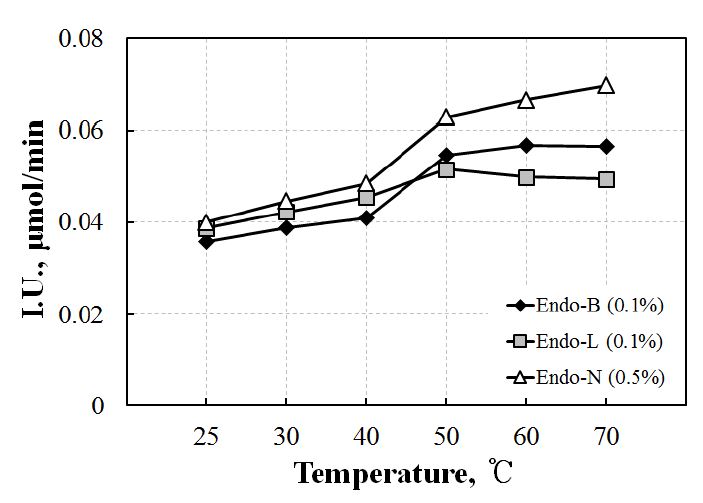
pH를 6.0으로 고정하고 온도에 따른 3가지 효소의 활성을 I.U.로 환산하여 비교한 결과를 Fig. 3에 나타냈다. 그 결과 50℃전에는 비슷한 활성이 나타났지만 그 이상의 온도에서는 Endo-N, Endo-B 및 Endo-L의 순서로 활성이 좋게 나타났다. 하지만 Endo-N의 경우 같은 흡광도를 얻기 위하여 더 높은 농도의 효소를 사용하였기 때문에 더 적은 양의 효소로 같은 흡광도를 얻을 수 있는 Endo-B가 50℃이상에서 가장 좋은 활성을 나타냈다고 판단하였다.
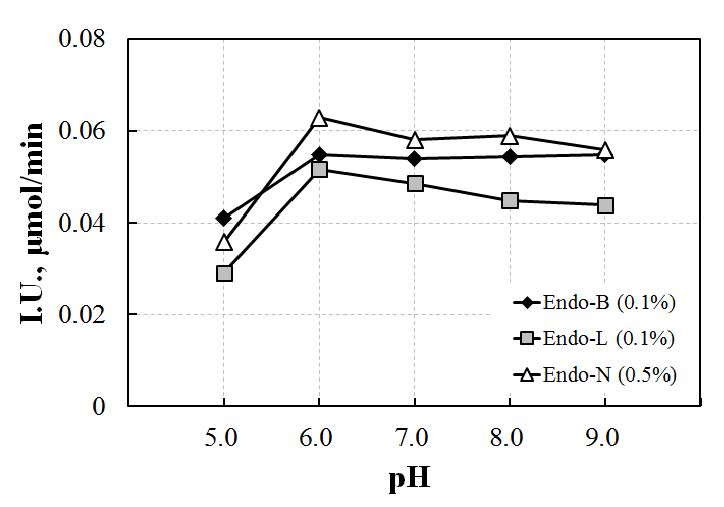
Table 2에서 알 수 있듯이, 대체로 효소의 활성은 pH 6.0에서 최대로 나타났다. 특히 Endo-L은 모든 온도에서 pH 6.0이 가장 좋은 활성을 보였으나 그 이상의 pH에서 점차 활성이 떨어졌다. 이와 마찬가지로 Endo-N도 모든 온도에서 pH 6.0에서 가장 좋은 활성을 나타났으나 그 이상의 pH에서는 활성이 소폭 감소하였다. Endo-B의 경우 pH 7.0에서 대체로 가장 높은 활성을 보였으나 pH 6.0 이상에서 활성 차이는 거의 없었다. 이는 Kim 등18)의 연구결과와 일치하는 것으로 최적 pH 이상에서는 효소 단백질이 변성되어 효소 활성이 변질되기 때문에 효소활성이 저하되기 때문인 것으로 판단된다. 온도를 50℃로 고정하고 pH에 따른 3가지 효소의 활성을 비교하여 Fig. 4에 나타냈다.
Endo-B가 Endo-N보다 적은 양의 효소로 비슷한 활성을 보였으며 pH 6.0 이상에서도 활성의 감소가 거의 없었기 때문에 중성뿐만 아니라 약알칼리 조건에서도 충분한 효소활성이 나타날 수 있을 것으로 판단하였다. Kim 등19)의 연구결과에서 보고 했듯 Endo-B는 중성 및 약알칼리성 cellulase이므로 중성과 약알칼리에 가까운 범위에서도 효소활성이 좋게 나타났다. 3종류의 효소를 50℃에서 pH 6의 최적조건에서 Endo-L, Endo-B 및 Endo-N의 흡광도를 I.U.로 환산하면 각각 0.052, 0.055 및 0.063 I.U.가 된다.
3.4 효소 전처리 펄프의 고해 특성
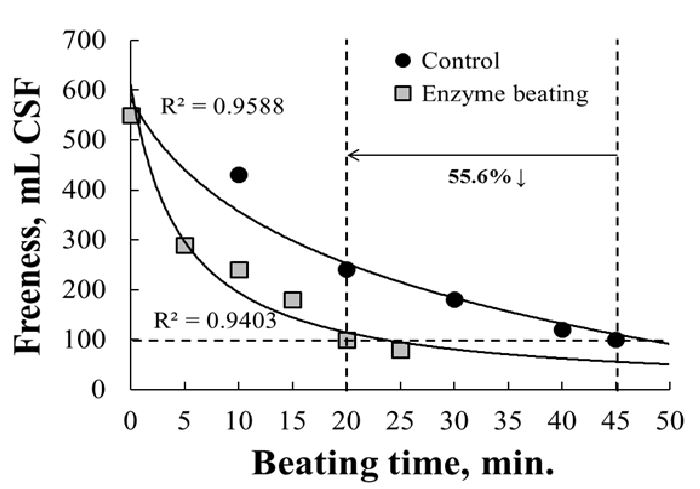
3종류의 효소 중 가장 활성이 좋고 중성과 알칼리의 pH에서도 활성 변화가 적은 Endo-B를 선택하여 펄프에 적용하여 여수도가 100 mL CSF가 될 때 까지 고해한 펄프의 여수도 및 고해 효율을 Fig. 5에 나타냈다. 무처리 펄프를 고해하여 여수도가 100 mL CSF가 될 때까지 걸리는 시간은 45분이었으며 50℃에서 1시간동안 효소와 반응시킨 펄프의 경우, 고해한지 20분 만에 여수도가 100 mL CSF에 도달하였다. 이렇게 측정된 여수도를 바탕으로 고해효율을 계산한 결과, 효소반응을 시킨 펄프가 무처리 펄프에 비해 55.6% 정도 고해 에너지를 절감시킬 수 있었다. 이는 Song 등20)의 연구결과와도 일치하는 것으로 셀룰라아제가 펄프 섬유의 외벽을 가수분해하여 표면적을 넓혀 고해도를 증가시키기 때문이다. 따라서 효소 전처리를 통해 기존의 펄프보다 고해시간을 단축시켜 50% 이상의 고해 동력을 줄일 수 있으므로 MFC 제조 시 효소 전처리가 효과적으로 적용될 수 있음을 확인하였다.
4. 결 론
MFC 제조를 위한 효소 전처리 시 endo-glucanase를 사용할 수 있으며 상업적 효소 3종류를 이용하여 효소 활성을 비교한 결과는 다음과 같다. 세 가지 효소 중 Endo-N의 활성이 가장 낮았고 0.1% 농도 미만에서는 Endo-L의 활성이 조금 높았지만 0.1% 농도 이상에서는 Endo-B의 활성이 급격히 증가하는 것으로 나타났다. 같은 흡광도를 보이는 농도의 효소액을 각각 사용하여 온도와 pH에 따른 최적의 활성 조건을 탐색해본 결과, Endo-B는 pH 7.0, 60℃에서 가장 좋은 활성을 나타냈으나 pH 6.0 이상에서 효소 활성은 거의 차이가 없었으며 50℃이상의 온도에서 활성 감소가 거의 없었다. Endo-L은 pH 6.0, 50℃에서 활성이 가장 좋았으며 Endo-N는 pH 6.0, 60℃에서 가장 좋은 활성을 보였다. 따라서 pH와 온도에 따른 최적 활성 범위가 가장 넓고 활성이 가장 좋은 Endo-B가 이후의 실험에 적용하기 알맞을 것으로 평가하였으며 이 때 최적의 조건은 pH가 중성 혹은 약알칼리이며 온도는 에너지를 절감을 위하여 활성이 크게 감소하지 않는 범위에서 가장 낮은 온도인 50℃가 선별되었다. 최적조건에서 가장 활성이 좋은 Endo-B를 펄프에 첨가하여 1시간동안 반응시킨 후 고해한 결과 여수도가 100 mL CSF가 되는데 걸리는 시간이 무처리 펄프보다 25분이 단축되었으며 이때 고해효율이 55.6%로 나타나 효소 전처리가 고해 동력을 줄이는데 효과를 보였다.