1. 서 론
반탄화(torrefaction)란 이산화탄소, 물, 유기산과 같이 발열량을 낮추는 반탄화 가스를 200~300°C의 온도 범위에서 노출시켜 산소를 제거한 공정을 말하며,1) 이러한 공정을 목재에 적용시킨 것을 반탄화 목재라고 한다. 반탄화는 목질계 바이오매스의 열적 전처리 방법 중의 하나로 탄화에서 발생하는 원료의 손실을 개선시키기 위해 연구되고 있으며, 반응 온도 및 반응 시간의 변화에 따른 반탄화 생성물의 특성이 평가되고 있다. 주로 이용되는 목재 반탄화 방법으로는 일정량의 목재를 Kiln 내 적재한 후 장시간 동안 건조 및 고온처리를 하여 회수하는 건식방법과 과열증기를 이용한 digester를 이용한 방법 등이 있으며 이를 통해 목질원료 내 탄소함량을 증가시켜 여러 특성을 부여하고 있다.
산화적 스트레스와 그로 인해 유발되는 질병 및 예방과 치료를 위한 항산화 활성의 측정은 매우 중요하다. 항산화능 측정에 가장 보편적으로 이용되는 방법은 총 폴리페놀 함량 및 DPPH 라디칼 소거 활성 측정이 있다. 폴리페놀 화합물은 flavonoids, anthoxyanins, tannins, catechins, isoflavones, lignans, resveratrols 등을 총칭하며, 식물계에 널리 분포되어 있다.2,3) 폴리페놀에 존재하는 다수의 히드록실기(-OH)는 여러 화합물과 쉽게 결합하는 특성을 가지고 있어 항산화 효과 및 항암 효과가 뛰어나다.4,5) 플라보노이드는 폴리페놀에 속하는 성분으로, 플라보노이드의 C6-C3-C6를 기본 골격으로 하며 노란색 내지는 담황색을 나타내는 페놀계 화합물의 총칭으로 자연계에 널리 분포하고 있다. 플라보노이드는 활성산소종을 효과적으로 제거하여 항산화능이 높다고 알려져 있으며 폴리페놀과 마찬가지로 항바이러스, 항염증, 항암효과가 있는 것으로 알려져 있다.6-9) 한편 DPPH는 분자 내 radical을 함유하고 있어서 토코페롤, 아스코르빈산, polyhydroxy 방향족 화합물 및 방향족 아민류에 의해 환원시 radical이 소거되어 짙은 자색이 탈색되는데, 이 정도를 항산화 물질의 전자공여능으로 측정하는 방법이 DPPH assay법이다.10) 이때 DPPH 분자의 움직임은 hydroxyl radical과 유사하여 free radical 소거 실험에 활용 된다.11) 이러한 DPPH에 의한 항산화 활성 측정법은 항산화 물질의 전자공여능으로 인하여 방향족 화합물과 아민류 등이 환원되는 것을 지표로 하여 항산화 활성을 측정하는 유용한 방법이다.12) Ahajji 등13)의 연구에 따르면 열처리 한 반탄화 목재는 페놀 함량, 페녹시 라디칼 농도 및 항산화 작용을 증가시키며, 이러한 증가는 페놀 기능의 수소 공여 능력으로 리그닌 및 목재 추출물에 대해서 반탄화 목재가 항산화 기능을 가지고 있다고 밝힌 바 있다. 또한, 반탄화 목재에는 리그닌에서 유래된 vanillin, syringaldehyde, acetosyringone 및 총 페놀성분과 특유의 냄새성분으로 sinapaldehyde, acetic acid 등의 성분을 포함하고 있으며, 이 중 vanillin, syringaldehyde, acetosyringone의 성분은 항산화 성분으로 알려져 있다.14)
따라서 본 연구에서는 반탄화 목분 추출물의 항산화 활성을 검증하기 위하여, 열처리온도를 달리하여 과열증기처리를 한 반탄화 목분 추출물의 항산화 효과 및 항산화 활성을 평가하여 그 이용성을 증대시키고자한다.
2. 재료 및 방법
2.1 공시재료
과열증기처리는 과열증기처리장치를 이용해 300°C 이상의 고온 증기로 반탄화 분말을 만드는 목재의 부가가치 향상을 위하여 연구되고 있는 열처리 방법으로,15) 본 실험에 사용된 재료는 구미소재의 S사에서 과열증기처리가공을 거친 반탄화 칩을 사용하였다. 분양받은 반탄화 칩의 수종은 굴참나무(Quercus variabilis Blume)이며, 반탄화 추출물의 항산화 특성을 조사하기 위하여 처리시간은 10분으로 처리온도는 300°C와 350°C로 실험구를 설정하여 과열증기처리한 반탄화 칩을 사용하였다.
2.2 실험방법
2.2.1 시료의 제조
각 조건별 시료는 분쇄기(WB-1, Wonder Blender, Japan)로 분쇄한 다음 분쇄한 시료 25 g에 증류수 100 mL를 가하여 24시간 동안 상온 추출하였으며, 추출물은 여과지(chm. F1001 filter paper)로 여과하여 1.5, 3, 6, 12, 25 g/mL로 희석하고 이 여과액을 냉장보관 하면서 실험에 사용하였다.
2.2.2 총 폴리페놀 함량 측정
총 폴리페놀 함량 측정은 Folin-Denis법16)을 응용하여 측정하였다. 각 시료 추출물 1 mL에 1 N Folin-Ciocalteu reagent(Sigma-Aldrich Co., St. Louis, MO, USA) 1 mL를 혼합하고, 20% sodium carbonate 1 mL를 첨가하고 실온의 암소에서 1시간 반응 시킨 후 UV-vis spectrophotometer(HS-3300, Humas, Korea)를 이용하여 725 nm에서 흡광도를 측정하였다. 총 폴리페놀 함량은 gallic acid를 이용하였으며 표준 검량 곡선(y=0.0001x+0.0067, R2=0.9739)으로부터 총 폴리페놀 함량을 계산하였다.
2.2.3 총 플라보노이드 함량 측정
총 플라보노이드 함량 측정은 Davis법17)을 변형한 방법에 따라 시료 추출물 1 mL에 diethylene glycol 10 mL를 첨가하고, 1 N NaOH 1 mL를 가한 다음 37°C 항온수조에서 1시간 동안 방치한 후 UV-vis spectrophotometer (HS-3300)를 이용하여 420 nm에서 흡광도를 측정하였다. 총 플라보노이드 함량 측정은 Quercetin을 이용하였으며 표준 검량 곡선(y=0.0022x+0.0334, R2=0.9618)으로부터 총 플라보노이드 함량을 계산하였다.
2.2.4 DPPH 라디칼 소거 활성 측정
DPPH(2,2-diphenyl-1-picrylhydrazyl) 라디칼에 대한 소거 활성은 Blois의 방법18)을 본 실험에 맞게 변형하여 측정하였다. 각 시료 추출물 1 mL에 0.15 mM DPPH(Sigma-Aldrich Co.) 4 mL를 첨가하여 혼합한 후 실온에서 30분간 반응시킨 다음 UV-vis spectrophotometer(HS-3300)를 이용하여 517 nm에서 흡광도를 측정하였다. DPPH 라디칼 소거능은 다음 식으로 나타내었다.
2.2.5 환원력 측정
환원력은 potassium ferricyanide법19)을 본 실험에 맞게 변형하여 측정하였다. 각 시료 추출물 0.5 mL에 0.2 M sodium phosphate buffer(pH 6.6) 2.5 mL와 1% potassium ferricyanide 2.5 mL를 혼합한 후 50°C 항온수조에서 20분 동안 반응시켰다. 반응 후 10% trichloroacetic acid(TCA) 2.5 mL를 첨가하고, 이 혼합액을 1,790 rpm에서 10분간 원심분리하였다. 원심분리하여 얻은 상층액 2.5 mL에 증류수 2.5 mL와 1% ferric chloride 0.5 mL를 혼합한 다음 UV-vis spectrophotometer(HS-3300)를 이용하여 700 nm에서 흡광도를 측정하였으며, 측정한 흡광도의 값으로 환원력을 나타내었다.
2.2.6 FRAP 측정
FRAP(ferric reducing antioxidant power)는 Benzie와 Strain의 방법20)을 본 실험에 맞게 변형하여 측정하였다. FRAP reagent는 300 mM acetate buffer(pH 3.6) 300 mL와 40 mM hydrochloric acid에 용해한 10 mM TPTZ(2,4,6-tris(2-pyridyl)-s-triazine)(Sigma-Aldrich Co.) 30 mL와 20 mM ferric chloride 30 mL 첨가하여 제조하였다. 각 시료 추출물 0.3 mL에 제조된 FRAP reagent 6 mL를 혼합하여 37°C 항온수조에서 5분간 반응시킨 후에 UV-vis spectrophotometer(HS-3300)를 이용하여 593 nm에서 흡광도를 측정하였다. FRAP 함량은 Trolox를 이용하였으며 표준 검량 곡선(y=0.0015x+0.073, R2=0.9956)으로부터 총 FRAP 함량을 계산하였다.
2.3 통계 처리
모든 실험은 3회 반복 실시하였으며, 실험 결과는 SPSS(ver. 24.0, SPSS Inc., USA)를 이용하여 일원배치 분산분석(One-way ANOVA)을 실시하였다. 각 측정 평균값의 유의성(P<0.05)은 Duncan’s multiple range test로 검정하였다.
3. 결과 및 고찰
3.1 총 폴리페놀 함량 변화
총 폴리페놀 함량 변화는 시료에 함유되어 있는 폴리페놀의 화합물의 양을 측정함으로써 항산화능을 예측할 수 있는 방법이다. 반탄화 추출물에 함유된 페놀성 화합물의 함량을 조사하기 위하여 Folin-Denis법을 응용하여 측정실험을 진행하였다. 300°C-10분과 350°C-10분의 반탄화 추출물을 1.5, 3, 6, 12, 25 g/mL로 희석하여 농도별 함량을 조사한 결과는 Fig. 1과 같다. 300°C와 350°C 두 조건의 총 폴리페놀 함량은 농도 의존적으로 증가하는 것으로 나타났다. 300°C-10분 조건의 25 g/mL 농도의 추출물이 879.67±40.41 mg/mL로 가장 높은 값을 나타냈으며, 350°C-10분 조건의 25 g/mL 농도의 추출물은 759.67±25.17 mg/mL를 나타내었다. 300°C 조건의 값은 350°C 조건의 값에 비해 15.79% 더 많은 함량을 나타내었다.
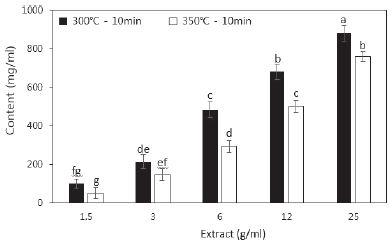
Fig. 1.
Content of total polyphenol content in torrefied wood (All values are expressed as mean±SD (n=3). Means with different letters (a-g) above the bars are significantly different by Duncan’s multiple range test (P<0.05)).
3.2 총 플라보노이드 함량 변화
반탄화 추출물에 함유된 총 플라보노이드 함량 변화를 조사하기 위하여 Davis법을 응용하여 측정실험을 진행하였다. 1.5~25 g/mL 농도에서 총 플라보노이드 함량 변화를 측정한 결과는 Fig. 2와 같다. 총 폴리페놀 함량 변화와 같은 경향으로 300°C-10분의 25 g/mL의 농도에서 111.18±3.55 mg/mL로 가장 높은 값을 나타냈으며, 350°C-10분의 25 g/mL의 농도에서는 80.58±2.58 mg/mL의 값으로 300°C 조건의 값이 350°C 조건의 값보다 37.97% 더 많은 함량을 나타냈다. 총 플라보노이드 함량 변화의 경우도 총 폴리페놀 함량 변화와 같이 농도 의존적으로 증가하였다.
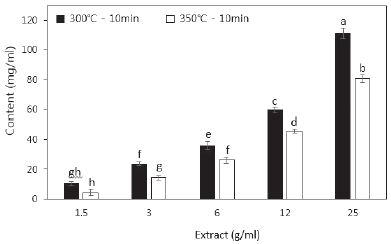
Fig. 2.
Content of total flavonoid content in torrefied wood (All values are expressed as mean±SD (n=3). Means with different letters (a-h) above the bars are significantly different by Duncan’s multiple range test (P<0.05)).
3.3 DPPH 라디칼 소거 활성 변화
DPPH 라디칼은 식물이나 식품 추출물 또는 단일 화합물의 항산화능을 측정하기 위해 사용되는 방법으로 빠르고 간단하게 이용할 수 있는 측정법이다.21) DPPH는 라디칼을 갖는 물질 중에서 비교적 안정한 화합물로 짙은 보라색으로 발색되며, 항산화 활성을 갖는 물질을 만나면 항산화 활성 물질이 DPPH의 라디칼을 소거시켜 탈색되는 점을 이용하여 측정하는 방법이다.22)
농도별 반탄화 추출물의 DPPH 라디칼 소거 활성을 나타낸 결과는 Fig. 3과 같다. 300°C-10분의 경우 1.5~25 g/mL 농도 전체에서 높은 수치의 DPPH 라디칼 소거율로 최저 83.47±1.10%, 최고 89.83±0.03%의 높은 소거율을 나타냈다. 반면에 350°C-10분의 경우 농도별 차이가 나타났는데 6, 12, 25 g/mL 농도에서는 300°C 조건의 값과 유사하게 값을 나타냈으며, 저농도인 1.5, 3 g/mL 농도에서는 낮은 수치의 DPPH 라디칼 소거율을 나타냈다. 저농도의 1.5, 3 g/mL 농도 값에서는 각각 30.29±1.57%와 76.08±1.65%를 나타냈으며, 가장 높은 값의 농도를 가지는 6 g/mL에서는 87.99±0.1%를 나타냈다. 반탄화 추출물의 DPPH 라디칼 소거활성을 검증한 결과, 300°C-10분에서는 농도별 전체적으로 유사한 값을 가졌으며 350°C-10분에서는 저농도와 고농도의 값이 차이를 나타냈다. 두 가지 조건에서 가장 우수한 소거율을 나타낸 농도는 동일하게 6 g/mL 로 300°C 조건의 경우 89.83±0.03%이며 350°C 조건의 경우 87.99±0.1%로 300°C 조건의 경우가 350°C 조건의 경우보다 2.09% 증가된 소거율을 나타냈다.
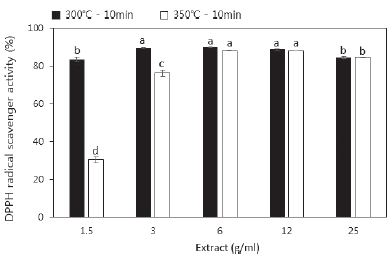
Fig. 3.
DPPH radical scavenger activity in torrefied wood (All values are expressed as mean±SD (n=3). Means with different letters (a-d) above the bars are significantly different by Duncan’s multiple range test (P<0.05)).
3.4 환원력 변화
환원력은 항산화 활성과 밀접한 관련이 있는 항산화능 측정법이며 항산화 활성은 환원력에 의한 free radical 소거능으로 나타내어진다.23) 항산화 물질의 환원제는 수소 원자를 제공하여 free radical chain reaction을 중단시킴으로써 환원력을 제공하며24) 식물 추출물에서 나타나는 환원력은 항산화 활성과 밀접한 관계를 나타낸다.25)
농도별 반탄화 추출물의 환원력을 나타낸 결과는 Fig. 4와 같다. 환원력의 결과 또한 총 폴리페놀 및 총 플라보노이드 함량 결과와 같이 농도 의존적으로 증가하는 것으로 300°C-10분 조건의 추출물이 350°C-10분 조건의 추출물보다 높은 수치를 가지는 경향을 나타냈다. 300°C-10분의 추출물의 경우 최저 0.47±0.04, 최고 3.59±0.04를 나타냈으며, 350°C-10분의 추출물의 경우 최저 0.25±0.02, 최고 2.92±0.1을 나타냈다. 300°C-10분의 가장 높은 값은 3.59±0.04로 350°C-10분의 가장 높은 값인 2.92±0.1보다 22.94% 증가된 환원력을 나타냈다.
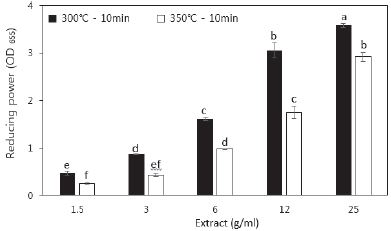
Fig. 4.
FRAP value in torrefied wood (All values are expressed as mean±SD (n=3). Means with different letters (a-h) above the bars are significantly different by Duncan’s multiple range test (P<0.05)).
3.5 FRAP 변화
FRAP는 대부분의 항산화제가 환원력을 가지고 있다는 점에 착안하여 고안된 분석방법으로 낮은 pH에서 환원제에 의해 ferric tripyridyltriazine(Fe3+-TPTZ) 복합체가 ferrous tripyridyltriazine(Fe2+-TPTZ)으로 환원되는 원리를 이용한 것이다.26)
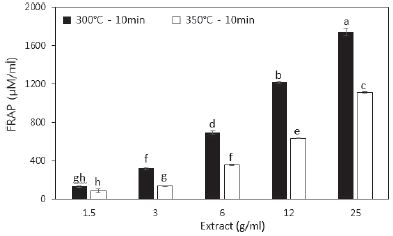
Fig. 5.
Reducing power activity in torrefied wood (All values are expressed as mean ±SD (n=3). Means with different letters (a-f) above the bars are significantly different by Duncan’s multiple range test (P<0.05)).
농도별 반탄화 추출물의 FRAP 측정 결과는 Fig. 5와 같다. FRAP 또한 농도 의존적으로 증가하는 것으로 결과를 나타냈다. 300°C-10분 추출물의 경우 최저 129±6 μM, 최고 1742±37 μM을 나타냈으며, 350°C-10분의 추출물의 경우 최저 84±18 μM, 최고 1,106±8 μM을 나타냈다. 300°C-10분의 가장 높은 값은 최고 1,742±37 μM로 350°C-10분의 가장 높은 값인 1,106±8 μM보다 57.50% 증가된 FRAP를 나타냈다.
4. 결 론
본 연구에서는 항산화 성분을 함유하고 있는 반탄화 목분을 사용하여 그 추출물의 항산화 효과를 검증하고자 하였다. 총 폴리페놀 함량, 총 플라보노이드 함량, DPPH 라디칼 소거 활성, 환원력, FRAP를 측정하여 다음과 같은 결론을 얻었다.
총 폴리페놀 함량을 측정한 결과, 300°C와 350°C 두 조건의 총 폴리페놀 함량은 농도 의존적으로 증가하는 것으로 나타났다. 300°C-10분 조건의 25 g/mL 농도에서 879.67±40.41 mg/mL로 가장 높은 값을 나타냈으며, 350°C-10분 조건의 25 g/mL 농도에서 759.67±25.17 mg/mL를 나타내었다. 300°C 조건의 값은 350°C 조건의 값에 비해 15.79% 더 많은 함량을 나타냈다. 총 플라보노이드 함량을 측정한 결과, 총 폴리페놀 함량과 같은 경향으로 300°C-10분의 25 g/mL의 농도에서 111.18±3.55 mg/mL로 가장 높은 값을 나타냈으며, 350°C-10분의 25 g/mL의 농도에서는 80.58±2.58 mg/mL의 값으로 300°C 조건의 값이 350°C 조건의 값보다 37.97% 더 많은 함량을 나타냈다. DPPH(2,2-diphenyl-1-picryl-hydrazyl) 라디칼 소거 활성을 측정한 결과, 300°C-10분에서는 농도별 전체적으로 유사한 값을 가졌으며 350°C-10분에서는 저농도와 고농도의 값이 차이를 나타냈다. 두 가지 조건에서 가장 우수한 소거율을 나타낸 농도는 동일하게 6 g/mL로 300°C 조건의 경우 89.83±0.03%이며 350°C 조건의 경우 87.99±0.1%로 300°C 조건의 경우가 350°C 조건의 경우보다 2.09% 증가된 소거율을 나타냈다. 환원력을 측정한 결과, 총 폴리페놀 및 총 플라보노이드 함량 결과와 같이 농도 의존적으로 증가하는 것으로 나타났다. 300°C-10분의 가장 높은 값은 3.59±0.04로 350°C-10분의 가장 높은 값인 2.92±0.1보다 22.94% 증가된 환원력을 나타냈다. FRAP를 측정한 결과, 또한 농도 의존적으로 증가하는 것으로 결과를 나타냈다. 300°C-10분의 가장 높은 값은 최고 1,742±37 μM로 350°C-10분의 가장 높은 값인 1,106±8 μM보다 57.50% 증가된 FRAP를 나타냈다.
결론적으로 처리온도 300°C와 350°C 조건의 과열증기처리가공을 거친 반탄화 추출물에서 두 조건 모두 농도 의존적으로 항산화 활성이 증가함을 알 수 있었으며, 300°C의 조건에서 350°C보다 높은 항산화 활성의 결과를 나타내었다. 이러한 항산화 활성이 측정된 과열증기처리가공의 반탄화는 향후 다양한 용도 및 효과적인 소재로 적용 가능할 것으로 사료된다.
Acknowledgements
이 연구는 충남대학교 학술연구비에 의해 지원되었음.
Literature Cited
T. I. Ohm, J. S. Chae, J. K. Kim, S. A. Choi and S. C. Oh, Study on the characteristics of bio-mass according to various process of torrefactionKosco Symposium; 375-378 (2014)
Ohm, T. I., Chae, J. S., Kim, J. K., Choi, S. A., and Oh, S. C., Study on the characteristics of bio-mass according to various process of torrefaction, Kosco Symposium, pp. 375-378 (2014).
I. N. E. S. Urquiaga and F. LEIGHTON, Biological Research,
Plant polyphenol antioxidants and oxidative stress,
33(2); 55-64 (2000)
Urquiaga, I. N. E. S. and LEIGHTON, F., Plant polyphenol antioxidants and oxidative stress, Biological Research 33(2):55-64 (2000).
10.4067/s0716-97602000000200004J. Dai and R. J. Mumper, Molecules,
Plant phenolics: extraction, analysis and their antioxidant and anticancer properties,
15(10); 7313-7352 (2010)
Dai, J. and Mumper, R. J., Plant phenolics: extraction, analysis and their antioxidant and anticancer properties, Molecules 15(10):7313-7352 (2010).
10.3390/molecules15107313Y. Lu and L. Y. Foo, Food Chemistry,
Antioxidant and radical scavenging activities of polyphenols from apple pomace,
68(1); 81-85 (2000)
Lu, Y. and Foo, L. Y., Antioxidant and radical scavenging activities of polyphenols from apple pomace, Food Chemistry 68(1):81-85 (2000).
10.1016/s0308-8146(99)00167-3J. Y. Cha, H. J. Kim, C. H. Chung and Y. S. Cho, Journal of Korean Society of Food Science and Nutrition,
Antioxidative activities and contents of polyphenolic compound of Cudrania tricuspidata,
28(6); 1310-1315 (1999)
Cha, J. Y., Kim, H. J., Chung, C. H., and Cho, Y. S., Antioxidative activities and contents of polyphenolic compound of Cudrania tricuspidata, Journal of Korean Society of Food Science and Nutrition 28(6):1310-1315 (1999).
R. Tsao, Nutrients,
Chemistry and biochemistry of dietary polyphenols,
2(12); 1231-1246 (2010)
Tsao, R., Chemistry and biochemistry of dietary polyphenols, Nutrients 2(12):1231-1246 (2010).
10.3390/nu2121231K. E. Heim, A. R. Tagliaferro and D. J. Bobilya, Journal of Nutritional Biochemistry,
Flavonoid antioxidants: chemistry, metabolism and structure-activity relationships,
13(10); 572-584 (2002)
Heim, K. E., Tagliaferro, A. R., and Bobilya, D. J., Flavonoid antioxidants: chemistry, metabolism and structure-activity relationships, Journal of Nutritional Biochemistry 13(10): 572-584 (2002).
10.1016/s0955-2863(02)00208-5R. J. Williams, J. P. Spencer and C. Rice-Evans, Free Radical Biology & Medicine,
Flavonoids: antioxidants or signalling molecules?,
36(7); 838-849 (2004)
Williams, R. J., Spencer, J. P., and Rice-Evans, C., Flavonoids: antioxidants or signalling molecules? Free Radical Biology & Medicine 36(7):838-849 (2004).
10.1016/j.freeradbiomed.2004.01.001E. J. Kim, J. Y. Choi, M. R. Yu, M. Y. Kim, S. H. Lee and B. H. Lee, Korean Journal of Food Science and Technology,
Total polyphenols, total flavonoid contents, and antioxidant activity of Korean natural and medicinal plants,
44(3); 337-342 (2012)
Kim, E. J., Choi, J. Y., Yu, M. R., Kim, M. Y., Lee, S. H., and Lee, B. H., Total polyphenols, total flavonoid contents, and antioxidant activity of Korean natural and medicinal plants, Korean Journal of Food Science and Technology 44(3):337-342 (2012).
10.9721/kjfst.2012.44.3.337M. H. Kang, C. S. Choi, Z. S. Kim, H. K. Chung, K. S. Min, C. G. Park and H. W Park, Korean Journal of Food Science and Technology,
Antioxidative Activities of Ethanol Extract Prepared from Leaves, Seed, Branch and Aerial Part of Crotalaria sessiflora L.,
34(6); 1098-1102 (2002)
Kang, M. H., Choi, C. S., Kim, Z. S., Chung, H. K., Min, K. S., Park, C. G., and Park, H. W, Antioxidative Activities of Ethanol Extract Prepared from Leaves, Seed, Branch and Aerial Part of Crotalaria sessiflora L., Korean Journal of Food Science and Technology 34(6):1098-1102 (2002).
S. Y. Cho, Y. B. Han and K. H. Shin, Korean Journal of Food Science and Technolog,
Screening for antioxidant activity of edible plants,
30(1); 133-137 (2000)
Cho, S. Y., Han, Y. B., and Shin, K. H., Screening for antioxidant activity of edible plants, Korean Journal of Food Science and Technolog, 30(1):133-137 (2000).
Y. J. Yang, H. J. Kim, S. H. Kang and S. C. Kang, Korean J. Plant Res,
Screening of natural herb resources for anti-oxidative effects in Korea,
24(1); 1-9 (2011)
Yang, Y. J., Kim, H. J., Kang, S. H., and Kang, S. C., Screening of natural herb resources for anti-oxidative effects in Korea, Korean J. Plant Res, 24(1):1-9 (2011).
10.7732/kjpr.2011.24.1.001A. Ahajji, P. N. Diouf, F. Aloui, I. Elbakali, D. Perrin, A. Merlin and B. George, Wood Sci. Technol,
Influence of heat treatment on antioxidant properties and colour stability of beech and spruce wood and their extractives,
43; 69-83 (2009)
Ahajji, A., Diouf, P. N., Aloui, F., Elbakali, I., Perrin, D., Merlin, A., and George, B., Influence of heat treatment on antioxidant properties and colour stability of beech and spruce wood and their extractives, Wood Sci. Technol. 43:69-83 (2009).
10.1007/s00226-008-0208-3A. M. Asamarai, P. B. Addis, R. J. Epley and T. P. Krick, J. Agric. Food Chem,
Wild rice hull antioxidants,
44; 126-130 (1996)
Asamarai, A. M., Addis, P. B., Epley, R. J., and Krick, T. P., Wild rice hull antioxidants, J. Agric. Food Chem. 44:126-130 (1996).
10.1021/jf940651cY. G. Park, C. D. Eom, J. H. Park, Y. S. Chang, K. M. Kim, C. W. Kang and H. Y. Yeo, Korean J. Wood Sci. Technol,
Evaluation of physical properties of Korean Pine (Pinus koraiensis Siebold & Zucc) lumber heat-treated by superheated steam,
40(4); 257-267 (2012)
Park, Y. G., Eom, C. D., Park, J. H., Chang, Y. S., Kim, K. M., Kang, C. W., and Yeo, H. Y., Evaluation of physical properties of Korean Pine (Pinus koraiensis Siebold & Zucc) lumber heat-treated by superheated steam, Korean J. Wood Sci. Technol. 40(4):257-267 (2012).
10.5658/wood.2012.40.4.257O. Folin and W. Denis, J. Biol. Chem,
On phosphotungastic-phosoho-mdybdic compounds as color reagents,
12; 239-249 (1912)
Folin, O. and Denis, W., On phosphotungastic-phosoho-mdybdic compounds as color reagents, J. Biol. Chem. 12:239-249 (1912).
D. C. Abeysinghe, X. Li, C. Sun, W. Zhang, C. Zhou and K. Chen, J. Agric. Food Chem,
Bioactive compounds and antioxidant capacities in different edible tissues of citrus fruit of four species,
104; 1338-1344 (2007)
Abeysinghe, D. C., Li, X., Sun, C., Zhang, W., Zhou, C., and Chen, K., Bioactive compounds and antioxidant capacities in different edible tissues of citrus fruit of four species, J. Agric. Food Chem. 104: 1338-1344 (2007).
10.1016/j.foodchem.2007.01.047W. Brand-Williams, M. E. Cuvelier and C. Berset, LWT-food Science and Technology,
Use of a free radical method to evaluate antioxidant activity,
28(1); 25-30 (1995)
Brand-Williams, W., Cuvelier, M. E., and Berset, C., Use of a free radical method to evaluate antioxidant activity, LWT-food Science and Technology 28(1):25-30 (1995).
10.1016/s0023-6438(95)80008-5M. Oyaizu, The Japanese Journal of Nutrition and Dietetics,
Studies on products of browning reactions: antioxidative activities of products of browning reaction prepared from glucosamine,
44; 307-315 (1986)
Oyaizu, M., Studies on products of browning reactions: antioxidative activities of products of browning reaction prepared from glucosamine, The Japanese Journal of Nutrition and Dietetics 44:307-315 (1986).
10.5264/eiyogakuzashi.44.307IF. Benzie and JJ. Strain, Analytical Biochemistry,
The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: the FRAP assay,
239; 70-76 (1996)
Benzie, IF. and Strain, JJ., The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: the FRAP assay, Analytical Biochemistry 239:70-76 (1996).
10.1006/abio.1996.0292J. Shi, J. Gong, J. Liu, X. Wu and Y. Zhang, LWT-Food Science and Technology,
Antioxidant capacity of extract from edible flowers of Prunus mume in China and its active components,
42; 477-482 (2009)
Shi, J., Gong, J., Liu, J., Wu, X., and Zhang, Y., Antioxidant capacity of extract from edible flowers of Prunus mume in China and its active components, LWT-Food Science and Technology 42:477-482 (2009).
10.1016/j.lwt.2008.09.008J. H. Choi and S. K. Oh, Korean J. Food Sci. Technol,
Studies on the antiaging of Korean Ginseng,
17; 506-515 (1985)
Choi, J. H. and Oh, S. K., Studies on the antiaging of Korean Ginseng, Korean J. Food Sci. Technol. 17:506-515 (1985).
P. Siddhuraju, P. S. Mohan and K. Becker, Food Chemistry,
Studies on the antioxidant activity of Indian Laburnum (Cassia fistula L.): A preliminary assessment of crude extracts from stem bark, leaves, flowers, and fruit pulp,
79; 61-67 (2002)
Siddhuraju, P., Mohan, P. S., and Becker, K., Studies on the antioxidant activity of Indian Laburnum (Cassia fistula L.): A preliminary assessment of crude extracts from stem bark, leaves, flowers, and fruit pulp, Food Chemistry 79:61-67 (2002).
10.1016/s0308-8146(02)00179-6A. Kumaran and R. J. Karunakaran, LWT-Food Science and Technology,
In vitro antioxidant activities of methanol extracts of five Phyllanthus species from India,
40; 344-352 (2007)
Kumaran, A. and Karunakaran, R. J., In vitro antioxidant activities of methanol extracts of five Phyllanthus species from India, LWT-Food Science and Technology 40:344-352 (2007).
10.1016/j.lwt.2005.09.011P. D. Duh, Journal of the American Oil Chemists’ Society,
Antioxidant activity of burdock (Arctium lappa Linne): Its scavenging effect on free radical and active oxygen,
75; 455-461 (1998)
Duh, P. D., Antioxidant activity of burdock (Arctium lappa Linne): Its scavenging effect on free radical and active oxygen, Journal of the American Oil Chemists’ Society 75:455-461 (1998).
10.1007/s11746-998-0248-8D. H. Lee and J. H. Hong, Journal of the Korean Society of Food Science and Nutrition,
Physicochemical properties and antioxidant activities of fermented mulberry by lactic acid bacteria,
45(2); 202-208 (2016)
Lee, D. H. and Hong, J. H., Physicochemical properties and antioxidant activities of fermented mulberry by lactic acid bacteria, Journal of the Korean Society of Food Science and Nutrition 45(2):202-208 (2016).
10.3746/jkfn.2016.45.2.202








