1. 서 론
리그닌은 목재 내에 다량 함유되어 있는 페놀 고분자로 셀룰로오스 다음으로 지구상에서 풍부한 천연 고분자이다.1-3) 주로 펄프 생산 과정에서 제거되어 흑액(black liquor)으로 배출되며 제지 공정의 에너지원으로 순환되는 자원이다.4,5) 최근에는 환경적으로 순환되는 리그닌을 활용해 복합 소재, 바이오 플라스틱, 접착제, 전자 소재 등의 응용 분야에 적용하고자 하는 다양한 연구가 진행되고 있다.6-8) 이와 같은 응용 소재를 제조하는 원료로써 technical lignin은 펄프화의 부산물로 대량 생산되며 크라프트, 설파이트, 소다 및 유기용매 리그닌 등을 포함한다.9)
리그닌은 펄프 제조과정에서 구조가 변형될 수 있으며 방향족 C9 formula에 여러 작용기를 가지고 있기 때문에 이들 분자는 불규칙적으로 결합해 효과적인 원료 물질로 사용되기 어렵다.10,11) 또한 응용 가능한 신소재의 원료로 이용하기 위해서 흑액으로부터 리그닌을 회수하는 다양한 공정은 최종 리그닌의 품질에 영향을 미친다. 예를 들어 대표적인 technical lignin에서 크라프트 펄프화 공정을 통해 생산되는 크라프트 리그닌의 경우, 일반적으로 산을 이용해 리그닌을 회수한다. 산의 종류는 무기산 혹은 유기산으로 다양할 수 있고 주로 황산을 사용해 pH는 2-13까지 다양하게 조절 가능하지만 주로 pH 9-10에서 형성되어 이산화탄소의 주입과 함께 사용해 수율을 극대화한다.12-14) 하지만 여전히 높은 분자량, 크라프트 공정 특유의 냄새, 펄프화 공정을 통해 발생하는 여러 작용기 및 헤미셀룰로오스의 혼합으로 인해 균질한 리그닌의 생산력을 높이기 어렵다.15-17)
반면 유기용매 리그닌을 응용하는 것이 하나의 대안이 될 수 있다.18,19) 특히, Valmet 사에서는 LignoBoost라는 공정을 통해 리그닌을 상업화하여 연료 및 신소재로 사용하기 위한 연구를 진행하고 있다.20) 따라서 기존의 펄프 및 제지 산업에 초점을 맞춰 그 부산물로 발생하는 리그닌을 정제하는 것이 아니라 성능이 우수하고 균질한 리그닌을 생산하는 것에 목적을 둔다면 상업적인 이용 가능성을 극대화할 수 있을 것으로 판단된다.
이전의 Kim 등21,22)의 연구에서 고비점 유기용매 및 산을 촉매로 하는 유기용매 펄프를 제조하고 펄프의 특성에 대해 평가한 바 있다. 하지만 알칼리로 세척되고 난 후의 리그닌 흑액에 대한 연구는 면밀히 조사된 바가 없다. 따라서 본 연구에서는 유기용매 펄프화에 의해 발생하는 흑액을 이용해 산에 의해 최적화된 리그닌 회수 방법을 알아보고자 하였다.
2. 재료 및 방법
2.1 공시재료
유기용매 펄프화법을 위해 사용된 목재 칩은 국내산 혼합 참나무류로 칩의 크기는 H(40±2) mm×W(9±3) mm×T(8±3) mm로 M사로부터 공급받아 사용하였다. 반응에 사용된 고비점 용제는 glycol ether(Daejung Chemical & Materials Co., Ltd., Korea)이며 반응 촉매는 95.0% 염산(Daejung Chemical & Materials Co., Ltd., Korea)을 사용하였다. 펄프 세척에는 98% 아세톤(DUKSAN Chemical & Materials Co., Ltd., Korea) 및 99.5% 수산화나트륨(Daejung Chemical & Materials Co., Ltd., Korea)을 사용하였다. 리그닌의 회수를 위해 95.0%의 황산(Daejung Chemical & Materials Co., Ltd., Korea) 및 35.0% 염산(Daejung Chemical & Materials Co., Ltd., Korea)을 사용하였다. 분자량에 대한 비교 분석을 위해 M사에서 제공받은 활엽수 리그닌을 사용하였다.
2.2 유기용매 펄프화법을 통한 흑액 제조
리그닌 흑액은 유기용매 펄프화법을 통해 다음과 같은 방법에 의해 제조되었다. 약 10 g의 목재 칩의 2배에 해당하는 혼합 시약(glycol ether:염산=97:3, v/v)을 둥근 플라스크에 투입한 후 목재 칩과 혼합 시약을 가볍게 흔들어 교반하였다. 가열 맨틀(MS-DM 603, Misung Scientific Co., Ltd., Korea) 및 교반기(PL-FS701, POONG LIM Tech Co., Ltd., Korea)를 이용해 150 rpm으로 120℃에서 30-90분간 반응하였다. 반응이 종료된 후 흑액은 감압 여과를 통해 증류수, 0.5N NaOH 수용액 및 아세톤으로 순차 세정하여 펄프와 분리되었다.
2.3 유기용매 흑액으로부터 리그닌 회수
리그닌을 회수하기 위한 산 촉매로 95% 황산 및 35% 염산을 사용하였다. 총 4가지 방법을 통해 pH를 조절하고 리그닌을 분급하였으며 각 단계를 Table 1에 나타냈다. M1은 리그닌 흑액의 pH를 M1(13→9), M1(9→5), M1(5→2)의 총 3가지 단계로 조절하였고 M2 및 M3은 M2(13→9), M2(9→2) 및 M3(13→5), M3(5→2)로 2가지 단계를 통해 pH를 조절하였다. 마지막으로 M4는 M4(13→2)로 한 가지 단계로 조절되었다. 여기서 M1(13→9) 및 M2(13→9)는 동일한 조건이며 모든 결과 값의 편차는 pH 0.1 내외의 평균값을 나타내었다. 상온에서 500 mL의 흑액을 교반하며 산을 투입하고 목표한 pH에 도달하면 30분간 교반한 후 원심분리기(LABO-GENE 1580, Korea)를 이용해 20,000 rpm으로 상등액과 침전된 리그닌을 분리하였다. 응집된 리그닌은 동결 건조하여 무게를 칭량하였다. 상등액은 다시 산을 이용해 목표한 pH로 맞추고 분리와 세척을 반복하였다.
Table 1.
Lignin recovery yield fractionated from the black liquor
2.4 측정
흑액의 전체 전건 중량(total dry solid, TDS)은 TAPPI T650 om-09에 의거하여 105℃에서 24시간 건조한 후 측정되었으며 2.19 wt%이었다. 리그닌 분급 방법에 따른 회수율을 알아보기 위해 Zhu 등23)이 제안한 lignin 수율 계산법을 응용하여 계산하였다. 동결 건조를 통해 회수된 리그닌의 중량 및 원료 흑액의 전전 중량을 이용해 다음과 같이 계산하였다(Eq. 1). 리그닌의 Klason lignin은 TAPPI T 222 om-02를 통해 측정되었다. 약 0.2 g의 리그닌 분말에 72% 황산 수용액 5 mL를 투입해 4시간 동안 유리봉으로 교반한 후 196 mL 증류수를 이용해 250 mL 삼각 플라스크에 옮겼다. Autoclave에 120℃로 120분간 반응한 후 여과해 105℃ 건조기에 12시간 이상 건조하여 산 불용성 리그닌 함량을 측정하였다. 산 촉매 및 회수 방법에 따른 분자량을 측정하기 위해 리그닌을 아세틸화하였다. 100 mg의 건조된 리그닌은 5 mL의 피리딘에 용해한 후 5 mL의 무수초산을 추가로 주입하여 12시간 반응하였다. 반응 후 0-10℃의 증류수 500 mL에 반응물을 적하하며 아세틸화된 리그닌을 침전시키고 원심분리기를 이용해 20,000 rpm으로 리그닌을 분리했다. 탈 이온수로 반복 세척된 반응물은 동결 건조를 통해 회수하였다. 아세틸화된 리그닌은 0.1 g/L로 THF에 용해되어 gel permeation chromatography (Alliance e2695, Waters, USA)에서 Waters Styragel (HR3, HR4, HR5E) column 및 RI-detector을 통해 35℃에서 1 mL/min의 유속으로 측정되었다. 검량선은 1,000-4,000,000 g/mol 범위의 polystyrene으로 작성하여 보정하였다.
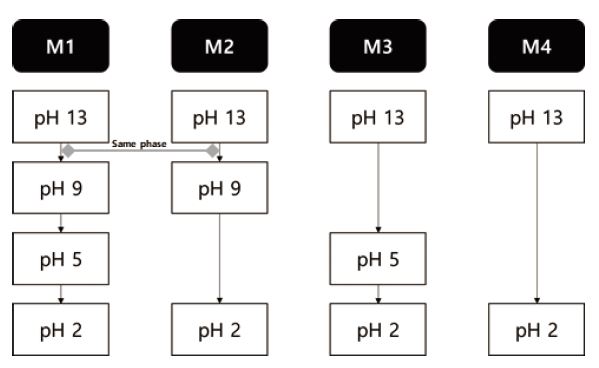
Fig. 1.
Schematic fractionations of organosolv black liquors (M1: 3 step fractinations through M1(13→9), M1(9→5), M1(5→2), M2: 2 step fractionations through M2(13→9), M2(9→2), M3: 2 steps fractionation through M3(13→5), M3(5→2), M4: 1 step fractionation through M4 (13 →2)). The fractionation of M1(13→9) and M2(13→9) are indicated the same phase.
3. 결과 및 고찰
3.1 리그닌 분급 방법에 따른 회수율
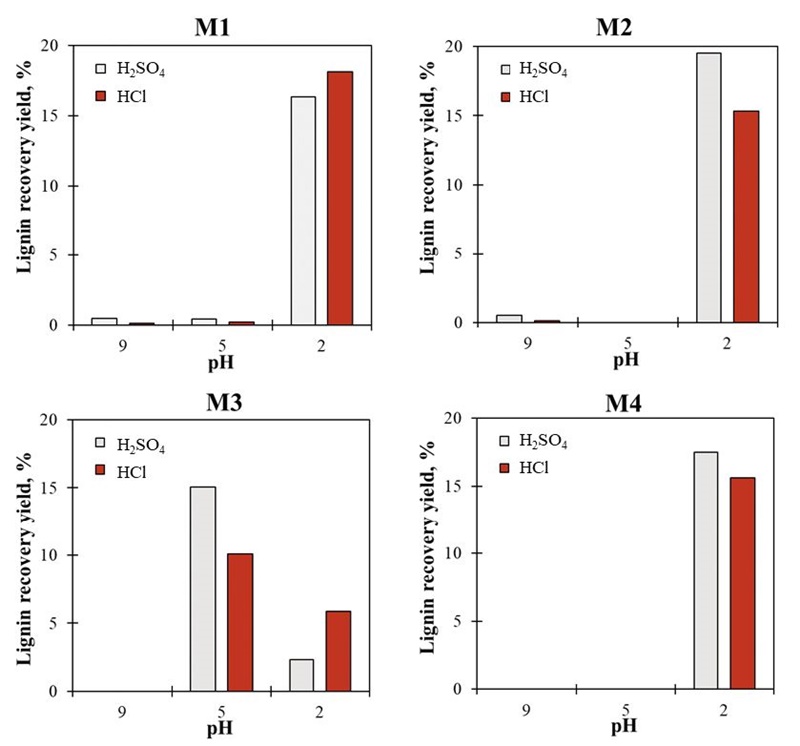
Fig. 2는 리그닌의 분급 방법에 따른 회수율을 나타낸 결과로 M1은 총 3단계로 pH를 낮추었을 때의 회수율이다. 95% 황산을 사용해 리그닌을 분급한 경우 M1 pH 13-9의 회수율은 0.5%, M1 pH 9-5 또한 0.5%로 낮은 수준이었다. 하지만 M1 pH 5-2에서 회수된 리그닌은 16.3%로 산성 조건으로 변함에 따라 급격히 증가하였다. 리그닌 흑액에 산이 첨가되면 pH가 감소하게 되는데 리그닌 분자의 페놀성 그룹이 양성자화되어 리그닌 분자 사이의 반발력이 감소함에 따라 흑액으로부터 단리가 이루어진다고 보고된 바 있다.23,24)
M2 및 M3은 총 2단계의 pH 조절을 통해 최종적으로 pH 2까지 리그닌을 단리하는 방법이다. M2 pH 13-9의 리그닌 회수율은 0.5%로 M1 pH 13-9과 같은 조건이며 M2 pH 9-2는 19.5%로 M1 방법과 마찬가지로 pH가 감소함에 따라 회수율이 증가하는 경향성을 나타냈다. 반면 M3의 경우 M3 pH 13-5에서 15.1%의 회수율을 보였으며 M3 pH 5-2에서 2.3%로 pH가 5가 될 때 대부분 리그닌이 회수되었다. 이는 황산에 의해 pH 13-9의 단계를 거치지 않고 바로 pH 5에 도달한 것으로 서서히 pH를 조절한 M1과 달리 산의 첨가 속도가 순간적으로 증가하면서 산에 인접한 리그닌 분자가 다량 양성자화되어 회수율이 증가한 것으로 보인다. 마지막으로 pH 2까지 단계 조절 없이 황산을 투입한 M4 pH 13-2는 17.5%의 리그닌 회수율을 나타냈다.
염산을 사용해 리그닌을 회수하더라도 단리 방법에 따른 경향성은 유사하게 나타났으며 특징적인 차이는 전체 리그닌 회수율에서 M1을 제외한 M2, M3 그리고 M4의 방법에서 염산을 이용한 리그닌 회수율이 낮게 측정된 것이었다(Table 2). Ibrahim 등25)이 황산, 염산, 인산 및 질산을 이용해 soda 흑액으로부터 pH 2까지 수소 이온 농도를 조절해 리그닌을 단리한 결과 인산, 황산, 염산 및 질산 순으로 리그닌 회수율이 가장 높은 것을 확인하였다. 이와 같은 차이는 산의 양이온 수에 의한 것으로 상대적으로 양 이온수가 더 많은 황산이 리그닌의 정전기적 인력에 더 많은 영향을 끼쳤기 때문인 것으로 판단하였다.
Table 2.
Klason lignin content of fractionated lignin precipitated by different types of acids
| Fractionation phase | H2SO4 | HCl | |
|---|---|---|---|
| M1 | pH 13-9 | 16.2 | 18.4 |
| pH 9-5 | 22.0 | 47.1 | |
| pH 5-2 | 58.7 | 54.7 | |
| M2 | pH 13-9 | 16.2 | 18.4 |
| pH 9-2 | 59.2 | 59.1 | |
| M3 | pH 13-5 | 34.2 | 63.5 |
| pH 5-2 | 57.0 | 66.0 | |
| M4 | pH 13-2 | 58.6 | 67.8 |
따라서 네 가지의 분급 방법 및 양이온 수가 서로 다른 산을 이용해 리그닌의 응집에 영향을 끼치는 것은 양이온 수에 따른 리그닌 분자 간의 힘에 따라 결정됨을 검토하였다.
3.2 리그닌 분급 방법에 따른 잔존 리그닌 함량
Table 2는 네 가지 방법 및 산을 이용해 분급된 리그닌의 클라손 리그닌을 측정한 결과로 전체적인 클라손 리그닌 함량의 수치가 낮은 이유는 제조된 리그닌에 염이 존재하기 때문이다. 이때 발생하는 염은 pH가 감소함에 따라 정량적으로 발생하기 때문에 보정이 필요하다. 하지만 염의 존재 여부와 별개로 단리되는 pH가 감소할수록 산 불용성 리그닌의 함량이 증가한 것을 확인하였다. 이와 같은 결과는 pH가 감소함에 따라 양성자화되는 리그닌 분자의 페놀성 그룹 수가 증가했기 때문으로 Fig. 2의 결과에서도 확인할 수 있다. 그리고 펄프화 과정에서 일부 당 성분이 용출되기 때문에 흑액에 존재하는 헤미셀룰로오스가 리그닌과 함께 응집되었을 수 있다고 추측하였다. Zhu 등26)은 크라프트 리그닌 흑액의 pH가 감소함에 따라 회수된 리그닌의 헤미셀룰로오스 함량이 감소하는 것을 정량적으로 확인하였다. 따라서 유기용매 리그닌 흑액에서도 pH가 감소함에 따라 리그닌에 존재하는 헤미셀룰로오스 함량이 감소해 상대적으로 리그닌 함량이 증가하는 결과로 이어졌다고 판단하였다.
염산을 통해 분급된 리그닌의 잔존 리그닌 함량은 황산으로 분급된 리그닌보다 비슷하거나 높게 나타났다. 리그닌 흑액을 단리하는 산의 종류에 따라 리그닌의 순도에 영향을 끼칠 수 있는데 염산으로 단리된 리그닌의 경우 황산에 비해 약 17% 높은 잔존 리그닌을 가지며 약 3분의 1 수준의 당량을 가진다고 보고된 바 있다.24) 이처럼 잔존 리그닌의 함량이 높은 이유가 헤미셀룰로오스의 회수에 의한 결과라면 염산을 흑액의 회수 용도로 사용한다면 순도 높은 리그닌을 얻을 수 있는 방법이 될 수 있다고 판단하였다.
3.3 pH 조절에 따른 리그닌의 분자량
Table 3은 3단계로 pH를 낮춘 M1 방법 중 M1 pH 13-9 및 M1 pH 5-2의 분자량을 측정한 결과이다. pH 9에서 단리된 크라프트 리그닌의 중량 평균 분자량(Mw)은 4,169, 수 평균 분자량(Mn)은 2,439 그리고 PDI는 1.71인 반면 유기용매 리그닌은 모든 조건에서 Mw, Mn 및 PDI가 낮게 측정되었다. 크라프트 리그닌은 펄프화 조건이 유기용매 펄프화 조건보다 상대적으로 가혹하기 때문에 biphenyl 및 축합형 구조가 형성되어 최소 200에서 200,000의 다소 높은 분자량을 가질 수 있다고 보고된 바 있으며 그 범위도 다양하다고 보고된 바 있다.27,28) PDI 수치 또한 유기용매 리그닌보다 일반적으로 크게 나타나는 것을 확인되었다. 따라서 유기용매 리그닌은 모든 조건에서 크라프트 리그닌보다 상대적으로 저분자이면서도 분자량 분포도가 좁은 리그닌으로 제조된 것을 확인하였다.
Table 3.
Weight-average molecular weight (Mw) precipitated M1 lignin by acids
| Fractionation phase | Molecular weight (Mw) | Molecular number (Mn) | Polydispersity index** (PDI) | |
|---|---|---|---|---|
| Kraft lignin* | 4,169 | 2,439 | 1.71 | |
| H2SO4 | M1 pH 13-9 | 2,146 | 1,739 | 1.23 |
| M1 pH 5-2 | 2,234 | 1,798 | 1.24 | |
| HCl | M1 pH 13-9 | 2,062 | 1,681 | 1.23 |
| M1 pH 5-2 | 2,137 | 1,756 | 1.21 | |
유기용매 리그닌의 경우 전체적으로 유사한 수준이지만 단리 조건이 pH 13-9보다 pH 5-2에서 높은 Mw 및 Mn을 나타냈다. 이와 같은 결과는 Table 2의 잔존 리그닌 함량의 결과와 유사한 것으로 단리된 리그닌이 함유하고 있는 당에 의한 영향일 것으로 판단했고 Wang 등7)의 연구에서도 탄수화물 복합체(LCC)에 존재하는 탄수화물 및 무기물 함량에 의해 잔존 리그닌 함량이 변할 수 있으며 분자량 역시 변할 수 있다고 보고하였다. Andeme 등29)에 따르면 크라프트 리그닌 흑액의 pH를 달리하여 회수하였을 때 pH가 감소함에 따라 리그닌 거대 고분자가 형성된다고 보고한 바 있다. 따라서 유기용매 리그닌 역시 pH에 따라 단리되는 리그닌의 구성 성분 및 응집 현상에 차이가 나타날 수 있다고 판단하였다.
마지막으로 산 종류에 따른 리그닌 단리 결과, 황산으로 단리된 리그닌 및 염산으로 단리된 리그닌 분자량은 유사한 수준으로 나타났다. 양성자 수가 더 많은 황산을 이용했을 때 리그닌의 응집 현상을 가중시키는 Fig. 1의 단리 리그닌 수율 결과와 달리 분자량에서는 큰 차이를 나타내지 않는 것을 확인하였다.
4. 결 론
본 연구에서는 유기용매 펄프화법으로 제조된 리그닌 흑액을 총 4가지 방법으로 단리해 회수율, 잔존 리그닌 함량 및 분자량을 평가하였다. 흑액으로부터 리그닌 회수율을 측정한 결과 황산 및 염산 모두 M1, M2 및 M4 방법에서 pH 5-2일 때 대부분의 리그닌이 회수되었다. M3 방법에서는 대부분의 리그닌이 pH 13-5일 때 회수되었다. 이를 통해 유기용매 흑액의 리그닌 회수가 가능한 pH는 최소 pH 5에서 최대 pH 2로 확인되었다. 분급된 리그닌의 클라손 리그닌 함량을 측정한 결과 pH가 감소함에 따라 리그닌에 존재하는 당량 감소로 인해 클라손 리그닌 함량이 증가하는 것을 확인하였다. 마지막으로 리그닌의 분자량 측정 결과 동일한 조건으로 단리된 크라프트 리그닌에 비해 유기용매 리그닌의 분자량이 낮은 균일한 리그닌으로 제조됨을 확인하였다.