1. 서 론
기술 개발과 산업화 및 인구 증가로 인해 세계의 에너지 수요는 지속적으로 증가하고 있다. 오늘날 화석 연료는 많은 산업분야에서 가장 광범위하게 사용되는 에너지 자원이지만 대기 오염과 다른 천연자원의 파괴를 야기한다. 따라서 화석 연료를 대체하기 위한 대체 에너지 개발이 절실히 요구되고 있다. 목질 바이오매스는 화석연료를 대체할 수 있는 재생 가능한 자원 중 하나이다. 목질 바이오매스 내 포함된 다른 다당류와 페놀계 고분자를 이용함으로써 지속가능한 에너지를 생성할 수 있다. 이러한 바이오연료를 생산하기 위해 바이오매스 처리에 대한 많은 연구가 진행되고 있다.1-5)
바이오매스의 대표적인 변환공정은 열화학적 변환으로, 바이오매스 또는 바이오 리파이너리(bio-refinery) 잔류물을 바이오 오일이나 합성 가스와 같은 중간생성물로 전환하는 방법이다. 열화학적 변환에는 열분해(pyrolysis), 가스화(gasification) 및 액화(liquefaction)로 나눌 수 있다. 먼저 열분해 공정은 공기나 산소가 없는 상태에서 바이오매스가 열분해 되어 고체형태의 숯, 응축되지 않은 가스 및 산소 함유 화합물이 풍부한 액체를 생성하는 방법이다. 열분해 시 해중합, 탈수, 탈카르복실화, 에스테르화 및 C-C 결합 파괴와 같은 다양한 반응이 발생하여 바이오매스에서 반응성 증기 화학종을 형성한다.6,7) 가스화 공정은 유기물이 산소가 없는 조건에서 열분해가 발생하며 이때 비응축성 연료나 합성가스가 생성되는 방법이다. 일반적으로 가스화는 열분해뿐만 아니라 흡열 열분해 반응을 위해 열을 제공하기 위한 연소를 포함한다.8) 액화 공정은 복잡한 물리적 구조와 화학적 변화를 통해 바이오매스가 액상으로 전화되는 방법이다. 이때 바이오매스는 열, 압력, 촉매 및 용매와 같은 요소로 인해 작은 분자로 분해되며 이 작은 분자는 불안정하고 반응성이 있기 때문에 넓은 범위의 분자량 분포를 갖는 오일과 같은 물질로 중합될 수 있다. 액화 시 용매화, 해중합, 탈카르복실화, 수소화 분해 및 수소화와 같은 여러 종류의 공정이 액화 공정 중에 발생한다.9) 액화는 직접 또는 간접적으로 이루어질 수 있다. 직접 액화는 액상 타르와 오일 또는 응축성 유기 증기를 생성하기 위한 열분해, 가용매 분해 액화(solvolysis liquefaction), 고압 열수/가용매 액화(high pressure hydrothermal/solvolytic liquefaction) 등을 수반한다. 간접 액화는 열분해 또는 가스화의 비응축 가스 생성물을 액체 생성물로 전화시키는 촉매의 사용을 포함한다.8)
과거의 대부분의 바이오매스의 액화는 오일배스, 염욕, 샌드배스 및 대류 열원으로 이루어졌다. 최근 몇몇 연구에 따르면 목재 액화의 가열방법으로 마이크로파 오븐을 적용하였다. 기존의 열분해 방식에 비해 마이크로파의 장점은 마이크로파가 시료에 침투하여 동시에 전체 시료가 가열되므로 반응시간을 몇 시간에서 몇 분으로 줄일 수 있다는 점이다.10-12) 하지만 마이크로파를 사용할 경우 일정한 시간 간격으로 시료를 교반시켜야 하며, 시료를 충분히 교반시키는 과정에서 실험자의 오차에 따라 실험 결과에 영향을 미칠 가능성이 존재한다.
이전의 연구에서는 소나무 목분을 이용하여 글리콜 에테르 용매와 산 촉매 하에서 마이크로파와 샌드배스와 교반을 통해 미세화 하는 연구를 진행한 바 있다. 반응시간과 촉매의 농도에 따라 미세화된 시료는 잔사율이 30-60%로 조절되었으며 잔존 리그닌 함량도 5-20%로 다양하게 얻어졌다. 미세화된 시료는 100-1,000 µm의 크기를 갖게 되며 이를 LMCFs(lignin rich micro-cellulosic fines)로 명명한 바 있다.13,14) 제조된 LMCFs는 나노셀룰로오스 제조 원료나 용해용 펄프 원료로 사용 가능할 것으로 기대하고 있다. 그러나 마이크로파 조사를 통한 미세화 시료 제조에서 균일한 시료를 얻기 힘들다는 점이 이전의 연구를 통해 관찰되어 균일한 LMCFs를 제조할 수 있는 방법을 모색할 필요가 있다.
본 연구에서는 마이크로파 오븐, 오일배스 및 고압증기 처리의 3가지 방법으로 화학적 미분화 처리를 실시하고 이를 통해 얻어진 LMCFs(lignin rich micro-cellulosic fines)의 특성을 비교하였다.
2. 재료 및 방법
2.1 공시재료
2.2 실험방법
2.2.1 LMCFs(lignin rich micro-cellulosic fines)의 제조
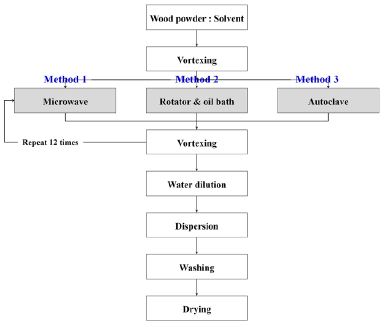
20-60 메쉬의 소나무 목분으로부터 LMCFs를 제조하는 방법은 Fig. 1과 같이 3가지로 나누어 수행하였다. 우선 5 g의 소나무 목분 시료에 글리콜 에테르와 황산 혼합시약을 1:2(w/v)로 투입하였다. 사용된 혼합시약은 글리콜 에테르 용매에 대하여 3.0%(v/v)로 황산 촉매를 혼합하여 제조하였다. 혼합시약과 반응된 시료는 3가지의 방법으로 RLCFs를 제조하였다. 첫 번째 방법(Method 1)은 700 W로 조절된 마이크로파 오븐(SE-MW 50018, Sun Enterprise, Korea)으로 반응시켰다. 마이크로파 반응 시 10초 간격으로 시료를 꺼내어 Vortex mixer (G-560, Scientific Industries Inc., USA)를 사용하여 shaking level 5에서 최대 2분간 충분히 vortexing 시켰다. 이 과정을 12회 반복하여 마이크로파 반응 시간이 총 120초가 되도록 하였다. 두 번째 방법(Method 2)은 120℃로 조절된 오일배스에 회전반응기를 부착시켜 100 rpm에서 120분 동안 반응시키고 약 1분가량 vortexing 시켜 반응을 종료하였다. 마지막 방법(Method 3)은 고압증기처리 장치(autoclave)에 시료를 투입하고 120℃에서 0.15 MPa로 90분간 반응을 시킨 후 1분간의 vortexing 하여 반응을 완료하였다. 3가지 방법으로 반응이 완료된 시료는 20배수의 증류수를 투입하여 희석한 다음 2,700 rpm의 균질기(WiseTis homogenizer, HG-15A, DAIHAN Scientific Co. Ltd., Korea)에서 5분간 처리를 하였다. 미분화된 각각의 시료들은 0.5 N NaOH와 아세톤으로 순차 세정을 실시하고 8시간 이상 105±2℃의 건조기에서 건조하여 LMCFs를 제조하였다.
2.2.2 수율 및 잔존 리그닌 함량
제조 방법에 따라 얻어진 LMCFs는 반응 전·후의 중량 측정을 통해 수율을 얻었다. 잔존 리그닌 함량은 TAPPI T 222의 방법에 따라 Klason 리그닌법을 적용하여 측정하였다.
2.2.3 현미경 관찰 및 파티클 사이즈
각 제조 방법에 따라 얻어진 LMCFs는 광학현미경(BX 50, Olympus Optical Co. Ltd., Japan)을 사용하여 60배율로 관찰하였다. 관찰된 이미지의 파티클 사이즈를 측정하기 위해 이미지분석기(i-Solution, IMT I-Solution Inc., Canada)로 200개 이상의 LMCFs 입자 크기를 측정하였다.
2.2.4 중성당 분석
반복적인 화학적 미분화에 의해 얻어진 RLCFs는 alditol-acetate법15)에 의거하여 전처리하고 2 mL의 아세톤에 용해시켜 가스 크로마토그래피(GC, HP-6890, Agilent, USA)로 중성당 분석을 실시하였다. 중성당 분석을 위한 GC 분석 조건을 Table 1에 나타내었다.
2.2.5 IR 분석
제조된 LMCFs는 ATR-IR spectroscopy(Alpha-P model, Bruker Optics, Germany)로 분석을 실시하였다. IR의 측정 영역은 4,000-400 cm-1이고 2 cm-1 단위로 측정되었다. 한 시료당 24회의 스캔을 통해 측정된 값을 하나의 스펙트럼으로 나타내었다. 측정된 IR 스펙트럼 데이터로부터 피크 세기(intensity)를 이용하여 Široky 등13)이 적용한 TCI(total crystallinity index) 및 HBI(hydrogen-bond intensity)를 계산하였다. 메틸렌기의 흡수에 대응하는 2,893 cm-1 대의 흡수밴드와 1,367 cm-1대의 셀룰로오스 내 C-H 굽힘 진동에 해당하는 흡수밴드의 비로 TCI를 계산하였으며 셀룰로오스의 분자간 수소결합(3,330 cm-1)을 나타내는 수산기(-OH)의 흡수밴드 및 수산기의 평면 변형(plane deformation)을 나타내는 1,334 cm-1대의 흡수밴드의 비로 HBI를 계산하였다.
2.2.6 주성분 분석(PCA, principal component analysis)
제조 방법별로 제조된 LMCFs의 분류 패턴을 분석하기 위해 다변량 분석 중 주성분 분석을 실시하였다. ATR spectrometer로 각 시료당 10회씩의 측정을 진행하여 스펙트럼 데이터를 수집하였다. 수집된 스펙트럼 데이터는 Savitzky-Golay 알고리즘14)에 의거하여 2차 미분 데이터로 변환하였다. 변환된 2차 미분 데이터들은 Unscrambler® Ver. 9.8(CAMO Software Inc., Norway)을 이용하여 IR 스펙트럼 전 영역대를 대상으로 분석하였다. 분석된 PCA score plot으로부터 주성분을 역추적하여 각 제조방법에 따른 LMCFs의 분류 패턴을 최종적으로 확인하였다.
3. 결과 및 고찰
3.1 LMCFs의 수율 및 잔존 리그닌 함량
LMCFs의 용도 개발을 위해 이전의 연구에서 10-15%의 잔존 리그닌 함량을 보이는 조건이 본 연구의 기준이 되었다. 이전의 연구에서는 이러한 기준을 충족하는 마이크로파 처리 조건(Method 1)은 황산 촉매의 농도 2.0%에 120초간 마이크로파에 조사되는 것이다.15) 따라서, 예비실험을 통해 Method 2와 Method 3의 조건을 설정하여 본 연구에 적용하였다.
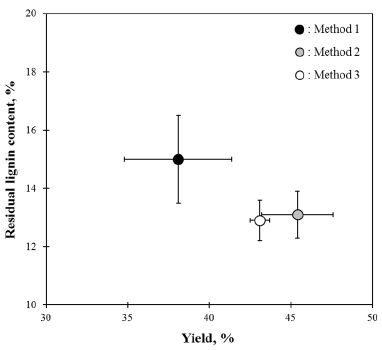
Fig. 2에서는 각각의 제조방법에 제조한 LMCFs의 수율과 잔존 리그닌 함량을 비교하였다. LMCFs는 제조방법에 따라 Method 1은 38.1%, Method 2가 45.4%, 그리고 Method 3은 43.1%의 수율을 보였으며 이때의 잔존 리그닌 함량은 각각 15.0, 13.1 및 12.9%로 나타났다. Method 1은 3 가지의 방법 중 가장 높은 리그닌 함량과 가장 낮은 수율을 보였다. 리그닌의 활용 측면이나 처리 시간적인 측면에서는 가장 효율적인 방법일 수 있으나 탄화의 문제로 인해 연속적인 마이크로파 조사를 진행할 수 없으며 반복 실험에 따라 결과의 편차가 상대적으로 크다는 문제를 보였다. Huang 등16)과 Li 등17)의 연구결과에서도 마이크로파 처리를 통해 바이오매스를 액화하였을 때 잔사의 수율이 3-10%의 편차를 보였기 때문에 본 연구의 결과와 유사하다고 할 수 있다. 한편, Method 2와 Method 3은 LMCFs의 수율과 잔존 리그닌 함량이 거의 유사하였다. Method 1의 LMCFs와 비교하면 Method 2와 Method 3의 LMCFs는 약 2%의 잔존 리그닌 함량 차이를 보이지만 수율은 5% 이상 높았다. 따라서, 생산량의 측면에서는 Method 1보다 상대적으로 유리하다고 볼 수 있다. 그러나 두 처리방법은 처리시간이 Method 1에 비해 길다는 단점이 있다.
3.2 LMCFs의 형태 및 파티클 사이즈
제조방법에 따라 얻어진 LMCFs의 현미경 관찰 결과를 Fig. 3에 도시하였다. Fig. 3(a)의 목분은 20–60 mesh이며 길이 방향이 0.41–1.67 mm, 폭 방향이 85–644 μm 범위에서 다양하게 관찰되었다. 그러나 다양한 방법으로 제조한 LMCFs는 Fig. 3(b)-(d)와 같이 파티클의 크기가 확연히 줄어든 것을 확인할 수 있다. LMCFs는 길이 방향이 0.06–1.05 mm이며 폭 방향은 8–68 μm이었으며 제조방법에 관계없이 확인된 LMCFs의 크기이다. 제조방법에 따라서는 마이크로파 처리를 한 LMCFs (Method 1)의 크기가 평균 0.21 mm, 24 μm로서 Nah 등의 연구결과15)와 비교하여 비슷하거나 조금 더 작은 크기를 보였다. Method 2의 LMCFs는 길이방향과 폭 방향의 크기가 각각 0.34 mm와 38 μm이고 Method 3의 LMCFs는 0.23 mm와 31 μm로 측정되었다. 물질의 내부에서부터 열적 반응이 일어나는 마이크로파 처리가 가장 많은 세포벽의 파괴가 일어나 다른 반응에 비해 미세 조각들이 더욱 많이 관찰되었다. 각 LMCFs의 정확한 크기 확인을 위하여 Fig. 4와 같이 입자들의 면적으로 파티클 사이즈의 분포를 측정하였다.
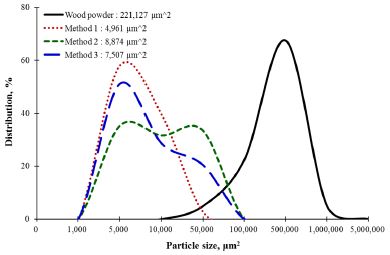
Fig. 3의 현미경 관찰로부터 얻어진 목분 및 LMCFs의 현미경 사진을 이용하여 각 LMCFs의 면적을 계산하여 파티클 사이즈의 분포도를 Fig. 4에 나타내었다. 목분은 평균 221,127 μm2의 파티클 사이즈를 보였으며 각각의 제조방법에 따라 얻어진 LMCFs들은 순서대로 4,961, 8,874 및 7,507 μm2로 측정되었다. 파티클 사이즈의 분포에서 보면 약 500,000 μm2에서 가장 많은 크기를 보이는 목분이 LMCFs(Method 1)로 제조되면서 크기가 급격히 줄어들었다. 마이크로파를 처리한 LMCFs는 주로 5,000 μm2의 면적을 가지는 입자들로 구성되며 오일배스로 처리한 LMCFs(Method 2)는 5,000 μm2와 50,000 μm2에서 거의 유사한 분포 비율을 보였다. 고압증기처리에 의해 제조된 LMCFs(Method 3)는 Method 2의 LMCFs와 유사한 분포 패턴을 보이지만 5,000 μm2의 분포율이 더욱 높게 나타났다. 즉, 본 연구에 사용된 목분은 약 500,000 μm2의 크기로부터 50,000 μm2로 세포벽의 파괴가 일어나며 제조방법에 따라 5,000 μm2까지 미세화되면서 LMCFs가 제조된다는 것을 알 수 있었다. 이는 흥미로운 결과로 추후 연구를 통해 더욱 가혹한 조건에서의 LMCFs 제조에서도 파티클 사이즈가 일정 수준에서 유지되는지를 확인해 보고자 한다.
3.3 중성당 분석
제조방법이 상이함에 따라 목분으로부터 LMCFs가 제조되면서 얻어지는 구성성분의 차이가 나타날 수 있다. 이에 소나무 목분으로부터 제조방법에 따른 LMCFs의 구성성분의 변화를 확인하기 위해 alditol-acetate법에 의거하여 당조성을 분석하였다.
Table 2는 제조방법에 따라 얻어진 각각의 LMCFs로부터 중성당 분석을 실시한 결과를 나타낸 것이다. 소나무 목분의 당조성은 침엽수 목분의 일반적인 당조성과 유사한 결과로서 침엽수 헤미셀룰로오스의 주성분인 글루코만난(glucomannan)으로 인해 높은 만노오스 함량을 보였다. 이에 비해 제조방법에 따라 미분화된 LMCFs들은 헤미셀룰로오스를 구성하는 단당류의 함량이 크게 감소하였다. 특히, 만노오스의 감소가 뚜렷하게 확인되었다. 제조방법에 따른 LMCFs의 단당류 함량에서는 Method 1과 Method 2에서는 유사한 수준의 당조성을 보인 반면 Method 3에서는 다른 두 제조 방법에 의한 LMCFs의 당조성과는 달리 만노오스의 함량이 현저히 감소하였으며 아라비노오스의 함량이 높게 나타났다. 침엽수를 구성하는 헤미셀룰로오스 성분 중 아라비노글루쿠로노자일란(arabinoglucuronoxylan)으로부터 유래되는 아라비노오스가 상대적으로 적게 용출된 것으로 유추할 수 있으나 보다 정확한 이해를 위해서는 미분화 메커니즘에 관한 추가적인 연구가 필요할 것으로 보인다. 추후 셀룰로오스를 이용한 연구를 위해서는 당조성의 차이가 다소 발생하더라도 글루코오스의 함량에는 큰 영향을 미치지 않으므로 세 종류의 LMCFs 제조방법이 모두 적용 가능하다고 보여진다.
3.4 RLCFs의 분광학적 특성
세 종류의 제조방법에 따른 LMCFs의 특성을 전술한 바와 같이 수율, 잔존리그닌 함량, 파티클 사이즈 및 당조성을 통해 확인할 수 있었다. 제조방법이 상이함에 따라 제조된 LMCFs의 분광학적 특성에서의 차이를 확인하기 위해 IR을 통한 비교를 다음과 같이 실시하였다.
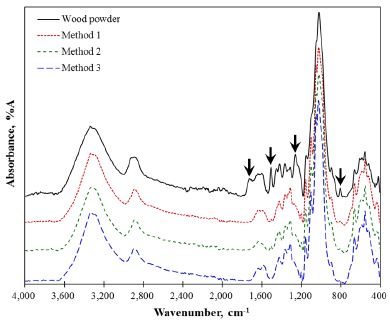
Fig. 5는 3가지 방법에 의해 제조된 LMCFs의 IR 스펙트럼 결과이다. 제조방법에 관계없이 3종류의 IR 스펙트럼 상 피크 패턴은 모두 유사하였으며 목분과는 상이한 패턴을 보였다. 목분과 LMCFs는 크게 4개의 피크에서 차이점이 나타났다. 대립되는 4개의 피크에 대한 설명은 다음과 같다. 먼저, 1,704 cm-1 영역대는 C=O에 해당하는 피크이고,18) 1,506 cm-1의 영역대는 리그닌 유래의 방향족 환을 나타내는 것이다.19) 1,258 cm-1은 리그닌의 과이아실기(guaiacyl unit)가 확인되는 피크 영역이며 800 cm-1 영역대의 피크는 피란 진동(pyran vibration)에 의해 나타나는 부분이다.20) 즉, 목분의 IR 스펙트럼에서 피크의 세기가 강하게 나타나는 4개의 피크 영역대는 LMCFs에서 상대적으로 약하게 확인된다. 1,704 cm-1와 800 cm-1의 피크들은 헤미셀룰로오스 유래의 피크들이다. 미분화 반응에서 촉매로 사용된 황산과 목재 내에 존재하는 우론산(uronic acid) 등에 의해 가수분해가 일어나 헤미셀룰로오스가 용출되었기 때문에 LMCFs에서는 이들의 피크가 약하게 확인되는 것이다. 또한, 1,506 및 1,258의 리그닌 유래의 피크들도 헤미셀룰로오스 분해 시 함께 LMCFs로부터 제거되어 리그닌의 피크 세기도 약하게 나타나게 되었다. 목분과 LMCFs 사이의 화학적 특성은 분명히 확인되지만 제조방법에 따른 LMCFs 간의 차이는 IR 스펙트럼으로 확인되기 어려웠다. 따라서 Široky 등13)의 방법에 따라 TCI와 HBI를 계산하여 Fig. 6에 나타내었다.
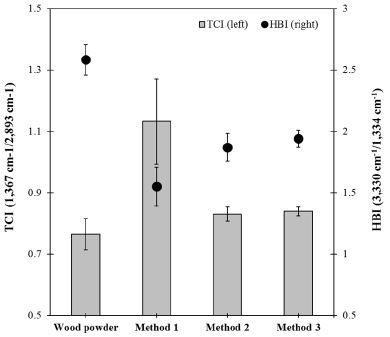
Fig. 6.
TCI and HBI of LMCFs by three preparation methods. TCI means the total crystallinity, and HBI means the hydrogen-bond intensity.
Fig. 6은 제조방법에 따른 LMCFs의 IR 스펙트럼결과로부터 특정 피크의 세기를 이용하여 TCI와 HBI를 계산한 결과이다. TCI는 물질 내에 결정화지수를 나타내는 지표로서13) 목분에서는 0.76의 결정화지수를 보였다. Method 2와 Method 3는 각각 0.83과 0.84로 분석된 모든 특성들이 유사하게 나타났다. 그러나 마이크로파 처리를 한 Method 1의 LMCFs에서는 1.13의 높은 결정화지수를 나타내었다. 이는 마이크로파에 의해 목재의 내부부터 반응이 일어나고 순간적으로 고온의 열에 노출되어 가수분해가 많이 이루어지기 때문이다. HBI는 주로 탄수화물에 존재하는 수산기의 양을 의미한다.13) 목분의 경우, 2.58의 HBI를 보이는 반면, Method 1, 2, 3의 LMCFs에는 각각 1.55, 1.87 및 1.94의 HBI 지수를 보여준다. 앞선 TCI의 결과와 같이 Method 2와 Method 3의 LMCFs에 존재하는 수산기의 양은 비슷하였지만 미분화 과정 중 가수분해가 상대적으로 많이 일어난 Method 1의 LMCFs에서는 가장 낮았다. 따라서 유사한 잔존 리그닌 함량을 보이는 LMCFs를 각각의 제조방법에 따라 제조하여도 미분화된 시료 내에 존재하는 성분은 다소간의 차이가 발생할 수 있다는 것이다.
3.5 주성분분석
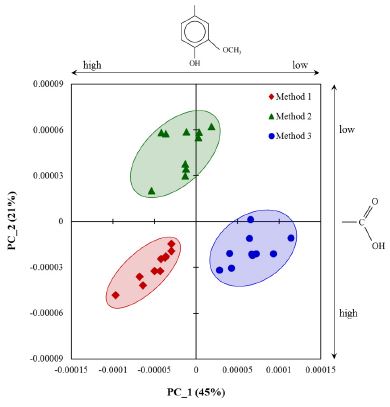
세 종류의 제조방법에 따라 제조된 LMCFs가 TCI와 HBI 결과를 통해 결정화지수와 수산기의 양이 서로 상이하다는 Fig. 6을 통해 확인할 수 있었다. Fig. 7에서는 각각의 LMCFs들의 스펙트럼 데이터들로부터 주성분 분석을 실시하여 PCA 스코어 그래프(score plot)을 작성하고 이를 통해 분류 패턴을 확인하였다.
세 종류의 LMCFs는 PC_1과 PC_2에 따라 각각의 클러스터를 형성하였다. PC_1과 PC_2의 성분을 역추적하기 위해 PCA 적재값(loading data)와 2차 미분 IR 데이터를 비교 분석하였다.21) 이 결과에서 PC_1과 PC_2의 주성분은 각각 리그닌의 방향족 환과 가수분해 등에 의해 생성되는 카르복실기로 나타났다. 이 결과를 바탕으로 유추하면, Method 1의 LMCFs는 다른 제조방법에 비해 가수분해가 많이 일어났으며 리그닌 함량도 높은 물질이라는 것이다. Method 2의 LMCFs는 세 종류의 제조 방법 중 가장 가수분해를 적게 발생시키는 방법이며 Method 3의 LMCFs는 제조 반응 시 가수분해가 발생되지만 리그닌 함량이 가장 낮다는 특징을 갖는다. 즉, 세 가지의 제조방법 중 어느 방법으로도 LMCFs를 제조할 수 있으며 처리 시간의 면을 고려하면 마이크로파 조사법을, 에너지 비용적 측면에서는 오일배스 처리법을, 그리고 균일한 시료의 수급면에서는 고압증기처리법(오토클레이브 처리법)의 적용이 적합하다고 판단된다.
4. 결 론
세 종류의 제조 방법에 따라 제조한 LMCFs의 특성을 평가한 결과는 다음과 같다. 유사한 잔존 리그닌 함량을 보이는 제조 방법이라 하더라도 제조된 LMCFs의 수율은 서로 상이하였다. 마이크로파 조사에 의해 제조된 LMCFs는 오일배스 처리나 고압증기처리에 비해 가수분해가 많이 일어나 가장 낮은 파티클 사이즈를 보였으며 수산기의 양도 가장 적었다. 반면, 마이크로파 조사에 의한 LMCFs의 결정화지수가 가장 높은 특징을 보였다. 각각의 제조 방법에 따른 LMCFs는 형태적으로는 유사한 경향을 보이지만 리그닌의 방향족 환과 카르복실기의 함량이 서로 상이하다는 것을 알 수 있었다. 이러한 결과를 바탕으로 LMCFs의 제조 시간, 에너지 비용 및 시료의 균일성 등의 측면에 따라 효율적으로 LMCFs의 제조가 가능하며 본 연구에서는 균일한 시료의 고정적 수급이 가능한 고압증기처리법을 적용하는 것이 가장 효율적인 방법이라고 할 수 있다.