1. 서 론
목질 바이오매스의 화학적 주성분은 셀룰로오스, 헤미셀룰로오스 및 리그닌으로 구성되어 있으며 그 중 셀룰로오스는 가장 풍부한 재생 가능한 천연고분자 자원으로서 전 세계적으로 매년 1011-1012톤 정도 생산되고 있다. 셀룰로오스는 가수분해 과정을 통해 단당 형태인 글루코오스로 전환이 가능하며 바이오연료 및 바이오화학제품 등 바이오화학 산업에 효과적으로 사용될 수 있다.1) 목질 바이오매스 내 탄수화물을 정확하게 정량하기 위해서는 1, 2차 가수분해를 거치는데 이는 상대적으로 많은 양의 시료가 요구되는 단점이 있다.2) 시료의 양이 제한되는 문화재의 경우 보존적 측면을 위하여 주로 비파괴적 분석 방법을 이용하지만3,4) 유기물로 구성된 목재 및 지류 문화재의 경우 분광분석법과 같은 비파괴적 분석은 한정된 정보의 수집만 가능하기 때문에5) 손상 원인 분석 및 보존 대책 연구를 위해서는 화학 조성 분석이 불가피하다. 최소한의 시료를 사용하여 최대한의 정보를 얻을 수 있는 극소량 파괴(micro-destructive) 분석 방법이 현재까지는 최선이다.6,7) 이러한 화학 조성 분석 시 요구되는 시료 양의 감소는 수많은 시료 중 유망한 바이오매스를 선별하거나 제한된 양의 시료를 사용할 때 시료 손실을 최소화할 수 있다.2)
본 연구에서는 다양한 유기물 분석 방법 중 목질 바이오매스의 주성분이 되는 중성 당 분석을 대상으로 미량 시료를 이용한 분석 데이터의 신뢰성 평가를 수행하였다. 현재까지 유기물로부터 유래된 당을 분석하는 기기분석 방법으로는 자외선/가시광선 분광법(UV/Vis), 가스크로마토그래피(GC), 질량분석기(MS), 고성능 액체크로마토그래피(HPLC) 등이 있다. 자외선 분광법은 유기화합물 및 생물학적 고분자의 정량·정성 분석에 이용된다. 용매 사용량이 적고 조작이 간편하지만 시료 양이 적은 경우 확인이 불가능하고 동시에 여러 성분을 정량 분석할 수 없다는 단점이 있다.8) 가스크로마토그래피(GC)는 당의 정량·정성 분석이 가능하지만 시료의 유도체화를 요구하며 분석 시 방해 물질이 많아 정확한 피크 분리가 어렵다.9,10) 다변량 분석 기술과 연결된 근적외선 분광분석기(NIR)와 열분해 분자 빔 질량분석기(Py-MBMS)는 빠르고 정확하게 바이오매스의 구성 성분을 결정할 수 있지만 이러한 방법은 상당한 정교함이 요구되고 광범위한 검정 데이터가 요구된다.2) 고성능 액체크로마토그래피(HPLC)는 당 분석에 있어 범용적으로 이용 가능하며, 전술한 방법들에 비해 방해 물질이 적으며 높은 재현성 및 정확성을 가진다. 또한, 유도체화 과정 없이 선택적으로 분리할 수 있으며 민감한 검출이 가능하다는 것이 장점이다.11) 본 연구에서는 중성 당 분석 결과의 높은 신뢰성 확보 및 다양한 중성 당의 동시 분석을 위하여 고성능 액체크로마토그래피법을 선택하였다. 그러나 이와 같은 분석기기의 발달로 정밀도와 정확도를 높여 왔음에도 불구하고 미량의 시료를 이용하는데 있어서 기기오차, 방법오차, 개인오차에 따른 계통오차가 발생되며 측정되는 양이 감소됨에 따라서 오차는 더욱 심각하게 나타날 수 있다.12) 따라서 본 연구는 미량의 시료를 분석에 이용 시 기존 결과와 비교하여 재현성이 높은 분석 결과를 얻기 위한 방법을 확립하고 각 분석 단계별 발생하는 시료의 손실과 오차를 종합적으로 평가하여 미량 분석의 신뢰성을 높이고자 하였다.
2. 재료 및 방법
2.1 공시재료
본 연구에서 사용한 목질 바이오매스는 신갈나무(Quercus mongolica) 목재 칩 및 상용 열기계펄프(thermomechanical pulp, TMP)로 모든 분석 시료는 Wiley micro-mill(Thomas Wiley, USA)을 이용하여 40 mesh 이하의 크기로 분쇄하여 사용하였다.
2.2 실험방법
2.2.1 산 가수분해
중성 당 분석을 위한 시료의 전처리로서 TAPPI T 222 om-02 및 NREL/TP-510-42618에 따라 산 가수분해를 수행하였다. 이 때, 시료 양을 1/10(normal scale)과 1/100(micro-scale)로 나누어 1, 2차 가수분해를 실시하였다. Normal scale에서의 1차 가수분해는 72%(w/w) 황산을 3 mL 투입하였고, micro-scale에서의 1차 가수분해는 72%(w/w) 황산을 0.3 mL 투입하여 상온에서 2시간 반응시켰다. 1차 가수분해 후 증류수를 사용하여 3% 농도로 희석하였다. Normal scale과 micro-scale은 동일하게 희석된 시료를 사용하여 2차 가수분해 진행하였다. 2차 가수분해는 121°C 오토클레이브에서 1시간 동안 반응시켰다. 1, 2차 가수분해가 끝난 후 normal scale은 glass filter(1G4), micro-scale은 membrane filter(45 μm)로 여과 후 HPLC 분석에 사용하였다. 1, 2차 산 가수분해 과정에서 발생하는 당 손실을 구하고자 5종의 중성 당(glucose, galactose, xylose, mannose, arabinose)을 사용하여 단당 표준용액을 제조하였다. 위 용액을 사용하여 1, 2차 가수분해를 순차적으로 수행하였고 최초 당 농도와 1, 2차 가수분해 후 농도 차이를 이용하여 당 손실률을 비교 평가하였다.
2.2.2 중성 당 조성 분석
중성 당 조성 분석을 위한 HPLC 시료 주입량은 5 μL이며, 분석에는 CarboPacTM PA1(4×250 mm, Dionex, USA) 음이온 교환 컬럼이 장착된 HPAEC(ICS-3000, Dionex, USA) 기기를 이용하였고, pulsed amperometric detection(PAD)으로 검출하였다. 본 시스템은 isocratic mode에서 2:1 비율로 탈이온수(18.2 MΩ/cm)와 250 mM NaOH를 이동상으로 사용하였으며 시료 당 분석 시간은 50분이다. 각 표준 중성 당의 검출 시간은 Table 1과 같다.
Table 1.
Retention time and separation factor of standard sugars
| Sugar | Retention time (min) | Separation factor (α) |
|---|---|---|
| Arabinose | 16.6 | 2.4 |
| Galactose | 21.4 | 1.2 |
| Glucose | 24.8 | 1.2 |
| Xylose | 30.2 | 1.2 |
| Mannose | 32.8 | 1.0 |
중성 당 분석 결과 값을 이용하여 분석 시료 내 상대 glucose 함량과 절대 glucose 함량을 각각 Eq. 1과 Eq. 2로 산출하였다.
중성 당 분석 결과를 검증하기 위하여 검출한계(limit of detection, LOD) 및 정량한계(limit of quantification, LOQ), 직선성 등 유효성 검사12)를 실시하였다. 검출한계(LOD)는 signal/noise(S/N)>3으로 계산하였고, 정량한계(LOQ)는 S/N>10으로 계산하였다. 분석 실험에 사용된 각종 데이터 분석은 Origin Pro 2015 소프트웨어를 이용하여 계산하였다.
3. 결과 및 고찰
3.1 분석 데이터 유효성 검사
각 표준 중성 당의 검출한계(LOD)와 정량한계(LOQ)는 Table 2와 같다. 검출한계와 정량한계는 중성 당의 종류에 따라 각각 4.3-5.9 mg/L, 13.1-17.9 mg/L의 범위로 나타났다. 중성 당 종류에 따라 그 차이는 크지 않았으나 glucose가 다른 중성 당에 비해 상대적으로 높은 LOD 및 LOQ가 요구되었다. 따라서 glucose를 기준으로 정량 분석을 위한 이론적 최소 농도는 17.9 mg/L로 나타났다.
Table 2.
Limit of detection (LOD) and limit of quantification (LOQ) of standard sugars
| Sugar | LOD (ppm (mg/L)) | LOQ (ppm (mg/L)) |
|---|---|---|
| Arabinose | 4.3 | 13.1 |
| Galactose | 4.4 | 13.2 |
| Glucose | 5.9 | 17.9 |
| Xylose | 4.9 | 14.7 |
| Mannose | 4.9 | 14.8 |
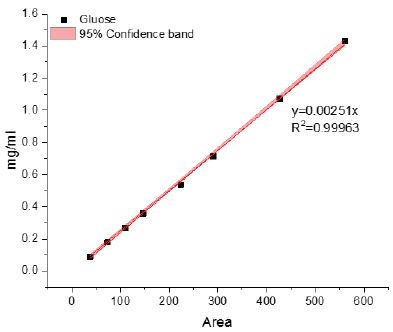
제조된 표준 당을 사용하여 HPLC로 분석한 후 면적 대 농도 값으로 검정곡선을 작성한 결과, glucose의 경우 Fig. 1의 직선 식을 얻었을 수 있었다. 표준 시료 내 각 중성 당은 Table 3과 같이 직선 식을 얻었으며, R2 값이 0.99963-0.99998 범위 내에 분포하여 정확도가 높은 검정곡선을 분석에 사용할 수 있었다.
Table 3.
The slope and coefficient of determination (R2) of standard sugars from calibration curves
| Glucose | Xylose | Galactose | Mannose | Arabinose | |
|---|---|---|---|---|---|
| Slope | 2.51×10-3 | 2.61×10-3 | 2.25×10-3 | 2.59×10-3 | 2.58×10-3 |
| R2 | 0.99963 | 0.99997 | 0.99996 | 0.99998 | 0.99997 |
각 구성 당 별로 95% 신뢰도에서 오차 범위를 계산한 결과는 Table 4와 같다. 이 값은 각 중성 당의 상대값으로 50%의 glucose를 함유한 시료에 적용 시 50±1.61% (신뢰도 95%) 범위에서 검출된다. 이와 같은 오차는 분석기기 자체의 오차와 시료 제조 과정 등 분석기기 외부 요인의 오차가 복합적으로 작용한 결과이다. 따라서 각각의 차이를 평가하기 위하여 분석기기 오차(instrumental errors)를 확인하였다. 표준 당을 이용하여 7번의 각기 다른 batch에서 분석기기의 재현성을 평가한 결과 Table 5와 같이 오차 범위가 약 0.01-0.10%(신뢰도 95%) 이내로 나타났다. 그러므로 분석 시 총 오차 값의 약 10%는 분석기기 내부 오차에서, 그리고 나머지 약 90%는 시료 전처리 과정에서 발생되는 것으로 사료되었다.
3.2 가수분해 반응의 영향
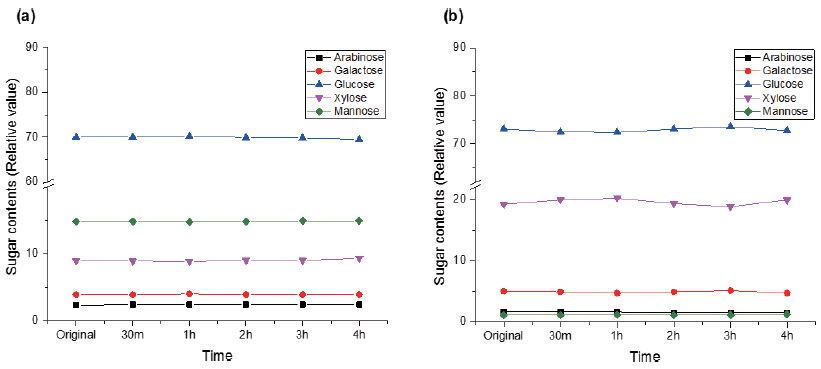
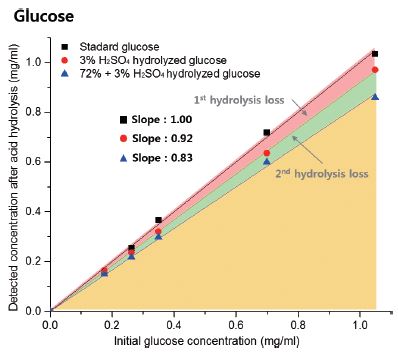
1차 가수분해에 따른 당 손실률 변화 결과를 바탕으로 Table 6과 같이 시간에 따른 중성 당의 상대적 손실률을 구할 수 있었다. 1차 가수분해가 지속됨에 따라 TMP의 경우 xylose를 제외하면 상대적 손실률은 시간당 0.02% 이하로 그 영향이 크지 않았으나, 목재 시료인 신갈나무 칩의 경우 시료에 따라 시간당 약 1-3% 수준의 감소를 나타내었다(Fig. 2). 이와 같은 차이는 TMP와 목재 시료 간의 약품의 접근성에 기인하는 것으로 TMP와 같은 펄프 이용 시 TAPPI 표준 시험방법(T 222 om-02)에서 제안한 2시간의 가수분해 시간 기준보다 1시간을 단축해도 결과 값에는 최대 0.02% 이하의 오차만을 나타낼 것으로 사료된다. 1, 2차 가수분해 과정 중 손실되는 당의 비율을 평가하고자 각 단계별로 단당 표준용액을 사용하여 분석하였다. Fig. 3은 가장 많은 함량을 차지하는 glucose의 가수분해 전 농도 값과 가수분해 후 검출된 농도 값의 관계식을 이용하여 시료 양에 따른 손실 양을 계산하여 각각의 당에 대한 손실률을 나타낸 것이다. Xylose에서 가장 손실률이 높았으며 1차 가수분해보다 2차 가수분해에서 손실률이 평균 약 30% 정도 더 큰 것으로 나타났다. 2차 가수분해는 산의 농도는 낮지만 높은 반응성을 위하여 고온, 고압에서 반응하기 때문에 반응 조건이 가혹하여 일부 당의 경우 추가적인 부반응으로 인한 손실이 더 발생된 것으로 사료된다.
Table 6.
The loss factor of sugars as a function of acid hydrolysis
| Standard sugar | Sugar loss factor | |
|---|---|---|
| 1st hydrolysis | 2nd hydrolysis | |
| Arabinose | 0.08 | 0.14 |
| Galactose | 0.09 | 0.09 |
| Glucose | 0.08 | 0.09 |
| Xylose | 0.11 | 0.17 |
| Mannose | 0.08 | 0.10 |
3.3 분석 시료 양의 영향
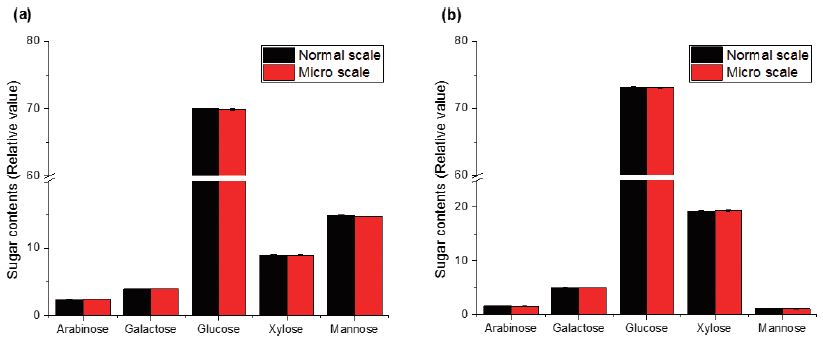
Normal scale과 micro-scale 분석 간 가장 큰 변화는 감소된 시료 양에 적합한 용량의 vial을 사용하는 것과 stirrer를 이용하여 반응시간 내 연속 교반을 시켜주는 것이다. Fig. 4는 TMP와 신갈나무 목재 시료의 normal scale과 micro-scale에서의 전체 구성 당을 기준으로 상대 당 함량을 비교한 그래프로 TMP와 신갈나무 목재 시료가 모든 구성 당에서 각각 ±0.1% 및 ±0.2% 이하의 낮은 오차 결과를 얻을 수 있었다. 이는 전처리 과정 중 발생하는 각 중성 당의 손실률을 보정한 결과보다 미량시료 분석의 정확도를 높일 수 있었다.
이와 같은 결과를 통해 micro-scale의 시료 전처리 방법이 기존의 분석 방법과 비교해 큰 차이가 없음을 확인할 수 있었으며, 시료 양이 더 감소하더라도 각 중성 당의 예상되는 손실률을 계산하여 상대 당 함량을 추정할 수 있을 것으로 사료되었다. 그러나 시료 내 각 구성 당의 절대 함량 비교 시 5종의 중성 당 총량은 TMP와 신갈나무 목재 칩의 경우 normal scale에서 각각 55.0±0.2% 및 69.5±0.4%, micro-scale에서는 53.4±0.3% 및 68.6±0.9%로, 이는 당 총량 기준으로 micro-scale에서 0.9-1.6%가 적으며 각 구성 당을 기준으로는 당의 함량에 따라 최대 0.7%에서 최소 0.1% 이하의 차이를 나타냈다. 총 중성 당 함량을 기준으로 한 상대 당 조성과 비교 시 시료 양을 기준으로 한 당 조성에 오차가 증가한 것은 미량의 시료 중량 측정 시 발생한 오차로 인한 것으로 사료되었다. 따라서 칭량 저울의 정확도와 정밀도 향상, 그리고 칭량 시의 온·습도 변화로 인하여 발생될 수 있는 외계오차의 개선을 통하여 분석의 신뢰성을 향상시킬 수 있을 것으로 사료된다.
4. 결 론
HPLC를 이용한 목질 바이오매스의 중성 당 조성 분석의 유효성 및 신뢰성을 평가한 결과, 각 전처리 과정 중 발생되는 시료 손실 양을 확인하고 이를 보정할 수 있었다. 미량 시료 분석 경우 normal scale의 결과와 비교 시 상대 당 함량 차이는 TMP, 신갈나무 목재 칩 모두 ±0.2% 이하의 오차로 미량의 시료에서도 신뢰성 높은 결과를 얻을 수 있었다. 또한, 분석 시료 양의 감소에 따라 기존 전처리 방법으로 처리 시간을 설정하였을 때 중성 당 함량에는 큰 변화를 보이지 않았으며, 처리 시간 단축의 가능성을 확인할 수 있었다. 다만 분석 시료 내 절대 당 함량 분석에서는 미량 시료의 중량 측정 시 발생되는 기기 및 외계 오차로 인하여 시료에 따라 glucose는 최대 0.7%까지 차이가 있었다. 따라서 분석 시료 칭량의 정확성 및 정밀성이 확보된다면 미량의 시료로도 정확한 중성 당 분석이 가능할 것으로 사료되었다.