1. 서 론
화석연료를 대체하는 바이오매스 기반 에너지와 소재는 지구환경의 보전에 대한 전 세계적인 관심의 증대와 함께 더욱 중요한 이슈가 되고 있다. 대표적인 바이오매스 자원인 목재의 경우 산림의 보존과 수요에 비해 제한적인 조림 등1)으로 목재자원의 공급이 제한되면서 새로운 대체 자원 확보가 시급한 실정이다. 이를 위해 초본류를 포함한 농산부산물, 유기성폐기물 등 다양한 바이오매스의 활용가능성이 평가되어 왔는데 특히, 발생량과 경제성면에서 많은 장점을 가지는 오일팜 바이오매스는 많은 관심의 대상이 되고 있다.
오일팜은 팜오일의 생산을 위해 주로 인도네시아와 말레이시아 등의 열대지방에서 집중적으로 재배되고 있다. 특히 인도네시아의 경우 8.9백만 ha(한국 국토 면적 9.9 백만 ha)로 넓은 재배 면적을 가지고 있는데, 팜오일 열매 수확량은 2010년 2억 2천만톤, 2013년 2억 7천만 톤으로 매년 생산량이 꾸준히 증대되고 있으며2), 인도네시아 23.5 백만톤(2011년 기준)3), 말레이시아 11.9 백만톤의 팜오일이 매년 생산되고 있다. 오일팜의 재배와 팜오일 생산을 통해 오일팜 중 빈오일팜 열매송이(EFB, Empty fruit bunch), 오일팜 씨박(PKS, Palm kernel shell), 오일팜 잎(OPF, Oil palm frond), 오일팜트렁크(OPT, Oil palm trunk) 등 다양한 폐기성 바이오매스가 대량으로 발생된다. 특히, 팜오일 생산과정을 통해 지속적으로 발생되는 EFB(Empty fruit bunch)는 인도네시아와 말레이시아 각각 25.9, 19.8 백만톤이 발생한다고 알려져 있으며5), 현재 특별한 활용 용도 없이 버려지거나 연료로 활용되는데, 섬유활용6), 플라스틱 복합체7), 보드8) 및 활성 탄소 제조9) 등의 다양한 연구가 진행되고 있으나, 대부분 저급한 용도로 활용되고 있어 고부가가치화 활용방안에 대한 관심이 높아지고 있다.
EFB는 셀룰로오스 44.2%, 헤미셀룰로오스 33.5 %, 리그닌이 20.4 %로로 구성되어 있는데10), EFB 구성성분 중 가장 큰 구성을 차지하는 셀룰로오스는 바이오매스의 주요 성분으로, 최근 고부가가치화를 위한 다양한 연구개발이 집중되고 있는데, 특히 식의약 소재 등의 주요 원료로 활용되는 MCC(Microcrystalline cellulose, 미세결정셀룰로오스)제조에 대한 관심이 증대되고 있다.
글루코스의 β-D-1,4 글루코시드 결합을 이루고 있는 구조로 구성된 MCC11)는, 순도가 높고 불순물이 거의 없고, 높은 결정화도(약 55 ~ 80%)를 가지며12), 친환경적이고 인체에 무해한 이점을 활용하여 증점제, 수분보유제, 제제 제조 등의 목적으로 화장품, 식품, 제약산업 등에 1960년대 이후 널리 사용되고 있는 주요 소재로써12,13), 주로 목재를 가수분해하여 추출하거나, 면섬유를 무기산 용매로 용해하여 MCC를 제조 및 사용되어지고 있다.
MCC는 추출소재의 종류 혹은 가수분해의 조건에 따라 셀룰로오스의 결정화도, 비표면적, 공극구조, 입자크기 및 분자량 등의 차이가 발생됨을 보고된 바 있으며13-15), 주로 산 가수분해를 이용하여 MCC를 제조하는데16), 최근 다양한 비목질 바이오매스 소재의 MCC의 제조를 통한 고부가가치화 활용을 위해 쥬트17), 밀과 볏집18,19), 부레옥잠20), 코코넛 껍질21), 사탕수수 찌꺼기22), 모시23), 콩껍질24), EFB를 이용하여 MCC를 추출하는 등 다양한 바이오매스 소재의 MCC 추출에 관한 연구가 보고되었으며25,26), MCC의 고도 활용을 위해 MCC를 추출 공정의 개선 연구27), MCC의 다양한 활용을 위한 nanowhisker 제조28), 인산 합성을 통한 활용26) 등 다양한 연구가 진행되고 있다. 특히 MCC는 다른 소재에 비해 의약용 제제 제조가 용이하여 제제의 주요 소재로 사용되고 있으며29), 다양한 소재를 활용한 제제의 제조특성 및 대체 소재에 다양한 연구가 진행되고 있다30,31). 본 연구에서는 EFB의 고도활용을 위한 방안으로 고순도셀룰로오스 소재인 EFB 기반 MCC의 제조 및 활용특성을 알아보았다. 특히, EFB 유래 MCC의 특성과 이를 활용하여 제제(tablets)를 제조하여 기존 상업적으로 사용되고 있는 Avicel-MCC(PH 101)과 제품적용 특성을 비교평가해 보았다. 이러한 실험들을 통해 향후 EFB를 기반으로 한 고부가가치 셀룰로오스 소재개발을 위한 기반자료를 제공하고자 하였다.
2. 재료 및 실험방법
2.1. 공시재료
본 연구에서는 인도네시아에서 공수받은 EFB(Empty fruit bunch)를 적용하여 실험을 실시하였다. EFB는 제조 및 채취 공정 시 다량의 불순물이 표면에 붙게 되는데, 이를 제거하고 MCC(Micrycrystalline cellulose) 제조 시 원료에 대한 영향을 최소화 하기 위해 세척 후 건조하여 사용하였다. 제조된 EFB-MCC(Empty fruit bunch – Microcrystalline cellulose)의 비교 평가를 위해 상업적으로 사용되고 있는 Avicel-MCC(PH 101)을 이용하였다.
2.2 오일팜 EFB 펄핑
오일팜 EFB MCC의 제조를 위한 펄핑방법으로는 소다펄핑(Soda Pulping)을 적용하였는데, 소다펄핑의 경우 분리된 리그닌이 Sulphur-free의 특성을 가지고 있기 때문에32), 페놀릭 레진33), 동물사료34), 분산제35) 등으로 이용이 가능한 장점을 가지고 있다. 본 실험에서는 170 ℃, NaOH 20%, 액비 1: 6, 2 시간의 조건으로 소다 펄핑을 실시하였고(Table 1), 소다 펄핑을 실시 후 흑액을 제거한 섬유분에서, 40 mesh와 200 mesh 분급을 실시하여 본 셀룰로오스 추출을 위해 40~200 mesh 사이의 분급분을 사용하였다. 분급을 실시한 섬유분에 잔류 흑액 성분이 남아있지 않도록 충분히 세척을 실시하였다.
Table 1
Pulping conditions for EFB pulp
| Methods | Concentration | Temp (℃) | Time (min) | Liquor ratio |
|---|
| Soda | 20 | 170 | 120 | 6 : 1 |
2.3 셀룰로오스 추출
2.3.1 홀로셀룰로오스 추출
펄핑 공정에서 수득한 EFB 섬유를 이용하여 홀로 셀룰로오스 추출을 실시하였다. 셀룰로오스 추출을 위하여 TAPPI Method 중 홀로셀룰로오스 추출 방법을 참고하여(TAPPI standard method T203 cm-99) 1000 mL 삼각플라스크(Erlenmeyer flask)에 펄프 섬유 10 g, 증류수(distilled water) 600 mL, 아세트산(acetic acid) 0.8 mL, NaClO2(sodium chlorite) 4 g을 넣은 후 water bath에서 70 ℃의 온도 조건에서 1시간 동안 반응을 진행시켰다. 그 후 삼각플라스크에 따로 세척 및 수득공정 없이, 추가적으로 아세트산 0.8 mL, NaClO2 4 g을 넣은 후 다시 1 시간동안 70 ℃의 온도조건에서 반응을 진행시켰으며, 이 공정을 2번 더 반복하여, 총 4시간동안 반응을 진행시켰다. 그 후 아스필레이터를 이용하여 glass filter(1G3)에 반응이 진행된 EFB 펄프섬유를 추출하였으며, 산이 잔류하지 않도록 충분히 증류수로 세척 한 후 아세톤으로 한번 더 세척을 실시하였으며, 105 ℃에서 건조를 실시하였다.
2.3.2 알파 셀룰로오스 추출
홀로셀룰로오스 추출 후 건조된 시료를 이용하여 알파셀룰로오스 추출을 실시하였다. NaOH 17.5%의 용액에 EFB 홀로셀룰로오스를 첨가한 후 약 30 분간 침지를 실시하였다. 침지 된 시료를 glass filter(1G3)를 이용하여 추출을 실시하였다. 추출한 후 알칼리 용액이 남아있지 않도록 충분히 세척하였다.
2.3.3 MCC 추출
건조 된 알파셀룰로오스를 2M HCL의 용액에 액비 1:10 의 비율로 삼각플라스크에 첨가한 후 환류냉각기를 이용, 30분 동안 가열한 후 Glass filter(1G3)를 이용하여 필터링을 실시하였다. 필터링 된 MCC를 잔여 산 성분이 남아있지 않도록 충분히 세척한 후 40℃에서 건조 하였다. 그 후 건조된 EFB-MCC를 막자사발을 이용하여 최대한 고르게 분산시킨 후 사용하였다.
2.4 MCC의 물리적 특성 평가
2.4.1 SEM 분석
EFB-MCC와 AVICEL-MCC의 비교 평가 및 제제를 제조한 후 표면 및 단면의 형태를 분석하기 위하여 전자주사현미경(Field emission scaning electron microscope, EF SEM, Philps XL30 ESEM TMP)을 사용하여 평가하였다.
2.4.2 입도분석
EFB-MCC와 AVICEL-MCC의 입자 크기를 파악하기 위하여 입도분석기를 이용한 입도분포를 측정하였다. 입도분석기는 Sympatec GmbH(Germany)사의 레이저회절입도분석기(HELOS (H1433) & RODOS)로, 측정범위는 0.1μm ~ 3500μm 까지 가능한 기기를 사용하였다.
2.4.3 백색도 측정
백색도는 KS M ISO 2470-1에 의거하여 Spectrophotometer(Technidyne, Color touch 2)를 이용하여 EFB-MCC와 AVICEL-MCC의 비교 평가를 실시하였다. 리그닌 등의 잔류 불순물의 함량에 따라 백색도의 차이가 나타나기 때문에 이를 활용하여 셀룰로오스 순도 대체 평가를 실시하였다.
2.5 화학적 특성 평가
2.5.1 결정화도 분석
결정화도를 평가 및 측정을 하기위하여 X-ray 회절, IR, FT-IR, Ramen, NMR 분광법 등36)의 방법들 중 X-ray 회절 방법을 이용하였다. EFB-MCC와 Avicel-MCC를 X선 회절 분석기(X-ray Diffractometer, Bruker AXS(Germany)/D8 ADVANCE)를 이용하여 분석을 실시하였으며, 다양한 X-ray 방법 중 널리 쓰이고 있는 Segal 법을 이용하여 EFB-MCC와 AVICEL-MCC의 결정화도 평가를 실시하였다37). 110 plane 과 200 plane 사이에서 최소값을 나타내는 값(I am)과 최대값을 나타내는 값(I 200)을 Eq.1를 이용하여 나타내었다.
χCR : Crystallinity index of a specimen,
I 200 : max intensity in 200 plane peak,
I am : min intensity between the 200 plane and 110 plane peaks.
2.5.2 FT-IR 분석
EFB-MCC와 AVICEL-MCC의 화학적 관능기를 비교평가하기 위하여 적외선분광분석장치(Fourier transform infrared spectroscopy, FT-IR)을 이용하여 분석을 실시하였다. 각각의 시료를 전반사 측정(attenuated total reflectance, ATR) 분석 시 나타나는 peak point를 이용하여 분석하였다.
2.6 MCC 제제 제조
AVICEL-MCC와 EFB로 제조한 MCC로 제제를 제조하여 특성의 비교평가를 실시하였다. 제제의 제조 시 결정화도, 수분함량, 분말크기 등에 따른 압축특성 변화가 보고된 바 있는데36), 각각의 MCC의 수분 함량을 약 7.5±0.5 % 로 조절하여, Single punch press(가로 :19.10 mm, 세로 : 9.90 mm)를 이용, 전건기준 0.3 g의 시료를 10, 20, 30, 40 kg/cm2 의 압력으로 약 1분간 압착하여 제제를 제조하였다. 제조된 제제를 이용하여 제조 특성 평가를 실시하였다.
2.7 제제 제조 특성 평가
2.7.1 압축 특성 평가
제조된 tablet을 버니어 켈리버스(Vernier Calipers, mitutoyo)를 이용하여 원료의 종류 및 압력에 따라 동일양으로 제조된 제제의 최종 두께 측정을 통해 각 MCC 원료의 압축 특성 평가를 실시하였다. 두께는 가장 높은 두께가 나타나는 지점을 측정하여 압력별 EFB-MCC와 AVICEL-MCC의 압축성형 조건에 따른 두께의 차이를 통해 압축성을 평가하였다.
2.7.2 물풀림성 평가
제조 조건에 따른 제제의 특성 변화에 따라 물속에서의 물풀림성이 달라지게 되는데, 이는 의약용 제제의 제조 시 고려해야할 매우 중요한 특성으로 알려져 있다38). 본 실험에서는 MCC 원료의 종류 및 압착 압력에 따른 제제 물풀림성 평가를 실시하였다. 삼각플라스크(300 mL)에 증류수 50 mL를 추가한 후 제조된 제제를 약 30초간 침지시켰다. 30초간 침지시킨 삼각플라스크를 Shaker(Lab companion, SI-600R)를 이용하여 회전수가 200 rpm에 도달한 후 1분 동안 200 rpm으로 회전시킨 후 삼각플라스크를 40 mesh에 필터링하여 물속에서 풀리지 않은 제제 잔여분의 무게측정을 통해 물풀림성을 평가하였다.
3. 결과 및 고찰
3.1 물리적 특성 평가
3.1.1 MCC의 형태적 특성 평가
EFB-MCC의 형태적 특성을 기존의 AVICEL-MCC와 비교 평가하였다. AVICEL-MCC의 경우 약 50 um 이상의 크기를 가진 것으로 알려져 있는데, 제조된 EFB-MCC와 비교하였을 때, 시료의 형태가 다소 긴 형태를 가지고 있는 것으로 나타났고 EFB-MCC의 경우 상대적으로 다양한 형태와 입자로 구성되어 있는 것을 확인할 수 있었다.
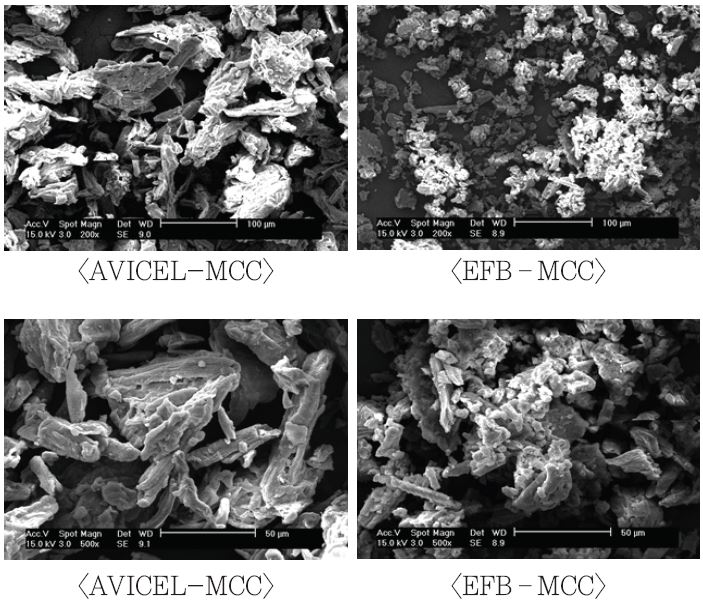
Fig. 1
Scanning electron micrographs of AVICEL-MCC and EFB-MCC.
3.1.2 입도분석
AVICEL-MCC와 EFB-MCC의 입자 크기의 분포를 확인하기 위해 입도분석을 실시하였다. AVICEL-MCC의 경우 입자 크기의 분포가 균일한 것과는 달리 EFB-MCC의 경우 입자의 분포가 매우 광범위하게 분포하고 있는 것을 Fig.2를 통해 확인할 수 있었다. Table 2에서 보여지는 것과 같이 누적 분포를 통한 입자 크기의 분포 분석 결과 X50 에서 AVICEL-MCC는 68.58 μm, EFB-MCC 26.59 μm 으로 나타났으며, 이후의 누적 분포에서는 EFB-MCC의 크기가 AVICEL-MCC에 비해 다소 커지는 것으로 볼 때, EFB-MCC의 경우 상대적으로 작은 입자들이 많이 존재하고 있는 것으로 판단되었다.
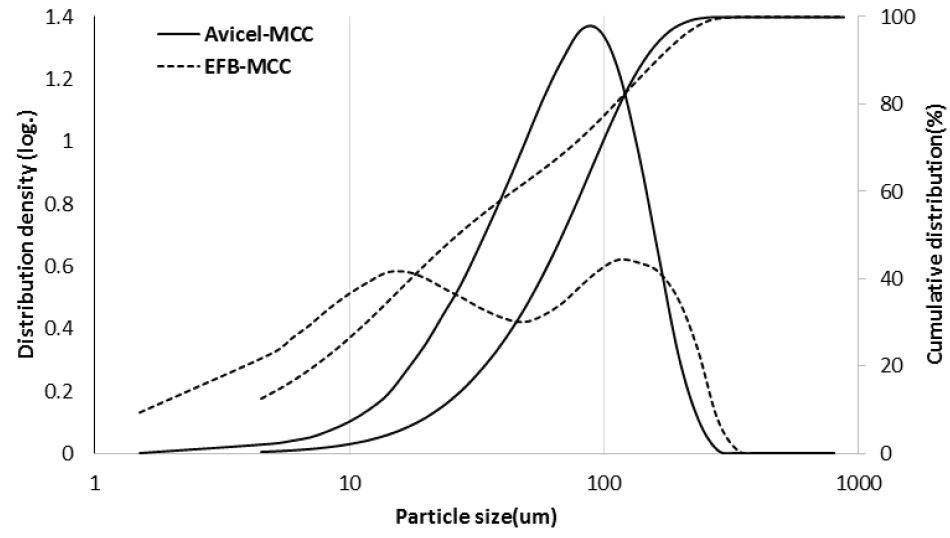
Fig. 2
Particle size distribution of AVICEL-MCC and EFB-MCC.
Table 2
Cumulative distribution of AVICEL-MCC and EFB-MCC
| Cumulative distribution |
|---|
| X10 | X16 | X50 | X84 | X90 | X99 |
|---|
| AVICEL-MCC (μm) | 22.26 | 29.38 | 68.58 | 124.56 | 144.25 | 213.06 |
| EFB-MCC (μm) | 3.68 | 5.74 | 26.59 | 127.87 | 127.87 | 253.73 |
3.1.3 백색도 평가
MCC의 백색도가 높을 경우 잔여 리그닌의 함량이 적은 것으로 볼 수 있는데39), EFB로 제조된 MCC와 AVCEL-MCC와과의 백색도 평가를 실시를 통해 외관 특성 및 리그닌의 잔여 등에 따른 셀룰로오스의 순도 특성 평가를 실시하였다. 평가를 실시한 결과 AVICEL-MCC와 EFB-MCC가 각각 80.05, 79.69로 유사한 수준의 백색도를 나타내는 것을 확인하였다.
Table 3
ISO brightness of AVICEL-MCC and EFB-MCC
| ISO brightness |
|---|
| Average | Std Dev. | High | Low |
|---|
| AVICEL-MCC | 79.69 | 0.93 | 80.28 | 78.61 |
| EFB-MCC | 80.05 | 1.907 | 81.50 | 77.89 |
3.2 화학적 특성 평가
3.2.1 MCC 결정구조 평가
셀룰로오스의 구조는 결정영역과 비결정영역으로 나누어지고 이러한 셀룰로오스 결정화도는 제제의 제조 시 영향을 미치는 데, 결정화도가 낮을 경우 결정화도가 높은 제제에 비해 강도적 특성이 낮게 나타난다는 보고가 있다40). XRD를 이용하여 각 시료의 결정구조를 측정한 후 Segal식을 이용하여 AVICEL-MCC와 제조된 EFB-MCC의 결정화도를 Eq.1 공식으로 계산하였다. 본 실험에서 AAVICEL-MCC 75.6 %, EFB-MCC 75.1 %의 결정화도를 나타내어 선행연구와 유사한 결정화도를 가지는 것을 확인하였으며27,41),이러한 결과를 바탕으로 결정화도는 제제 제조 특성에 주요한 차이를 가져오지 않을 것으로 판단하였다.
Table 4
Crystallinity of AVICEL-MCC and EFB-MCC
| Crystallinity |
|---|
| Min | Max | Crystallinity(%) |
|---|
| AVICEL-MCC | 550 | 2253 | 75.6 |
| EFB-MCC | 603 | 2423 | 75.1 |
3.2.2 MCC의 관능기 평가
FT-IR을 이용하여 EFB-MCC와 AVICEL-MCC의 화학 관능기 평가를 실시하였다. 스펙트럼에서 1(669 cm-1)은 C-H의 bending 피크, 2(896 cm-1)은 방향족 알켄의 C-H bending 피크42), 3,4는(1050-1165 cm-1) 피크는 C-O-C 신축 진동 피크43), 5,6(1320~1425 cm-1)은 –OH 면내 변동 피크26), 1425는 아로마틱 링 그룹의 수소결합의 상호작용에 대한 피크이며44), 6(1645 cm-1)은 물의 흡수물분자의 상호작용에 따른 셀룰로오스와 물 사이의 강한 상호작용으로 인하여 나타나는 피크43,45), 7(2900 cm-1)은 CH2 그룹의 신축 피크45), 8(3350 cm-1)은 –OH 신축 진동 피크43,46) 나타낸다. AVICEL-MCC와 EFB-MCC의 FTIR 스펙트럼이 유사한 것으로 보아 화학적 관능기의 특성차이는 거의 없는 것으로 확인하였다.
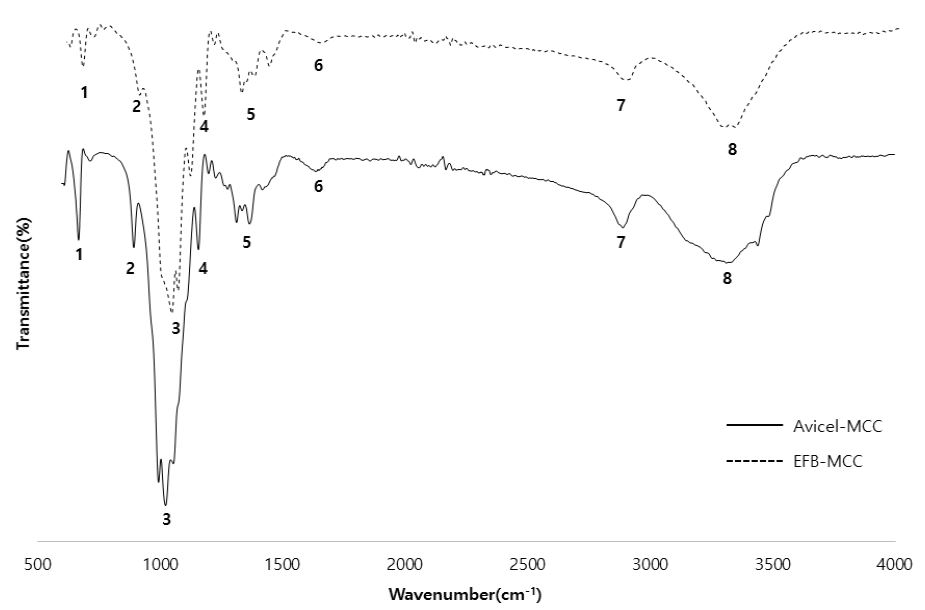
Fig. 3
FT-IR spectra of AVICEL-MCC and EFB-MCC.
3.3 제제 제조 특성 평가
3.3.1 제제 압축성 평가
AVICEL-MCC와 EFB-MCC를 각각 이용하여 제조한 제제의 압력별 두께 측정 평가를 실시하여 압축성을 평가하였다. 또한 제조 후 제제의 형태적 특성을 전자현미경을 통해 평가하였다. EFB-MCC의 동일압력 조건에서 AVICEL-MCC에 비해 밀도가 높은 제제가 형성되는 것으로 확인되었는데 이는 EFB-MCC의 넓은 입자 크기 분포로 AVICEL-MCC에 비해 상대적으로 제제 제조시 팩킹 특성이 우수하게 나타나는 것으로 판단되었다. 이러한 영향으로 실제 Fig 5에서 나타나는 것과 같이 제제 표면에서도 상대적으로 균일하고 매끈한 표면을 가지게 되는 것으로 나타났다. 제제의 단면의 비교시에서는 특별한 차이점이 나타나지 않았다.
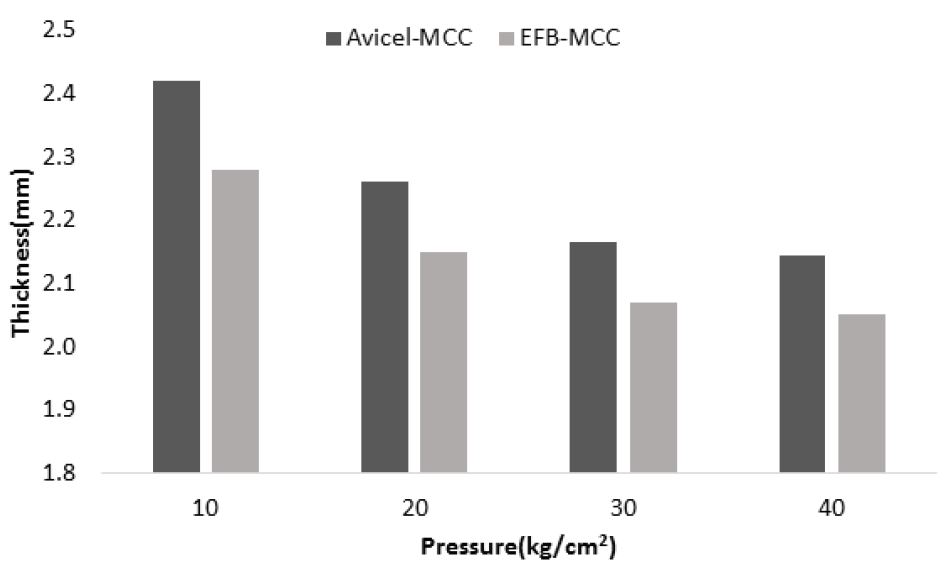
Fig. 4
Change in thickness of tablets depending on press pressure of AVICEL-MCC and EFB-MCC.

Fig. 5
Scanning electron micrographs of the tablets made of AVICEL-MCC and EFB-MCC.
3.3.2 물풀림성 평가
제조된 제제가 물속에서 자연해리되는 특성을 물풀림성으로 비교 평가하였다. AVICEL-MCC와 EFB-MCC 모두에서 제제 제조시 압착압력이 증가함에 따라 물에 풀리지 않고 남아있는 제제의 양이 증가함을 보였으며, 10 kg/cm2 으로 제조한 제제를 제외하고는 EFB-MCC가 상대적으로 물속에서 덜 해리되는 것으로 나타났다. 이러한 현상은 EFB-MCC의 형태적 특성에서 작은 크기의 입자들이 AVICEL-MCC 보다 많이 존재하기 때문인 것으로 판단되었다. 이러한 특성으로 낮은 압력으로 압착하여 제조되는 경우 입자 사이즈가 균일하지 못하기 때문에 AVICEL-MCC에 비하여 풀어짐성이 높아지나, 20 kg/cm2의 압력 이상으로 압착하여 제조되는 경우 상대적으로 높은 강도의 제제가 제조됨에 따라 물풀림성이 감소하는 것으로 판단되었다.
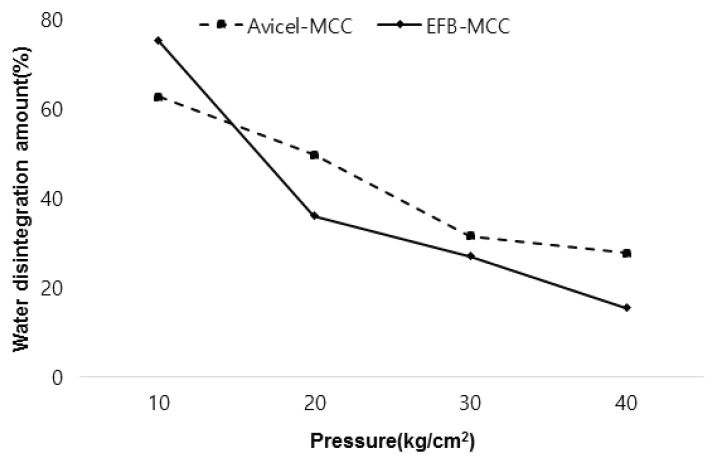
Fig. 6
Changes in water disintegration depending on the tablet making pressure of AVICEL-MCC and EFB-MCC.
4. 결 론
본 논문에서는 동남아시아를 중심으로 매년 많은 양으로 발생되는 폐기성 바이오매스인 오일팜 EFB의 고도활용 방안을 모색해보고자 EFB로부터 고순도 셀룰로오스 소재인 MCC를 제조하여 그 특성을 평가하여 보았다. 특히, 제약산업의 소재로 적용가능성을 평가하기 위하여 다양한 공정조건에서 고밀도 제제를 제조하여 제제의 품질특성변화를 기존의 AVICEL-MCC와 비교 평가하였고 그 결과는 다음과 같다.
1) EFB-MCC와 AVICEL-MCC와의 물리적 특성을 평가한 결과, EFB-MCC가 AVICEL-MCC에 비해 입자크기 분포가 넓게 분포하였고, 상대적으로 작은 크기의 입자분포가 높은 것을 확인할 수 있었다.
2) XRD, FT-IR을 이용한 결정화도 및 화학 관능기 평가 결과 AVICEL-MCC와 EFB-MCC와의 화학적 조성과 결정화도는 매우 유사한 것을 수 있었다.
3) 원료에 따른 제제 제조 특성 평가를 위해 압축성, 물풀림성 특성을 평가한 결과, EFB-MCC가 AVICEL-MCC에 비해 압축성이 더 높은 것을 확인할 수 있었으며, EFB-MCC가 20kg/cm2 압력 이상에서 제조 시 AVICEL-MCC에 비해 제제강도가 우수하여 상대적으로 물 풀림성이 낮게 나타나는 것을 알 수 있었다. 이러한 결과를 통해 입자크기의 분포를 조절함으로써 제제의 강도적 특성의 개선효과를 가져올 수 있을 것으로 판단되었다.
EFB-MCC의 적용성을 평가한 본 연구의 결과를 기반으로 하여 효율적 제조방안과 적용성 개선 방안 연구 등 추가적인 관련 연구가 진행된다면 EFB의 고부가가치 활용방안을 확보할 수 있을 것으로 생각된다.
Acknowledgements
본 연구는 산림청 ‘산림과학기술개발사업(과제번호: S111215L070110)’의 지원에 의하여 이루어진 것입니다.
Literature Cited
D. S. Kim, Y. J. Sung, C. H. Kim and S. B. Kim, Journal of Korea TAPPI, Effects of pre-treatments on the oil plam EFB fibers, 44(6); 36-42 (2012)
D. S. Kim, Y. J. Sung, C. H. Kim and S. B. Kim, Journal of Korea TAPPI, Changes in the water absorption properties of pulp mold manufactured with oil palm EFB by surface treatments, 47(1); 75-83 (2016)
T. B. Bardant, H. Abimanyu and N. Adriana, International Journal of Environment and Bioenergy, Effect of pretreatment technology on enzyme susceptibility in high substrate loading enzymatic hydrolysis of palm oil EFB and water hyacinth, 3(3); 193-200 (2012)
H.P.S. Abdul Khalil, M. Y. Nur Firdaus, M. Jawaid, M. Anis, R. Ridzuan and A. R. Mohamed, Materials and Design, Development and material preperties of new hybrid medium density fibreboard from empty fruit bunch and rubberwood, 31; 4229-4236 (2010)10.1016/j.matdes.2010.04.014
L. Tan, M. Wnag, X. Li, H. Li, J. Zhao, Y. Qu, Y. M. Choo and S. K. Loh, Bioresource Technology, Fractionation of oil palm empty fruit bunch by bisulfite pretreatment for the production of bioethanol and high value products, 200; 572-578 (2016)10.1016/j.biortech.2015.10.079
L. Jiménez, L. Serrano, A. Rodríguez and R. Sánchez, Bioresource and Technology, Soda-anthraquinone pulping of palm oil empty fruit bunches and beating of the resulting pulp, 100; 1262-1267 (2009)10.1016/j.biortech.2008.08.013
L. L. Chai, S. Zakaria, C.H. Chia, S. Nabihah and R. Rasid, Iranian Polymer Journal, Physicomechanical preperties of PF composite board from EFB fibres suing liquefaction technique, 18(11); 917-923 (2009)
M. Khalid, C. T. Ratnma, T. G. Chuah, S. Ali and T.S.Y. Choong, Materials and Design, Comparative study of polypropylene composites reinforced with oil palm empty fruit bunch fiber and oil palm derived cellulose, 29(1); 173-178 (2008)10.1016/j.matdes.2006.11.002
M. Z. Alam, E. S. Ameem, S. A. Muyii and N. A. Kabbashi, Chemical Engineering Journal, The factors affecting the performance of activated carbon prepared from oil palm empty fruit bunches for adsorption of phenol, 155(1-2); 191-198 (2009)10.1016/j.cej.2009.07.033
F. Hamzah, A. Idris and T.K. Shuan, Biomass and Bioenergy, Preliminary study on enzymatic hydrolysis of treated oil palm (Elaeis) empty fruit bunches fibre (EFB) by using combination of cellulase and β 1-4 glucosidase, 35; 1055-1059 (2011)10.1016/j.biombioe.2010.11.020
Y. J. Sung, Y. J. Lee, J. W. Lee, S. B. Kim, G. S. Park and S. J. Shin, Journal of Korea TAPPI, Study of preparation and characterization of microcrystalline cellulose from Miscanthus sinensis, 42(4); 56-63 (2010)
S. Chuayjuljit, S. Su-uthai and S. Charuchinda, Waste Management & Research, Poly(vinyl chloride) film filled with microcrystalline cellulose prepared from cotton fabric waste : Properties and biodegradability study, 28; 109-117 (2010)10.1177/0734242X09339324
M. El-Sakhawy and M. L. Hassan, Carbohydrate Polymer, Physical and mechanical properties of micro-crystalline cellulose prepared from agricultural residues, 67; 1-10 (2007)10.1016/j.carbpol.2006.04.009
A. J. De Menezes, G. Siqueira, A. A. S. Curvelo and A. Dufresne, Polymer, Extrusion and characterization of functionalized cellulose whiskers reinforced polyethylene nanocomposites, 50; 4552-4563 (2009)10.1016/j.polymer.2009.07.038
R. Li, J. Fei, Y. Cai, Y. Li, J. Feng and J. Yao, Carbohydrate Polymers, Cellulose whiskers extracted from mulberry : a novel biomass production, 76; 94-99 (2009)10.1016/j.carbpol.2008.09.034
O.A. Battista, Industrial and Engineering Chemistry, Hydrolysis and crystallization of cellulose, 42(3); 502-507 (1950)10.1021/ie50483a029
F. Fahma, S. Iwamoto, N. Hori, T. Iwata and A. Takemura, Cellulose, Isolation, prepa-ration, and characterization of nanofibers from oil palm empty-fruit-bunch (OPEFB), 17; 977-985 (2010)10.1007/s10570-010-9436-4
J. K. Jain, V. K. Dixit and K. C. Varma, Indian Journal of Pharmaceutical Science, Preparation of microcrystalline cellulose from cereal straw and its evaluation as a tablet excipient, 45; 83-85 (1983)
J. N. Chen, S. Q. Yan and J. Y. Ruan, Journal of Macromolecular Science, Pure and Applied Chemistry, A Study on the preparation and properties of microcrystalline cellulose, A33; 1851-1862 (1996)
S. M. Gaonkar and P. R. Kulkarni, Textile Dyer Printer, Improved method for the preparation of microcrystalline cellulose from water hyacinth, 20(26); 19-22 (1987)
S. M. Gaonkar and P. R. Kulkarni, Acta Polymerica, Microcrystalline cellulose from coconut shells, 40(4); 292-294 (1989)10.1002/actp.1989.010400419
D. A. Shah and Y. D. Shah, Research and Industry, Trivedi, B. M. Production of microcrystalline cellulose from sugar cane bagasse on pilot plant and its evaluation as pharmaceutical adjund, 38(3); 133-137 (1993)
A. D. Castro and J. H. Bueno, Revista CIE Pollo Ncias Farmace Pollo Uticcas, Associacoes de celluloses microfina e microcristalina Na compressao direta. Estudos preliminaries, 15; 169-181 (1996)
Y. U. Nelson, A. G. Edgardo and A. W. Ana, International Journal of Pharmaceutics, Microcrystalline cellulose from soybean husk: effects of solvent treatments on its properties as acetylsalicylic acid carrier, 206; 85-96 (2000)10.1016/S0378-5173(00)00532-9
W. D. Wanrosli, M. K. Mohamad Haafiz and S. Azman, Bioresource, Cellulose phosphate from oil palm biomass as potential biomaterials, 6; 1719-1740 (2011)
W. D. Wanrosli, R. Rohaizu and A. Ghazali, Carbohydrate Polymers, Synthesis and characterization of cellulose phosphate from oil palm empty fruit bunches microcrystalline cellulose, 84; 262-267 (2011)10.1016/j.carbpol.2010.11.032
R. Ramli, N. Junadi, M. D. H. Beg and R. M. Yunus, World Academy of Science, Engineering and Technology International Journal of Chemical, Nuclear, Materials and Metallurgical Engineering, Microcrystalline cellulose (MCC) from oil palm empty fruit bunch (EFB) fiber via simultaneous ultrasonic and alkali treatment, 9(1); 8-11 (2015)
M. K. M. Haafiz, A. Hassan, Z. Zakaria, I. M. Inuwa and M. S. Islam, Materials Letters, Physicochemical characterization of cellulose nanowhiskers extracted from oil palm biomass microcrystalline cellulose, 113; 87-89 (2013)10.1016/j.matlet.2013.09.018
D. Wang, S. B. Shang, Z. Song and M. K. Lee, Journal of Industrial and Engineering Chemistry, Evaluation of microcrystalline cellulose prepared from kenaf fibers, 16; 152-156 (2010)10.1016/j.jiec.2010.01.003
R. F. Shangraw and D. A. Demarest, Pharm. Tech, A survey of current industrial practices in the formulation and manufacture of tablets and capsules, 17(1); 32-32 (1993)
S. Suvachittanont and P. Ratanapan, J. Chem. Chem. Eng, Optimization of micro crystalline cellulose production from corn cob for pharmaceutical industry investment, 7; 1136-1141 (2013)
J. Gullichsen and C. J. Fogelholm, Book 6: Chemical pulping, Helsinki [etc.]: Fapet Oy [etc.] (1999)
R. J. A. Gosselink, A. Abächerli, H. Semke, R. Malherbe, P. Käuper, A. Nadif and J. E. G. Van Dam, Industrial Crops and Products, Analytical protocols for characterisation of sulphur-free lignin, 19(3); 271-281 (2004)10.1016/j.indcrop.2003.10.008
B. Baurhoo, C. A Ruiz-Feria and X Zhao, Animal Feed Science and Technology, Purified lignin: Nutritional and health impacts on farm animals—A review, 144(3); 175-184 (2008)10.1016/j.anifeedsci.2007.10.016
A. Nadif, D. Hunkeler and P. Käuper, Bioresource Technology, Sulfur-free lignins from alkaline pulping tested in mortar for use as mortar additives, 84(1); 49-55 (2002)10.1016/S0960-8524(02)00020-2
Y. D. Heo, Y. J. Sung, Y. J. Joung, D. K. Kim and T. Y. Kim, Journal of Korea TAPPI, Changes in the properties of cotton cellulose by hydrogen peroxide bleaching, 45(3); 59-68 (2013)10.7584/ktappi.2013.45.3.059
J. E. Ahn, H. J. Youn, Y. J. Joung and T. Y. Kim, Journal of Korea TAPPI, Determination of crystallinity index of cellulose depending on sample preparation and analysis insturments, 44(4); 43-50 (2014)
M. M. Rawas-Qalaji, F. E. R. Simons and K. J. Simons, AAPS PharmSciTech, Fast-disintegrating sublingual tablets: effect of epinephrine load on tablets characteristics, 7(2); E1-E7 (2006)10.1208/pt070241
Y. J. Lee and Y. J. Sung, Journal of Korea TAPPI, Preparation purified cellulose from rice hull, 44(3); 79-85 (2013)10.7584/ktappi.2012.44.3.079
Y. Nakai, E. Fukuoka, S. Nakajima and J. Hasegawa, Powder Technol, Crystallinity and physical characteristics of microcrystalline cellulose, 54; 161-164 (1977)
V. Kumar and S. H. Kothari, International Journal of Pharmaceutics, Effect of compressional force on the crystallinity of directly compressible cellulose excipients, 177; 173-182 (1999)10.1016/S0378-5173(98)00340-8
A. Alemdar and M. Sain, Bioresource Technology, Isolation and characterization of nanofibers from agricultural residues - wheat straw and soy hulls, 99; 1664-1671 (2008)10.1016/j.biortech.2007.04.029
SML. Rosa, N. Rehman, MIG. De Miranda, SMB. Nachtigall and CLD. Bica, Carbohydrate Polymers, 82; 1131-1138 (2012)
V. Kumar, LRM. Maria De La and D. Yang, International Journal of Pharmaceutics, Preparation, characterization, and tabletting properties of a new cellulose-based pharmaceutical aid, 235; 129-40 (2002)10.1016/S0378-5173(01)00995-4
M. Jonoobi, J. Harun, PM. Tahir, A. Shakeri, SS. Azry and MD. Makinejad, Materials letters, Physicochemical characterization of pulp and noanofibers from kenaf stem, 65(7); 1098-1100 (2011)10.1016/j.matlet.2010.08.054
R. G. Zhbankov, Infrared spectra of cellulose and its derivatives, New York. Consultants Bureau, Plenum Publishing Corporation, Springer. (2013)










