1. 서 론
최근의 펄프, 제지산업은 전자매체의 발전으로 인하여 인쇄용지의 수요가 급감하고 있으며 포장용지 등 산업용지의 부분에서도 플라스틱과 같은 소재에 밀려나고 있다. 국내 펄프·제지업체들은 이러한 위기를 벗어나기 위해 다양한 방법을 시도하고 있다. 그 중 목질 바이오매스를 이용한 신소재 개발이 매우 주목받고 있는 분야이다. 목재는 가장 풍부하고 널리 분포 된 바이오매스 자원 중 하나이지만, 복잡한 다중 구성 요소 구조로 인해 화학적인 공급 원료로 직접 사용되기가 상당히 어렵다.1) 목질 바이오매스는 일반적으로 셀룰로오스, 헤미셀룰로오스 및 리그닌과 같은 주성분으로 분리할 수 있으며 목재를 통한 바이오매스 액화제품이 대체에너지, 재생 가능한 자원으로 제안되어 폴리우레탄 발포체나 접착제 구성요소에서 폴리올 대체자원으로 사용 가능성이 연구되어 왔다.2,3) 그 외에도 목질 바이오매스를 이용한 신소재는 셀룰로오스 나노섬유와 탄소섬유가 있다. 셀룰로오스 나노섬유는 섬유의 형태에 따라서 크게 2종류로 나눌 수 있는데 먼저 셀룰로오스의 비결정영역을 화학적으로 가수분해하여 얻어지는 장폭비가 작고 나노크기의 크리스탈 형태를 갖고 있는 섬유는 whisker 또는 microcrystalline cellulose(MCC), nanocrystalline cellulose(NCC), cellulose nanocrystal(CNC) 등으로 부른다. 이와 달리 기계적 처리에 의해 소섬유화하여 얻어진 장폭비가 크고 수 마이크로 이상의 크기를 갖는 섬유는 microfibrillated cellulose(MFC), nanofibrillated cellulose (NFC), cellulose nanofibrill(CNF) 등으로 부르고 있다.4,5) 그리고 폐목재를 기반으로 페놀-포름알데히드 수지를 이용하여 탄소섬유를 제조하는 방법,6) 목재로부터 분리된 리그닌을 이용하여 탄소섬유를 제조하는 것7) 등 목질 바이오매스를 이용한 다양한 신소재 개발이 진행 중이다.
지금까지 바이오매스 액화를 위한 대부분의 처리방법은 오일베스, 염욕, 샌드베스, 및 대류의 열원으로 수행되었고,8) 촉매에 따라서는 산 촉매와 적당한 온도(120-180°C)에 의한 방법 그리고 촉매를 투입하지 않고 높은 온도(250°C)에서 반응을 시키는 액화방법 등이 있다. 상기의 방법으로 바이오매스의 충분한 액화를 위해서는 30-180분의 상대적으로 긴 반응시간이 소요된다. 2003년 일본 교토의 그린바이오 기관에서는 염욕을 사용하여 목재의 액화반응 시간을 줄이는 연구를 진행한 바 있다. 그 결과, 반응시간을 현저히 줄일 수 있었지만 염욕의 반응온도가 250-450°C로 지나치게 높은 단점이 있었다.9) 이 방법과는 대조적으로 마이크로파는 혼합물에 존재하는 분자와 직접 반응함으로써 효율적으로 균일하게 내부에 열을 가하게 된다.10,11) 이에 기존의 열분해에 비해 반응속도가 빨라 반응시간이 단축되며 과도하게 높은 온도를 필요로 하지 않는다. 2005년 영국 요크대학교의 한 연구진에 따르면 기존의 오일베스 액화에서 마이크로파 오븐 액화로 전환하였을 때 소모되는 에너지와 비용이 85배 감소했다고 하였다. 이 문헌의 결과에서 보면 마이크로파를 사용하는 것이 오일베스를 사용하는 것에 비해 에너지와 비용적인 측면에서 훨씬 효율적이다.12) 또한, Mašek 등은 파일럿규모에서도 효과적이라고 하였다.13) 그리하여 마이크로파는 현대에 들어 가장 각광받고 있는 열분해 장치 중 하나이다.
본 연구에서는 바이오매스의 신소재화 연구의 기초연구로서 다양한 조건에서 마이크로파를 이용한 glycol ether 용매에서의 바이오매스의 화학적 분산을 진행하여 분산 잔류물의 특성을 비교하고자 하였다.
2. 재료 및 방법
2.1 공시재료
2.1.1 소나무 목분(pine wood meals)
본 연구에서는 함수율이 6.4%인 국내산 소나무(Pinus densiflora) 목분을 사용하였으며 그 크기는 40-80 mesh로 조절하였다. 소나무 목분은 실험을 위해 에탄올-벤젠 혼합용액(1:2, v/v)으로 24시간 동안 추출하여 탈지 목분을 제조하였다. 본 연구의 소나무 목분은 Klason 리그닌 함량이 28.0%이며 산 가용성 리그닌 함량은 0.5%였다.
2.1.2 시 약
본 연구에서 사용된 반응시약은 이전 연구14)의 용매 중 하나로 끓는점이 약 197°C인 glycol ether 용매(pure grade, Sigma Aldrich Co.)를 사용하였다. 촉매로는 순도 95%의 황산(H2SO4, Daejung Chemicals & Metals, Korea, extra pure grade)을 사용하였다.
2.2 실험방법
2.2.1 소나무 목분의 화학적 분산(chemical micronization)
40-80 mesh의 소나무 목분의 화학적 분산 방법은 이전의 연구15)에서 소개한 바 있다. 우선 5 g의 소나무 목분 시료에 glycol ether와 황산 혼합시약을 1:2(w/v)로 투입하였다. 사용된 혼합시약은 glycol ether 용매에 대하여 0.5-3.0%(v/v)로 촉매를 혼합하여 제조하였다. 혼합시약과 반응된 시료는 400 W로 조절된 마이크로파 오븐(SE-MW 50018, Sun Enterprise, Korea)으로 60초 및 120초 동안 반응시켰다. 마이크로파 반응 시 20초 간격으로 시료를 꺼내어 Vortex mixer(G-560, Scientific Industries Inc., USA)를 사용하여 shaking level 5에서 20초간 충분히 교반시켰다. 반응 종료 후 0.5 N NaOH 용액 250 mL를 사용하여 충분히 교반한 후 세척하였다. 1차적으로 세척된 반응 시료는 중성이 될 때까지 증류수로 세척을 실시한 후 필터 페이퍼와 감압기를 이용하여 여과하였다. 여과 후에 생성된 잔류물은 105±3°C의 건조 오븐에서 8시간 이상 건조시켰다.
2.2.2 분 석
소나무 목분의 화학적 분산 반응 전·후의 중량을 측정하여 시료의 잔사율(Eq. 1)을 계산하였다. 반응이 완료된 시료의 형태학적 특성을 관찰하기 위해 실체현미경(SDC-411, Samsung, Korea)을 이용하여 150배율로 관찰하였으며 반응 잔류물의 형태와 입도분석(i-Solution, IMT I-Solution Inc, Canada)을 실시하였다. 반응 잔류물의 리그닌 함량을 측정하기 위해 TAPPI T 222 om-02에 의거하여 Klason lignin(KL) 함량과 TAPPI UM 250에 의거하여 산 가용성 리그닌(acid soluble lignin, ASL) 함량을 측정하였다.
Rw: 화학적 분산 반응 후 잔사의 중량(g),
Tw: 전건 목분의 중량(g).
또한, 목분의 화학적 분산 반응 전후의 작용기 변화를 관찰하기 위해 ATR-IR spectroscopy(Alpha-P Model, Bruker Optics Inc., Germany)를 이용하여 4,000-400 cm-1의 영역을 16회 스캔하여 스펙트럼을 측정하였다. 분산 반응 잔류물의 결정화 지수(crystallinity index)는 IR spectrum의 1,446 cm-1(CH2 bending in cellulose) 대와 900 cm-1(C-O stretching in cellulose) 대 피크 intensity의 비로 계산하였다(Eq. 2).16)
3. 결과 및 고찰
3.1 화학적 분산 잔류물의 잔사율과 리그닌 함량
3.1.1 잔사율
Fig. 1은 반응시간과 촉매의 농도에 따라 화학적 분산 반응을 진행한 시료의 잔사율을 나타낸 것이다. 마이크로파에 의해 화학적 분산 반응 후 시료의 잔사율은 반응시간과 촉매의 농도가 증가함에 따라 감소하였다. 60초의 반응시간에서는 촉매의 투입량이 3.0% 일 때 가장 낮은 잔사율(28.9%)을 보였고, 120초의 반응시간에서는 촉매의 투입량이 2.5%의 경우 가장 낮은 잔사율인 24.6%가 나타났다. 화학적 분산에 사용되는 촉매의 농도가 낮으면 목재 세포벽의 파괴가 용이하게 일어나지 않아 높은 잔사율을 보이며 촉매량이 많아질수록 목재 주성분의 파괴가 많이 일어나 잔사율이 급격히 줄어드는 것으로 보인다. 한편, 60초의 반응시간과 3.0%의 촉매 조건에서의 화학적 분산 반응물의 잔사율은 120초의 반응시간과 2.0%의 촉매 조건의 것(30.4%)과 유사한 수치를 보였다. 즉, 반응시간과 촉매의 농도를 조절하면 화학적 분산 반응 잔류물의 양을 조절할 수 있는 것으로 판단된다.
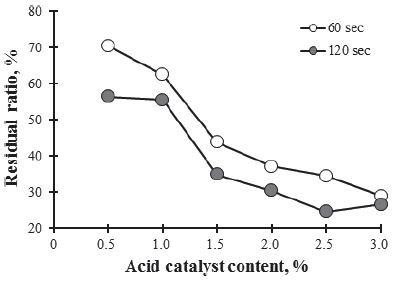
Fig. 1.
Ratio of wood residues by chemical micronization using different catalyst contents and dispersion times.
3.1.2 잔존 리그닌 함량
Fig. 2는 반응시간과 촉매의 농도에 따라 화학적으로 반응된 잔류물의 잔존 리그닌 함량을 측정한 것이다. 반응시간에 따른 Klason 리그닌의 함량은 촉매의 농도가 높아질수록 감소하였다. 60초의 경우, 2.5%의 촉매를 첨가하였을 때 약 7.5%의 잔존 리그닌이 존재하는 것으로 나타났으며 1.5% 이상의 촉매에서는 9% 전후의 리그닌이 잔존해 있었다. 그러나 3.0%의 촉매 조건에서는 잔존 리그닌의 함량이 9.5%로 2.5%의 촉매 조건에서보다 약간 증가하였다. 이는 분산 반응을 통해 용출된 리그닌들의 재축합으로 인해 발생된 것으로 보이며 이러한 결과는 Alriols 등17), Li 등18) 및 Hong 등19)의 결과와 일치하였다. 120초의 반응시간에서는 촉매의 농도에 따라 잔존 리그닌의 함량이 감소하다가 2.5% 이후부터는 측정이 불가하였다. 2.5% 이후의 시료는 반응시간과 촉매의 함량이 높아 탄화로 추정되는 덩어리 형태의 잔류물들이 발견되었다(Fig. 3). 이러한 덩어리 형태의 잔류물들은 72%의 황산에서도 분해되지 않아 Klason 리그닌 함량을 측정할 수 없었다. 60초 반응시간의 산 가용성 리그닌에서는 촉매의 농도가 증가함에 따라 목분(0.5%)보다 약간 높은 함량(0.8-1.0%)을 보였다. 그리고 농도에 따라 산 가용성 리그닌의 함량이 불규칙적으로 측정되지만 그 수치는 미미한 편이므로 크게 차이가 없다고 할 수 있다. 120초의 반응시간에서는 촉매를 투입함에 따라 목분에 비해 0.1% 정도 높은 0.6%의 산 가용성 리그닌 함량을 보였다. 따라서 화학적 분산 반응 잔류물의 리그닌 중 저분자 리그닌에 속하는 산 가용성 리그닌의 함량은 목분과 큰 차이를 보이지 않고 있었다. 이러한 결과로 보아, 본 연구의 화학적 분산 반응은 리그닌을 저분자화 하여 용출시키는 것이 아니라 헤미셀룰로오스를 분해하여 고분자 리그닌 자체를 제거시킨다고 유추할 수 있다.
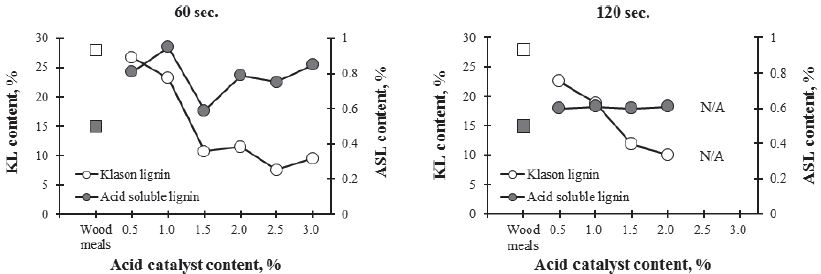
Fig. 2.
Klason lignin and acid soluble lignin content of wood residues by chemical micronization.
3.2 IR 스펙트럼 및 crystallinity index
Fig. 2의 잔존 리그닌 함량 결과에서 가장 낮은 함량을 보인 두 조건과 화학적 분산 반응 전 목분의 IR 스펙트럼 데이터를 Fig. 4에 나타내었다. 목분과 화학적 분산 잔류물 두 종류를 비교하면 Fig. 4와 같이 여섯 부분의 피크 영역이 다르게 나타나는 것을 확인 할 수 있다. 1,717 cm-1 대의 영역은 주로 홀로셀룰로오스에 의한 카르보닐기(C=O)의 영역으로20) 목분에서는 나타나지만 화학적 분산 반응 잔류물에서는 피크가 나타나지 않고 있다. 이는 glycol ether 용매와 산촉매에 의해 화학적 분산 반응이 진행되면서 리그닌과 함께 주로 헤미셀룰로오스가 용출되었기 때문으로 예상할 수 있으며 이러한 결과는 Fig. 2의 산 가용성 리그닌의 결과와 일치한다고 볼 수 있다. 1,504 cm-1 대와 1,258 cm-1 대의 영역은 각각 리그닌 유래의 방향족 환(aromatic ring)21)과 구아이아실 단위(guaiacyl units)22)를 의미한다. 이들 영역 대에서는 화학적 분산 반응에 의해 잔류물 내에 리그닌의 intensity가 상대적으로 많이 낮아졌다. 이는 화학적 분산 반응에 의해 잔존 리그닌 함량이 낮아지는 것(Fig. 2)과 일치하는 결과를 보인다. 그러나 제거된 리그닌의 화학적 생성이나 잔존해 있는 리그닌의 화학구조 등에 관해서는 더욱 상세한 검토가 필요하다. 1,446 cm-1 대의 영역은 주로 셀룰로오스에 있는 CH2 bending과 관련된 피크이다.23) 즉, 화학적 분산 반응에 의해 리그닌의 제거가 많이 일어났지만 셀룰로오스 또한 공격을 받아 Fig. 1의 잔사율의 결과와 같이 상대적으로 intensity도 감소한 것으로 확인되었다. 당분석 등을 통해 제거된 당의 종류를 확인하면 더욱 정확한 결과를 얻을 수 있을 것으로 보인다. 1,153 cm-1과 1,123 cm-1의 피크는 모두 셀룰로오스의 C1-O-C5간의 결합을 나타낸 것이다.23,24) IR 스펙트럼의 결과만으로 해석하면 화학적 분산 반응에 의해 C1-O-C5간의 결합보다 C1-O-C4간의 결합(linear structure)의 파괴가 상대적으로 많이 일어나 세포벽이 찢어지거나 섬유의 형태를 유지하지 못하는 현상이 발생하는 것으로 예상할 수 있으며 이는 다음에 나오는 Fig. 6의 결과를 뒷받침할 수 있을 것으로 보인다.

Fig. 3.
Photographs of dispersed sample (2.0% H2SO4) and carbonized sample (2.5% H2SO4) by chemical micronization for 120 seconds.
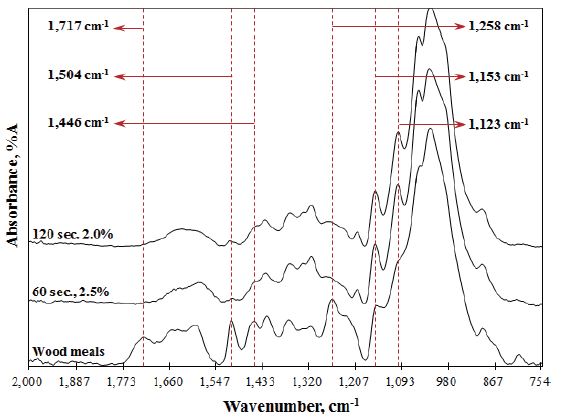
Fig. 4.
IR spectra of wood residues by chemical micronization.
Fig. 5는 화학적 분산 잔류물의 IR 스펙트럼 결과에서 1,446 cm-1 대의 intensity와 900 cm-1 대의 intensity의 비를 이용하여 결정화 지수를 계산한 결과이다. 목분의 경우, 결정화 지수가 약 1.34이었으나 60초(3.0%)와 120초(2.0%)에서 화학적 분산 반응 후 잔류물의 결정화 지수는 각각 0.77과 0.70으로 낮은 결과를 보였다. 이는 마이크로파를 이용한 화학적 분산 반응에서 용매와 촉매가 고온의 열에서 단시간동안 셀룰로오스의 결정영역을 파괴하였기 때문이다. 즉, 단시간에 나타난 반응으로 인해 목분의 형태에서 셀룰로오스의 결정영역이 파괴되고 리그닌이 용출되어 섬유의 결정화도가 감소된 것으로 판단된다. 이와 같은 결과는 세포벽이 찢어지는 등 섬유가 무정형의 형태로 변화된 Fig. 6의 현미경 사진에 상응한다.
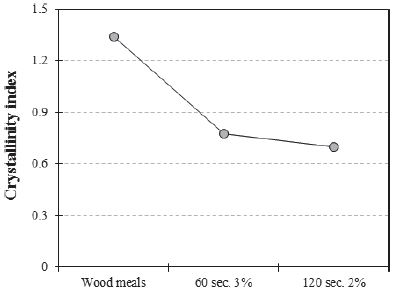
Fig. 5.
Crystallinity index calculated from the IR spectra intensity of wood residues by chemical micronization.

Fig. 6.
Micrographs of wood residues by chemical micronization.
3.3 형태학적 특성
마이크로파 오븐에서 시간과 촉매의 농도에 따라 처리된 후 화학적 분산 잔류물의 형태를 Fig. 6에 나타내었다. Fig. 6(a)와 (b)는 반응시간이 60초로 동일하며 반응 촉매가 각각 1.5%, 3.0%이다. Fig. 6(c)와 (d)는 반응시간이 120초이며 반응 촉매가 각각 1.0%, 2.0%이다. 소나무 목분은 평균 1.5-3.0 mm의 길이와 1.0-2.0 mm의 두께를 가지고 있었다. 반응시간 60초에 반응 촉매 1.5%(a)는 뚜렷한 섬유의 파괴가 많이 발생하지 않았고 3.0%(b)의 경우는 섬유의 파괴가 많이 확인되어 찢어지거나 터진 형태를 보였다. 반응시간 120초에 반응 촉매 1.0%(c)의 경우는 (a)의 경우와 같이 뚜렷한 섬유의 파괴가 진행되지 않았으나 2.0%(d)는 일정부분 섬유의 파괴와 절단이 나타났다. 그러나 (b)에 비해 큰 입자들이 존재하는 것으로 보아 완전한 가수분해가 발생하지는 않은 것으로 보인다. 결론적으로 반응시간 60초와 120초는 모두 반응 촉매가 증가함에 따라 목재 섬유가 찢어지고 절단되며 파괴가 발생하여 입자의 크기가 점점 줄어든다는 것을 알 수 있다. 이를 통해 화학적 분산이 많이 진행되었다는 것을 형태적으로 알 수 있다.
Fig. 6으로부터 얻어진 현미경 사진을 바탕으로 화학적 분산 반응 잔류물의 입자 크기와 폭 및 분포율을 Figs. 7과 8에 나타내었다. Fig. 7은 60초의 반응시간동안 촉매의 함량에 따른 입자의 크기를 나타낸 것이고 Fig. 8은 120초의 반응시간에서 촉매에 따른 화학적 분산 반응 잔류물의 입자 크기를 나타낸 것이다. 반응 잔류물의 입자 크기는 촉매의 함량이 증가함에 따라 감소하였다(Figs. 7과 8의 입자 사이즈 그래프). Figs. 7과 8의 분포 그래프와 같이 각 촉매별로 제조된 잔류물의 입자 분포를 보면 평균 2.0 mm의 길이와 1,000 μm의 폭을 가지는 목분이 촉매의 함량에 따라 화학적 분산 반응이 진행되면서 점점 작은 크기로 변하였다. 이는 Fig. 6의 현미경 결과와 같이 촉매의 함량이 증가함에 따라 목재 섬유가 찢어지거나 터지는 등의 섬유 파괴 현상이 관찰되는 것과 일치하는 결과이다.
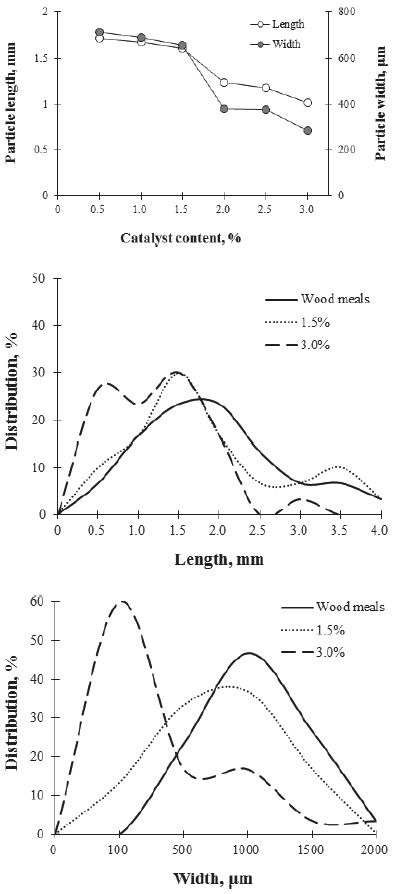
Fig. 7.
Particle size and distribution of wood residues by chemical micronization for 60 seconds.
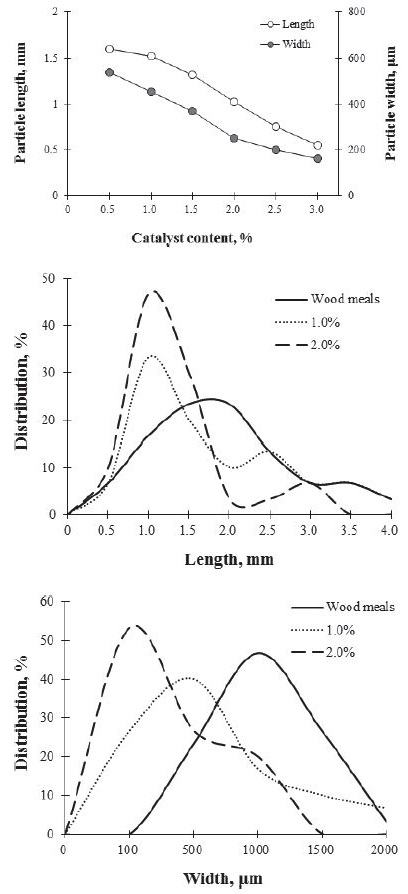
Fig. 8.
Particle size and distribution of wood residues by chemical micronization for 120 seconds.
4. 결 론
바이오매스의 신소재화를 위한 기초연구로서 다양한 조건에서 마이크로파를 이용한 glycol ether 용매에서의 바이오매스의 화학적 분산을 진행하여 분산 잔류물의 특성을 비교한 결과는 다음과 같다. 마이크로파의 반응 조건에 따라 화학적 반응에 의한 잔사율이 감소하였으며, 잔류물의 Klason 리그닌도 감소하였다. 하지만 산 가용성 리그닌의 함량은 큰 차이를 보이지 않았다. 화학적 분산 잔류물의 형태학적 특성에서는 반응시간과 촉매의 함량이 증가함에 따라 목재 섬유가 찢어지고 절단되는 등의 파괴가 일어나 입자의 크기가 작아졌다. 이상의 결과를 종합하면 마이크로파를 이용한 화학적 분산 반응은 60초, 2.5%의 촉매 조건 혹은 120초, 2.0%의 촉매 조건에서 가장 낮은 잔존 리그닌 함량이 나타났으며 형태적으로도 목분의 분산이 가장 잘 이루어졌다. 이와 같은 결과들로 볼 때 화학적 분산 반응에서 나타나는 촉매와 반응시간 조절을 통해 잔사율과 잔존 리그닌 함량의 조절이 가능하다고 할 수 있다.
Acknowledgements
이 논문은 2016년도 정부(교육과학기술부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업임(NRF-2016R1D1A3A03918987).
Literature Cited
A. Kržan and E. Žagar, Bioresource Technology,
Microwave driven wood liquefaction with glycols,
100(12); 3143-3146 (2009)
Kržan, A. and Žagar, E., Microwave driven wood liquefaction with glycols, Bioresource Technology 100(12):3143-3146 (2009).
S. H. Imam, S. H. Gordon, L. Mao and L. Chen, Polymer Degradation and Stability,
Environmentally friendly wood adhesive from renewable plant polymer: Characteristics and optimization,
73(3); 529-533 (2001)
Imam, S. H., Gordon, S. H., Mao, L., and Chen, L., Environmentally friendly wood adhesive from renewable plant polymer: Characteristics and optimization, Polymer Degradation and Stability 73(3):529-533 (2001).
10.1016/s0141-3910(01)00114-8Y. P. Wei, F. Cheng, H. P. Li and J. G. Yu, Journal of Applied Polymer Science,
Synthesis and properties of polyurethane resins based on liquefied wood,
92(1); 351-356 (2004)
Wei, Y. P., Cheng, F., Li, H. P., and Yu, J. G., Synthesis and properties of polyurethane resins based on liquefied wood, Journal of Applied Polymer Science 92(1):351-356 (2004).
10.1002/app.20023M. Pääkkö, M. Ankerfors, H. Kosonen, A. Nykänen, S. Ahola, M. Österberg, J. Ruokolainen, J. Laine, P. T. Larsson, O. Ikkala and T. Lindström, Biomacromolecules,
Enzymatic hydrolysis combined with mechanical shearing and high pressure homogenization for nanoscale cellulose fibrils and strong gels,
8(6); 1934-1941 (2007)
Pääkkö, M., Ankerfors, M., Kosonen, H., Nykänen, A., Ahola, S., Österberg, M., Ruokolainen, J., Laine, J., Larsson, P. T., Ikkala, O., and Lindström, T., Enzymatic hydrolysis combined with mechanical shearing and high pressure homogenization for nanoscale cellulose fibrils and strong gels, Biomacromolecules 8(6):1934-1941 (2007).
E. B. Ahn, S. B. Hong, K. J. Kim and T. J. Eom, Journal of Korea TAPPI,
Micro-fibrillated cellulose preparation with enzyme beating pretreatment and effect on paper strength improvement,
47(6); 57-65 (2015)
Ahn, E. B., Hong, S. B., Kim, K. J., and Eom, T. J., Micro-fibrillated cellulose preparation with enzyme beating pretreatment and effect on paper strength improvement, Journal of Korea TAPPI 47(6):57-65 (2015).
10.7584/ktappi.2015.47.6.057C. Yoshida, K. Okabe, T. Yao, N. Shiraishi and A. Oya, Journal of Material Science,
Preparation of carbon fibers from biomass-based phenol-formaldehyde resin,
40(2); 335-339 (2005)
Yoshida, C., Okabe, K., Yao, T., Shiraishi, N., and Oya, A., Preparation of carbon fibers from biomass-based phenol-formaldehyde resin, Journal of Material Science 40(2):335-339 (2005).
10.1007/s10853-005-6087-1K. Sudo and K. Shimizu, Journal of Applied Polymer Science,
A new carbon fiber from lignin,
44(15); 127-134 (1992)
Sudo, K. and Shimizu, K., A new carbon fiber from lignin, Journal of Applied Polymer Science 44(15):127-134 (1992).
10.1002/app.1992.070440113H. Pan, Z. Zheng and C. Y. Hse, European Journal of Wood and Wood Products,
Microwave- assisted liquefaction of wood with polyhydric alcohols and its application in preparation of polyurethane foams,
70(4); 461-470 (2012)
Pan, H., Zheng, Z., and Hse, C. Y., Microwave- assisted liquefaction of wood with polyhydric alcohols and its application in preparation of polyurethane foams, European Journal of Wood and Wood Products 70(4):461-470 (2012).
S. H. Lee and T. Ohkita, Wood Science and Technology,
Rapid wood liquefaction by supercritical phenol,
37(1); 29-38 (2003)
Lee, S. H. and Ohkita, T., Rapid wood liquefaction by supercritical phenol, Wood Science and Technology 37(1):29-38 (2003).
10.1007/s00226-003-0167-7M. Miura, H. Kagaa, A. Sakuraib, T. Kakuchic and K. Takahashic, Journal of Analytical and Applied Pyrolysis,
Rapid pyrolysis of wood block by microwave heating,
71(1); 187-199 (2004)
Miura, M., Kagaa, H., Sakuraib, A., Kakuchic, T., and Takahashic, K., Rapid pyrolysis of wood block by microwave heating, Journal of Analytical and Applied Pyrolysis 71(1):187-199 (2004).
10.1016/s0165-2370(03)00087-1C. O. Kappe, Chemical Society Reviews,
Microwave dielectric heating in synthetic organic chemistry,
37; 1127-1139 (2008)
Kappe, C. O., Microwave dielectric heating in synthetic organic chemistry, Chemical Society Reviews 37:1127-1139 (2008).
M. J. Gronnow, R. J. White, J. H. Clark and D. J. Macquarrie, Organic Process Research & Development,
Energy efficiency in chemical reactions: A comparative study of different reaction techniques,
9(4); 516-518 (2005)
Gronnow, M. J., White, R. J., Clark, J. H., and Macquarrie, D. J., Energy efficiency in chemical reactions: A comparative study of different reaction techniques, Organic Process Research & Development 9(4):516-518 (2005).
10.1021/op0498060O. Mašek, V. Budarin, M. Gronnow, K. Crombie, P. Brownsort, E. Fitzpatrick and P. Hurst, Journal of Analytical and Applied Pyrolysis,
Microwave and slow pyrolysis biochar - Comparison of physical and functional properties,
100; 41-48 (2013)
Mašek, O., Budarin, V., Gronnow, M., Crombie, K., Brownsort, P., Fitzpatrick, E., and Hurst, P., Microwave and slow pyrolysis biochar - Comparison of physical and functional properties, Journal of Analytical and Applied Pyrolysis 100:41-48 (2013).
K. J. Kim, J. D. Jung, S. E. Jung, S. B. Hong and T. J. Eom, Journal of Korea TAPPI,
Delignification of lignocellulosic biomass with high-boiling point solvent and acidic catalyst,
48(1); 119-126 (2016)
Kim, K. J., Jung, J. D., Jung, S. E., Hong, S. B., and Eom, T. J., Delignification of lignocellulosic biomass with high-boiling point solvent and acidic catalyst, Journal of Korea TAPPI 48(1):119-126 (2016).
10.7584/ktappi.2016.48.1.119G. B. Nah, S. E. Jung, S. B. Hong, K. J. Kim, J. M. Lee and T. J. Eom, Chemical dispersion of lignocellulosic materials (LCM) by glycol etherProceeding of Spring Conference of the Korea TAPPI; 87 (2017)
Nah, G. B., Jung, S. E., Hong, S. B., Kim, K. J., Lee, J. M., and Eom, T. J., Chemical dispersion of lignocellulosic materials (LCM) by glycol ether, Proceeding of Spring Conference of the Korea TAPPI, pp. 87 (2017).
M. A. Yousef, A. A. Shabaka, A. M. A. Nada and K. N. AbdEl-Nour, Indian Journal of Pure and Applied Physics,
Physical properties and IR spectroscopy of thermally treated bagasse paper sheet,
29; 6-8 (1991)
Yousef, M. A., Shabaka, A. A., Nada, A. M. A., and AbdEl-Nour, K. N., Physical properties and IR spectroscopy of thermally treated bagasse paper sheet, Indian Journal of Pure and Applied Physics 29:6-8 (1991).
M. G. Alriols, A. Tejado, M. A. Blanco, I. Mondragon and J. Labidi, Chemical Engineering Journal,
Agricultural palm oil tree residues as raw material for cellulose, lignin and hemicellulose production by ethylene glycol pulping process,
148(1); 106-114 (2009)
Alriols, M. G., Tejado, A., Blanco, M. A., Mondragon, I., and Labidi, J., Agricultural palm oil tree residues as raw material for cellulose, lignin and hemicellulose production by ethylene glycol pulping process, Chemical Engineering Journal 148(1):106-114 (2009).
10.1016/j.cej.2008.08.008G. Li, C. Hse and T. Qin, Journal of Forestry Research,
Wood liquefaction with phenol by microwave heating and FTIR evaluation,
26(4); 1043-1048 (2015)
Li, G., Hse, C., and Qin, T., Wood liquefaction with phenol by microwave heating and FTIR evaluation, Journal of Forestry Research 26(4):1043-1048 (2015).
10.1007/s11676-015-0114-0S. B. Hong, K. J. Kim and T. J. Eom, Journal of Korea TAPPI,
Delignification of pine wood meals using high boiling point solvents and acidic catalysts,
48(6); 131-136 (2016)
Hong, S. B., Kim, K. J., and Eom, T. J., Delignification of pine wood meals using high boiling point solvents and acidic catalysts, Journal of Korea TAPPI 48(6):131-136 (2016).
10.7584/jktappi.2016.12.48.6.131K. J. Kim, G. B. Nah, J. A. Ryu and T. J. Eom, Journal of Korea TAPPI,
Preparation of lignin rich micro-cellulose fines (LMCFs) by chemical micronization method and characteristics of LMCFs handsheet,
49(3); 109-117 (2017)
Kim, K. J., Nah, G. B., Ryu, J. A., and Eom, T. J., Preparation of lignin rich micro-cellulose fines (LMCFs) by chemical micronization method and characteristics of LMCFs handsheet, Journal of Korea TAPPI 49(3):109-117 (2017).
10.7584/jktappi.2017.06.49.3.109J. M. Lawther, R. Sun and W. B. Bank, Journal of Agricultural and Food Chemistry,
Fractional characterization of wheat straw lignin components by alkaline nitrobenzene oxidation and FT-IR spectroscopy,
44(5); 1241-1247 (1996)
Lawther, J. M., Sun, R., and Bank, W. B., Fractional characterization of wheat straw lignin components by alkaline nitrobenzene oxidation and FT-IR spectroscopy, Journal of Agricultural and Food Chemistry 44(5):1241-1247 (1996).
10.1021/jf9502764Y. Huang, L. Wang, Y. Chao, D. S. Nawawi, T. Akiyama, T. Yokoyama and Y. Matsumoto, Journal of Wood Chemistry and Technology,
Analysis of lignin aromatic structure in wood based on the IR spectrum,
32(4); 294-303 (2012)
Huang, Y., Wang, L., Chao, Y., Nawawi, D. S., Akiyama, T., Yokoyama, T., and Matsumoto, Y., Analysis of lignin aromatic structure in wood based on the IR spectrum, Journal of Wood Chemistry and Technology 32(4):294-303 (2012).
10.1080/02773813.2012.666316X. Colom, F. Carrillo, F. Nogués and P. Garriga, Polymer Degradation and Stability,
Structural analysis of photodegraded wood by means of FTIR spectroscopy,
80(3); 534-549 (2003)
Colom, X., Carrillo, F., Nogués, F., and Garriga, P., Structural analysis of photodegraded wood by means of FTIR spectroscopy, Polymer Degradation and Stability 80(3):534-549 (2003).
10.1016/s0141-3910(03)00051-xM. L. Nelson and R. T. O’Connor, Part I: Spectra of Lattice type I, II, III and of amorphous cellulose, Journal of Applied Polymer Science,
Relation of certain infrared bands to cellulose crystallinity and crystal Lattice type,
8(3); 1311-1324 (1964)
Nelson, M. L. and O’Connor, R. T., Relation of certain infrared bands to cellulose crystallinity and crystal Lattice type, Part I: Spectra of Lattice type I, II, III and of amorphous cellulose, Journal of Applied Polymer Science 8(3):1311-1324 (1964).












