1. 서 론
전 세계적으로 지구 온난화 및 대기, 수질 오염 등의 환경문제가 발생하고 있으며, 석유계 자원의 매장량이 고갈되어감에 따라 고유가 현상이 지속되고 있다.1,2) 따라서 석유 의존성과 환경에 대한 유해성을 줄이기 위해 대체자원에 대한 연구가 다방면에서 이뤄지고 있는 실정이다. 특히, 피셔트롭스(Fisher-Tropsch)반응은 석탄, 바이오매스 및 천연가스로부터 합성석유 및 화학물질을 제조하기 위한 핵심기술로 각광받고 있으며 환경오염의 주범인 매연과 황성분의 발생이 적은 원료를 생산할 수 있는 장점이 있다.3) 또한 dimethyl ether(DME)는 다양한 원료를 기반으로 생산되는 합성연료 중의 하나로 제조비용이 저렴하고 이산화탄소 저감효과가 있어 디젤 대체연료로의 활용가능성이 높다.4-7) 그러나 이러한 대체 합성연료의 제조를 위해서 사용되고 있는 자원 중 석탄과 천연가스 등의 매장량은 유한하며 현재의 석유와 같이 분명한 한계치가 존재한다. 따라서 지속가능한 자원인 바이오매스에 대한 관심이 증가하고 있으며 이 중 benzene, toluene, xylene(BTX) 등과 유사한 화학구조를 지닌 C6-C3 phenylpropane 기반의 리그닌에 대한 연구가 꾸준히 이뤄지고 있다.
목재를 구성하는 성분 중 리그닌은 일반적으로 초본류에 10-15%, 침엽수에 20-35% 그리고 활엽수에 20-25%의 수준으로 존재한다.8) 리그닌의 구조를 정확하게 정의할 순 없지만 리그닌의 주요 골격과 구조를 파악하기 위한 연구는 꾸준히 진행되어 왔다. 리그닌의 전구체는 coniferyl alcohol, syringyl alcohol, ρ-coumaryl alcohol 3가지로 분류할 수 있고 3종류의 전구체 함량과 결합방식에 따라 상이한 특성을 나타낸다.9)
리그닌을 제조하기 위한 전처리 방법에는 화학펄핑, 증기폭쇄(steam explosion), 이온성액체를 이용한 리그닌 추출과 부후균을 이용하여 탄수화물을 분해시킨 후 리그닌을 추출하는 방법 등이 이용되고 있다.10) 다양한 전처리 방법 중 전세계적으로 가장 많은 양의 리그닌을 생산하는 방법은 화학펄프화법이며9) 화학펄프화법에는 크라프트 펄프화법, 아황산 펄프화법, 소다펄프화법 등이 있다.11) 또한 크라프트 펄프화법은 우수한 강도의 펄프생산과 증해약품의 회수가 용이한 점으로 인해 현재 화학펄프 중 80%는 크라프트 펄프화법을 이용해 제조되고 있다.12,13)
크라프트 펄프화법에서 발생하는 흑액(black liquors)에는 다량의 리그닌이 함유되어 있으나 펄프공정의 흑액으로부터 약품을 회수한 후 생성된 부산물들은 주로 보일러의 에너지원으로 이용되고 있다. 전세계적으로 발생하는 크라프트 리그닌 중 1-2%를 제외한 대다수는 소각이나 매립을 통해 처리되고 있고 적극적으로 활용되지 못하는 실정이다.14) 하지만 리그닌은 천연으로부터 유래된 방향족 화합물 중 가장 많이 존재하며 지속가능한 자원이기 때문에 바이오연료나 페놀계 화학약품의 제조, 바이오플라스틱, 탄소섬유 제조 원료로의 활용 등과 같이 리그닌의 상용화를 위한 연구가 급증하고 있다. Chen 등15)은 리그닌을 이용해 바이오연료를 제조하였고, Goheen16)은 benzene계 물질 제조에 리그닌을 사용한 바 있다. 또한 Kim 등17)은 리그닌-폴리아크릴로나이트릴 공중합체를 제조했는데 폴리아크릴로니트릴 공중합체가 리그닌의 지방족 알코올기에 주로 치환되기 때문에 dimethylformamide(DMF), dimethyl sulfoxide(DMSO), tetrahydrofuran(THF) 등의 유기용매에 잘 용해되는 특성을 나타냈다고 보고하였다. Kim 등18), Seo 등19), 그리고 Seydibeyoğlu 등20)은 리그닌 기반의 탄소섬유 제조에 대해 연구하였는데 리그닌을 탄소섬유 제조에 이용할 경우 기존의 polyacrylonitrile(PAN)기반의 탄소섬유에 비해 공급 및 가격경쟁력이 우수한 장점이 있는 것으로 보고하였다.
하지만 크라프트 펄핑 시 증해약품과 반응한 리그닌은 1,800-5,000 g/mol 정도의 분자량 범위를 가지며 다분자성이 비교적 높은 편이다.11) 또한 일반적인 합성고분자가 일정한 구조를 가져 균일한 특성을 나타내는 데 반해 리그닌은 무정형의 3차원 고분자 구조이기에 별도의 정제과정 없이는 매우 불균일한 특성을 가진다.21) 따라서 크라프트 리그닌의 고도활용을 위해서는 균일한 특성을 가진 리그닌의 제조가 우선되어야 하며 명확한 특성규명이 필요하다. 본 연구에서는 활엽수 크라프트 리그닌의 유기용매 분획을 통해 균질성이 높은 리그닌을 얻고자 하였으며 각 분획분에 대한 화학적, 열적 특성을 규명함으로써 크라프트 리그닌의 고도활용을 위한 기반을 구축하고자 하였다.
2. 재료 및 방법
2.1 공시재료
M 사로부터 제공 받은 고형분 형태의 활엽수 크라프트 리그닌(KL)을 각 유기용매 처리에 따라 분획하였다. CDCl3(99.8%), hydriodic acid(99.95%), ethyl iodide (99%), pentane(99%) 등은 Sigma-aldrich에서 구매하였으며 pyridine(99.5%)과 acetic anhydride (98.0%), tetrahydrofuran(THF, 99.5%) 등은 Daejung Chemicals의 제품을 사용하였다. 분획에 이용되는 ethyl acetate(99.5%), acetone(99.5%), 1,4-dioxane(99.5%), diethyl ether(99.0%)는 Daejung Chemicals의 제품을 사용하였고, chloroform(99.0%)은 Junsei에서 구매하였다.
2.2 실험방법
2.2.1 리그닌의 분획
리그닌 분획을 위해 유기용매에 리그닌을 투입한 후 약 12시간 동안 충분히 용해하고 직경 47 mm, 공극 직경 0.45 μm의 nylon membrane filter를 이용해 용해분과 미용해분을 분리하였다. 분리된 용해분은 rotary evaporator(N-1110, EYELA, Japan)를 통해 농축하고 소량의 1,4-dioxane을 이용해 재용해한 후 교반 중인 증류수에 한 방울씩 첨가하여 응집이 일어나는 것을 방지하였다. 이후 약 30분간 교반하고 2시간 동안 침전하여 필터링하였다. 최종적으로 membrane filter상에 남은 리그닌을 회수해 냉동고에서 얼린 후 동결건조기(FDCF-12006, OPERON)를 사용하여 파우더 형태의 시료를 획득하였다. 미용해분은 40℃ 건조기에서 유기용매를 날려 버린 후 회수하였다. 각각의 용해분과 미용해분의 시료를 선정된 유기용매에 다시금 용해하여 분획을 실시하였으며 분획 체계도를 Fig. 1에 나타냈다. Ethyl acetate 용해분 중 diethyl ether에 용해된 분획분은 F1이라 명명했으며 diethyl ether에 미용해된 리그닌 중 chloroform 용해분은 F2, 미용해분은 F3으로 표기하였다. 또한 ethyl acetate 미용해분 중 acetone에 용해된 분획분은 F4로 명명하고 미용해분은 96% dioxane을 이용해 다시 분획하여 용해분은 F5, 최종 미용해분은 FI라고 표기하였다. 수율은 최초 크라프트 리그닌 투입량을 기준하여 각 분획분의 양의 비율로 산출하였다.
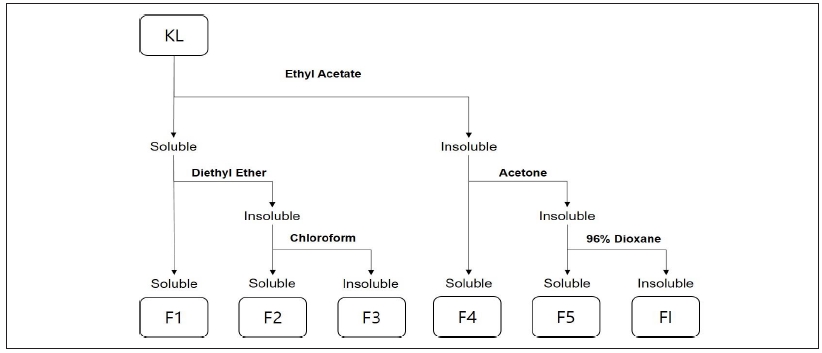
Fig. 1.
Scheme diagram of solvent fractionation of hardwood kraft lignin.
2.2.2 리그닌의 아세틸화 반응
리그닌의 proton-NMR(1H-NMR)분석과 분자량 분석을 위해서 리그닌 수산기를 아셀틸기로 치환 시키는 아세틸화(acetylation) 반응을 실시하였다. 100 mg의 리그닌을 4 mL의 pyridine에 용해하고 acetic anhydride 4 mL를 첨가하여 실온에서 약 12시간 동안 교반하였다. 반응종료 후 아세틸화 반응물을 약 400 mL의 차가운 증류수에 한 방울씩 첨가하여 응집현상을 방지하면서 침전시키고 직경 47 mm, 공극 직경 0.45 μm의 nylon membrane filter를 이용해 여과하였다. 이후 탈이온수로 세척하고 동결건조하여 회수된 리그닌을 Fourier transform infrared(FT-IR)분석을 통해 아세틸화 여부를 확인하고 분석에 사용하였다.
2.2.3 분획 리그닌의 분자량 분석
아세틸화된 리그닌 1 mg을 정량하여 THF 1 mL에 용해 후 gel permeation chromatography(GPC, Shimadzu, UV and RI detectors)를 이용해 분자량 분포를 분석하였다. 분석에 사용된 column(GPC/SEC Columns, Agilent)은 PLgel 5 μm mixed-C, -D, 그리고 PLgel 3 μm mixed-E column을 연결하여 사용하였으며 oven 온도 40℃ 조건에서 분석을 실시하였다. Injection volume은 100 μL, UV detector 파장은 280 nm로 설정하였으며 flow rate 100 mL/min의 조건 하에 THF를 이동상으로 사용하였다. 1,480-1,233,000 g/mol 범위의 polystyrene을 이용하여 검량선을 작성한 후 리그닌의 분자량 분포 분석에 사용하였다.
2.2.4 분획 리그닌의 화학적 특성 분석
2.2.4.1 분획 리그닌의 1H-NMR
분획 리그닌의 phenolic 및 aliphatic OH group 함량을 파악하고자 아세틸화된 리그닌의 1H-NMR분석을 실시하였으며 Bruker 사의 FT-NMR 600 MHz spectrometer(Bruker Avance Ⅱ 600)를 이용하였다. Acquisition time 1.3초, relaxation delay 7초, 90° pulse로 조건을 설정하였으며 시료당 스캔은 128회 실시하였다. Methoxyl group의 적분값을 1로 설정한 후 각 OH group의 적분을 통해 각 group 간의 비율을 분석하였고 이후 methoxyl group의 정량분석 값을 다음 식에 대입하여 각 OH group의 정량값을 산출하였다.
OH group (mmol/g) = Methoxyl group (mmol/g)×ratio (Integral value of OH group/Integral value of OCH3)
2.2.4.2 분획 리그닌의 methoxyl group 함량 분석
Methoxyl 함량 분석은 Park 등22)의 방법에 기초하였으며 gas chromatography/flame ionization detector (GC/FID)를 이용하여 분석하였다. 40 mL의 바이얼에 4 mL의 hydriodic acid와 30 mg의 리그닌을 투입한 후 oil bath에서 130℃ 조건 하에 5분 간격으로 흔들어주면서 30분간 반응시켰다. 반응 후 얼음물에서 냉각하고 내부표준물질로 ethyl iodide(300 mg/mL pentane) 200 μL를 투입하였으며 3 mL의 pentane을 첨가하여 실험실용 shaker(VS-202P, Vision Science)에서 2분간 흔들어주었다. 이후 반응물을 차가운 얼음물에서 충분히 냉각하여 상분리가 발생하도록 유도하였으며 상분리된 용액의 pentane상에 해당하는 상등액 부분을 취하여 분석에 사용하였다. Agilent 사의 GC(7890B)를 이용하여 분석을 실시하였으며 중극성의 DB-624 column(30 m×0.25 mm i.d.)을 분석에 사용하였다. Injector 및 detector는 200, 230℃의 조건으로 설정하였으며 질소를 이동상으로 하여 분당 1.1 mL의 유속으로 흘려주었다. 이 때 split ratio는 1/120으로 설정하였다. Oven온도는 40℃에서 5분간 머무른 후 10℃/min의 조건으로 180℃까지 가열하였다.
2.2.4.3 분획 리그닌의 FT-IR
FT-IR분석은 분획 리그닌의 OH group과 carbonyl group, aromatic ring 등 리그닌에서 나타나는 다양한 작용기를 확인하기 위해서 각 시료당 256번의 스캔을 실시하였고, PerkinElmer 사의 attenuated total reflectance(ATR)가 장착된 Frontier 모델을 이용하였다.
2.2.4.4 Py-GC/MS를 이용한 분획 리그닌의 열분해산물 분석
분획 리그닌의 열분해산물과 syringyl/guaiacyl ratio(S/G ratio)를 파악하기 위해 Py-GC/MS분석을 실시하였다. GC/MS는 Agilent 사의 5975C, 7890A 모델을 이용하였으며 column은 DB-5MS(30 m×0.25 mm×0.25 μm)를 이용하였다. 열분해기는 The Frontier lab 사의 Oy-2020iD의 모델을 사용하였다. 비활성화된 SUS컵에 약 0.5 mg의 리그닌을 투입하고 550℃ 조건에서 열분해하였으며 분해된 가스를 GC/MS에 주입하여 분석하였다. Oven의 온도 조건은 40℃에서 5분의 holding time을 가진 후 310℃까지 10℃/min의 속도로 승온시키고 다시 10분간 동일온도에서 유지하였다. 이동상은 질소를 사용하였으며 flow rate는 0.7 mL/min, 분할비는 1/70으로 설정하여 분석을 실시하였다.
2.2.5 리그닌의 열적특성 분석
2.2.5.1 분획 리그닌의 열중량 분석
분획 리그닌의 열분해거동 및 분해산물의 생성정도를 파악하기 위해서 열중량 분석기(thermogravimetric analyzer, TGA 8000, PerkinElmer)를 이용하여 분석을 실시하였다. 리그닌 1 mg을 20℃/min의 승온속도로 650℃까지 가열하였고 sample gas는 helium을 이용하였다.
2.2.5.2 분획 리그닌의 유리전이온도 분석
분획 리그닌의 유리전이온도(Tg)를 파악하기 위해서 시차주사 분석기(differential scanning calorimetry, DSC Q2000, TA Instrument)를 이용하여 분석을 실시하였다. 첫 스캔 시 리그닌 약 2 mg을 10℃/min의 조건으로 105℃까지 가열하고 20℃까지 동일한 조건으로 냉각하였다. 두 번째 스캔과 세 번째 스캔은 5℃/min의 승온조건으로 180℃까지 가열하였으며 두 번째 스캔에서 생성된 DSC thermogram을 이용하여 Tg를 분석하였다.
3. 결과 및 고찰
3.1 분획 리그닌의 수율 및 분자량 분석 결과
유기용매를 이용한 활엽수 크라프트 리그닌의 분획 결과 F1은 6.15%, F2는 9%, F3은 9.05%, F4는 31.65%, F5는 10.9%로 측정되었으며 최종 미용해분인 FI는 10.9%로 분석되었다. 활엽수 크라프트 리그닌에 대한 분획 리그닌의 전체 수율은 79.3%이다.
유기용매에 의해 분획된 리그닌의 분자량 분포를 확인하기 위해 GPC분석을 실시하였고 그 결과를 Table 1과 Fig. 2에 나타냈다. 크라프트 리그닌의 중량평균분자량(Mw)은 5,680 g/mol, polydispersity index(PDI)는 4.0으로 유기용매 분획분에 비해 상대적으로 넓은 범위의 분자량 분포를 가진 것으로 분석되었다. F1의 Mw는 1,060 g/mol, F5의 Mw는 9,200 g/mol로 측정되었으며 F1에서 F5로 분획이 진행됨에 따라 분자량이 증가하는 경향을 나타냈다. FI는 THF에 용해되지 않아 분자량 측정이 불가능하였으며 크라프트 리그닌 내에 존재하는 소량의 미반응 목분에 의한 영향으로 추정된다. F5를 제외한 분획분의 PDI는 1.1-1.4로 비슷한 경향을 보였으나 F5는 2.3으로 다른 분획 리그닌에 비해서 높게 측정되어 분자량의 분포가 넓다는 것을 확인할 수 있었다. Fig. 2의 분자량 분포곡선을 보면 PDI값과 동일하게 크라프트 리그닌의 분자량이 넓은 범위에 분포하는 것을 확인할 수 있고 상대적으로 분획분의 분자량이 좁은 범위 내에 존재하는 것을 알 수 있다. 따라서 리그닌의 유기용매 분획은 보다 좁은 범위의 분자량 분포를 가진 리그닌을 제조함에 있어 상당히 유용한 방법인 것으로 판단된다.
Table 1.
Molecular weight of kraft lignin and fractionated lignins
| Mn (g/mol) | Mw (g/mol) | PDI |
|---|
| KL | 1,430 | 5,680 | 4.0 |
| F1 | 870 | 1,060 | 1.2 |
| F2 | 1,540 | 1,750 | 1.1 |
| F3 | 1,980 | 2,390 | 1.2 |
| F4 | 2,650 | 3,680 | 1.4 |
| F5 | 3,920 | 9,200 | 2.3 |
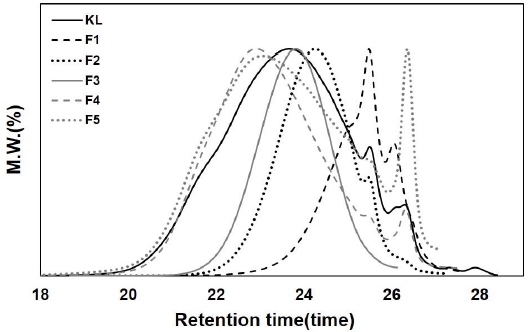
Fig. 2.
Molecular weight distribution curves of kraft lignin and fractionated lignins.
3.2 분획 리그닌의 화학적 특성 분석 결과
3.2.1 분획 리그닌의 주요 작용기 분석
각 분획 리그닌의 phenolic OH group과 aliphatic OH group 함량을 분석하기 위해서 1H-NMR 분석을 실시하였다. methoxyl group에 대한 정량분석 값을 기준으로 하여 4.0-3.5 ppm에서의 methoxyl group 영역의 적분값을 1로 설정하였고 각각 2.4-2.2 ppm, 2.2-1.8 ppm 영역에서의 phenolic OH, aliphatic OH group의 적분값의 비율을 분석하였다. 따라서 methoxyl group과 각 OH group의 함량을 산출하고 Table 2에 나타냈다. 전체적으로 분획 리그닌의 분자량이 감소할수록 methoxyl group과 phenolic OH group의 함량이 높게 나타났는데 이는 크라프트 펄핑으로 인해 β-O-4결합의 파괴가 발생하였기 때문으로 판단되며,21) phenolic OH group 함량이 높은 저분자 분획분이 보다 용해도가 높아 비교적 저극성의 용매에도 쉽게 용출된 것으로 보인다. F1의 methoxyl group 함량은 6.2 mmol/g으로 다른 분획분에 비해 과도하게 높은 값을 나타냈는데 이는 크라프트 펄핑 과정 중에 생성된 methyl mercaptan에 의한 영향으로 판단된다. 크라프트 펄핑 중 리그닌에 대한 SH- 이온의 작용으로 demethoxylation반응이 발생하며 탈리된 methoxyl group은 methyl mercaptan과 같은 황 화합물을 형성하게 된다.23) 본 논문의 Py-GC/MS결과에서도 볼 수 있듯이, F1의 경우 다량의 sulfur compound가 존재하며 이 중 methyl mercaptan과 같은 compound의 methyl기가 methoxyl group 함량 분석에 영향을 주어 다른 분획분에 비해 높은 값을 나타낸 것으로 사료된다. 또한 F1의 phenolic OH group 함량은 methoxyl group 함량의 정량분석 결과와 NMR 스펙트럼 상의 적분값의 비율을 기반으로 산출되었기 때문에 methoxyl group 함량에 비례적으로 높은 값을 나타내었다.
Table 2.
The contents of methoxyl and OH groups of kraft lignin and fractionated lignins
| Methoxyl groups
(mmol/g) | Phenolic OH
(mmol/g) | Aliphatic OH
(mmol/g) | Total OH
(mmol/g) |
|---|
| KL | 1.80 | 1.83 | 0.41 | 2.24 |
| F1 | 6.20 | 6.30 | 0.86 | 7.15 |
| F2 | 2.40 | 2.03 | 0.45 | 2.49 |
| F3 | 2.00 | 2.01 | 0.43 | 2.44 |
| F4 | 1.95 | 1.95 | 0.81 | 2.76 |
| F5 | 1.60 | 1.24 | 0.66 | 1.90 |
3.2.2 분획 리그닌의 FT-IR 분석
Fig. 3은 각 분획 리그닌의 FT-IR분석결과이며 스펙트럼에 대한 분석은 Boerju 등24)과 Lisperguer 등25)의 연구에 기초하였다. 모든 분획 리그닌의 스펙트럼은 유사한 형태를 보였으며 FI 분획분의 스펙트럼만 다른 형태를 나타냈다. 3,400 cm-1 부근의 파장에서 OH기의 피크가 나타났으며 2,900 cm-1 부근의 파장에서 C-H stretching으로부터 유래된 피크를 관찰할 수 있었다. 또한 1,800-1,600 cm-1 범위의 파장에서 carbonyl group의 unconjugated C=O stretching에 기인한 피크가 관찰되었으며, phenolic OH group의 C-O 유래의 피크를 확인할 수 있었다. Methoxyl group의 C-O deformation 피크는 1,030-1,020 cm-1 파장에서 확인할 수 있었으며 830-820 cm-1 파장에서 C-H deformation이 나타났다. FI는 리그닌의 스펙트럼보다 전형적인 셀룰로오스의 스펙트럼과 유사한 형태를 나타냈으며 크라프트 펄핑 후 잔존한 미반응 목분으로 구성되어 있는 것으로 판단된다.
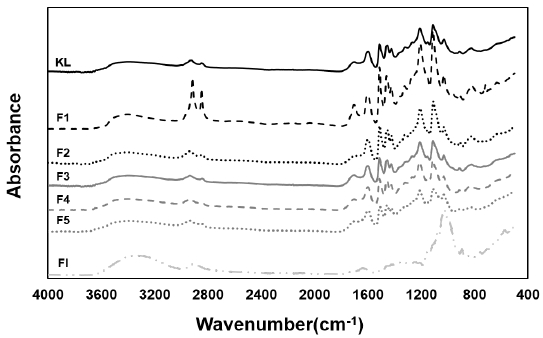
Fig. 3.
FT-IR spectra of kraft lignin and fractionated lignins.
3.2.3 분획 리그닌의 성분 분석
각 분획 리그닌의 열분해산물을 파악하기 위해 Py-GC/MS분석을 실시하였으며 분석결과를 Table 3에 나타냈다. 각 분획 리그닌의 guaiacyl유형 리그닌은 4-methylguaiacol, 4-ethylguaiacol, 4-vinylguaiacol, isoeugenol, vanillin 등이 검출되었으며 syringyl유형 리그닌으로는 3,4-dimethoxyphenol, 4-methylsyringol, 4-vinylsyringol, 4-allylsyringol, 4-propylsyringol, syringylaldehyde, acetosyringone, benzoic acid, 2,6-xylenol 등의 성분이 분석되었다. 전체적으로 syringyl유형 리그닌의 함량이 더 높게 분석되었으며 그 종류도 다양하게 검출되었다. 또한 분획 리그닌의 S/G ratio는 1.41-1.67 범위로 분석되었으며 일정한 경향성은 나타나지 않았다. Park 등22)은 organosolv 리그닌과 milled wood 리그닌 분획분에 대한 Py-GC/MS분석을 통해 S/G ratio를 분석하였으나 Py-GC/MS분석의 무작위적인 열분해 파괴방식으로 인해 일정한 경향성을 얻을 수 없었으며 본 연구의 결과 또한 동일한 원인으로 인해 뚜렷한 경향을 나타내지 않은 것으로 판단된다. F1은 크라프트 펄핑 공정 중에 발생하는 carbon disulfide, sulfur compounds 등이 주요물질로 검출되었다. 또한 FI는 furfural, levoglucosan 등이 주요성분인 것으로 분석되었으며 FT-IR결과와 함께 고려할 때 carbohydrate 기반의 물질들로 구성되어 있는 것으로 판단된다.
Table 3.
Pyrolysis products of kraft lignin and fractionated lignins
| Compounds | Relative distribution of pyrolysis products (%) |
|---|
| KL | F1 | F2 | F3 | F4 | F5 | FI |
|---|
G-lignin
(Guaiacyl) | 4-Methylguaiacol | 6.26 | - | 3.67 | 4.94 | 5.43 | 6.08 | 2.67 |
| 4-Ethylguaiacol | 8.47 | 0.69 | 11.17 | 11.74 | 10.88 | 10.41 | 1.11 |
| 4-Vinylguaiacol | 5.00 | - | 7.26 | 6.65 | 5.55 | 4.88 | - |
| Isoeugenol | 4.90 | 0.37 | 3.39 | 4.47 | 5.16 | 6.78 | - |
| Vanillin | 4.61 | - | 4.24 | 5.27 | 5.72 | 0.82 | - |
| S-lignin (Syringyl) | 3,4-Dimethoxyphenol | 17.65 | 0.45 | 15.90 | 17.21 | 18.66 | 15.71 |
| 4-Methylsyringol | 8.47 | 1.02 | 17.84 | 15.18 | 13.78 | 9.80 | - |
| 4-Vinylsyringol | 5.25 | 0.07 | 5.30 | 5.40 | 7.89 | 6.74 | - |
| 4-Allylsyringol | 2.90 | - | 3.22 | 3.50 | 5.14 | 5.15 | - |
| 4-Propylsyringol | 0.72 | - | 1.22 | 1.20 | 1.18 | 0.97 | - |
| Syringylaldehyde | 0.75 | - | 1.79 | 0.94 | 1.04 | 1.63 | - |
| Acetosyringone | 2.08 | - | 2.38 | 2.40 | 1.82 | 2.21 | - |
| Syringic acid | 0.58 | - | 0.53 | 0.56 | 0.00 | - | - |
| 2,6-Xylenol | 1.19 | - | 3.91 | 2.78 | 2.70 | 1.51 | - |
| CARBONDISULFIDE | - | 10.28 | - | - | - | - | - |
| Hexathiepane (S compound) | - | 2.15 | - | - | - | - | - |
| Sulfur (S8) (S compound) | - | 14.30 | - | - | - | - | - |
| Sulfur (S8) (S compound) | - | 13.18 | - | - | - | - | - |
| Sulfur (S8) (S compound) | - | 11.78 | - | - | - | - | - |
| Sulfur (S8) (S compound) | - | 43.60 | - | - | - | - | - |
| Thiophene,2,5-diphenyl- | - | 1.03 | - | - | - | - | - |
| Furan,2-methyl- | - | - | - | - | - | - | 2.65 |
| Acetic acid | - | - | - | - | - | - | 1.15 |
| Furfural | - | - | - | - | - | - | 72.78 |
| 4-Hydroxy-5,6-dihydro-2H-pyran-2-one | - | - | - | - | - | - | 7.82 |
| Levoglucosan | - | - | - | - | - | - | 11.48 |
| Sum (G type) | 31.18 | 1.07 | 31.16 | 34.48 | 33.69 | 30.99 | 3.79 |
| Sum (S type) | 39.59 | 1.55 | 52.10 | 49.17 | 52.20 | 43.71 | - |
| Total (G+S type) | 70.77 | 2.62 | 83.26 | 83.65 | 85.89 | 74.70 | 3.79 |
| S/G ratio | 1.27 | 1.45 | 1.67 | 1.43 | 1.55 | 1.41 | - |
3.3 분획 리그닌의 열적특성분석
열중량 분석(thermogravimetric analysis, TGA)은 열분해기작과 열안정성을 분석하기 위한 방법으로 널리 사용되고 있으며 리그닌의 열분해 특성은 최근의 리그닌 응용분야 확장에 있어 매우 중요한 특성 중 하나이다. 본 연구에서는 TGA 분석을 통해 유기용매별 분획 리그닌의 열적 특성에 대해 파악하고자 하였으며 TGA 분석 결과를 Table 4와 Fig. 4에 나타냈다.
Table 4.
Char residues, maximum degradation temperature and glass transition temperature of kraft lignin and fractionated lignins
| KL | F1 | F2 | F3 | F4 | F5 | FI |
|---|
| Char residues (%) | 41.3 | 9.7 | 33.1 | 39.2 | 47.6 | 49.8 | 26.7 |
Max. degradation
temp. (℃) | 369.7 | 210.3
367.5 | 390.3 | 370.7 | 388.5 | 412.2 | 232.0
360.4 |
| Glass transition temp. (℃) | 113.06 | 61.60 | 107.40 | 110.67 | 119.58 | 121.67 | - |
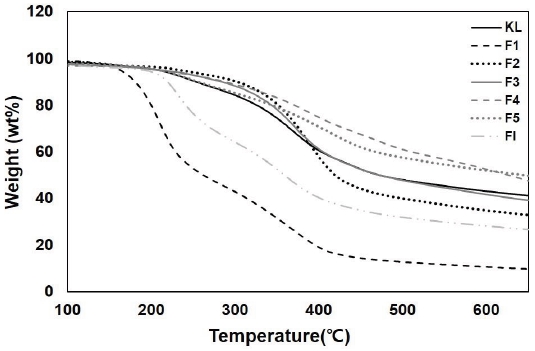
Fig. 4.
TG thermograms of kraft lignin and fractionated lignins.
F1-F5의 char residue는 9.7%, 33.1%, 39.2%, 47.6%, 49.8%로 측정되었고 분자량이 높을수록 열안정성이 우수한 경향을 나타냈다. 또한 F1을 제외한 분획분의 경우 주요 발열성 분해는 250-570℃ 범위에서 발생하는 것으로 분석되었다. Liu 등26)은 이 온도 범위의 열분해가 3단계로 분류할 수 있다고 보고한 바 있는데, 1단계는 270℃까지의 범위에서 phenolic compounds, OH group, alkyl group의 열분해, 2단계는 380℃까지의 범위에서 methoxyl group의 hydrogenation반응에 의한 methanol의 방출단계, 그리고 3단계는 530℃에서의 2차 methane의 형성으로 분류하였다. 본 연구에서도 동일한 범위에서 주요 열분해가 발생하였으며 동일한 기작이 작용한 것으로 판단된다. 또한 Park 등22)에 의하면 리그닌의 작용기와 분자량이 열분해에 대한 주요 영향인자라고 하였으며, Jakab 등27)은 methoxyl group이 다량으로 존재할 경우 리그닌의 char residue가 감소하는 것으로 보고하였다. 본 연구에서 분석한 분획 리그닌의 methoxyl group 함량도 char residue와 반비례하는 것으로 분석되었으며 methoxyl group의 함량이 열안정성에 크게 기여한 것으로 판단된다. 최종 미용해분인 FI의 char residue는 26.7%로 나타났으며 F1과 FI의 초기분해는 다른 용해분에 비해 비교적 낮은 200℃ 부근에서 형성되는 경향을 보였다. F1의 경우 크라프트 펄핑 과정에서 형성된 황 화합물이 초반부에 열분해되면서 변곡점이 형성된 것으로 판단되며28) FI는 미반응 목분에 의한 영향으로 추정된다.
열시차(derivative thermogravimetry, DTG) 분석은 온도변화에 따른 상대적 무게 감소율을 나타내며 분석시료의 최대열분해온도에 대한 확인이 가능하다. 크라프트 리그닌과 각 분획분의 DTG thermogram을 Fig. 5에 나타냈으며 최대열분해온도를 Table 4에 기입하였다. 분획분의 분자량이 증가할수록 최대열분해온도가 증가하는 경향을 보였으며, 전체적으로 370-410℃ 범위에서 최대열분해온도가 형성되었다. Sun 등29)과 Tejado 등30)은 리그닌의 구조에 따라 결합에너지가 다르기 때문에 각각의 구조가 다른 온도범위에서 파괴된다고 보고하였으며 350-425℃ 범위에서 inter-unit 결합의 파괴와 가스상 페놀단량체의 방출이 발생하는 것으로 분석하였다. 본 연구에서도 동일한 온도 범위에서 최대열분해온도가 형성되는 유사한 결과를 얻을 수 있었다. F1과 FI의 최대분해온도는 220℃와 360℃ 부근의 두 영역에서 확인되었다. Sahore 등28)의 연구에 따르면 sulfur류 물질의 최대열분해온도가 200-300℃ 부근에서 형성되었으며 Xu 등31)과 Nowakowski 등32)은 furfural, levoglucosan과 같은 carbohydrate 유래의 물질이 200-300℃ 범위에서 열분해된다고 보고하였다. 본 논문에서 분석한 py-GC/MS 결과를 함께 고려할 때 F1의 최대열분해온도 중 210℃는 크라프트 펄핑 후 리그닌 내에 생성된 황 화합물에 의한 영향으로 판단되며 230℃ 부근에 형성된 FI의 최대열분해온도는 carbohydrate 유래물질의 분해에 의한 것으로 보인다.
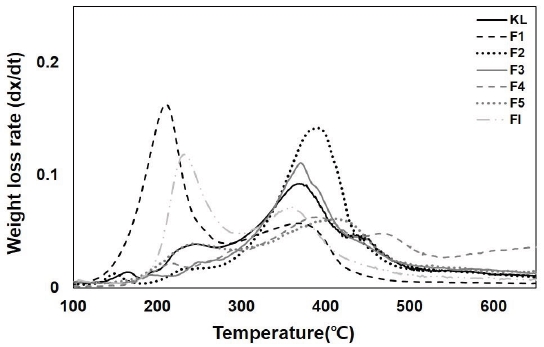
Fig. 5.
DTG thermograms of kraft lignin and fractionated lignins.
시차주사 열랑(differential scanning calorimetry, DSC) 분석 결과를 바탕으로 유리전이온도(Tg)의 분석을 실시하였으며 결과를 Table 4에 나타냈다. 일반적으로 유리전이온도는 화학구조, 분자량, 가교, 결정 영역 등에 의해 영향을 받는데21) 특히 고분자에 있어 분자량은 양말단의 자유부피와 밀접한 관련이 있고 자유부피의 감소는 유리전이온도의 증가를 유발한다.33) 분획 리그닌의 분자량이 증가할수록 유리전이온도도 증가하는 경향을 보였으며, F1의 경우 110-120℃ 범위에서 melting point가 나타났다. Ryu 등34)의 연구에 의하면 sulfur compound의 melting이 100-120℃ 범위에서 발생하는 것으로 보고하였으며 DTG분석결과와 종합적으로 판단할 때 F1은 주로 크라프트 펄핑 중에 생성된 황 화합물을 많이 함유하고 있는 것으로 판단된다.
4. 결 론
본 연구에서는 활엽수 크라프트 리그닌의 효율적 이용을 위해 다양한 유기용매로 분획을 실시하였으며 각 분획 리그닌의 물리·화학적 특성을 평가하고자 하였다.
각 분획 리그닌은 분획 전 크라프트 리그닌에 비해 좁은 분자량 분포를 보였으며 분자량 크기별로 뚜렷하게 구분되었다. 열분해 분석결과, 분획분의 분자량이 높을수록 열안정성이 우수한 것으로 나타났으며 유리전이온도도 증가하는 경향을 나타냈다. 또한 FI를 제외한 모든 분획 리그닌의 FT-IR 스펙트럼은 유사한 경향을 나타냈다. 리그닌의 특징적 작용기인 methoxyl group과 phenolic OH group은 분획분 중 가장 저분자에 해당하는 F1에서 가장 높은 값을 나타냈으며, 분획분의 분자량이 증가할수록 감소하는 경향을 보였다. 모든 분획 리그닌에서 syringyl유형의 리그닌이 guaiacyl유형의 리그닌보다 다량 검출되었으며 F1의 경우 펄핑공정 중에 생성된 sulfur compounds가 주요 구성성분인 것으로 분석되었다. 또한 최종 미용해분인 FI는 carbohydrate 유래의 물질이 주로 검출됨에 따라 펄핑 후 미반응 목분으로 구성되어 있음을 알 수 있었다. 따라서 본 연구를 통해 유기용매를 이용한 리그닌의 분획이 보다 균일한 특성을 가진 리그닌을 생산하는 데 있어 효과적인 방법임을 확인할 수 있었으며, 크라프트 리그닌의 적합한 용도개발을 위한 기반이 될 수 있을 것으로 판단된다.
Acknowledgements
이 연구는 2018년도 정부(교육부)의 재원으로 한국연구재단의 기초연구(No. 2018R1D1A1B07041578) 및 2017년도 강원대학교 전임교원 연구비(관리번호 520170364)를 지원 받아 수행하였음.
Literature Cited
A. Y. Khodakov, W. Chu and P. Fongarland, Chemical Reviews,
Advances in the development of novel cobalt Fischer-Tropsch catalysts for synthesis of long-chain hydrocarbons and clean fuels,
107(5); 1692-1744 (2007)
Khodakov, A. Y., Chu, W., and Fongarland, P., Advances in the development of novel cobalt Fischer-Tropsch catalysts for synthesis of long-chain hydrocarbons and clean fuels, Chemical Reviews 107(5):1692-1744 (2007).
10.1021/cr050972vR. Oukaci, A. H. Singleton and J. G. Goodwin Jr., Applied Catalysis A: General,
Comparison of patented Co F–T catalysts using fixed-bed and slurry bubble column reactors,
186(1-2); 129-144 (1999)
Oukaci, R., Singleton, A. H., and Goodwin Jr., J. G., Comparison of patented Co F–T catalysts using fixed-bed and slurry bubble column reactors, Applied Catalysis A: General 186(1-2):129-144 (1999).
10.1016/s0926-860x(99)00169-6M. E. Dry, Catalysis Today,
The Fischer-Tropsch process: 1950–2000,
71(3-4); 227-241 (2002)
Dry, M. E., The Fischer-Tropsch process: 1950–2000, Catalysis Today 71(3-4):227-241 (2002).
10.1016/s0920-5861(01)00453-9S. Kajitani, Z. L. Chen, M. Konno and K. T. Rhee, Engine performance and exhaust characteristics of direct-injection diesel engine operated with DME (No. 972973), SAE Technical Paper. (1997)
Kajitani, S., Chen, Z. L., Konno, M., and Rhee, K. T., Engine performance and exhaust characteristics of direct-injection diesel engine operated with DME (No. 972973), SAE Technical Paper (1997).
R. Verbeek and J. van der Weide, Global assessment of dimethyl-ether: Comparison with other fuels (No. 971607), SAE Technical Paper. (1997)
Verbeek, R. and van der Weide, J., Global assessment of dimethyl-ether: Comparison with other fuels (No. 971607), SAE Technical Paper (1997).
H. K. Suh, S. W. Park, M. S. Chon and C. S. Lee, Effect of ambient conditions on spray characteristics of DME fuelIn Proceeding of Conference of ILASS-Korea 2005; 41-47 (2005)
Suh, H. K., Park, S. W., Chon, M. S., and Lee, C. S., Effect of ambient conditions on spray characteristics of DME fuel, In Proceeding of Conference of ILASS-Korea 2005, pp. 41-47 (2005).
J. H. Park, H. K. Seo, S. W. Park and C. S. Lee, Spray development process of dimethyl etherIn Spring Conference Proceedings of KSAE; 369-374 (2005)
Park, J. H., Seo, H. K., Park, S. W., and Lee, C. S., Spray development process of dimethyl ether, In Spring Conference Proceedings of KSAE, pp. 369-374 (2005).
J. F. D. Dean, Holzforschung,
Biotechnological modification of lignin structure and composition in forest trees,
46(2); 135-147 (1992)
Dean, J. F. D., Biotechnological modification of lignin structure and composition in forest trees, Holzforschung 46(2):135-147 (1992).
T. Wells and A. J. Ragauskas, Innovative Energy & Research,
On the future of lignin-derived materials, chemicals and energy,
5(2), e117 (2016)
Wells, T. and Ragauskas, A. J., On the future of lignin-derived materials, chemicals and energy, Innovative Energy & Research 5(2): e117 (2016).
A. K. Kumar and S. Sharma, Bioresources and Bioprocessing,
Recent updates on different methods of pretreatment of lignocellulosic feedstocks: A review,
4(1); 7 (2017)
Kumar, A. K. and Sharma, S., Recent updates on different methods of pretreatment of lignocellulosic feedstocks: A review, Bioresources and Bioprocessing 4(1):7 (2017).
10.1186/s40643-017-0137-9B. H. Yoon, S. L. Yoon, L. G. Wang and G. H. Choi, Lignin and Chemistry of Pulp, Chun Cheon. Publishing Department of Kangwon National University. (2017)
Yoon, B. H., Yoon, S. L., Wang, L. G., and Choi, G. H., Lignin and Chemistry of Pulp, Publishing Department of Kangwon National University, Chun Cheon (2017).
S. P. Moon, Utilization of lignin: Past, present, futureIn Proceeding of Fall Conference of Korea TAPPI; 34 (2013)
Moon, S. P., Utilization of lignin: Past, present, future, In Proceeding of Fall Conference of Korea TAPPI, p.34 (2013).
A. W. Bhutto, K. Qureshi, K. Harijan, R. Abro, T. Abbas, A. A. Bazmi, S. Karim and G. Yu, Energy,
Insight into progress in pre-treatment of lignocellulosic biomass,
122; 724-745 (2017)
Bhutto, A. W., Qureshi, K., Harijan, K., Abro, R., Abbas, T., Bazmi, A. A., Karim, S., and Yu, G., Insight into progress in pre-treatment of lignocellulosic biomass, Energy 122:724-745 (2017).
10.1016/j.energy.2017.01.005F. Chen and R. A. Dixon, Nature Biotechnology,
Lignin modification improves fermentable sugar yields for biofuel production,
25(7); 759 (2007)
Chen, F. and Dixon, R. A., Lignin modification improves fermentable sugar yields for biofuel production, Nature Biotechnology 25(7):759 (2007).
10.1038/nbt1316D. W. Goheen, Chemicals from lignin, Organic Chemicals from Biomass; 143-161, CRC Press. (2018)
Goheen, D. W., Chemicals from lignin, Organic Chemicals from Biomass, CRC Press, pp. 143-161 (2018).
Y. S. Kim, O. K. Lee, S. J. Kim, S. S. Lee and S. T. Cho, Preparation of lignin copolymer by atomic-transfer radical polymerizationIn Conference Proceeding of the Korean Wood Science and Technology; 56-57 (2013)
Kim, Y. S., Lee, O. K., Kim, S. J., Lee, S. S., and Cho, S. T., Preparation of lignin copolymer by atomic-transfer radical polymerization. In Conference Proceeding of the Korean Wood Science and Technology, pp. 56-57 (2013).
S. J. Kim and Y. S. Kim, Journal of the Korean Wood Science and Technology,
The analysis of products from base-catalyzed depolymerization of kraft lignin,
41(6); 583-593 (2013)
Kim, S. J. and Kim, Y. S., The analysis of products from base-catalyzed depolymerization of kraft lignin, Journal of the Korean Wood Science and Technology 41(6):583-593 (2013).
10.5658/wood.2013.41.6.583D. K. Seo, J. P. Jeun, H. B. Kim and P. H. Kang, Rev. Adv. Mater. Sci,
Preparation and characterization of the carbon nanofiber mat produced from electrospun PAN/lignin precursors by electron beam irradiation,
28(1); 31-34 (2011)
Seo, D. K., Jeun, J. P., Kim, H. B., and Kang, P. H., Preparation and characterization of the carbon nanofiber mat produced from electrospun PAN/lignin precursors by electron beam irradiation, Rev. Adv. Mater. Sci. 28(1):31-34 (2011).
M. Ö. Seydibeyoğlu, J. Biomed. Biotechnol,
A novel partially biobased PAN-lignin blend as a potential carbon fiber precursor,
(Article ID 598324); 1-8 (2012)
Seydibeyoğlu, M. Ö., A novel partially biobased PAN-lignin blend as a potential carbon fiber precursor, J. Biomed. Biotechnol. (Article ID 598324): 1-8 (2012)
J. H. Seo, J. H. Bae, C. S. Choi, H. W. Lee, H. Jeong and Y. S. Kim, Journal of Korea TAPPI,
Studies on the physical and chemical properties of lignins extracted from various pretreatment methods,
50(5); 5-15 (2018)
Seo, J. H., Bae, J. H., Choi, C. S., Lee, H. W., Jeong, H., and Kim, Y. S., Studies on the physical and chemical properties of lignins extracted from various pretreatment methods, Journal of Korea TAPPI 50(5):5-15 (2018).
10.7584/jktappi.2018.10.50.5.76S. Y. Park, J. Y. Kim, H. J. Youn and J. W. Choi, International Journal of Biological Macromolecules,
Fractionation of lignin macromolecules by sequential organic solvents systems and their characterization for further valuable applications,
106; 793-802 (2018)
Park, S. Y., Kim, J. Y., Youn, H. J., and Choi, J. W., Fractionation of lignin macromolecules by sequential organic solvents systems and their characterization for further valuable applications, International Journal of Biological Macromolecules, 106:793-802 (2018).
10.1016/j.ijbiomac.2017.08.069J. Gierer, Wood Science and Technology,
Chemical aspects of kraft pulping,
14(4); 241-266 (1980)
Gierer, J., Chemical aspects of kraft pulping, Wood Science and Technology 14(4):241-266 (1980).
10.1007/bf00383453C. G. Boeriu, D. Bravo, R. J. Gosselink and J. E. van Dam, Industrial Crops and Products,
Characterisation of structure-dependent functional properties of lignin with infrared spectroscopy,
20(2); 205-218 (2004)
Boeriu, C. G., Bravo, D., Gosselink, R. J., and van Dam, J. E., Characterisation of structure-dependent functional properties of lignin with infrared spectroscopy, Industrial Crops and Products 20(2):205-218 (2004).
10.1016/j.indcrop.2004.04.022J. Lisperguer, P. Perez and S. Urizar, Journal of the Chilean Chemical Society,
Structure and thermal properties of lignins: Characterization by infrared spectroscopy and differential scanning calorimetry,
54(4); 460-463 (2009)
Lisperguer, J., Perez, P., and Urizar, S., Structure and thermal properties of lignins: Characterization by infrared spectroscopy and differential scanning calorimetry, Journal of the Chilean Chemical Society 54(4):460-463 (2009).
10.4067/s0717-97072009000400030Q. Liu, S. Wang, Y. Zheng, Z. Luo and K. Cen, Journal of Analytical and Applied Pyrolysis,
Mechanism study of wood lignin pyrolysis by using TG–FTIR analysis,
82(1); 170-177 (2008)
Liu, Q., Wang, S., Zheng, Y., Luo, Z., and Cen, K., Mechanism study of wood lignin pyrolysis by using TG–FTIR analysis, Journal of Analytical and Applied Pyrolysis 82(1):170-177 (2008).
10.1016/j.jaap.2008.03.007E. Jakab, O. Faix and F. Till, Journal of Analytical and Applied Pyrolysis,
Thermal decomposition of milled wood lignins studied by thermogravimetry/mass spectrometry,
40; 171-186 (1997)
Jakab, E., Faix, O., and Till, F., Thermal decomposition of milled wood lignins studied by thermogravimetry/mass spectrometry, Journal of Analytical and Applied Pyrolysis 40:171-186 (1997).
R. Sahore, L. P. Estevez, A. Ramanujapuram, F. J. DiSalvo and E. P. Giannelis, Journal of Power Sources,
High-rate lithium–sulfur batteries enabled by hierarchical porous carbons synthesized via ice templation,
297; 188-194 (2015)
Sahore, R., Estevez, L. P., Ramanujapuram, A., DiSalvo, F. J., and Giannelis, E. P., High-rate lithium–sulfur batteries enabled by hierarchical porous carbons synthesized via ice templation, Journal of Power Sources 297: 188-194 (2015).
10.1016/j.jpowsour.2015.07.068R. Sun, J. Tomkinson and G. L. Jones, Polymer Degradation and Stability,
Fractional characterization of ash-AQ lignin by successive extraction with organic solvents from oil palm EFB fibre,
68(1); 111-119 (2000)
Sun, R., Tomkinson, J., and Jones, G. L., Fractional characterization of ash-AQ lignin by successive extraction with organic solvents from oil palm EFB fibre, Polymer Degradation and Stability 68(1):111-119 (2000).
10.1016/s0141-3910(99)00174-3A. Tejado, C. Pena, J. Labidi, J. M. Echeverria and I. Mondragon, Bioresource Technology,
Physico-chemical characterization of lignins from different sources for use in phenol–formaldehyde resin synthesis,
98(8); 1655-1663 (2007)
Tejado, A., Pena, C., Labidi, J., Echeverria, J. M., and Mondragon, I., Physico-chemical characterization of lignins from different sources for use in phenol–formaldehyde resin synthesis, Bioresource Technology 98(8):1655-1663 (2007).
10.1016/j.biortech.2006.05.042Z. Xu, W. Li, Z. Du, H. Wu, H. Jameel, H. M. Chang and L. Ma, Bioresource Technology,
Conversion of corn stalk into furfural using a novel heterogeneous strong acid catalyst in γ-valerolactone,
198; 764-771 (2015)
Xu, Z., Li, W., Du, Z., Wu, H., Jameel, H., Chang, H. M., and Ma, L., Conversion of corn stalk into furfural using a novel heterogeneous strong acid catalyst in γ-valerolactone, Bioresource Technology 198:764-771 (2015).
10.1016/j.biortech.2015.09.104D. J. Nowakowski and J. M. Jones, Journal of Analytical and Applied Pyrolysis,
Uncatalysed and potassium-catalysed pyrolysis of the cell-wall constituents of biomass and their model compounds,
83(1); 12-25 (2008)
Nowakowski, D. J. and Jones, J. M., Uncatalysed and potassium-catalysed pyrolysis of the cell-wall constituents of biomass and their model compounds, Journal of Analytical and Applied Pyrolysis 83(1):12-25 (2008).
10.1016/j.jaap.2008.05.007J. D. Menczel and R. B. Prime, Thermal Analysis of Polymers: Fundamentals and Applications, New Jersey. John Wiley & Sons. (2014)
Menczel, J. D. and Prime, R. B., Thermal Analysis of Polymers: Fundamentals and Applications, John Wiley & Sons, New Jersey (2014).
H. Ryu, T. Kim, K. Kim, J. H. Ahn, T. Nam, G. Wang and H. J. Ahn, Journal of Power Sources,
Discharge reaction mechanism of room-temperature sodium–sulfur battery with tetra ethylene glycol dimethyl ether liquid electrolyte,
196(11); 5186-5190 (2011)
Ryu, H., Kim, T., Kim, K., Ahn, J. H., Nam, T., Wang, G., and Ahn, H. J., Discharge reaction mechanism of room-temperature sodium–sulfur battery with tetra ethylene glycol dimethyl ether liquid electrolyte, Journal of Power Sources 196(11):5186-5190 (2011).
10.1016/j.jpowsour.2011.01.109








