1. 서 론
최근 화석연료의 고갈, 온실가스 배출량 감소 등 다양한 이유로 대체에너지 개발에 박차를 가하고 있다. 그 중 휘발유를 대체 할 수 있는 바이오 알코올 보급이 빠르게 확산되고 있으며 바이오에탄올은 단독연료 혹은 휘발유와 혼합하여 자동차 연료로 사용 될 수 있어 대표적인 재생 가능한 대체 에너지로 각광받고 있다.1) 하지만 바이오 에탄올을 생산하는 주원료는 감자, 옥수수, 사탕수수 등 식용작물이 대부분을 차지해 왔으며 그로인해 식량자원과 경쟁을 피할 수 없었다. 이러한 문제 해결을 위해 식용작물이 아닌 목질계 바이오매스를 이용하여 단당을 분리하고 발효하여 바이오 에탄올을 생산한다면 식량 자원으로 바이오 알코올 생산을 할 때 발생하는 윤리적 문제를 해결할 수 있을 뿐 아니라 재료단가를 절감할 수 있다.2)
목질 바이오매스를 당화하는 방법은 산 당화와 효소 당화가 대표적이다. 효소 당화의 경우 목질 바이오매스의 복잡한 구조로 인해 전처리가 필수적이며 효소의 비용이 높지만 단당 이후 2차 반응 산물인 Furan계열 화합물과 유기산의 발생이 없다는 장점이 있다. 산을 이용한 당화에는 진한 산 가수분해와 묽은 산 가수분해로 구분할 수 있다.3) 묽은 산 가수분해의 장점은 적은양의 산을 사용하는 공정이지만 고온, 고압 조건 하에서 진행되는 반응에 적합한 반응기를 제조해야 하고, 또한 묽은 산 가수분해 반응조건에서 단당 생성반응과 당의 분해반응이 경쟁적으로 일어나게 되면서 높은 수율의 단당 생산이 어렵다는 점이다.4) 반면 진한 산 가수분해의 경우 고농도의 산과 저온에서 1차 가수분해 후 희석하여 2차 가수분해를 진행한다. 묽은 산 가수분해에 비해 상대적으로 저온과 저압에서 반응을 진행시키며 황산 회수 후 재사용을 위한 농축필요량이 적다는 장점이 있다. 하지만 공정에 사용한 산의 양이 묽은산 가수분해 공정보다 많기 때문에 공정 이후 중화에 의하여 당화 공정을 진행 시키는 경우 중화에 필요한 염기의 소비가 늘어나면서 전체적인 공정비용이 증가하게 된다.
하지만 최근 전기 투석법 (electrodialysis), Simulated Moving bed(SMB) chromatography와 같은 산을 효과적으로 분리, 회수 할 수 있는 기술이 개발됨에 따라5) 진한 산 가수분해가 묽은 산 가수분해에 비해 가지는 산 회수의 단점을 보완하고 황산 재사용시 필요한 농축량이 적어지면서 오히려 경제적인 장점을 보일 수 있다. 이로인해 진한 산 가수분해를 사용한 다양한 연구가 진행되고 있으며 진한 산 가수분해 반응 중 반응기 내에 어떠한 현상이 일어나는지에 대한 정보를 얻기 위한 동역학적 연구가 필요하다. 묽은 산 가수분해와 달리 산 농도가 높은 경우 HPLC를 이용하기 위한 중화과정 중 발생하는 gypsum에 의해 중화액의 확보가 어렵고, 중화액을 확보하더라도 상당량의 당이 gypsum에 흡착되어 정확한 분석이 어렵다.6) 따라서 본 연구에서는 중화과정이 필요 없는 1H-NMR 분광분석을 통해 진한 산 가수분해를 사용하는 경우 높은 포도당 수율을 얻으며 5-HMF 및 formic acid와 같은 포도당 분해 산물을 최소화하기 위해 가장 적합한 변인을 설정하기 위해 진행되었다.
2. 재료 및 실험방법
2.1 공시재료
Sigma-Aldrich사에서 구입한 AvicelⓇ PH-101을 본 실험에 사용하였다. AvicelⓇ PH-101은 기건상태를 유지하며 함수율을 측정한 후 전건으로 환산하여 사용하였다. 내부 표준물질은 α-L(+) Rhamnose Monohydrate (Wako사, HPLC등급)을 사용하였으며, 반응에 필요한 용매는 D2O (Cambridge Isotope Laboratories사, D 99.9%)와 H2SO4(대정화금, Extra pure 등급)를 사용하였다.
2.2 진한 산 가수분해
산 가수분해를 실시할 때 반응 온도, 황산의 농도, 반응 시간에 따라 산물의 형태가 달라진다. 이에 적절한 진한 산 가수분해 조건을 확인하기 위해 Table 1과 같은 다양한 2차 가수분해 조건에서 실험을 실시하였다. 시료와 72% 황산을 1:1.5의 질량비로 압력튜브에 넣어 항온수조를 이용하여 30℃에서 1시간 동안 1차 가수분해를 진행하였다. 샘플의 액비가 낮아 가수분해 반응 초기에 강한 점성이 생겨 균일한 반응을 기대할 수 없으므로 유리막대를 이용하여 10분 간격으로 교반하였다. 1차 가수분해 후 중수를 사용하여 가수분해 액을 희석하였으며 이 때 중수를 투입하며 유리막대에 붙어있는 황산과 시료를 제거한 후 뚜껑을 닫고 항온수조를 이용하여 2차 가수분해 반응을 진행하였다.
핵자기 공명 분석을 위하여 냉각한 가수분해액에 내부표준물질로 α-L(+) Rhamnose Monohydrate 0.200 g을 용해시켰다. 이 후 가수분해액의 점성을 완화시키고 시료 내 당 조성과 표준물질의 원활한 비교를 위해 D2O를 1.500 mL 첨가한 후 walter crucible holder와 글라스필터(P4, poro. 10~16μm)를 이용하여 가수분해액을 여과하였다.
2.3 1H-NMR (Nuclear Magnetic Resonance) 분석
반응 후 시료 내 당 조성 및 당 분해산물의 조성을 측정하기 위해 핵자기공명 분석을 실시하였다. 여과된 가수분해액에 유리 스포이드를 사용하여 진한 황산을 한 방울씩 떨어뜨려 물의 수소 피크가 아노머성 수소 피크 영역에 영향을 미치지 못하도록 화학이동값을 조정하였다. 각 샘플을 500 MHz 핵자기공명분광기 (Avance 500MHz, Bruker, Germany)를 통해 분석하였다. 분석 조건은 Table 2와 같다.
Table 2.
1H-NMR spectroscopy operation condition
Bruker사의 Topspin프로그램을 이용, 아노머성 수소 피크 영역의 적분을 통해 단당의 조성을 파악하였으며7) 방향족 수소 피크 영역의 적분을 통하여 glucose에서 산 분해된 5-HMF와 formic acid의 수소 피크 영역을 적분하여 포도당의 분해 산물도 정량 분석하였다.8)
3. 결과 및 고찰
3.1 시료 조성 분석
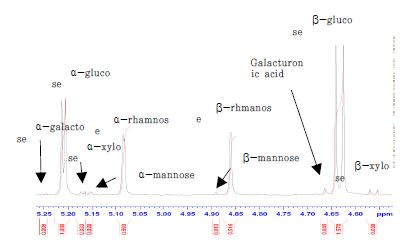
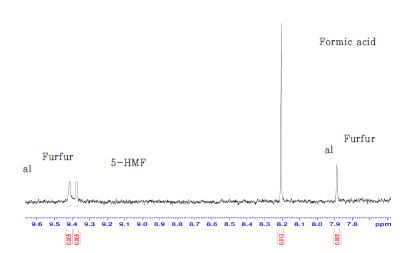
리그닌과 퓨란계 화합물의 합성 반응으로 인해 포도당의 산 가수분해 반응 산물에 대한 정량적 분석이 어렵다.9) 따라서 가수분해 조건에 따른 당화율 및 단당의 분해 산물 정량 분석을 위해서는 리그닌이 존재하지 않는 시료를 사용해야 한다. 이에 적합한 시료인지를 판단하기 위해 AvicelⓇ PH-101을 72% 황산을 이용하여 30℃에서 1시간 1차 가수분해 후 황산 농도를 12%로 희석하였고, 그 후 100℃에서 1시간 동안 2차 가수분해를 실시10) 후 Fig. 1과 Fig. 2의 수소 영역 피크를 적분하여 시료의 조성을 분석하였다(Table 3). 단당에 존재하는 수소중 아노머성 수소는 다른 수소와 달리 특이한 화학이동값을 가질 뿐만 아니라 단당 별로 상이한 화학이동값을 갖기 때문에 단당조성 분석에 아노머성 수소 피크의 면적으로 추정할 수 있다. 방향족 수소는 화학이동값이 7.8-9.4 ppm 범위에 존재하며 당 분해 산물중 furan계 화합물은 방향족 수소 영역에서 화학이동값을 갖는다. Furan계 화합물뿐만 아니라 5-HMF (5-hydroxymethylfurfural)의 분해에 의해서 만들어지는 formic acid도 이 영역에서 화학이동값을 갖는다. 방향족 수소 영역에서 피크 해석을 통하여 단당에서 전환된 furan계 화합물과 furan계 화합물의 분해 산물인 formic acid의 정량적 분석도 가능하다.
Fig. 1과 Fig. 2의 피크 해석을 바탕으로 시료 조성을 분석한 결과 주성분은 셀룰로오스이고 헤미셀룰로오스 오염에 의한 xylan과 glucomannan계 성분도 5.7% 존재하였으며 단당의 분해 산물인 furan계 화합물과 그 분해산물도 5.4% 검출되었다. 정량 분석 결과 리그닌은 존재하지 않는 것으로 판단되었다.
3.2 조건 별 진한 산 가수분해 산물 변화 분석
셀룰로오스는 산 촉매 하에서 단당인 glucose로 분해된다. 하지만 강한 산성 조건에서 단당류가 안정적인 최종 산물이 아니기 때문에 산에 의한 탈수 반응으로 인해 5-HMF나 furfural과 같은 형태로 전환되며 이러한 aldehyde 형태의 산물 역시 불안정한 상태이기 때문에 formic acid과 같은 형태로 최종 산물을 생산하게 된다.9)
본 실험 조건에서는 단당에서 furan계로의 분해 반응 보다는 다당에서 단당으로의 반응이 더 진행되기 때문에 조건의 변화에 따라 단당의 수율이 증가하였다.
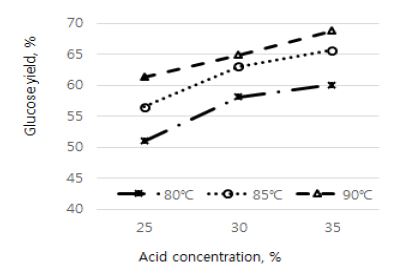
하지만 Fig. 3에서와 같이 당화율이 70%에도 미치지 못한 이유는 진한 산 가수분해가 공정에서 사용될 때와 달리 2차 가수분해 실험 중 가수분해액에 충분한 교반이 가해지지 않아 2차 가수분해가 균일하게 일어나지 않은 것이 영향을 끼쳤을 것으로 생각된다.
또한 시료의 재료적 특성상 진한 산 가수분해 반응 시 셀룰로오스의 나노파티클화가 일어나게 된다. 셀룰로오스의 나노파티클화는 80℃, 50% 황산 농도, 30 min 조건에서 최대 62% 수율까지 생성된다. 나노셀룰로오스 수율은 반응시작 후 꾸준히 증가하다 일정해지고 이후 일부 감소하는 경향을 보이는데 90℃, 50% 황산 농도로 25분 이상의 반응시간부터 감소경향을 보인다. 이는 반응시간이 늘어남에 따라 당으로 가수분해 되는 양이 증가하기 때문이다.11) 본 실험의 2차 가수분해에서도 진한 산과 고온 반응으로 인해 나노셀룰로오스가 생성되어 단당으로의 충분한 분해가 이루어지지 않아 수율이 감소한 것으로 판단된다. 추가적인 실험을 통해 이 과정에서 생성 된 나노셀룰로오스의 양과 분해되지 못한 당량의 분석이 필요하다.
특이한 사항으로는 상대적으로 가혹한 반응일수록 일반적으로 목질계 바이오매스에서 나타나지 않는 형태의 아노머성 수소가 관찰되었다(Fig. 4와 Fig. 5 참조). 미지 피크의 발생은 glucose의 산 촉매 하 이성질화 반응에 의한 것으로 추정된다.12) 더 강한 조건에서의 추가 실험을 할 경우 미지 아노머성 수소의 양이 더욱더 증가할 것으로 예상되기 때문에 이에 대한 추가적인 확인이 필요하다.
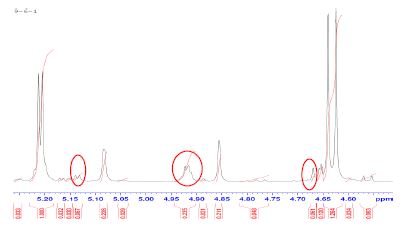
Fig. 4.
Unknown anomeric peaks of Avicel cellulose concentrated acid hydrolysis (90℃, 35%, 60min conditions).
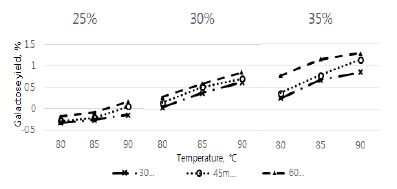
또한 실험 조건에 따라 galactose 함량이 변화하였다. 시료 내 당 조성 분석과 비교하여 galactose 함량 변화를 Fig. 6에 나타내었다. 실험 조건 중 상대적으로 낮은 농도에서의 반응에서는 시료의 당 조성 분석에 비해 적은 양의 galactose가 검출되었는데 이는 반응 조건이 충분치 않아 시료 내 다당의 분해가 충분하지 않은 것으로 생각된다. 반면 실험 조건 중 상대적인 고농도, 고온에서 반응시간이 길어질수록 galactose 함량이 증가하였는데 이는 시료 내 다당의 분해에 의한 galactose의 함량 외 가수분해 된 glucose의 산 촉매 하 이성질화 반응에 의한 것으로 추정 된다.12)
3.3 변인에 따른 당 분해 산물 수율 분석
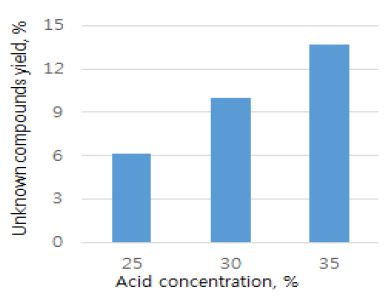
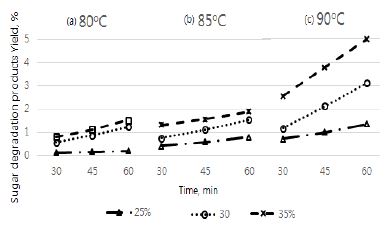
2차 가수분해 조건이 가혹해짐에 따라 furfural, 5-HMF 및 formic acid와 같은 단당 분해 산물의 양이 꾸준하게 증가하는 것을 확인할 수 있다. Fig. 7에 나타난 것과 같이 당 분해산물은 80℃와 85℃에서도 꾸준히 증가했지만 다른 변인 증가에 따라 수율의 증가가 눈에 띄게 높아지는 부분은 보이지 않았다. 하지만 90℃에서는 다른 변인이 강해짐에 따라 당 분해산물의 수율이 급격하게 증가하였다.
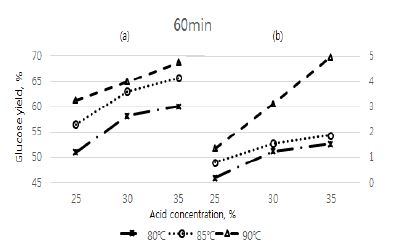
가장 가혹한 조건에서의 당화율과 당 분해산물 수율 경향을 비교하였을 때(Fig. 8) 당화율은 다른 조건에서의 증가율보다 낮은 증가율을 보이는 반면 당 분해산물 수율의 증가량은 급속히 증가하는 것을 보아 90℃ 조건부터 당의 분해반응이 단당으로의 전환반응과 경쟁적으로 일어나기 시작하는 것을 확인할 수 있었다.
4. 결 론
본 연구에서는 1H-NMR 분석을 이용하여 진한 산 가수분해에서의 당화율 및 당분해산물 수율을 분석하였으며 얻어진 결과는 다음과 같다.
1. 산 당화액의 분석 방법 중 중화액을 분석하는 GC, HPLC 분석법에서 황산칼슘에 당화액이 흡착하여 정량적인 분석에 어려움이 있었지만 본 연구에서 사용한 1H-NMR 분광분석으로 정량적 분석이 가능하였다. 특히 2차 가수분해에서 상대적으로 고농도의 산을 사용하는 공정의 분석에 1H-NMR 분광분석이 적합하다.
2. 정량 분석 결과 본 연구 조건에서 산의 농도가 높을수록, 반응 온도가 높을수록, 반응시간이 더 길수록 셀룰로오스에서 포도당으로 전환율이 높았다. 셀룰로오스의 일부는 나노휘스커 형태로 잔류 하였으며, 일부의 glucose은 galactose로 이성질화 반응이나 확인 불가능한 물질로 전환되었다. 단당에서 furan계 화합물을 거쳐 유기산으로의 분해도 관찰되었다.