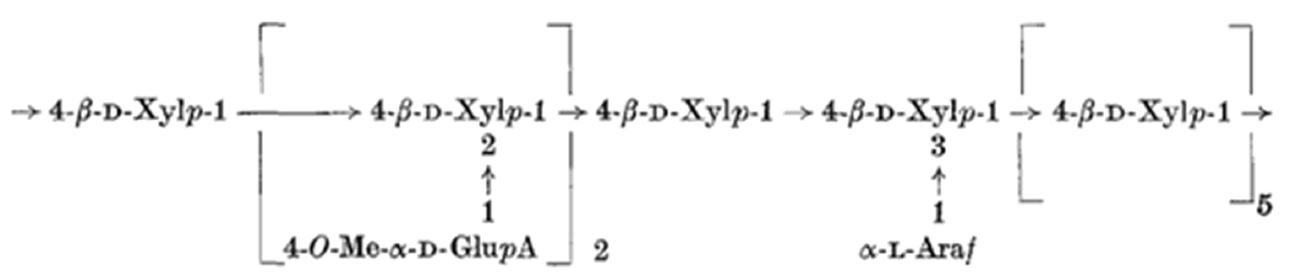1. 서 론
우리나라 소나무는 성장하는 지역의 기후와 지형에 따라 소나무 형상을 여섯 가지로 구분하여 사용해 왔다.1) 그중에서도 금강송은 태백산맥줄기를 타고 금강산에서 영덕, 청송 일부에 자라는 소나무를 말한다. 금강송은 다른 소나무와는 달리 수간이 매우 곧고, 수피는 비교적 얇다고 보고되고 있고, 이러한 금강송은 분포지역과 외형에 따라 미인송, 춘양목, 황장목 등으로 불린다.2)
금강송은 조선왕조실록에서 그 쓰임을 알 수 있다. 실록에서는 재궁 또는 재판 판곽 등을 만들 때에는 황장목(금강송)을 사용하였다고 기록되어 있다. 이러한 용도로 사용되는 금강송은 적황색을 띄는 심재부가 크게 발달하고 연륜 폭이 매우 조밀한 최소 수령이 100년 이상되는 소나무이다.3) 또한 수형이 통직하고 수피가 붉은 색을 띄고 있다. 때문에 조선시대에는 금강송을 왕실의 재궁용으로 사용하였고, 동시에 궁궐, 사찰 등 건축용으로 사용하는 중요 자원으로 지정하였다. 이러한 이유로 현재 금강송은 문화재 보수와 같은 특수용도로 사용되어 왔지만 자원부족으로 공급이 거의 중단되었다.4,5)
금강송의 해부학적 특성에 관한 이전 연구 내용을 살펴보면 금강송의 수피는 붉은 암회색이며, 적송과 달리 심재와 변재의 차이가 뚜렷하게 나타났다. 또한 연륜 폭이 좁고, 만재율은 적송에 비해 높은 것으로 나타났고, 가도관의 길이는 수심부에서 수피부로 향할수록 길어지는 경향이 있다고 보고되었다.6) 금강송의 재질발현 수령 판단 기준에 대한 수지구와 방사조직의 출현 형태에 관해 연구된 Kim 등7)의 연구에서는 방사조직의 경우 적송과 뚜렷한 차이가 나지 않으며 방사조직의 분포수가 연륜이 증가함에 따라 감소한다고 보고 하였다.
그 외 물리학적 특성 연구에서는 금강송과 일반 소나무의 강도를 비교했을 때 종 압축강도는 금강송이 다소 낮지만 휨강도는 더 높게 나타났고, 이러한 강도에 영향을 주는 요인은 연륜 폭보다는 비중에 의한 영향이 크다고 보고되었다.8)
국내산 일반 소나무와 금강송의 상이성에 대한 대부분 연구는 구조적, 물리적 특성 분석에 제한되어져 왔으며, 화학적 특성 분석에 대한 연구는 거의 이루어진 바 없다. 따라서 본 연구에서는 금강송과 적송의 차이를 화학적 분석을 통해 확인하고자 하였으며, 특히 헤미셀룰로오스 분석을 통해 그 차이를 확인하고자 하였다.
2. 재료 및 방법
2.1 공시 재료
본 연구에 사용한 재료는 제천시 백운면 덕동리에서 벌목한 적송과 강원도 삼척에서 벌목한 금강송을 공시재료로 사용하였다. 적송과 금강송을 미분쇄기(MF 10B, IKA, Germany)를 사용하여 분쇄 후 1.0 mm 망을 통과한 샘플을 사용하였다.
2.2 실험 방법
2.2.1 화학조성 분석
2.2.1.1 아세톤 추출
소나무 내 소수성 추출물 함량을 측정하기 위하여 아세톤 추출을 진행하였다(Tappi 204 om-88). 목분 2.0 g을 100 mL 비커에 정량하여 넣은 후 아세톤 50 mL을 넣어 아세톤 추출을 실시하였다. 실온에서 7시간 방치 후 여과하여 소수성 추출물 함량을 측정하였다.
2.2.1.2 끓는물 추출
친수성 추출물 함량을 측정하기 위해 열수 추출물 함량 측정을 실시하였다(Tappi 207 om-93). 소수성 추출물이 제거된 목분 2.0 g을 250 mL 삼각플라스크에 넣은 후 증류수 150 mL을 첨가하여 1시간 끓인 후 여과하여 친수성 추출물 함량을 측정하였다.
2.2.1.3 리그닌 정량
산 불용성 리그닌 분석은 Tappi 222 om-88에 의거하여 진행하였다. 추출물이 제거된 목분 0.275 g를 100 mL 비커에 정량 후 72% 황산 4.5 mL를 첨가하여 30℃ 1시간 가수분해 하였다. 가수분해 후 증류수 145 mL를 첨가하여 250 mL 삼각플라스크에 옮겨 담은 후 120℃ 1시간 2차 가수분해 하였다. 가수분해 종료 후 12시간 실온에 방치 후 글라스필터로 여과하여 산 불용성 리그닌을 정량하였다. 산 가용성 리그닌은 Tappi useful method UM 250에 의거하여 산 불용성 리그닌 여과 후 남은 여과액을 UV-spectrometer로 205 nm에서의 흡광도를 측정하여 정량하였다.
2.2.2 1H-NMR 분석
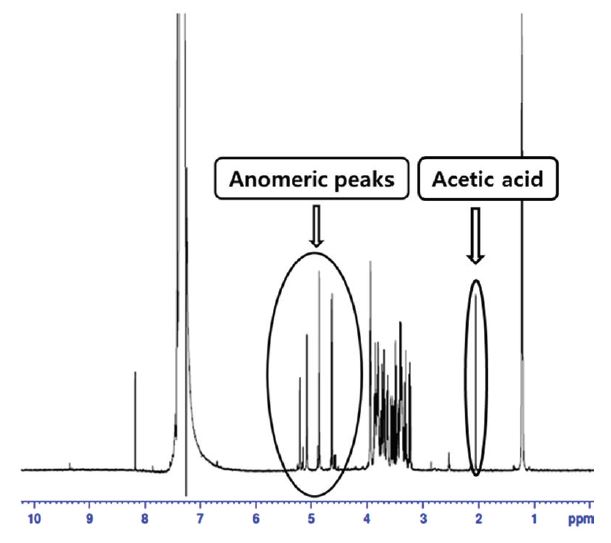
적송과 금강송의 헤미셀룰로오스 및 아세트산을 확인하기 위해 1H-NMR 분석을 실시하였다. 시료에 72% 황산을 이용하여 30℃에서 한 시간 동안 1차 가수분해 후, 중수(D2O)를 넣어 희석한 후 100℃에서 한 시간 동안 2차 가수분해를 실시하였다. 가수분해 후 여과과정을 거쳐 얻은 여과액을 모아 nuclear magnetic resonance spectrometer(Avance 500 MHz, Bruker, Germany)기기를 이용하여 분석하였다
1H-NMR 분석으로 얻어진 스펙트럼은 각각 아세트산 피크와 아노머성 수소 피크를 확인하고 적분하여 적송과 금강송의 탄수화물 구조를 확인하였다.
3. 결과 및 고찰
3.1 금강송과 적송의 화학조성 비교
금강송과 적송을 변재와 심재로 구분하여 화학 조성 분석을 실시한 결과 추출물 비율이 적송에 비해 금강송이 높은 것이 확인되었다. 특히 끓는 물 추출물의 양은 큰 차이를 보이지 않았지만, 아세톤 추출물은 금강송이 적송에 비해 더 높은 비율을 차지하고 있는 것으로 확인 되었다. 금강송의 유기용매 추출물이 적송에 비해 높게 나타난 이유는 금강송의 단위면적당 수직 수지구 분포가 소나무에 비해 40% 더 많이 존재하고 있기 때문으로 판단된다.7)
일반적으로 소나무의 리그닌은 25-35%가 존재한다. 금강송 변재, 심재의 리그닌비율은 25.1%, 25.7%로 일반적인 소나무 리그닌과 비슷하고, 변재와 심재의 차이는 적다. 하지만 적송의 경우 변재의 리그닌 비율은 21.8, 심재의 리그닌 비율은 26.2로 근 차이를 보이고 변재의 경우 일반적인 소나무 리그닌비율보다 적게 나타났다.
금강송의 적송의 리그닌 비율은 21.8-26.2%로 일반적으로 존재하는 침엽수의 리그닌 비율(25-35%)와 비교했을 때 리그닌의 비율이 낮은 것을 확인하였다. 특히 금강송의 경우 변재에서 리그닌 비율이 21.8%로 매우 적은 것이 확인 되었다. 금강송의 리그닌량은 변재와 심재사이에 큰 차이가 확인되지 않았다. 하지만 적송의 경우 변재와 심재의 차이가 4.4%로 변재가 심재에 비해 낮은 리그닌 함량을 보였다. Lodgepole pine의 심변재 리그닌 함량 분석에서 latifolia 변종에서는 변재(26.02%)가 심재(25.77%) 보다 높았지만 murrayana 변종에서는 심재(26.13%)가 변재(25.71%)보다 높았다.9) 독일 가문비나무 변재와 심재 및 변재에서 심재로 이행부의 리그닌 함량 분석 결과 Klason 리그닌을 기준으로 변재는 27.7%, 이행부는 27.3%, 심재에서는 28.3%의 함량을 보여 심재에 더 많은 리그닌이 존재하였다.10) Marine pine에서는 전체 총량 분석에서는 변재내 리그닌이 24.5%로 심재(23.1%)보다 더 많이 존재하지만 추출물 제거 후를 기준으로 하면 심재가 28.7%의 리그닌을 함유하여 변재(26.7%)보다 더 많은 리그닌을 함유하였다.11)
3.2 핵자기 공명을 이용한 헤미셀룰로오스 분석
목재의 헤미셀룰로오스는 주로 글루코만난계열과 자일란계열의 헤미셀룰로오스가 존재하고 곁사슬에 붙는 분자에 따라 이름이 조금씩 달라진다. 침엽수를 구성하는 헤미셀룰로오스는 글루코만난계열이 주로 존재하며 곁사슬로 갈락토스가 붙기도 한다. 그 외 자일란은 아라비노글루쿠로노자일란형태로 존재하며, 곁사슬로 아라비노스와 4-O-methylglucutonic acid가 붙어있는 형태이다.
헤미셀룰로오스는 일반적으로 염기용액(24% 수산화칼륨)으로 추출한 후 초산을 함유한 에탄올로 중화시켜면 침전이 된다. 이렇게 추출된 헤미셀룰로오스에는 아세틸기가 염기에 의하여 추출과정에서 제거가 되며 아세틸기가 붙어 있는 헤미셀룰로오스를 추출하기 위해서는 아염소산법으로 제조한 holocellulose를 dimethylsulfoxide(DMSO)용매로 추출해야 한다. 이런 분석 방법은 분석에 필요한 실험단계가 많고 분석 시간이 길 뿐만 아니라 각 실험 단계에 따른 비용이 크다. 때문에 간편하게 헤미셀룰로오스의 구조를 확인할 수 있는 방법이 필요하다.
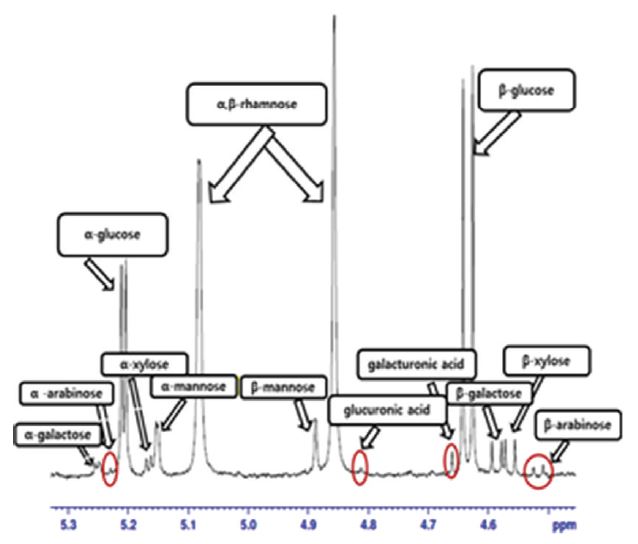
추출된 용매를 수산기를 치환 시킨 후 산 가수분해하여 단당으로 전환 시킨 후 가스크로마토그래피 분석을 위하여 다시 치환 시킨 후 분석을 실시하여 헤미셀룰로오스 구조를 추정하였다. 또 따른 분석 방법을 헤미셀룰로오스를 효소를 사용하여 올리고당 정도로 분해시킨 후 분해산물을 전기영동 분리 분석이나 핵자기 공명 분광법으로 분석하는 방법이 도입되었다(Figs. 1과 2).
3.3 적송과 금강송의 헤미셀룰로오스 구조 차이
침엽수의 자일란은 Fig. 3처럼 자일로스가 주 사슬을 이루고 있고 곁사슬로 4-O-methyl-glucuronic acid가 자일로스 10개당 2개가 존재하고, 아라비노스가 자일로스 10개당 1.3개 존재한다.
일반적으로 침엽수의 아라비노글루쿠로노자일란의 아라 비노스와 자일로스는 1:7로 존재한다. 하지만 1HNMR분석결과 금강송과 적송의 심재에서는 1:4로 존재하는 것으로 확인 되었다.
Glucuronic acid는 일반적으로 침엽수의 자일란 10개당 2개가 곁사슬로 존재한다. 금강송의 경우 glucuronic acid와 자일로스의 비율이 1:4.4로 존재하는 반면 적송은 변재의 경우 1:6.6, 심재는 1.2:4로 존재한다. 금강송과 적송 심재의 경우 일반적인 침엽수 자일란의 glucuronic acid와 자일로스 비율을 보였지만, 적송 변재의 경우 일반적인 침엽수에 비해 glucuronic acid가 다른 비율로 존재하는 것이 확인 되었다. 적송과 금강송의 glucuronic acid 함량은 거의 동일하지만 적송 변재의 경우 적송 심재와 금강송보다 자일로스 함량이 1.8-2.6% 차이로 적송 변재가 더 높게 확인 되었다.
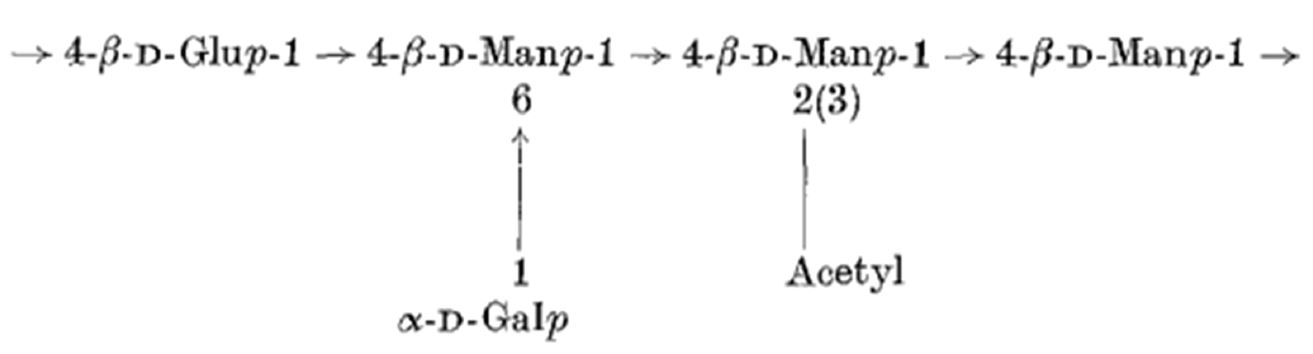
침엽수의 헤미셀룰로오스 주성분은 (갈락토)글루코만난계열이다. (갈락토)글루코만난의 주 사슬은 글루코스와 만노스로 구성되어 있고 곁사슬로 갈락토스와 아세틸기가 존재한다(Fig. 4). 갈락토스 함량이 상대적으로 높은 것은 갈락토글루코만난이라 부르며 Fig 4의 구조와 같이 갈락토스:글루코스:만노스 비율이 1:1:3으로 존재하고, 아세틸기의 경우 6탄당 10개당 3-4개가 존재한다. 갈락토스 함량이 상대적으로 낮은 것은 글루코만난이라 부르며 갈락토스:글루코스:만노스의 상대적 비율이 0.1:1:4로 보고되었다.
금강송과 적송의 심재와 변재 단당 분석 결과 Table 3에서와 같이 금강송의 변재와 심재는 글루코만난이 주로 존재하지만 적송의 경우 변재에서는 갈락토글루코만난이 존재하고 심재에는 갈락토스 함량이 적은 글루코만난이 존재 하는 것으로 생각된다. 포도당은 글루코만난 뿐만 아니라 셀룰로오스를 구성하는 단당이기 때문에 Table 3에서 상대적 조성의 계산에서 제외하였다.
4. 결 론
목재의 헤미셀룰로오스를 분석하는 방법으로는 일반적으로 헤미셀룰로오스를 추출하여 분석을 하는 것이다. 하지만 이러한 방법은 시간이 오래걸리기 때문에 본 연구에서는 산 가수분해를 후 핵자기 공명 분광분석을 통해 헤미셀룰로오스의 구조를 추정하는 방법을 사용하였다. 이 방법을 적송과 금강송에 적용하여 두 재료의 헤미셀룰로오스의 차이를 확인하였다. 적송과 금상송의 헤미셀룰로오스 중 아라비노글루쿠로노자일란의 경우 적송의 변재가 자일로스의 비율이 높은 것을 확인하였다. 또한 글루코만난의 경우 적송의 변재에서 갈락토스가 존재하는 갈락토글루코만난의 형태로 존재하는 것으로 판단된다. 적송과 금강송을 핵자기 공명 분광분석을 이용한 헤미셀룰로오스 분석법을 적용 했을 때 헤미셀룰로오스의 구조를 추정할 수 있을 뿐만 아니라 두 재료를 분별하는데 사용될 수 있을 것으로 생각된다.