1. 서 론
20세기형 ‘대량생산·대량소비’라는 경제 패러다임으로 인류는 지난 세기 동안 풍부한 화석연료를 이용하여 분리·정제 기술 진보로 인하여 풍족한 경제 소비 활동을 영위해왔다. 하지만, 이에 따른 부작용으로 지구온난화 및 기후변화라는 극심한 상황에 처해 있다. 이러한 기존의 화석연료를 기반으로 하는 20세기형 경제 개념의 한계를 극복하기 위해, 석유화석자원 대신에 기술 선진국에서는 새로운 경제 개념인 바이오 경제(Bio-based economy) 혹은 나아가 순환바이오경제(Circular BioEconomy) 개념 도입으로 바이오 자원에서 화학제품, 각종 소재 및 운송연료, 전력 및 열 생산을 목표로 광범위한 투자가 이루어지고 있다.1)
4차 산업 패러다임의 전환의 일환으로, 현재 선진국에서는 목재 및 초본류 등의 바이오 자원을 분리·정제하여 바이오 연료(bio-energy) 혹은 석유화학산업유래의 부재(bulk)·소재(fine chemicals)를 대체할 수 있는 원료로 사용하여 그 부가가치성(valorization)을 높이는 데 국가의 역량을 집중하고 있다.2)
세포벽에 존재하고 있는 다양한 형태의 셀룰로오스, 헤미셀룰로오스 및 리그닌 등의 천연 고분자 물질을 그 쓰임에 따라 경제적 혹은 산업적으로 용이하게 단량체(building block) 혹은 전구물질(platform molecular)로의 재조합(de-construction) 혹은 분리(fractionation) 변환하는 기술 개발이 그 핵심이라 볼 수 있다.3)
현재 이용되고 있는 식물세포벽 내의 바이오 고분자(셀룰로오스, 헤미셀룰로오스, 리그닌) 분리 변환기술은 기존의 펄프·제지산업에서 사용되고 있는 기술을 변형하여 약산(dilute acid), 알칼리(alkaline), 유기용제(organosolv), 이온성 용매(ionic liquid) 등의 조합으로 다양한 초본류 및 목재 등의 바이오 자원에 적용되고 있다. 하지만, 초본류 및 목질계 바이오 자원은 1·2차 대사합성의 산물인 리그닌이 셀룰로오스와 헤미셀룰로오스를 단단하게 감싸 안은 구조로 형성되어 있어, 선택적인 분리·제거가 어렵기 때문에 효율적으로 리그닌을 분리·제거하기 위한 다양한 전처리 기술이 개발되고 있다.4-7) 이러한 전처리 기술 중 글리콜 에테르 용매와 산 촉매를 이용하여 마이크로파 처리에 의한 목질 바이오 매스 자원의 전처리 기술로 많은 적용 가능성이 있다고 판단된다.8)
본 연구에서는 마이크로파 처리를 통해 침·활엽수 바이오매스를 제조하고, 처리조건에 따른 바이오매스의 특성 및 이를 통해 얻어진 미세 잔류물의 용해용제에 대한 용해성 차이를 비교하였다.
2. 재료 및 방법
2.1 공시재료 및 시약
2.1.1 공시재료
본 연구에서는 함수율이 9.1%인 국내산 소나무(Pinus densiflora)와 함수율이 5.5%인 유칼립투스(Eucalyptus globulus) 목편을 실험실용 햄머밀을 이용하여 분말화하여 사용하였다. 분말화한 시료는 40-60 mesh로 분급하여 에탄올-벤젠 혼합용액(1:2, v/v)으로 24시간 동안 추출하여 탈지 목분을 제조하였다.
2.1.2 시약
본 연구에서 사용된 반응시약은 용매 중 끊는 점이 약 197°C인 glycol ether 용매(pure grade, Sigma Aldrich Co., USA)를 사용하였고,9) 촉매로는 순도 95%인 황산(extra pure grade, Daejung Chemicals & Metals, Korea)를 사용하였다.
2.2 실험방법
2.2.1 화학적 분산
40-60 mesh의 탈지목분 시료의 화학적 분산은 이전의 연구8)에서 소개한 방법을 개조하여 실험을 진행하였다. 5 g의 시료에 glycol ether와 황산 혼합시약을 1:2 (w/v)로 투입하였다. 사용된 혼합시약은 glycol ether 용매에 대하여 0.5-3.0%(v/v)로 촉매인 황산을 첨가하여 제조하였다. 미세화 반응은 400 W로 조절된 마이크로파 오븐(SE-MW 50018, Sun Enterprise, Korea)으로 Table 1의 실험조건에 따라 60초, 120초, 180초 동안 진행하였다. 마이크로파 조사 시 10초 간격으로 반응시료를 꺼내어 Vortex mixer(G-560, Scientific Industries Inc., USA)를 사용하여 충분한 전단력 하에서 1분간 교반시켰다. 반응 종료 후 0.5 N NaOH 수용액 200 mL를 사용하여 감압 하에서 세척을 한 후, 여과물이 중성이 될 때까지 증류수로 세척을 실시하였다. 여과 후에 생성된 잔류물은 105±3°C의 건조 오븐에서 24시간 이상 건조하였다.
2.2.2 분석
화학적 분산 반응 전후의 잔류물의 중량을 측정하여 수율을 계산하였다. Klason lignin은 TAPPI T 222 om-02에 의거하여 측정하였다. 또한, 잔류물의 조성당 분석은 alditol-acetate법에 의해 전처리된 시료를 2 mL의 아세톤에 용해시킨 후, GC 분석을 통해 실시하였으며, 분석조건은 Table 2와 같다.
Table 2.
GC condition for neutral sugar analysis
잔류물의 용해도를 평가하기 위해 cupriethylenediamine(CED)(Sigma Aldrich Co., USA) 및 NaOH/Urea 수용액을 사용하였다. CED 용해 용제의 경우는 제조된 시료를 0.5%의 농도로 분산시킨 후, 90분간 상온에서 교반하였다. 반응이 끝난 용액을 감압 여과하고, 불용해 잔사는 증류수로 중성이 될 때까지 세척하였다. 중성이 된 불용해 잔사는 105±3°C에서 8시간 동안 건조하였다. 또한, 제조된 시료를 7% wt NaOH/12% wt Urea/81% wt H2O로 이뤄진 용해 용제에 0.5%의 농도로 분산시켰다. 분산된 용액을 -20±5°C에서 약 12시간 냉동 후, freezing-thawing 상온에서 voltex mixer(G-560, Scientific Industries Inc.)를 이용해 5분간 교반 하면서 반응시켰다. 이 과정을 4회 반복하며 용해를 진행하였다. 원심분리기를 이용하여 10분 동안 10,000 rpm으로 원심분리한 후, 상등액을 분리하였다. 용해되지 않은 잔류물은 용해 용제로 3번 세척 후, 증류수로 중성이 될 때까지 세척해주었다. 세척이 끝난 잔류물은 45°C에서 48시간 동안 진공 건조를 진행하였다. 용해율은 전건시료 대비 잔류물의 잔존량을 역산하여 측정하였다. X-선 회절분석기(D/Max-2500, Rigaku)를 이용하여 획득한 자료를 Segal법10)에 의거하여 결정화도를 계산하였다.
3. 결과 및 고찰
3.1 마이크로파 화학분산 처리 후 잔류물의 수율과 리그닌 함량
이전의 연구 결과8)에 의하면, 마이크로파 화학적 분산 반응 조건이 가혹한 경우(120초 반응시간, 2.5% 촉매 이상 실험조건) 탄화로 추정되는 입자가 발생되었고 또한 72%의 황산에도 분해되지 않아 Klason 리그닌의 정량이 불가능하다고 보고되었다. 이에 본 실험에서는 마이크로파 조사 시 반응용기내의 급격한 온도상승을 방지함으로써 탄화가 발생하지 않도록, 기존의 연구8)에서는 20초간 마이크로파 조사 반응 후 꺼내어 20초간 교반을 행한 것에 반하여, 10초간 마이크로파 반응 후 1분간 충분한 교반이 이루어짐으로써 반응액과 시료가 지엽적으로 탄화가 일어나지 않도록 조절하였다. 또한 120초 혹은 180초의 경우 반응 중 탄화가 일어나지 않도록 촉매의 사용량을 Table 1에서 보는 바와 같이 조절하였다.
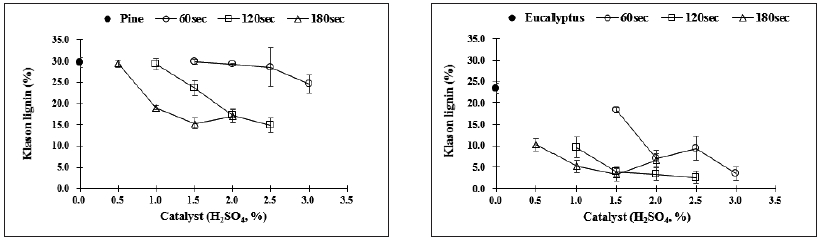
Fig. 1은 마이크로파 화학적 분산반응 시 마이크로파 조사 반응시간 및 촉매의 농도에 따른 바이오매스의 수율을 나타낸 것이다. 반응 시간별 촉매의 농도가 증가함에 따라 잔류물의 수율은 감소하였다. 동일한 반응조건에 있어서 침엽수보다는 활엽수의 수율 감소율이 최대 29.1%로 현저히 높았다. 이는 침·활엽수의 탄수화물 및 리그닌의 구성 성분의 차이, 함유량차이에 따른 결정화도, 중합도 등 반응성의 차이에서 기인한다고 할 수 있다.11,12) 하지만, 반응조건의 정도(severity)가 증가함에 따라 수종 간 수율 차이는 줄어드는 경향을 보이고 있다. 특히, 180초 반응시간 및 2.0%의 촉매첨가의 반응조건에서는 두 수종 간 수율 차이는 0.9%로 미미하였다.
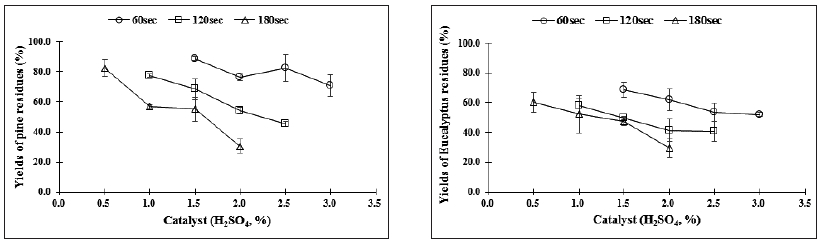
Fig. 1.
Yields of wood residues by microwave chemical micronization using different catalyst contents and reaction times (left: pine, right: eucalyptus).
Fig. 2에 각 반응조건에서 얻어진 잔류물의 잔존 리그닌 함량을 나타내었다. 공시재료로 사용한 목분의 Klason 리그닌의 양은 침엽수 29.7%, 활엽수 23.4%였다. 반응시간별 촉매의 농도가 증가함에 따라 활엽수의 경우 잔존 리그닌 양이 최대 20% 감소하여 120초/2.5%촉매 첨가량의 경우 잔존 리그닌 함량이 2.6%였다. 이에 비해 침엽수의 경우 같은 반응 조건에서 침엽수 목분에 비해 잔존 리그닌이 15% 정도 감소하였지만, 14.8%의 잔존 리그닌 함유량을 가진 잔류물이 얻어졌다. 활엽수의 경우 주어진 반응시간과 촉매첨가량 조절에 의한 크라프트 펄프화법에 상응하는 수율 및 잔존 리그닌 함량을 가진 잔류물을 제조할 수 있지만, 침엽수의 경우 본 실험에서 탐구된 반응조건(2:1 액비)으로는 14.8%의 상대적으로 높은 잔존 리그닌을 함유한 잔류물을 제조할 수 있다. 앞서 기술한 바와 같이 반응시간과 촉매의 첨가량을 조절하면 상대적으로 잔존 리그닌을 함유한 잔류물을 제조할 수는 있지만, 사용한 시료의 탄화입자로의 변환 가능성이 증대할 것으로 판단된다. 향후 마이크로 조사 반응시간 및 사용 액비(liquid-to-wood)를 조절함에 따라 촉매의 농도를 변화를 줌으로써 탄화발생도와 잔류물의 잔존 리그닌 양을 줄일 수 있는 연구를 진행하고자 한다.
3.2 마이크로파 조사에 따른 잔류물의 화학 조성 변화
Table 3에는 목분 및 마이크로파 조사에 따른 잔류물의 당 조성 변화를 나타내었다. 침엽수 목분의 경우 mannose의 함유량이 다른 헤미셀룰로오스 함유량보다 높고, 활엽수의 경우 xylose의 함량이 높게 나타나 전형적인 침·활엽수의 당 조성을 가지고 있음을 확인할 수 있었다. 반응조건 및 사용된 촉매의 양이 증가함에 따라 용출이 상대적으로 쉬운 헤미셀룰로오스들이 제거됨으로써6) 잔류물 내의 glucose 함유량이 증가한다. 반응정도(severity)에 따라서 glucose의 함유량이 90% 이상을 상회하였다.
Table 3.
Neutral sugar contents of micronized samples (top: pine, bottom: eucalyptus)
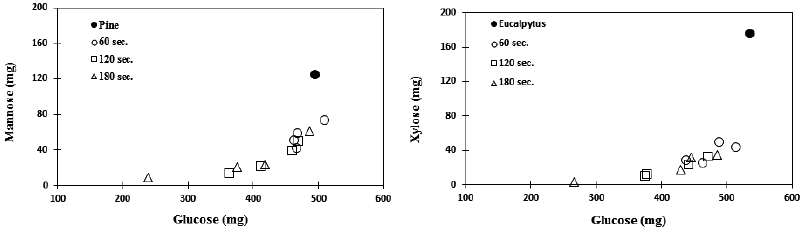
Fig. 3은 최초 목분의 투입량을 1,000 mg으로 환산하여 반응시간 및 첨가량에 따른 잔류물에 존재하고 있는 침·활엽수의 주요 헤미셀룰로오스에 대한 glucose의 물질수지를 비교한 그래프이다. 침엽수 내에 존재하는 mannose의 용출 시작은 반응정도(severity)가 120초/1.0 %에서 시작하는 것에 비해, 활엽수의 xylose의 용출은 반응정도가 60초/1.5%에서도 급격히 일어나는 것을 알 수 있다. 이는 활엽수에 존재하고 있는 리그닌 구성성분에 관련이 있다고 판단된다. 이전 연구결과8)에서도 보고한 바와 같이 마이크로파를 이용한 본 실험의 화학적 분산 반응은 용매와 촉매가 단시간에 세포벽을 찢어지거나 혹은 터지게 함으로써 잔류물을 미세화 함과 동시에 잔류물의 비결정영역부분과 헤미셀룰로오스를 제거함에 따라 리그닌이 같이 용출되어진다고 할 수 있다. 또한 촉매를 염산으로 고비점 용매와 같이 혼용하여 국내산 참나무 유기용매 펄프화에 대한 연구결과13)에서 참나무 목분의 syringaldehyde 함유량에 비해 펄프에 존재하는 syringaldehyde의 현저한 함유량의 감소로 볼 때 펄프에 잔존하는 리그닌의 대부분은 축합형 구조의 리그닌 형태로 존재한다고 보고되었다. 따라서, 마이크로파 조사에 따른 리그닌의 용출은 축합형 리그닌 고분자를 절단시켜 저분자화된 리그닌을 세포벽 외로 제거를 하는 것이 아니라 세포벽의 파괴와 함께 리그닌의 측쇄 부분을 파괴함으로써 잔류물의 입자가 미세화 됨에 따라 LCC (lignin-carbohydrate complex) 형태14)로 헤미셀룰로오스와 리그닌이 함께 용출되어진다고 유추할 수 있다. 이에 부산물인 흑액을 이용하여 리그닌 단리 및 동정으로 용출된 리그닌 구조에 관한 추가적인 연구가 필요하다고 생각된다.
3.3 마이크로파 조사에 따른 잔류물의 결정화도 변화
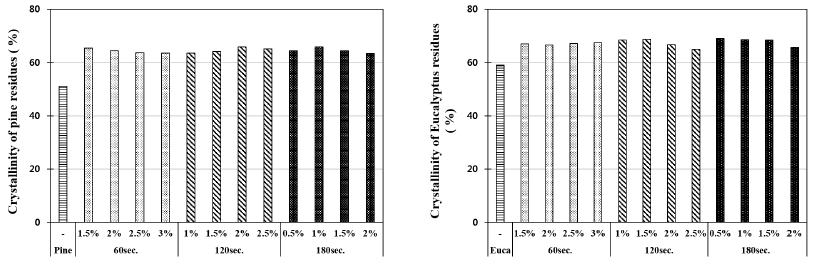
Fig. 4는 목분 및 잔류물의 결정화도를 측정한 그래프이다. 반응정도(severity)의 강약에 상관없이 사용된 침활엽수 목분 시료에 비해 잔류물의 결정화도는 모두 증가하였다. 활엽수 잔류물의 경우 목분에 대비 약 5-9% 정도 결정화도가 증가하였고, 침엽수의 경우는 12-14%정도 결정화도가 증가하였다. 이는 앞서 설명한 바와 같이 단시간의 급격한 열화학적 반응이 세포벽의 node, 결점부분, 혹은 비결정영역에 집중됨으로써 비결정영역 부분의 감소로 기인된 것으로 판단된다.
3.4 마이크로파 조사에 따른 잔류물의 용해용제에 대한 용해도 평가
Figs. 5-6은 마이크로파 처리되어 얻어진 잔류물의 용해 시 용해용제로 사용된 CED 용액 및 urea/NaOH 수용액의 상관관계 및 잔존 리그닌 함량에 대한 용해도를 표시하였다. 침·활엽수 모두 사용된 용해용제에 대한 용해도는 비슷한 경향을 나타내고 있으면 결정계수의 값이 0.85 이상의 상호 관계를 보이고 있다. 이런 경향은 마이크로파 처리 화학적 분산에 의해 얻어진 잔류물의 경우 상온(CED 용액) 혹은 freezing-thawing(urea/NaOH 수용액)15) 등의 용해 기작이 상이한 두 용해용제에 대해서 비슷한 반응성을 보인다고 할 수 있다. 하지만, Figs. 5-6에서 보는 바와 같이 침엽수 유래의 잔류물의 경우 두 용해용제에 대한 용해도가 전반적으로 전 범위로 골고루 분산이 되어 있는 반면에 활엽수의 경우에는 현저히 다른 두 군집을 형성하고 있다. Urea/NaOH 수용액 용해용제에 대한 침엽수 잔류물의 용해도는 32.7%-93.3%, 활엽수의 경우는 53.8%-93.7%로 활엽수 잔류물이 침엽수 잔류물에 비해 용해도가 우수하였다. 이러한 용해도의 차이는 잔류물의 중합도, 잔존 리그닌의 함유량 및 리그닌과 헤미셀룰로오스의 결합양식 등 다양한 영향인자들이 존재하고, 이러한 영향인자들의 상호관계에 대한 체계적인 연구가 필요하다고 판단된다.16)
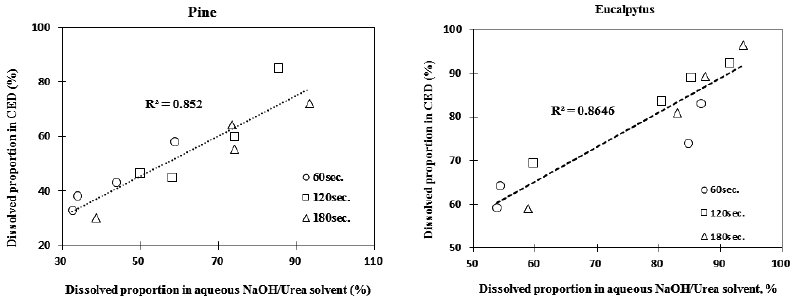
Fig. 5.
Relationship of solubility in CED and NaOH/Urea/water solvents (left: pine, right: eucalyptus).
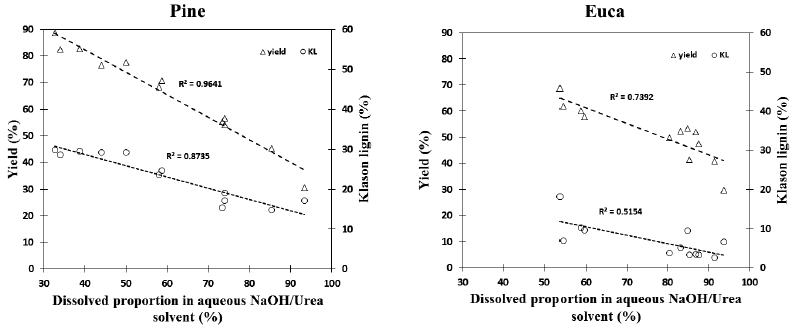
Fig. 6에서, 보는 바와 같이 이러한 침활엽수의 용해도의 차이는 리그닌의 함량이 주요한 영향인자로 판단된다. 잔류물의 수율이 반응정도(severity)에 의해 감소함에 따라 잔류물 내의 잔존 리그닌 함량이 감소한다. 활엽수 잔류물의 경우 잔류물의 잔존 리그닌의 함량이 9% 전후일 때 용해도가 50%에서 80% 이상으로 급격히 증가한 반면에 침엽수 잔류물의 경우 잔존 리그닌의 함량이 14%-17% 기점에서 용해율이 70%를 상회하는 경향을 보인다. 즉, 침엽수 잔류물의 경우 잔존 리그닌 함량이 활엽수 잔존 리그닌 함량에 비해 용해도에 미치는 영향이 덜 민감하다고 판단된다. 침엽수의 경우 주요 헤미셀룰로오스 성분인 mannose의 경우 리그닌과 공고히 결합을 한 상태로 존재한다고 알려져 있다. 다시 말해, 잔존 리그닌 함량이 14%-17% 이하인 잔류물의 경우 상대적으로 mannose의 함유량이 적다. 이에 반해 활엽수 경우에는 mannose의 함유량이 적고 또한 주요 헤미셀룰로오스 성분인 xylose의 함유량이 적기 때문에 용해도가 상대적으로 높다고 판단된다. 전술한 바와 같이 셀룰로오스의 중합도 역시 용해도에 대한 중요한 영향인자이다. 따라서 본 연구에서 잔류물의 중합도를 CED 용액으로 측정하고자 하였지만, 침엽수유래의 잔류물의 CED 용액에 대한 용해도가 낮아 신뢰성 있는 중합도 자료를 생산하지 못하였다.
4. 결 론
Glycol ether 용매와 황산 촉매 하에서 마이크로파를 조사하여 침·활엽수 바이오매스를 제조한 후, 마이크로파 조사 처리 조건별 미세 분산된 잔류물 시료들의 특성들을 비교 분석하였으며, 이에 따른 미세분산 잔류물의 특성이 용해용제에 대한 용해도를 조사하였다. 마이크로파 조사 및 화학적 미세화 분산반응 정도에 따라 침·활엽수 유래 잔류물의 수율이 감소하였으며, 리그닌 함유량 또한 감소하였다. 활엽수에 비해 화학적 미세화 분산반응에 덜 민감한 침엽수의 경우 분산 잔류물 내 리그닌 함량이 높았으며, 이에 기인하여 용해용제인 Urea/NaOH 수용액에 대한 용해도가 낮았다. 이와 같은 결과들로 볼 때 마이크로파 조사 및 촉매 농도에 조건을 달리하여 목질계 바이오매스의 반응정도를 조절함에 따라 그 성상이 다르고 다양한 형태의 바이오 소재를 제조할 수 있다고 판단된다.