1. 서 론
석유 기반의 고분자를 대체하기 위한 친환경 소재의 개발 측면에서 셀룰로오스 용해 기술에 주목하고 있다.1-3) 이와 같은 셀룰로오스의 용해를 통해 재생 셀룰로오스와 같이 변형된 형태의 셀룰로오스를 얻을 수 있으며 필름, 섬유, 폼 등의 형태로 다양하게 제조할 수 있다.4-7) 셀룰로오스 용해를 위해 사용되는 용해 용제는 알칼리 기반의 수용액, N-methylmorpholine-N-dxide (NMMO), ionic liquids, LiCl/DMAC 등을 사용할 수 있는데 그중에서도 알칼리 기반의 수용액은 환경 오염이 적은 친환경 용제로 NaOH, LiOH와 같은 알칼리 수용액에 thiourea, PEG 등을 첨가해 셀룰로오스의 용해율을 높일 수 있다고 보고된 바 있다.8-14)
이처럼 알칼리 기반 용해에 적용되는 원료는 주로 α-cellulose를 함유하는 면 펄프이다.15-17) 뿐만 아니라 목질 바이오매스는 α-cellulose를 포함하는 지속 가능한 천연 자원으로 면 펄프를 대체할 수 있는 잠재력 있는 용해 원료이다.3) 목질 바이오매스는 목재의 25-30%를 차지하는 리그닌을 활용할 수 있는 원료 물질로 높은 수율을 가지기 때문에 경제적인 이점을 가진다.18-20) 하지만 목질 바이오매스는 면 펄프와 달리 헤미셀룰로오스 및 리그닌을 함유하고 있기 때문에 용해 과정에 복잡한 영향을 끼친다.19,21,22) 따라서 목질 바이오매스의 각 구성 성분의 용해 기작을 이해하는 것이 중요하다.
셀룰로오스의 용해 정도는 최종 생산 수율에 영향을 끼칠 수 있다. 알칼리 수용액 기반의 셀룰로오스는 용해율을 증가시키기 위해 저온에서 1) 온도 조절을 이용한 동결 및 해동, 2) 물리적 처리를 통한 용해, 3) 2단계의 공정을 통해 용해하는 방법으로 용해된다.23,24) Micro-crystalline cellulose(MCC)의 경우, 7-10%의 NaOH 수용액으로 –5-–6℃에서 용해될 수 있다.11,25,26) 반면 NaOH/urea 수용액을 사용하는 경우 용해 온도를 0-5℃까지 조절할 수 있으며 시료를 두 차례 저온으로 반응시킴으로써 최종적인 용해율을 증가시킬 수 있다.24)
이전의 Ryu 등의27,28) 연구에서 유기용매 펄프화법을 통해 잔존 리그닌 함량이 14.2%인 침엽수 펄프를 제조하고 NaOH/urea 수용액으로 50-80%가량 용해시킬 수 있음을 확인하였다. 따라서 본 연구에서는 국내산 소나무를 원료로 하여 유기용매 미세화 시료를 제조하고 NaOH/urea 수용액에 2회 반복 적용하여 용해 정도를 파악하고 각 단계에서 셀룰로오스, 헤미셀룰로오스 및 리그닌 각 구성성분을 분석해 용해 과정에서 미세화 시료의 구성성분이 변동되는 과정을 알아보고자 하였다.
2. 재료 및 방법
2.1 공시재료
본 연구에서는 40-80 mseh인 국내산 소나무(Pinus densiflora) 목분을 사용하였다. 에탄올-벤젠 혼합용액(1:2, vol./vol.)으로 24시간 동안 추출된 시료의 Klason lignin 함량은 28.1%이며 산 가용성 리그닌 함량은 0.5%였다. 미세화 시료를 제조하기 위한 시약으로 이전의 연구에서 사용된 고비점 용매인 glycol ether(extra pure, Daejung Chemicals & Metals, Korea)를 사용하였다.29) 그리고 촉매로 순도 95%인 황산(extra pure, Daejung Chemicals & Metals, Korea)을 사용하였다. 미세화 시료는 수산화나트륨(extra pure, Daejung Chemicals & Metals, Korea), 요소(extra pure, Daejung Chemicals & Metals, Korea)를 이용한 용해 용제로 용해하였다.
2.2 황산 촉매를 이용한 미세화 시료의 제조
미세화 시료를 제조하기 위해 황산을 촉매로 목질 바이오매스 반응 시약을 제조하였다. 고비점 용매인 glycol ether에 황산 시약을 0.29 mol/L로 첨가해 제조하였다. 40-80 mesh의 소나무 목분과 약액의 비율을 1:2(wt./wt.)로 하여 충분히 교반한 후 110℃의 오일 배스에서 90분간 반응하였다. 반응 후 미세화 시료는 증류수, 0.5N NaOH 및 아세톤을 사용해 여액이 투명해질 때까지 순차 세정하였다. 최종적으로 세척된 미세화 시료는 105±3℃ 건조 오븐에서 8시간 이상 건조해 제조되었다.
2.3 미세화 시료의 NaOH/urea 수용액에서의 용해
미세화 시료를 용해하기 위한 용해 용제로 NaOH/urea 수용액을 NaOH 7 wt%, 요소 12 wt% 및 증류수 81 wt%로 제조하였다. 용해 원료인 미세화 시료(R) 5 g을 100 mL의 NaOH/urea 수용액에 투입한 후 –25℃ 조건에서 12시간 이상 동결하였다. 시료는 총 2회로 동결 및 해동을 반복하였다. 첫 번째로 동결 후 해동된 미세화 시료는 용해된 부분을 원심 분리를 통해 분리하고 5%의 황산을 통해 재생 셀룰로오스(D1)를 얻었다. 용해되지 않은 불용해 잔사(U1)는 용해에 사용되었던 용해 용제 및 증류수를 이용해 반복 세척하고 동결 건조하였다. 2회 용해는 앞선 방법과 동일하게 1회 동결한 후 해동한 뒤 –25℃ 조건에서 한번 더 동결하였다. 2회로 용해된 시료는 원심 분리를 통해 불용해 잔사(U2)로부터 분리하고 증류수로 세척되었다.
2.4 측정
2.4.1 용해율 및 성상
총 2회 용해 및 불용해된 시료는 다음과 같은 방법으로 분석되었다. 미세화 시료의 용해율은 용해 원료(R)와 불용해 잔사(U1 및 U2)로 계산하였다. 미세화 시료 및 각 단계에 따른 불용해 잔사(U1 및 U2)의 성상은 광학 현미경(BX50, OLYMPUS Co., Ltd., Japan)을 통해 분석하였다. 또한 잔존 리그닌 함량은 Klason lignin (TAPPI T 222 om-02)으로 측정되었다.
2.4.2 화학 조성분 분석 및 물질 수지
미세화 시료의 당 조성은 alditol-acetate법으로 분석하였으며 내부 표준물질의 피크 면적을 이용해 계산하였다.27,30) 측정은 silica capillary column(SP-2330, Supelco Inc., USA)이 장착된 Hewlett-Packard HP 6890 가스 크로마토그래피 기기를 사용하였으며 frame ionization detector(FID)로 검출하였다. 운반 기체로 사용된 질소 가스는 45.0 mL/min이었으며 초기온도 220℃, 2℃/min으로 240℃까지 승온하였다. Cellulose, (galacto)glucomannan 및 xylan은 다음과 같은 식에 의해 산출하였다.31,32) 용해 과정에서 발생한 물질수지(material balance)는 용해율, Klason lignin 및 중성 당 분석을 이용해 계산되었다. 전체 R, D1, U1, D2 그리고 U2의 중량은 용해율을 이용해 계산되었으며 화학 조성은 셀룰로오스, 헤미셀룰로오스 그리고 리그닌으로 분리하여 계산하였다. 셀룰로오스 및 헤미셀룰로오스는 중성 당 분석의 수율을 이용했고 헤미셀룰로오스는 (galacto)glucomannan 및 xylan의 합으로 계산되었다. 리그닌은 Klason lignin을 이용했다. 중성 당 분석 및 리그닌 정량은 R, D1, U1 그리고 U2만으로 측정되었기 때문에 D2는 U1 및 U2를 이용해 역산하였다. 용해율로부터 계산된 중량과 화학 분석을 통해 계산된 중량의 차이는 평균 2.6으로 나타났다.
3. 결과 및 고찰
3.1 반복 횟수에 따른 용해율
반복 횟수에 따른 미세화 시료의 용해 특성을 알아보기 위해 용해율을 관찰하였다(Fig. 1). 원료의 잔존 리그닌 함량은 11.8%로 1회로 용해된 시료의 용해율은 56.3%로 나타났다. 2회로 동결 및 해동 과정을 반복한 경우 용해율은 70.8%로 14.5% 증가한 결과를 나타냈다. 7-10 wt%의 NaOH 수용액은 저온에서 중합도 200-300의 셀룰로오스를 용해할 수 있다고 보고된 바 있다. 이와 더불어 Qi 등24)의 연구에 따르면 0℃에서 전처리를 하고 용해한 경우에 전체적인 용해율은 증가하며 완전히 용해되는 셀룰로오스의 함량은 증가하고 부분적으로 용해된 셀룰로오스의 함량은 감소한다고 보고된 바 있다. 이 결과는 반복되는 저온 처리로 인해 부분적으로 용해된 셀룰로오스가 완전히 용해되는 것을 의미한다. 따라서 2회 동결 및 해동이 반복되는 과정에서 용해율이 증가한 것으로 판단하였다.
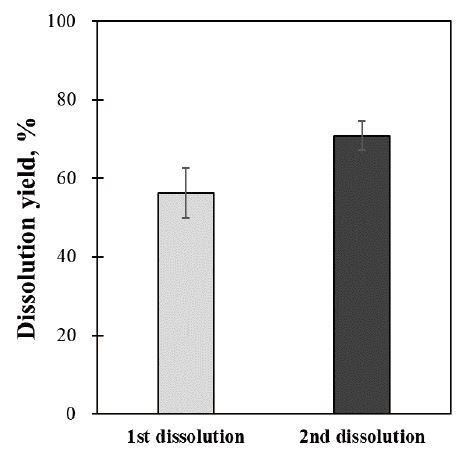
Fig. 1.
Dissolution yields of organosolv micronized residues.
3.2 형태학적 특성
용해되지 않은 미반응 잔사의 형태를 알아보기 위해 미세화 시료(R), 1차에서 용해되지 않은 미반응 잔사(U1) 및 2차에서 용해되지 않은 미반응 잔사(U2)를 광학 현미경을 통해 관찰하였다(Fig. 2). 황산 촉매에 의해 반응된 미세화 시료는 소나무 목분을 유기용매 펄프화한 것으로 단섬유를 가지고 표면에 존재하는 리그닌으로 인해 색이 짙은 것을 확인하였다. 반면 미세화 시료의 1차 용해를 통해 원료의 형태를 잃고 팽창된 형태가 발생하는 것을 확인하였다.33) 미세화 시료는 NaOH 및 urea 분자 및 저온 상태가 됨에 따라 팽창하여 섬유 혹은 섬유 다발 형태로 분리되는 것으로 관찰되었으며 표면에 있는 리그닌이 용해됨에 따라 미세화 시료보다 밝은색을 나타내었다. 2차 용해된 미반응 잔사를 관찰 한 결과 대부분이 Figs. 2(e) 및 (f)와 같이 용해되었고 Figs. 2(c) 및 (d)와 같은 원료 형태 또는 다발 형태의 섬유는 관찰되지 않았다. 이와 같은 결과는 1차에서 부분적으로 용해된 시료가 완전히 용해되거나 마이크로 피브릴 단위로 분리됨에 따른 현상으로 Fig. 1의 용해율 증가 결과와도 일치한다.34)
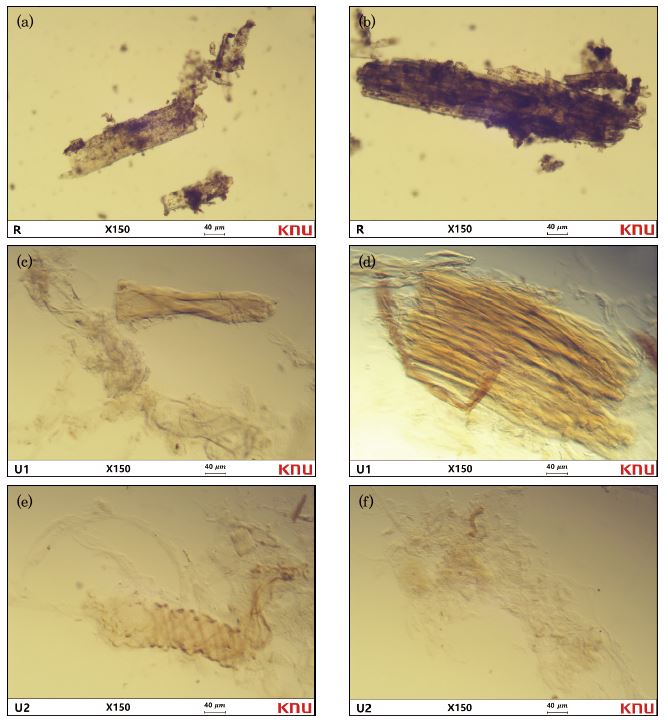
Fig. 2.
Microscopic images of insoluble residues (a,b: raw material, c,d: undissolved fraction in 1st dissolution and e,f: undissolved fraction in 2nd dissolution).
3.3 화학적 특성 분석
미세화 시료인 R의 잔존 리그닌 함량은 11.8%, 셀룰로오스 함량은 리그닌을 제외하고 91.1%였고 (galacto)glucomannan은 7.5%, xylan은 1.4%로 나타났다. 용해된 시료인 D1의 잔존 리그닌 함량은 6.4%로 미세화 시료의 잔존 리그닌 함량보다 낮게 측정되었고 당 조성은 유사하게 나타났다. 이와 같은 결과는 NaOH/urea 수용액에 의해 셀룰로오스, 헤미셀룰로오스 및 리그닌이 동일 구성 비율로 용해되지 않음을 의미한다. 반대로 용해되지 않은 미반응 잔사의 잔존 리그닌 함량이 21.2%로 미세화 시료보다 높은 잔존 리그닌 함량을 나타난 것이 이를 뒷받침하였다. 불용해 잔사의 당 조성 분석 결과 용해 원료인 미세화 시료와 비교해 U1의 셀룰로오스 함량은 감소하였고 (galacto)glucomannan 및 xylan의 함량은 소폭 증가하였다. U2의 경우, U1보다 1.3% 높은 잔존 리그닌 함량을 나타냈으며 셀룰로오스 함량은 감소하고 (galacto)glucomannan 및 xylan의 함량이 소폭 증가하였다. 이와 같은 결과는 NaOH/urea 수용액에 의해 헤미셀룰로오스가 상당량 제거되는 결과와 반대로 나타났으며 셀룰로오스 및 리그닌의 용해 정도가 영향을 끼칠 수 있다고 판단하였다.35)
3.4 물질 수지
셀룰로오스, 헤미셀룰로오스 및 리그닌을 모두 포함하고 있는 미세화 시료의 용해 특성을 보다 정량적으로 확인하기 위해 앞선 용해율, Klason lignin 및 중성 당 분석을 바탕으로 물질 수지를 계산하였다(Fig.3). 먼저 미세화 시료(R) 100 g을 기준으로 1차 용해를 진행했을 때 용해된 셀룰로오스는 76.0 g 중 47.9 g으로 약 63%, 헤미셀룰로오스는 5.6 g 중 3.9 g으로 약 69%, 그리고 리그닌은 11.8 g 중 3.6 g으로 약 31% 용해되었다. 따라서 대부분의 셀룰로오스 및 헤미셀룰로오스가 1차 동결 과정을 통해 대부분 용해됨을 확인하였다. 반면 불용해된 시료(U1)는 2차 과정에서 한번 더 용해되었다. 30.9 g의 셀룰로오스가 9.7g 용해되어 약 31% 용해되었고 헤미셀룰로오스는 2.3 g에서 0.7 g이 용해되어 약 30% 용해되었다. 리그닌은 9.3 g에서 2.0 g이 용해되어 약 22%가 용해되었다. 리그닌의 용해율은 2차에서도 가장 낮지만 용해율이 절반가량 감소한 셀룰로오스 및 헤미셀룰로오스에 비해 용해율 감소폭이 줄어든 결과를 나타냈다. 이와 같은 결과는 1차 용해를 통해 셀룰로오스 및 헤미셀룰로오스가 이미 다량 제거되었고 팽창된 상태에서 섬유 내부에 존재하는 리그닌이 수월하게 용해될 수 있음을 의미한다.36) 따라서 용해 횟수가 반복됨에 따라 리그닌에 대한 용해율을 증가시킬 수 있음을 확인하였다.
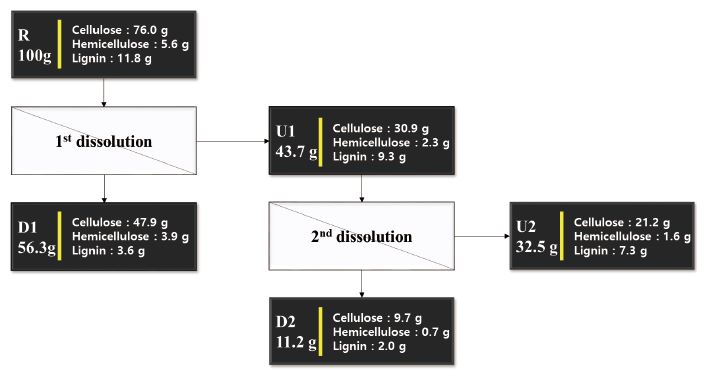
Fig. 3.
Material balance based on dissolution yields and chemical analysis.
최종적으로 용해되지 않은 U2와 용해 원료를 비교해 보았을 때, 셀룰로오스는 76.0 g에서 21.2 g이 용해되지 않아 약 72% 용해되었고 헤미셀룰로오스는 5.6 g에서 1.6 g으로 약 71% 용해되었다. 리그닌은 11.8 g에서 7.3 g으로 약 38% 용해되었다. 따라서 높은 리그닌 함량을 나타내고 헤미셀룰로오스의 함량이 소폭 증가하였던 Table 1의 화학 조성분의 결과는 가장 많은 양을 차지하는 셀룰로오스에 대한 용해율에 의해 상대적으로 헤미셀룰로오스 및 리그닌의 함량이 높게 나타난 것임을 확인하였다.
Table 1.
Chemical compositions of samples
(Unit: %)
| Klason lignin | Total sugar | Cellulose | (Galacto)glucomannan | Xylan |
|---|
| R | 11.8 | 83.4 | 91.1 | 7.5 | 1.4 |
| D1 | 6.4 | 93.4 | 91.2 | 7.1 | 1.8 |
| U1 | 21.2 | 78.1 | 90.5 | 7.8 | 1.8 |
| U2 | 22.5 | 72.7 | 89.6 | 8.6 | 1.8 |
4. 결 론
본 연구에서는 미세화 시료를 용해 원료로 NaOH/urea 수용액에서 동결 및 해동 과정을 반복함에 따라 용해율 및 화학 구성성분의 변화를 알아보고자 하였다. 용해율을 비교한 결과 1회로 용해된 시료의 용해율은 56.3%로 나타났고 2회로 동결 및 해동 과정을 반복한 경우 70.8%로 14.5% 증가한 결과를 나타냈다. 미반응 잔사의 성상을 확인하기 위해 광학 현미경을 관찰한 결과 미세화 시료의 1차 용해를 통해 원료의 형태를 잃고 팽창된 형태가 발생하는 것을 확인하였으며 2차에서는 대부분 섬유가 팽창 및 분리되어 부분적으로 용해된 상태로 관찰되었다. 용해 원료 구성성분 변화를 알아보기 위해 Klason lignin 및 중성 당 분석을 통해 물질수지를 분석한 결과 셀룰로오스, 헤미셀룰로오스는 1차에서 가장 많이 용해되는 것을 확인하였고 리그닌에 대한 용해율은 1차 및 2차에서 상대적으로 크게 차이가 나지 않음을 확인하였다.
Acknowledgements
본 연구는 2017년도 정부(교육과학기술부)의 지원으로 한국연구재단의 지원을 받아 수행된 기초연구사업(NRF-2017R1D1A1B03030710) 및 산림청(한국임업진흥원) 산림과학기술연구개발사업(FTIS-2019149B10-2023-0301)의 지원에 의하여 이루어졌습니다.
Literature Cited
Medronho, B. and Lindman, B., Competing forces during cellulose dissolution: from solvents to mechanisms, Current Opinion in Colloid & Interface Science 19(1):32-40 (2014).
10.1016/j.cocis.2013.12.001Tu, H., Zhu, M., Duan, B., and Zhang, L., Recent progress in high‐strength and robust regenerated cellulose materials, Advanced Materials 2000682 (2020).
10.1002/adma.202000682Le Moigne, N., Navard, P., Dissolution mechanisms of wood cellulose fibres in NaOH–water, Cellulose 17(1):31-45 (2010).
10.1007/s10570-009-9370-5Zhang, L., Ruan, D., and Zhou, J., Structure and properties of regenerated cellulose films prepared from cotton linters in NaOH/urea aqueous solution, Industrial & Engineering Chemistry Research 40(25):5923-5928 (2001).
10.1021/ie0010417Fink, H. -P., Weigel, P., Purz, H., and Ganster, J., Structure formation of regenerated cellulose materials from NMMO-solutions, Progress in Polymer Science 26(9):1473-1524 (2001).
10.1016/S0079-6700(01)00025-9Kevin, J., D'Emilio, E., Cranston, E. D., Geiger, T., and Nyström, G., Dual physically and chemically crosslinked regenerated cellulose–Gelatin composite hydrogels towards art restoration, Carbohydrate polymers 234:115885 (2020).
10.1016/j.carbpol.2020.115885Granja, P., Barbosa, M., Pouységu, L., De Jéso, B., Rouais, F., and Baquey, C., Cellulose phosphates as biomaterials. Mineralization of chemically modified regenerated cellulose hydrogels Journal of materials science 36(9):2163-2172 (2001).
10.1023/A:1017587815583Wang, S., Lu, A., and Zhang, L., Recent advances in regenerated cellulose materials, Progress in Polymer Science 53:169-206 (2016).
10.1016/j.progpolymsci.2015.07.003Kosan, B., Michels, C., and Meister, F., Dissolution and forming of cellulose with ionic liquids, Cellulose 15(1):59-66 (2008).
10.1007/s10570-007-9160-xCai, J. and Zhang, L., Rapid dissolution of cellulose in LiOH/urea and NaOH/urea aqueous solutions, Macromolecular bioscience 5(6):539-548 (2005).
10.1002/mabi.200400222Isogai, A. and Atalla, R., Dissolution of cellulose in aqueous NaOH solutions, Cellulose 5(4):309-319 (1998).
10.1023/A:1009272632367Yan, L. and Gao, Z., Dissolving of cellulose in PEG/NaOH aqueous solution, Cellulose 15(6):789 (2008).
10.1007/s10570-008-9233-5Striegel, A. M., Advances in the understanding of the dissolution mechanism of cellulose in DMAc/LiCl, Journal of the Chilean Chemical Society 48(1):73-77 (2003).
10.4067/S0717-97072003000100013Rosenau, T., Potthast, A., Sixta, H., and Kosma, P., The chemistry of side reactions and byproduct formation in the system NMMO/cellulose (Lyocell process), Progress in polymer science 26(9):1763-1837 (2001).
10.1016/S0079-6700(01)00023-5Olsson, C. and Westman, G., Direct dissolution of cellulose: background, means and applications, Cellulose-fundamental aspects 10:52144 (2013).
10.5772/52144Phinichka, N. and Kaenthong, S., Regenerated cellulose from high alpha cellulose pulp of steam-exploded sugarcane bagasse, Journal of materials research and technology 7(1):55-65 (2018).
10.1016/j.jmrt.2017.04.003He, L., Xin, L. -P., Chai, X. -S., and Li, J., A novel method for rapid determination of alpha-cellulose content in dissolving pulps by visible spectroscopy, Cellulose 22(4):2149-2156 (2015).
10.1007/s10570-015-0652-9Cuissinat, C. and Navard, P., Swelling and dissolution of cellulose part II: Free floating cotton and wood fibres in NaOH–water–additives systems, In Macromolecular Symposia 244(1):19-30 (2006).
10.1002/masy.200651202Heggset, E. B., Syverud, K., and Øyaas, K., Novel pretreatment pathways for dissolution of lignocellulosic biomass based on ionic liquid and low temperature alkaline treatment, Biomass and Bioenergy 93:194-200 (2016).
10.1016/j.biombioe.2016.07.023Gazi, S., Valorization of wood biomass-lignin via selective bond scission: A minireview, Applied Catalysis B: Environmental 257:117936 (2019).
10.1016/j.apcatb.2019.117936Cheng, D., An, X., Zhang, J., Tian, X., He, Z., Wen, Y., and Ni, Y., Facile preparation of regenerated cellulose film from cotton linter using organic electrolyte solution (OES), Cellulose 24(4):1631-1639 (2017).
10.1007/s10570-017-1215-zShi, Z., Yang, Q., Cai, J., Kuga, S., and Matsumoto, Y., Effects of lignin and hemicellulose contents on dissolution of wood pulp in aqueous NaOH/urea solution, Cellulose 21(3):1205-1215 (2014).
10.1007/s10570-014-0226-2Wang, Y. and Deng, Y., The kinetics of cellulose dissolution in sodium hydroxide solution at low temperatures, Biotechnology and bioengineering 102(5):1398-1405 (2009).
10.1002/bit.22160Qi, H., Yang, Q., Zhang, L., Liebert, T., and Heinze, T., The dissolution of cellulose in NaOH-based aqueous system by two-step process, Cellulose 18(2):237-245 (2011).
10.1007/s10570-010-9477-8Zhou, J., and Zhang, L., Solubility of cellulose in NaOH/urea aqueous solution, Polymer Journal 32(10):866-870 (2000).
10.1295/polymj.32.866Burchard, W., Solubility and solution structure of cellulose derivatives, Cellulose 10(3):213-225 (2003).
10.1023/A:1025160620576Ryu, J. -A., Park, S. -J., Eom, T. -J., and Lee, J. M., 3D Printer Application Properteis of MFC-PLA Composite Filament Fabricated with Organosolv-Derived MFC. Journal of Korea TAPPI 51:110-119 (2019).
10.7584/JKTAPPI.2019.12.51.6.110Ryu, J. -A., Jo Y. -S., and Lee, J. M., Dissolution of Lignin-Rich Organosolv Pulps by PEG and Urea Contents in Aqueous Alkaline Solution, Journal of Korea TAPPI 52(4):63-72 (2020).
10.7584/JKTAPPI.2020.08.52.4.63Kim, K. -J., Nah, G. -B., Ryu, J. -A., and Eom, T. -J., Low temperature, atmospheric pressure and short reaction time (LAS) pulping of Korean mixed oak with glycol ether, Journal of Korea TAPPI 50(2):44-51 (2018).
10.7584/JKTAPPI.2018.04.50.2.44Borchardt, L. G. and Piper, C. V., A gas chromatographic method for carbohydrates as alditol-acetates, Tappi 53(2):257-260 (1970).
Meier, H., Studies on hemicelluloses from pine, Acta Chem Scand 12:1911-8 (1958).
10.3891/acta.chem.scand.12-1911Zhu, W. and Theliander, H., Precipitation of lignin from softwood black liquor: an investigation of the equilibrium and molecular properties of lignin, BioResources 10(1):1696-1714 (2015).
10.15376/biores.10.1.1696-1715Zhang, S., Wang, W. -C., Li, F. -X., and Yu, J. -Y., Swelling and dissolution of cellulose in NaOH aqueous solvent systems, Cellulose chemistry and technology 47(9-10):671-679 (2013).
Ogihara, Y., Smith, R. L., Inomata, H., and Arai, K., Direct observation of cellulose dissolution in subcritical and supercritical water over a wide range of water densities (550–1000 kg/m3), Cellulose 12(6):595-606 (2005).
10.1007/s10570-005-9008-1Li, J., Liu, X., Zheng, Q., Chen, L., Huang, L., Ni, Y., and Ouyang, X., Urea/NaOH system for enhancing the removal of hemicellulose from cellulosic fibers, Cellulose 26(11):6393-6400 (2019).
10.1007/s10570-019-02587-7Sescousse, R., Smacchia, A., and Budtova, T., Influence of lignin on cellulose-NaOH-water mixtures properties and on Aerocellulose morphology, Cellulose 17(6):1137-1146 (2010).
10.1007/s10570-010-9448-0






