1. 서 론
목재의 주성분은 셀룰로오스와 헤미셀룰로오스의 다당류로 구성되어 있고 이런 다당류를 보호하기 위하여 리그닌이 둘러 싼 구조를 하고 있다.1) 셀룰로오스와 헤미셀룰로오스를 효과적으로 효소당화 하면 단당을 이용한 에너지 자원(에탄올, 부탄올 발효)이나2,3) 석유 화학 대체 물질(젖산 발효, succinic acid 발효)의 원료가 된다.4,5) 이런 공정에서 다당류의 복잡한 구조와 리그닌으로 인하여 다당류에서 단당류로 전환 효율이 낮다.
일반적인 화학적 전처리 방법은 리그닌 제거법이나 헤미셀룰로오스 제거법이 사용되었고 물리적이나 화학적으로 셀룰로오스의 결정화도를 파괴하는 방법도 시도되었다.6) 이런 전처리된 시료는 셀룰로오스 분해 효소의 접근성을 높여 다당에서 단당으로 전환이 높아 바이오매스 기반 석유화학 대체 분야에서 중요한 기술 분야이다.
셀룰로오스 나노 섬유는 셀룰로오스를 기계적인 방법으로 나노 단위로 가공하여 적용범위 넓은 산업에 적용할 수 있는 물질로 2000년대에 활발하게 연구되고 있다. 점탄성이 우수하고, 수분 친화력이 월등하여 이러한 특성을 응용하여 화장품, 시멘트, 도료에 셀룰로오스 나노 섬유 현탁액을 사용하는 연구가 진행되고 있다.7-9)
셀룰로오스 나노 섬유를 제조하기 위한 펄프화 공정, 표백 공정, 나노 섬유화 공정은 셀룰로오스 분해 효소나 미생물이 셀룰로오스를 효율적인 이용이 가능한 물질로 만들 수 있는 전처리가 될 수 있다. 셀룰로오스 나노 섬유는 셀룰로오스로만 구성된 유기물로 셀룰로오스 외 다른 물질이 적어 셀룰로오스를 영양분으로 하는 미생물이 쉽게 접근하여 영양분으로 사용가능하다.10,11) 특히 셀룰로오스 나노 섬유는 기존 셀룰로오스에 비해 크기가 작고, 나노피브릴화 된 상태이기 때문에 미생물이 셀룰로오스에 비해 더 쉽게 사용할 수 있다.
셀룰로오스 나노 섬유 현탁액은 수분이 풍부한 상태로 중량의 90% 이상 존재한다. 이러한 조건은 적절한 온도 조건에서 생육에 적합하여 미생물에 오염이 급격하게 일어 날 수 있다. 셀룰로오스 나노 섬유 현탁액이 오염될 경우, 셀룰로오스 나노 섬유가 분해되어 물성저하가 일어나며, 주요 물성인 점탄성이 저하될 수 있다.12)
자연계에 셀룰로오스를 분해할 수 있는 미생물은 박테리아, 효모, 진균이 존재한다. 박테리아는 원핵생물이며, 진균은 진핵생물로 진화적으로 진균이 더 진화된 생물이다. 진균은 박테리아와 다르게 핵막이 있으며, 핵 외에 다른 세포 소기관이 존재한다.13) 이렇듯 박테리아와 진균은 차이가 있으며, 이전 연구에서 박테리아를 연구한 결과를 진균에 적용할 수 없다.
본 연구에서는 셀룰라아제를 생산할 수 있는 진균들의 셀룰로오스 나노 섬유 분해에 의한 점도 저하 특성을 파악하고자 하였다. 현탁액 상태로 유통할 경우 진균에 의한 셀룰로오스 분해 문제를 해결할 수 있는 보존제의 종류와 첨가량을 확인하고자 하였다.
2. 재료 및 방법
2.1 공시재료
M 사의 활엽수 표백 크라프트 펄프를 원료로 사용하였으며, 수산화나트륨, 염화아세트산, 에탄올을 카르복시메틸화 반응에 사용하였다. 페녹시에탄올, 1,2-헥산디올, 아지드나트륨을 미생물 오염 방지를 위한 보존제로 사용하였다.
2.2 실험 방법
2.2.1 카르복시메틸화 전처리
원활한 셀룰로오스 나노섬유 제조를 위하여 카르복시메틸화 전처리를 실시하였다. 전처리 반응은 펄프 100.0 g에 수산화나트륨 19.7 g이 용해된 에탄올 2 L을 혼합하여 상온에서 두 시간 이상 방치하여 셀룰로오스 수산기의 이온화 반응을 유도하였다. 카르복시메틸화 반응의 완료를 위하여 이온화된 펄프에 염화아세트산 21.7 g이 용해된 에탄올 500 mL를 혼합하여 70℃에서 두 시간 반응하였다. 반응이 종료된 펄프는 에탄올을 제거한 후 세척한 후 나노셀룰로오스 제조에 사용하였다. 세척 후 펄프는 pH 6-7이 되도록 유지하였다.
2.2.2 셀룰로오스 나노 섬유 제조
셀룰로오스 나노섬유를 만들기 위하여 카르복시메틸화 전처리된 펄프를 1%(w/w)로 희석 후 고압균질기를 통과시켜 제조하였다. 고압균질기(PANDA PLUS, GEA, Italy)의 사용 조건은 1차 통과에서는 100 bar의 압력을 사용하였다. 1회 통과 이후 2회 통과부터는 600 bar로 압력을 조절하였다. 최종 통과 횟수는 최소 통과횟수를 포함하여 7회 통과시켜 셀룰로오스 나노피브릴을 제조하였다. 미생물 오염 방지 보존제는 셀룰로오스 나노 섬유 제조 공정에서 1.0, 2.0, 3.0%(w/w)를 첨가하여 제조하였다.
2.2.3 진균 미생물 배양액 제조
진균 미생물로 C. albicans(Candida albicans, KCCM 11282)와 A. niger(Aspergillus niger, KCCM 11239)를 한국미생물보존센터에서 분양받아 사용하였다. 진균 배양 배지는 C. albicans의 경우 YM배지(Yeast extract 3.0 g/L, Malt extract 3.0 g/L, Peptone 5.0 g/L, Dextrose 10.0 g/L)를 사용하였으며, A. niger의 경우 맥아 추출물배지(Malt extract 20.0 g/L, Glucose 20.0 g/L, Peptone 1.0 g/L)를 사용하였으며, 30℃ 진탕 배양기에서 하루 동안 배양하였다. 하루 동안 배양된 C. albicans와 A. niger 배양액을 5.0 mL를 취해 새로운 nutrient 배지 50 mL에 분주한 후 하루 동안 배양하여 셀룰로오스 나노 섬유 현탁액에 분주할 배양액을 제조하였다.
2.2.4 셀룰로오스 나노 섬유의 진균 오염 영향 실험
셀룰로오스 나노섬유의 현탁액의 진균에 대한 오염을 확인하기 위해 셀룰로오스 나노 섬유 현탁액에 진균 배양액을 접종 후 배양하였다. 셀룰로오스 나노 섬유 현탁액을 100 mL 삼각플라스크에 20.0 g을 넣은 후 고압멸균기로 121℃, 15분간 멸균을 실시하였다. 멸균된 셀룰로오스 나노 섬유 현탁액에 C. albicans와 A. niger 배양액 1 mL를 접종한 후 25℃ 진탕 배양기에서 3일간 배양하였다. 보존제가 첨가된 셀룰로오스 나노 섬유 현탁액도 같은 방법을 반복하여 실시하였다.
2.2.5 오염된 셀룰로오스 나노 섬유 현탁액의 미생물 검출
셀룰로오스 나노 섬유 현탁액의 진균 오염 여부를 확인하기 위해 셀룰로오스 나노섬유 현탁액에 진균을 3일간 배양한 후 현탁액을 고체배지에 도말하여 진균 오염 여부를 확인하였다. 사용된 진균 배양 배지는 C. albicans의 경우 YM배지(Yeast extract 3.0 g/L, Malt extract 3.0 g/L, Peptone 5.0 g/L, Dextrose 10.0 g/L)를 사용하였으며, A. niger의 경우 맥아 추출물배지(Malt extract 20.0 g/L, Glucose 20.0 g/L, Peptone 1.0 g/L)를 사용하였으며, 오염된 셀룰로오스 나노 섬유 현탁액을 1 mL를 고채배지에 도말한 후 25℃ 진탕 배양기에 24시간 배양 후 배양된 진균을 확인하여 콜로니 또는 오염 영역을 분석하여 진균 오염 여부를 확인하였다.
2.2.6 투과전자현미경 분석
카르복시메틸화 전처리된 활엽수 표백 크라프트 펄프로 제조된 나노피브릴의 크기를 분석하기 위하여 음영염색법을 이용하여 투과전자현미경 분석을 실시하였다. 분석하기 위한 그리드 제조 방법은 나노피브릴을 0.01%(w/w)로 희석한 후 300 mesh 카본그리드에 위치시킨 후 아세트산 우라늄으로 음영염색을 하여 관찰용 샘플을 제조하였다. 투과전자현미경(Libra 120, Carl zeiss, Germany) 관찰 조건은 가속전압 120 kV에서 관찰하였으며, 배율은 10,000배에서 관찰하였다. 나노피브릴 섬유 폭 크기는 나노피브릴 섬유 50개의 폭 크기를 측정하여 분석하였다.
2.2.7 오염된 셀룰로오스 나노 섬유의 점도 측정
셀룰로오스 나노 섬유 현탁액의 물성과 미생물 오염에 따른 물성 저하를 측정하기 위해 레오미터를 사용하여 점도 측정하였다. 점도측정기(MCR 102, Anton Paar, Austria) 사용조건은 D-PP 25 툴을 사용하여 셀룰로오스 나노 섬유 현탁액의 점도를 측정하였다. 측정된 점도를 이용하여 viscosity drop을 Eq. 1과 같이 계산하여 점도 변화를 평가하고자 하였다.
A: viscosity of cellulose nanofibril - before contamination
B: viscosity of cellulose nanofibril - after contamination
3. 결과 및 고찰
3.1 제조된 셀룰로오스 나노 섬유의 미생물 오염 특성
본 실험에 사용된 셀룰로오스 나노 섬유의 폭 크기를 측정하기 위해 투과전자현미경 분석 결과를 Fig. 1에 나타내었다. 셀룰로오스 나노섬유의 폭은 2.9-7.7 nm(평균 4.7 nm)의 크기로 제조되었다.
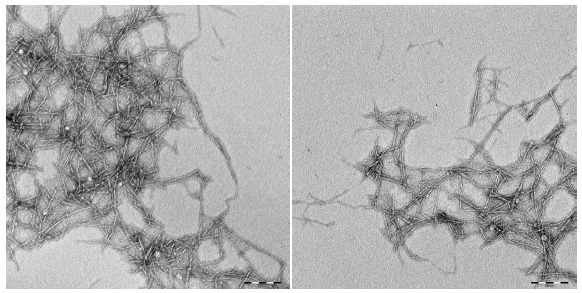
Fig. 1.
Transmission electron microscopy image of cellulose nanofibril from carboxymethylated hardwood kraft pulp (sacle bar: 200 nm).
셀룰로오스 나노 섬유 현탁액에 C. albicans와 A. niger를 3일간 배양 후 1% 셀룰로오스 나노 섬유 현탁액의 점도를 측정한 결과를 Fig. 2에 나타내었다. 미생물 오염 이전 셀룰로오스 나노 섬유의 점도는 12,860 mPa·s로 확인되었지만, C. albicans와 A. niger에 의해 셀룰로오스 분해된 현탁액의 점도가 감소하였으며, C. albicans의 경우 20% 감소한 반면 A. niger의 경우 60% 이상 감소되었다. C. albicans는 화장품 등의 미생물 평가에 사용되는 진균으로 칸디다증(Candidiasis)의 원인이 되는 균으로 일반적인 셀룰로오스 분해 균주가 아니지만, 진균에서 분비하는 다른 효소나 물질에 의해 점도 저하가 일어난 것으로 판단된다.14)A. niger의 경우 일반적인 셀룰로오스 분해 진균인 검은 곰팡이로,15)C. albicans에 비해 셀룰로오스 분해 효소의 분비가 많기 때문에 더 큰 점도 저하가 발생한 것으로 판단된다.
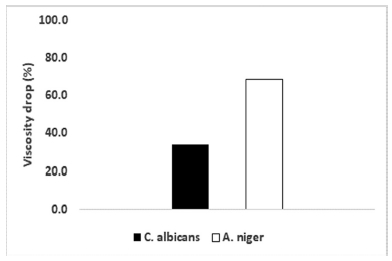
Fig. 2.
Viscosity drop by fungal degradation of cellulose nanofibril suspension with C. albicans and A. niger.
3.2 페녹시에탄올이 첨가된 셀룰로오스 나노섬유에서 진균에 의한 셀룰로오스 나노섬유 분해 저해
페녹시에탄올의 첨가가 진균에 의한 셀룰로오스 나노 섬유 분해 저해를 확인하기 위하여 셀룰로오스 나노섬유 고체배지에서 확인한 결과를 Table 1에 나타낸 결과 두 가지 균주 모두 콜로니나 균사가 확인되지 않았다. 의료, 화장품용에 사용되는 진균 방부제로 페녹시에탄올은 진균의 세포막에 작용하여 세포 내 물질 누출을 제어하지 못하도록 세포벽을 파괴하거나 TCA회로의 효소 억제에 관여하여 미생물의 성장을 방해한다.16,17) 본 실험에 사용된 진균은 모두 페녹시에탄올에 의해 생육을 억제 받은 것이 확인되었다. 특히 페녹시에탄올을 1% 첨가한 셀룰로오스 나노섬유 현탁액 내에서 생육이 크게 억제되었으며, 다시 생육에 유리한 조건으로 배양했음에도 더 이상 두 가지 진균 모두 성장하지 못한 것이 확인되었다.
Table 1.
Prevention of fungal degradation of cellulose nanofibril with phenoxyethanol
| C. albicans | A. niger |
|---|
| No phenoxyethanol | | +++ | +++ |
| Phenoxyethanol | 1.0% | --- | --- |
| 2.0% | --- | --- |
| 3.0% | --- | --- |
페녹시에탄올이 첨가된 셀룰로오스 나노 섬유 현탁액에 C. albicans와 A. niger를 배양, 셀룰로오스의 분해 정도를 분해 후 점도감소 효과를 Fig. 3에 나타내었다. 측정결과 두 가지 균주 모두 페녹시에탄올 첨가에 의해 셀룰로오스 나노섬유 현탁액의 점도 저하가 적게 일어난 것이 확인되었으며, C. albicans에 비해 A. niger의 점도가 더 높게 확인되었다. 특히 페녹시에탄올의 함량이 증가할수록 A. niger에 의한 점도 저하가 적은 것이 확인되었다. 셀룰로오스 나노섬유의 진균에 의한 생육 여부를 확인한 Table 1 결과와 비교했을 때, 고체 배지상에서 진균의 생장을 확인할 수 없었지만, 점도가 일부 감소한 것이 확인되었다. 이는 배양액을 접종하였을 때, 활성이 높은 균주에 의해 셀룰로오스 나노 섬유 현탁액의 점도가 감소하였지만, 배양이 끝난 후 고체배지로 옮겨 배양할 때는 모든 진균이 사멸하여 고체배지에서 균이 확인되지 않은 것으로 판단된다. 위 결과를 미루어 볼 때, 페녹시에탄올을 1% 첨가함으로써 점도 저하는 일부 발생하지만 더 이상 미생물이 셀룰로오스 나노섬유 현탁액 내에서 생육하지 못하도록 할 수 있다.
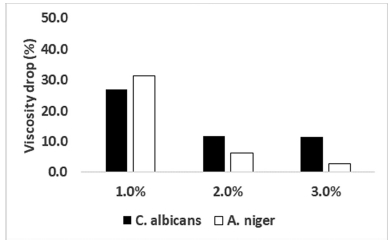
Fig. 3.
Viscosity drop by fungal degradation of phenoxyethanol added cellulose nanofibril suspension with by C. albicans and A. niger.
3.3 1,2-헥산디올이 첨가된 셀룰로오스 나노섬유 현탁액의 미생물 오염 특성
1,2-헥산디올이 첨가된 셀룰로오스 나노섬유 현탁액의 오염 여부를 Table 2에서 확인한 결과 1%와 2%를 첨가하였을 때, 두 균주가 남아 있는 것이 확인되었다. 특히 C. albicans의 경우 A. niger에 비해 잔류한 미생물의 오염이 크게 확인되었다. 1,2-헥산디올이 3%가 첨가되었을 때, 미생물의 오염이 확인되지 않았다. 1,2-헥산디올은 1,2-알칸디올계 화합물로, 알칸디올계 화합물이 진균의 세포막 형성과정을 방해하기 때문으로 알려져 있다.18) 이전 연구에서 세균과 진균에 대해 1,2-헥산디올의 방부력을 측정한 결과 첨가 농도에 따라 균의 성장을 억제하였으나, 완전히 균이 성장을 억제하지 못하는 것이 확인된 바 있다.19) 본 실험에서도 페녹시에탄올을 1% 이상 첨가할 경우 미생물의 생육이 크게 억제되고, 항균 능력을 발휘한 것에 비해 1,2-헥산디올의 경우 3% 미만 첨가하였을 때, 미생물의 생육이 완벽하게 억제되지 않은 것이 확인되었다.
Table 2.
Prevention of fungal degradation of cellulose nanofibril with 1,2-hexanediol
| C. albicans | A. niger |
|---|
| No 1,2-hexanediol | | +++ | +++ |
| 1,2-hexanediol | 1.0% | +++ | +-- |
| 2.0% | +-- | +-- |
| 3.0% | --- | --- |
1,2-헥산디올이 첨가된 셀룰로오스 나노섬유 현탁액의 오염 후 잔류하는 점도를 측정한 결과를 Fig. 4에 나타내었다. 점도 측정 결과 C. albicans와 A. niger 모두 1,2-헥산디올의 첨가량이 증가함에 따라 점도 감소 효과가 증가하였다. 1,2-헥산디올이 1% 첨가되었을 때 생육 억제작용을 하긴 하였지만, 완벽하게 억제하지 못해 점도 약 20%의 점도 감소가 확인되었다. 1,2-헥산디올을 첨가하여 미생물 오염에 의한 점도 저하 효과는 C. albicans와 A. niger 모두 비슷한 것으로 확인되었지만, C. albicans의 경우 A. niger에 비해 배양 후 남아 있는 미생물의 양이 많은 것으로 확인되었다. 이를 미루어 보아 1% 1,2-헥산디올이 첨가되었을 때, C. albicans의 경우 생존할 수 있지만, 효소나 다른 물질의 분비가 약해 점도 저하가 보존제가 없을 때에 비해 증가한 것으로 판단된다.
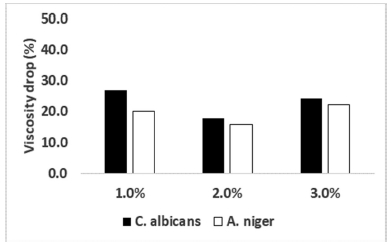
Fig. 4.
Viscosity drop by fungal degradation of 1,2-hexanediol added cellulose nanofibril suspension with by C. albicans and A. niger.
3.4 아지드나트륨이 첨가된 셀룰로오스 나노 섬유 현탁액의 미생물 오염 특성
아지드나트륨이 첨가된 셀룰로오스 나노섬유 현탁액의 오염 여부를 Table 3에 나타낸 결과 C. albicans의 경우 3% 미만이 첨가되었을 때, 미생물이 남아 있는 것이 확인되었으며, A. niger의 경우 1% 이상 첨가되었을 때, 현탁액에 남아 성장할 수 있는 균이 없는 것으로 확인되었다. 아지드나트륨은 질소 3개가 이중결합으로 연결되어 있는 질소 화합물로 생물에 대해 독성 물질이며, 유전자 변이를 일으켜 진균을 제거한다.20) 하지만 페녹시에탄올과 1,2-헥산디올과 다르게 인체에 대해 유해성이 보고된 바 있어, 인체에 사용하지 않고, 실험과정에서 진균, 세균을 제거, 방지하는 용도로 사용된다. 아지드나트륨은 특히 효소당화 공정에서 오염을 방지하기 위한 방부제로 사용된다. 하지만 아지드나트륨의 독성으로 인해 당화용액을 발효하는 과정에서 저해요소로 작용하여 효소당화 연구에만 사용되고 있다.21)C. albicans의 경우 1,2-헥산디올과 마찬가지로 1%, 2% 첨가에 의해서는 성장이 완전히 억제되지 않는 것이 확인되었다. A. niger의 경우에는 아지드나트륨을 1% 첨가함으로써 균의 성장이 억제된 것이 확인되었다. 위 결과를 미루어 볼 때, 아지드나트륨에 의해서 균의 성장을 억제하기 위해서는 3% 이상을 첨가하여야 두 가지 균주에 의한 오염을 방지할 수 있을 것으로 판단된다.
Table 3.
Prevention of fungal degradation of cellulose nanofibril with sodium azide
| C. albicans | A. niger |
|---|
| No sodium azide | +++ | +++ |
| Sodium azide | 1.0% | ++- | --- |
| 2.0% | +-- | --- |
| 3.0% | --- | --- |
아지드나트륨이 첨가된 셀룰로오스 나노섬유 현탁액의 오염 후 점도 감소 효과를 Fig. 5에 나타내었다. 측정결과 C. albicans의 경우 다른 보존제에 의한 점도 저하 그래프와 비슷하게 점도 감소가 크지 않았다. 하지만 A. niger의 경우 잔류하는 미생물이 확인되지 않았지만, 배양 기간 살아있는 미생물이 분비하는 효소에 의해서 셀룰로오스가 분해되어 점도 저하가 발생한 것으로 판단된다. 아지드나트륨을 2% 이상 첨가할 경우 A. niger의 효소 등의 물질 분비가 억제되어 점도 감소 효과가 적어진 것으로 판단된다. A. niger의 경우 아지드나트륨에 의한 점도 저하 방지 효과는 다른 보존제에 비해 떨어지는 것으로 확인되었다.
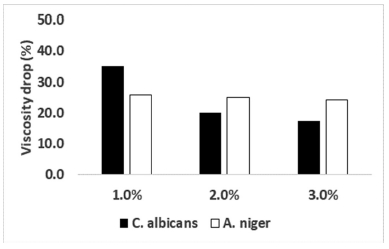
Fig. 5.
Viscosity drop by fungal degradation of sodium azide added cellulose nanofibril suspension with by C. albicans and A. niger.
4. 결 론
본 연구에서는 셀룰로오스 나노섬유 현탁액의 진균에 의한 오염에 따른 점도 저하와 이를 방지하기 위한 보존제를 사용하여 진균에 의한 오염을 방지하고자 하였다. 셀룰로오스 나노섬유 현탁액을 진균 오염에 노출시킨 결과 C. albicans와 A. niger 모두 점도가 저하된 것이 확인되었으며, 이를 방지하기 위해 보존제가 필요함을 확인하였다.
보존제를 첨가한 셀룰로오스 나노섬유 현탁액을 진균 오염에 노출시켰을 때, 페녹시에탄올을 첨가했을 때, 진균의 성장이 가장 낮은 것이 확인되었다. 특히 A. niger에 비해 C. albicans의 성장을 막기 위해서는 페녹시에탄올을 제외하고 다른 보존제를 2% 이상 첨가하여야 성장이 제한받는 결과를 얻을 수 있었다. 진균의 종류에 따라 다르지만, 오염 현상과 점도 저하를 막기 위해서는 모든 보존제를 2% 이상 첨가해야 할 것으로 판단된다.
Acknowledgements
이 논문은 2018학년도 충북대학교 연구년제 사업의 연구비 지원에 의하여 연구되었음.
Literature Cited
T. Hsu, R. Ladisch and G. Tsao, Chemical Technology,
Alcohol from cellulose,
10(5); 315-319 (1980)
Hsu, T., Ladisch, R., and Tsao, G., Alcohol from cellulose, Chemical Technology 10(5): 315-319 (1980).
P. Alvira, E. Tomás-Pejó, M. J. Ballesteros and M. J. Negro, Bioresource Technology,
Pretreatment technologies for an efficient bioethanol production process based on enzymatic hydrolysis: A review,
101(13); 4851-4861 (2010)
Alvira, P., Tomás-Pejó, E., Ballesteros, M. J., and Negro, M. J., Pretreatment technologies for an efficient bioethanol production process based on enzymatic hydrolysis: A review, Bioresource Technology 101(13):4851-4861 (2010).
10.1016/j.biortech.2009.11.093D. T. Jones and D. R. Woods, Microbiological Reviews,
Acetone-butanol fermentation revisited,
50(4); 484-524 (1986)
Jones, D. T. and Woods, D. R., Acetone-butanol fermentation revisited, Microbiological Reviews 50(4):484-524 (1986).
J. C. Parajo, J. L. Alonso and V. Santos, Process Biochemistry,
Lactic acid from wood,
31(3); 271-280 (1996)
Parajo, J. C., Alonso, J. L., and Santos, V., Lactic acid from wood, Process Biochemistry 31(3):271-280 (1996).
10.1016/0032-9592(95)00059-3D. Y. Kim, S. C. Yim, P. C. Lee, W. G. Lee, S. Y. Lee and H. N. Chang, Enzyme and Microbial Technology,
Batch and continuous fermentation of succinic acid from wood hydrolysate by Mannheimia succiniciproducens MBEL55E,
35(6-7); 648-653 (2004)
Kim, D. Y., Yim, S. C., Lee, P. C., Lee, W. G., Lee, S. Y., and Chang, H. N., Batch and continuous fermentation of succinic acid from wood hydrolysate by Mannheimia succiniciproducens MBEL55E, Enzyme and Microbial Technology 35(6-7):648-653 (2004).
10.1016/j.enzmictec.2004.08.018Y. Sun and J. Cheng, Bioresource Technology,
Hydrolysis of lignocellulosic materials for ethanol production: A review,
83(1); 1-11 (2002)
Sun, Y. and Cheng, J., Hydrolysis of lignocellulosic materials for ethanol production: A review. Bioresource Technology 83(1):1-11 (2002).
10.1016/s0960-8524(01)00212-7A. Šturcová, G. R. Davies and S. J. Eichhorn, Biomacromolecules,
Elastic modulus and stress-transfer properties of tunicate cellulose whiskers,
6(2); 1055-1061 (2005)
Šturcová, A., Davies, G. R., and Eichhorn, S. J., Elastic modulus and stress-transfer properties of tunicate cellulose whiskers, Biomacromolecules 6(2):1055-1061 (2005).
J. A. Shatkin, T. H. Wegner, E. T. Bilek and J. Cowie, TAPPI Journal,
Market projections of cellulose nanomaterial-enabled products-Part 1: Applications,
13(5); 9-16 (2014)
Shatkin, J. A., Wegner, T. H., Bilek, E. T., and Cowie, J., Market projections of cellulose nanomaterial-enabled products-Part 1: Applications, TAPPI Journal 13(5):9-16 (2014).
J. Cowie, E. T. Bilek, T. H. Wegner and J. A. Shatkin, TAPPI Journal,
Market projections of cellulose nanomaterial-enabled products-Part 2: Volume estimates,
13(6); 57-69 (2014)
Cowie, J., Bilek, E. T., Wegner, T. H., and Shatkin, J. A., Market projections of cellulose nanomaterial-enabled products-Part 2: Volume estimates, TAPPI Journal 13(6):57-69 (2014).
J. G. Wijman, P. P. de Leeuw, R. Moezelaar, M. H. Zwietering and T. Abee, Applied and Environmental Microbiology,
Air-liquid interface biofilms of Bacillus cereus: Formation, sporulation, and dispersion,
73(5); 1481-1488 (2007)
Wijman, J. G., de Leeuw, P. P., Moezelaar, R., Zwietering, M. H., and Abee, T., Air-liquid interface biofilms of Bacillus cereus: Formation, sporulation, and dispersion, Applied and Environmental Microbiology 73(5):1481-1488 (2007).
10.1128/aem.01781-06K. Huttunen, A. Hyvärinen, A. Nevalainen, H. Komulainen and M. R. Hirvonen, Environmental Health Perspectives,
Production of proinflammatory mediators by indoor air bacteria and fungal spores in mouse and human cell lines,
111(1); 85-92 (2003)
Huttunen, K., Hyvärinen, A., Nevalainen, A., Komulainen, H., and Hirvonen, M. R., Production of proinflammatory mediators by indoor air bacteria and fungal spores in mouse and human cell lines, Environmental Health Perspectives 111(1):85-92 (2003).
10.1289/ehp.5478L. E. Berghem and L. G. Pettersson, European Journal of Biochemistry,
The mechanism of enzymatic cellulose degradation: Purification of a cellulolytic enzyme from Trichoderma viride active on highly ordered cellulose,
37(1); 21-30 (1973)
Berghem, L. E. and Pettersson, L. G., The mechanism of enzymatic cellulose degradation: Purification of a cellulolytic enzyme from Trichoderma viride active on highly ordered cellulose, European Journal of Biochemistry 37(1):21-30 (1973).
10.1111/j.1432-1033.1973.tb02952.xJ. H. Garbutt, Essentials of food microbiology; 20, In The Naming, London, U.K.. Classification and Identification of Micro-Organisms. (1997)
Garbutt, J. H., Essentials of food microbiology, In The Naming, Classification and Identification of Micro-Organisms, London, U.K., p. 20 (1997).
D. J. Wohlbach, A. Kuo, T. K. Sato, K. M. Potts, A. A. Salamov, K. M. LaButti and S. Lucas, Proceedings of the National Academy of Sciences,
Comparative genomics of xylose-fermenting fungi for enhanced biofuel production,
108(32); 13212-13217 (2011)
Wohlbach, D. J., Kuo, A., Sato, T. K., Potts, K. M., Salamov, A. A., LaButti, K. M., and Lucas, S., Comparative genomics of xylose-fermenting fungi for enhanced biofuel production, Proceedings of the National Academy of Sciences 108(32):13212-13217 (2011).
10.1073/pnas.1103039108A. A. Hasper, J. Visser and L. H. de Graaff, Molecular Microbiology,
The Aspergillus niger transcriptional activator XlnR, which is involved in the degradation of the polysaccharides xylan and cellulose, also regulates d-xylose reductase gene expression,
36(1); 193-200 (2000)
Hasper, A. A., Visser, J., and de Graaff, L. H., The Aspergillus niger transcriptional activator XlnR, which is involved in the degradation of the polysaccharides xylan and cellulose, also regulates d-xylose reductase gene expression, Molecular Microbiology 36(1):193-200 (2000).
10.1046/j.1365-2958.2000.01843.xP. Gilbert, G. Beveridge and P. B. Crone, Journal of Pharmacy and Pharmacology,
The action of phenoxyethanol upon respiration and dehydrogenase enzyme systems in Escherichia coli,
28; 51 (1976)
Gilbert, P., Beveridge, G., and Crone, P. B., The action of phenoxyethanol upon respiration and dehydrogenase enzyme systems in Escherichia coli, Journal of Pharmacy and Pharmacology 28:51 (1976).
P. Gilbert, E. G. Beveridge and P. B. Crone, Microbios,
Effect of phenoxyethanol on the permeability of Escherichia coli NCTC 5933 to inorganic ions,
19(75); 17-26 (1977)
Gilbert, P., Beveridge, E. G., and Crone, P. B., Effect of phenoxyethanol on the permeability of Escherichia coli NCTC 5933 to inorganic ions, Microbios 19(75):17-26 (1977).
E.-Y. Choi, Asian Journal of Beauty and Cosmetology,
Effect of phenoxyethanol and alkane diol mixture on the anti-microbial activity and antiseptic ability in cosmetics,
13(2); 213-220 (2015)
Choi, E.-Y., Effect of phenoxyethanol and alkane diol mixture on the anti-microbial activity and antiseptic ability in cosmetics, Asian Journal of Beauty and Cosmetology 13(2):213-220 (2015).
S. J. Hwang, S. Park, J. K. Hwang and J. G. Pan, Letters in Applied Microbiology,
Food-grade antimicrobials potentiate the antibacterial activity of 1,2-hexanediol,
60(5); 431-439 (2015)
Hwang, S. J., Park, S., Hwang, J. K., and Pan, J. G., Food-grade antimicrobials potentiate the antibacterial activity of 1,2-hexanediol, Letters in Applied Microbiology 60(5): 431-439 (2015).
10.1111/lam.12398J. A. Jones, J. R. Starkey and A. Kleinhofs, Mutation Research-Genetic Toxicology,
Toxicity and mutagenicity of sodium azide in mammalian cell cultures,
77(3); 293-299 (1980)
Jones, J. A., Starkey, J. R., and Kleinhofs, A., Toxicity and mutagenicity of sodium azide in mammalian cell cultures, Mutation Research-Genetic Toxicology 77(3):293-299 (1980).
10.1016/0165-1218(80)90064-6M. F. Ibrahim, S. Abd-Aziz, M. E. M. Yusoff, L. Y. Phang and M. A. Hassan, Renewable Energy,
Simultaneous enzymatic saccharification and ABE fermentation using pretreated oil palm empty fruit bunch as substrate to produce butanol and hydrogen as biofuel,
77; 447-455 (2015)
Ibrahim, M. F., Abd-Aziz, S., Yusoff, M. E. M., Phang, L. Y., and Hassan, M. A., Simultaneous enzymatic saccharification and ABE fermentation using pretreated oil palm empty fruit bunch as substrate to produce butanol and hydrogen as biofuel, Renewable Energy 77:447-455 (2015).
10.1016/j.renene.2014.12.047








