1. 서 론
시설원예의 주요 자재인 피트모스와 암면(rock wool)을 대체하는 원예용 상토의 50% 이상을 차지하는 코코피트(Cocopeat)는 스리랑카, 인도네시아,필리핀 등의 국가로부터 수입이 용이하고, 적용성과 경제성 등이 우수하여, 국내 시설원예 면적의 급격한 증가와 함께 그 사용량도 크게 늘어나고 있다.1-3) 코코피트는 코코넛껍질(coconut husk) 부위에서 섬유질인 코코넛섬유질을 추출한 후 생기는 코코넛분진(coconut dust)과 파쇄, 팽윤-수침, 제선, 분리, 그리고 건조 등과 같은 물리화학적 과정을 거쳐 생산된 것을 의미한다. 그러나 생산국에 따라 기후 조건과 생산시기, 가공방법이나 인프라 등 생산환경에 따라 코코피트의 물리적 화학적 특성과 품질은 차이가 크다.4-6)
코코넛(Coconut)은 종려목 야자과(Coco nuciferu Linn)에 속하는 야자나무의 과일로서 핵과에 해당하는 코코넛 알맹이(coconut kernel)와 껍질에 해당하는 코코넛껍질로 분리한다. 코코넛껍질은 코코넛섬유질(co-conut fiber)과 해면상의 교질 성분인 코코넛분진(co-conut pith, dust)으로 구성되며 구조는 최외부에 섬세하고 얇은 섬유층이 있고 그 내부로 2-5 cm 두께를 갖는 치밀한 섬유층을 형성하고 있다. 조성을 살펴보면 유기물함량이 약 95%, 유기탄소는 약 29%, 구성성분을 살펴보면 Lignin이 약 41%, 그리고 셀룰로오스가 36-43% 정도를 차지하고 있으며 C/N율은 80-112 정도다.7,8)
일반적으로 건조중량 기준으로 코코넛껍질 전체 무게의 20-30%는 섬유이며 나머지는 중과피(pith)로 이루어져 있다. 그리고 분리공정과정에서 전단면에 30-300개 이상의 셀(cell)을 갖는 다중세포로 구성된 섬유(fiber)와 약 42%가 헤미셀룰로오스인 분진(dust)으로 분리된다.9,10) 그리고 섬유는 α-셀룰로오스와 Klason lignin이 각각 약 36.3%와 31.9%로 구성돼 있으나 중과피는 α-셀룰로오스와 Klason lignin이 각각 21.0%와 24.1%로 섬유에 α-셀룰로오스와 Klason lignin이 더 많이 존재한다.11) 코코넛껍질은 화학적 조성은 셀룰로오스 36-43%, 리그닌 41-45%, 헤미셀룰로오스 0.15-0.25%, 펙틴 3-4% 그리고 약간의 수용성 물질이 포함되어 있다. 한편 3-5개월 정도 기간이 소요되는 껍질(husk)의 팽윤 수침과정 중 코이어 속에 있는 탄닌과 염기성분이 제거되며 나머지는 2차로 작물재배 배지로 사용 기간 중 제거되어 코코피트의 구조와 화학적 특성도 변하는 것으로 알려져 있다.12) 그러나 코이어의 중요 구성요소인 셀룰로오스는 특이한 구조의 다당류로 미생물이나 자연 환경조건하에서 일어나는 화학적 반응에 의해 분해가 잘되지 않는다.
코코피트의 수분보유력은 분쇄된 코코피트 입자크기, 타 소재와 혼합비율과 사용기간에 따라 변하고 유효수분함량은 포화 후 시간이 지남에 따라 급격히 감소하여 유효수분함량은 토양에 비하여 낮다. 그러나 포화수리전도도는 코코피트의 사용기간이 증가함에 따라 감소하나 포장용수량 상태의 수분보유력은 증가한다.12) 한편 양이온교환용량을 기준한 양분보유력은 토마토 자루배지재배로 3년 정도 사용한 코코피트의 경우 CEC는 사용 전에 비하여 약 2.5배 정도 증가한다. 그러나 식물재배생육기준인 전기전도도는 초기에 비하여 1년간 사용한 경우 약 50% 정도로 감소하나 이후 3년 정도 연속으로 사용하더라도 EC값은 크게 변하지 않는 것으로 조사되었다.12) 한편 농가에서는 코코피트를 식물재배 배지로 다년간 사용하고 있으나 사용기간이 길어질수록 재배하는 작물의 품질이 저하될 뿐만 아니라 수량이 급격히 감소하는 문제점이 발생하고 있다. 그러나 시설원예에서 코코피트를 장기간 배지로 사용할 경우 발생하는 코코피트의 물리성과 화학성 변화 등에 대한 연구는 매우 미미하다.5,12) 따라서 본 연구에서는 코코피트를 시설원예용 배지로 사용할 때 발생하는 재배 작물의 품질 저하와 수량감소 등의 문제점을 구명하기 위하여 토마토를 재배한 시험포장에서 사용기간별로 코코피트 시료를 채취하여 코코피트 내 구성성분의 함량변화에 따른 코코피트의 구조와 화학성 변화를 조사하였다.
2. 재료 및 방법
2.1 공시재료
본 실험에서 사용한 코코피트 시료는 충청남도 부여에 위치한 부여 토마토시험장에서 사용한 토마토 양액재배용 코코피트 자루배지로 재배전부터 재배연도별로 3년간 매년 시료(시험전: NW, 1년차: 1st, 2년차: 2nd, 3년차: 3rd)를 채취하여 사용하였다. 시료채취는 연도별로 2회(토마토 정식 후 10주차 직후와 최종 수확 후인 20주차)에 걸쳐 5개의 토마토재배베드에서 임의로 2개씩 총 10개의 자루배지를 선정하여 균질하게 혼합한 후 원추 4분법으로 각 2 kg씩 4개의 시료를 채취하여 그늘에서 풍건하였다. 그리고 Wiley Mill을 이용하여 2 mm 이하로 분쇄한 후 분쇄한 시료를 증류수를 이용하여 3회 세척하여 이물질과 먼지 등을 제거하고 환풍건조기에서 60°C에서 약 72시간 정도 완전 건조하였다. 그리고 다시 건조한 시료를 5% NaOH 용액에 약 30분 정도 침지하였다가 이를 증류수로 10회 정도 세척하여 시료에 흡착된 양이온을 제거하였다. 이와 같은 과정을 거쳐 제조한 시료를 환풍건조기에서 60°C에서 약 48시간 정도 건조하여 4°C 저온저장고 저장하여 분석에 사용하였으며 모든 실험은 3반복으로 실시되었다.
2.2 코코피트 특성 분석
건조 후 저온저장고에 저장하였던 시료 중 년차별로 최종 수확 후에 채취한 시료를 채취하여 ESEM-TMP (XL30 Philips, USA)를 이용하여 코이어 구조를 조사하였다. 코코피트의 화학적 조성조사는 년차별 10주와 20주차 시료를 채취하여 TAPPI Standard Method T 264 cm-88에 따라 시료 10 g을 취하여 독일 Merck사 Quickfit 속시렛에 부피비로 벤진(benzene)과 에탄올(ethanol)을 2:1로 혼합한 용액을 6시간 동안 가하여 왁스와 기타 물질을 추출하였다.13) 그리고 TAPPI Stan-dard Method T 212 cm-93 방법으로 α-셀룰로오스를, T249-75 방법으로 홀로셀룰로오스(holocellulose)를 그리고 T 203 os-74와 T 211 cm-93 방식에 따라 리그닌과 재(ash)함량을 조사하였다. 셀룰로오스와 헤미셀룰로오스의 표준물질은 Sigma Aldrich에서 셀룰로오스 단당류로 순도 98% 이하인 D(+) glucose와 헤미셀룰로오스 단당류는 순도 98% 이하인 D(+) xylose, D(+) man-nose, D(+) arabinose, D(+) galactose를 구입하여 사용하였다. 셀룰로오스함량은 시료 2차분해 여과액에 CaCO3를 첨가하여 pH 5-6 범위로 중화한 후 HPLC-RID 1200(Agilent, USA)을 이용하여 정량분석하였다. HPLC Column은 BioRad Aminex, HPX-87P 300×7.8 mm를 이용하였다.
시료의 화학성 분석은 농촌진흥청식물·토양분석법에 준하여 pH와 EC는 1:5 포화침출법으로 pH 미터와 EC 미터를 이용하여 조사하였으며,14) 양이온교환용량(cat-ion exchange capacity, CEC)은 1M 암모니움아세테이트(NH4OAc)법으로 유기물함량(OM)은 Walkley-Black으로 조사하였다. 양이온 및 음이온의 분석은 pH 및 전기전도도(electrical conductivity, EC) 측정에서 얻은 포화침출용액을 사용하였으며, 음이온은 Ion chroma-tography(Dionex mod. DX-500, USA)로 양이온은 ICP-OES(Spectroflame mod. GBC Integra XM, EU)를 이용하여 분석하였다.
3. 결과 및 고찰
3.1 구조와 화학적 조성
본 연구에 사용한 공시시료의 구성물질을 조사한 결과 셀룰로오스와 리그닌의 함량은 무게비로 각각 40.7%와 41.3%를 차지하였다. 이외 펙틴, 수용성물질, 그리고 헤미셀룰로오스가 각각 3.0, 4.29 그리고 0.23%였으며 무기물질인 재(ash) 함량도 0.82%로 조사되었다(Table 1).
Table 1.
Composition of cocopeat sample used in this experiment (unit: %, wt wt-1)
| Sample | Cellulose | Hemicellulose | Lignin | Pectin | Water-soluble | Ash |
|---|---|---|---|---|---|---|
| New | 40.7 | 0.23 | 41.3 | 3.00 | 4.29 | 1.82 |
그리고 pH는 4.7로 산성에 해당하고, 전기전도도는 0.39 dS m-1, CEC는 71.0 cmolc kg-1 그리고 유기물함량은 96.2%인 것으로 조사되었다. 따라서 pH는 낮으나 높은 CEC로 인하여 대부분의 양이온은 코이어 표면에 흡착되어 있어 상대적으로 시료의 EC가 낮은 것으로 판단된다(Table 2).
3.2 사용기간별 구조와 화학적 변화
Fig. 1은 토마토 재배소재로 3년 동안 사용한 코코피트의 화학적 특성을 조사한 결과로 pH는 토마토를 재배하기 전인 시료(NW)는 4.47이었으나 사용 후 1년 후에는 6.47까지 증가하였다가 2년차와 3년차에는 각각 5.96과 4.76로 코코피트의 사용기간이 증가함에 따라 감소하였다. 이는 자루배지 상태로 토마토를 재배하여 코코피트가 자루배지내에서 반혐기상태로 분해가 진행되어 분해 중간산물이 옥살릭산과 같은 물질과 토마토재배 중 토마토 식물체 뿌리로부터 배출되는 산의 생성이 증가하였기 때문인 것으로 판단된다.
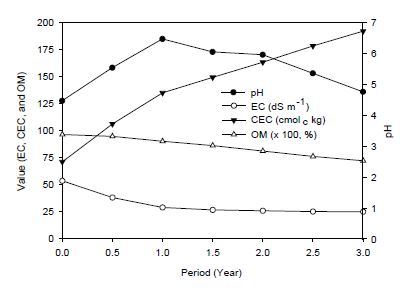
Fig. 1.
Changes of pH, EC, CEC, and OM of the cocopeat samples used as growth media for a tomato plant for three years of experimental period.
EC는 NW(53.5), 1st(22.2), 2nd(25.8), 3rd(24.9)로 사용기간이 증가함에 따라 급격하게 감소하였다. 특히 NW에서 1st로 사용기간이 증가하면서 초기 농도의 50% 정도로 급격하게 감소하고 이후 서서히 감소하였다. NW 코코피트시료의 EC가 53.5 dS m-1로 높은 것은 코코피트를 생산하는 과정 중 해수를 이용한 팽윤-수침과정 중에 해수의 염결정화합물이나 양이온 또는 음이온이 코코피트에 흡착돼 있던 것이 증류수로 추출하는 과정 중에 수용성상태로 전환된 것으로 판단되며 1st 이후 코코피트시료의 EC가 22 dS m-1와 이상으로 높은 것은 토마토재배 기간 동안 지속적으로 양액이 공급되어 코코피트에 흡착되었기 때문인 것으로 판단된다. CEC는 NW가 71.0 cmolc kg-1로 가장 낮았으나 1st는 134.7 cmolc kg-1, 2nd는 149.0 cmolc kg-1, 3rd는 191.7 cmolc kg-1로 사용연수가 증가함에 따라 점진적으로 증가하였다. 이는 코코피트의 사용년도가 증가함에 따라 코코피트의 구조가 파괴되어 코코피트의 표면전하가 증가하였을 뿐만 아니라 코코피트 중과피내에 박막층이 형성되면서 상대적 표면적이 증가하기 때문인 것으로 추정된다. 유기물함량은 NW가 96.2%로 가장 높게 나타났으며, 1st는 93.5%, 2nd는 81.9%, 3rd는 82.0%로 점점 감소하는 것으로 나타났다. 이는 식물이 재배되면서 섬유와 중과피를 채우고 있던 헤미셀룰로오스와 셀룰로오스와 같은 유기물의 분해가 진행되어 유기물함량이 감소하게 된 것으로 판단된다(Fig. 1).
Fig. 2는 사용년도별로 채취한 코코피트의 표면구조를 ESEM으로 조사한 결과로서 시험 전 시료(NW)의 시료표면은 셀룰로오스, 헤미셀룰로오스, 펙틴, 그리고 리그닌과 같은 복합 합성물질로 채워진 부분과 기공이 분명하게 관찰되었다. 그러나 코코피트의 사용기간이 1년차, 2년차로 증가함에 따라 코코피트 표면에 존재하던 세포벽이 분해되어 세포가 격리되는 현상이 관찰되었다. 그리고 3년차의 경우 코코피트의 표면을 구성하고 있던 복합 합성물질이 거의 사라지고 해면골격구조가 관찰되었다. 코코피트에서 다세포로 구성된 섬유는 펙틴에 의해 서로 결합되나 산이나 효소에 의해 쉽게 분해되는 특성에 의해 세포가 쉽게 격리된다.14) 또한 Alberts 등(2002)과 Kalia 등(2011)이 제시한 코코피트의 구조에서 보는 바와 같이 코코피트의 다중세포벽 구조와 세포벽과 세포간 층을 구성하고 있던 셀룰로오스, 헤미셀룰로오스, 펙틴 같은 복합 합성물질이 분해된 반명 분해저항성을 높은 리그닌과 같은 물질만 남았기 때문인 것으로 판단한다.15,16)
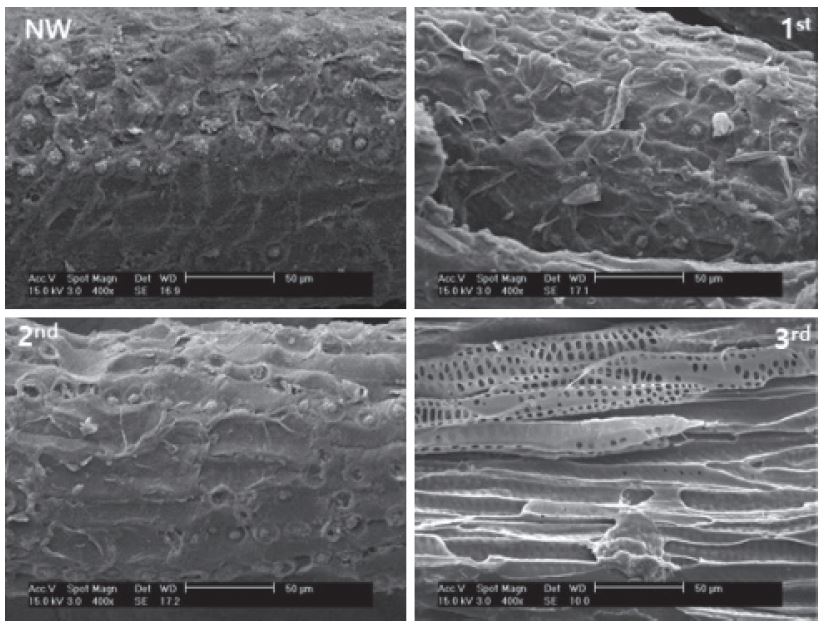
Fig. 2.
ESEM images of surface morphology of the coir fiver used as the tomato growth media for three years.
Fig. 2에서 살펴본 바와 같이 각각의 코코피트는 섬유와 섬유 사이에 존재하는 중간층으로 둘러 쌓여있으며 섬유조직은 1차와 3겹으로 구성된 2차세포벽으로 구성돼 있으며 이러한 섬유는 다발형태로서 각각의 섬유는 헤미셀룰로오스로 연결돼 있고 이러한 관다발형태의 섬유는 리그닌에 의해 공유결합으로 연결되어 있다. 이와 같은 코코피트 내 코이어섬유는 사용기간이 증가함에 따라 분해되기 쉬운 헤미셀룰로오스가 분해되어감에 따라 각각의 세포벽만 남게 되며(Fig. 3, 1st and 2nd), 3년차(3rd)의 경우 세포벽을 둘러싸고 있던 헤미셀룰로오스가 사라져 세포벽이 선명하게 구분되는 상태로 변하였다(Fig. 3).

Fig. 3.
ESEM images of surface cell morphology of the coir fiver used as the tomato growth media for three years.
한편 코코피트를 구성하는 코이어섬유는 리그노셀룰로오스(Lignocellulosic) 섬유구조로 리그닌과 헤미셀룰로오스로 연결된 결정구조(crystalline, highly ordered) 형태와 무정형(amorphous, disordered) 형태로 구분된다.14) 그러나 이러한 구조는 분명하게 구분되어 있지 않으며 셀룰로오스와 같이 질서있게 나열된 영역과 무정형형태의 섬유가 혼재한다.17) 본 조사 결과 코코피트내 코이어섬유의 전단면은 사용 전에는 기초섬유와 루멘이 물질 등으로 채워진 중심부만 관찰되다가 3년차의 경우 루멘을 채우고 있던 물질들이 소멸되며 중심부와 세포벽이 분명하게 관찰되는 구조로 변하였다(Fig. 4).

Fig. 4.
ESEM images of the cross-section of the cocopeat sample collected on NW and 3rd year from the tomato growth media.
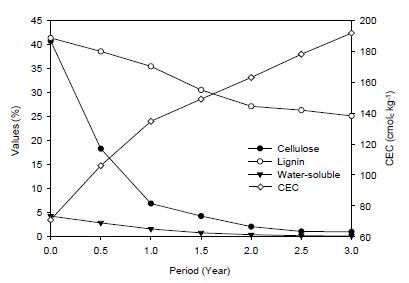
상기에서 살펴본 바와 같이 코코피트 표면구조 변화에 영향을 준 것으로 판단되는 셀룰로오스, 리그닌, 그리고 수용성 물질의 함량변화를 사용기간별로 조사한 결과(Fig. 5) 셀룰로오스함량은 NEW 40.7%에서 1년차 40.72%, 2년차 6.5%, 그리고 3년차 2.5%로 초기 대비 약 94% 정도의 셀룰로오스가 분해된 것으로 조사되었다. 그리고 리그닌 함량은 NEW 41.3%에서 1년차 33.2%, 2년차 25.4%, 그리고 3년차 25.1%로 초기 대비 약 40% 정도의 리그닌이 소멸된 것으로 조사되었다. 한편 NEW 시료에서 약 4.29%를 차지하였던 수용성물질도 3년차에는 0.15%로 약 97%가 감소하였다. 따라서 코코피트를 구성하는 리그닌이 셀룰로오스보다 분해 저항성이 높은 것으로 조사되었다. 따라서 코코피트 사용기간이 따른 코코피트의 구조는 리그닌 함량에 의해 결정될 것으로 판단되며 특히 코코피트의 사용기간이 증가함에 따라 양이온교환용량이 증가되는 것도 리그린의 분해에 따른 리그닌 구조표면에 생성되는 표면전하량이 증가하였기 때문인 것으로 추정된다.
4. 결 론
셀룰로오스와 리그닌 함량이 약 80%를 차지하고 있는 코코피트는 다중세포벽 구조의 복합구조물과 중과피로 이루어져 있다. 일반적으로 산성상태의 코코피트는 사용 초기에는 pH가 증가하나 사용기간이 증가할수록 작물재배 기간 중 수분함량 변화에 따른 배지의 분해상태나 작물의 생육 특성 등에 의해 pH는 다시 저하하는 경향을 보인다. 또한 사용기간이 증가함에 따라 유기물함량은 감소하나 CEC는 증가하였다. 이는 코코피트를 구성하는 구성물질의 분해가 증가함에 따라 유기물함량은 감소하나 반면 리그닌과 같은 물질의 분해가 증가되면서 코코피트내 표면전하가 증가하기 때문인 것으로 추정한다. 이러한 추정은 사용기간에 따른 코코피트의 구조변화를 통하여서도 추정이 가능하다. 코코피트를 구성하는 코이어는 헤미셀룰로오스와 리그닌 사이에 있는 다중세포벽, 섬유세포로 둘러싸인 세포내강(lumen), 박막층(lamella)으로 구성되어 있다. 사용연도별 코코피트의 구조변화를 살펴보면 세포벽을 둘러싸고 있던 헤미셀룰로오스가 사라져 중심부와 세포벽이 분명하게 관찰되는 구조로 변하였다. 결론적으로 코코피트의 구성물질의 분해조건에 따라 pH와 EC 변화가 결정되고 구성물질과 리그닌의 분해 정도가 코코피트내 전하량을 결정하는 요인으로 작용하여 CEC 등과 같은 화학성에 영향을 주는 것으로 판단된다.