1. 서 론
최근 국내 제지산업에서는 인쇄용지 제조에 사용되는 천연펄프 원료에 대한 원가 부담이 지속적으로 상승하고 있다. 이에 따라 이러한 문제를 부분적으로 해결하기 위해 재생펄프 활용에 관한 연구에 관심이 모아지고 있다. 재생펄프를 사용함으로써 천연펄프 섬유 원료에 대한 원가 부담을 줄일 수 있을 뿐만 아니라 펄프 생산에 투입되는 용수, 전력의 사용량을 절감함으로써 산림자원의 보호 및 사용량을 줄일 수 있다.1) 또한 폐지 자원을 재활용하는 것은 온실가스의 배출을 감소시키고 약품의 사용량을 감소시킬 수 있다는 측면에서 천연펄프를 생산하는 것 보다 환경 친화적인 산업으로 인식되고 있다. 하지만 재활용되는 폐지에는 스테이플, 클립, 모래, 잉크, 충전제, 염료, sticky 물질 등과 같은 각종 이물질들이 포함되어 있어 재활용 공정에서 이를 제거하기 위해서는 공정 운전의 어려움이 뒤따르며 다양한 문제점을 야기 시키고 있다.2) 이 중 대부분의 이물질들은 중량 클리너 및 스크린공정, 1차 탈묵공정 등을 통해 제거 되지만 일부의 잉크, 염료 및 sticky 물질들과 같은 이물질들은 입자의 크기가 작을 뿐만 아니라 섬유에 고착된 형태로 존재하기 때문에 제거하기 어려운 특징을 가진다.2) 이러한 문제를 해결하고 최종 제품의 품질을 개선시키기 위해 대부분의 재생펄프에서는 물리적·화학적 처리 공정을 거치고 있다. 일반적으로 탈묵펄프는 높은 물리적 특성을 필요로 하지 않기 때문에 추가적으로 고해 처리를 하지는 않지만, 탈묵펄프의 저하된 광학적 특성을 개선시키기 위해서는 표백 공정을 거쳐야 한다. 표백방법은 재생섬유 원료의 특징 및 표백제에 따라 크게 산화표백과 환원표백으로 나뉘며, 표백 공정에 따라서는 단일표백 공정과 다단표백 공정으로 나눌 수 있다. 주로 산화 표백제는 리그닌 발색단 내에 존재하는 carbonyl group, ethylenic group, aromatic ring의 이중결합을 개열시켜 구조를 변형시킴으로써 발색단을 감소시켜 백색도를 향상시키는 효과를 유도한다.3) 탈묵펄프에 사용되는 대표적인 산화 표백제는 과산화수소(H2O2)로서 사용하기 용이해 널리 이용되고 있다. 과산화수소를 사용해 표백할 경우 광학적 특성을 개선시킬 수는 있지만 과산화수소 표백 시 표백효율을 증가시키기 위해 첨가되는 알칼리에 의해 섬유가 손상되고 수율이 감소되는 현상이 나타나며, 이로 인해 환경부하가 증가되는 문제점을 야기한다.4,5) 반면, 탈묵펄프에 널리 적용되는 환원표백제는 산화표백제와 다르게 발색단의 이중결합을 개열시키는 것이 아니라 발색단의 불포화된 이중결합을 포화시킴으로서 발색을 억제하는 효과를 나타낸다.6) 탈묵펄프 표백에 널리 사용되는 환원표백제는 formamidine sulfinic acid ((H2N)2CSO2)와 sodium dithionite (Na2S2O4)으로 표백 효과가 우수하며 산화표백제 보다 섬유 손상이 적은 특징을 가지고 있다. 또한 이와 같은 환원표백제의 sulfinate(SO2-) 이온들에 의해 재생펄프 내에 존재하는 염료 성분인 azo group을 hydroazo group 또는 amine 형태로 환원시켜 저분자로 분해함으로써 발색단의 conjugation을 방해해 염료 색의 일부 또는 모두를 제거하는 특징을 가진다.7,8)
따라서 이와 같은 표백 특성을 바탕으로 본 연구에서는 탈묵펄프 표백 시 산화표백제로 사용되는 과산화수소와 환원표백제로 사용되는 FAS 및 차아황산나트륨을 이용해 단일 방식으로 표백하였을 때 표백제의 첨가량에 따라 개선되는 광학적 특성을 비교하여 표백효과를 평가하고자 하였다. 또한 회수된 폐수에는 표백약품 및 헤미셀룰로오스, 리그닌과 같이 탈묵펄프에서 용출되는 물질들이 포함9~11) 되어 있으며, 이와 같은 탈묵펄프의 성상에 따른 표백제의 종류와 첨가량에 따라 변화되는 표백공정에서의 환경부하 특성을 pH, 탁도, COD, 양이온 요구량 및 전기전도도 등을 측정하여 분석하였다.
2. 재료 및 방법
2.1 공시재료
2.1.1 펄프
본 실험에 사용된 재생펄프는 신문용지 제조공정에서 주원료로 사용되는 ONP를 국내 J 사로부터 분양받아 사용하였으며, 1차 탈묵과 정선과정을 거치고 표백 타워로 이송되기 전 단계인 스크류 프레스 공정 후단에서 채취한 탈묵펄프(백색도 56.54% ISO)를 공시재료로 사용하였다.
2.1.2 표백 약품
표백에 사용된 표백약품은 J 사에서 분양받은 산화표백제인 과산화수소(H2O2)와 환원표백제로 차아황산나트륨 (Na2S2O4)과 FAS ((H2N)2CSO2)를 공시 약품으로 사용하였다. 사용된 표백제의 기본 특성은 Table 1과 같다.
Table 1.
Basic properties of bleaching chemicals
과산화수소 표백 시 과산화수소의 활성을 높이기 위해 표백 전 첨가제로 NaOH를 과산화수소 대비 30%, Na2SiO3와 EDTA는 전건펄프 대비 각각 3%, 0.03%를 첨가하였다. 환원표백에서는 FAS 표백 시 FAS의 활성을 높이기 위해 FAS : NaOH를 1 : 0.5로 혼합해 사용하였고,12,13) 차아황산나트륨 표백제는 Sodium borohydride (SBH, NaBH4)와 Sodium bisulfite(SBS, NaHSO3)를 1 : 8 비율로 혼합하여 Sodium dithionite (Na2S2O4)를 제조하여 중환원 표백제로 사용하였다. 중환원 표백제가 제조되는 반응식은 [1]과 같다.14)
2.2 실험방법
2.2.1 표백 및 폐수채취
표백처리 시 전건 탈묵펄프 15 g을 polyethylene bag에 넣고 표백 조건별로 농도 10%가 되도록 표백약품 및 증류수를 첨가한 후 밀봉하였다. 표백은 항온수조 80℃ 조건에서 60 분 동안 실시하였다. 표백제로 사용된 약품의 종류와 첨가량은 Table 2와 같으며, 신문용지에 요구되는 백색도인 약 60%-ISO 이상이 되도록 첨가하였다. 표백 시 표백제가 고르게 분산되도록 매 10 분마다 혼합시켜 균일하게 하였다. 표백처리 후 발생하는 폐수를 분석하기 위해 GF/C 필터를 이용하여 여과된 폐수를 회수 하였다.
2.2.2 수초지 제조
표백 처리된 탈묵펄프는 RDA(retention and drainage analyzer)를 이용하여 평량 50±2 g/m2이 되도록 수초지를 제조하였다. 수초지 제조 시 미세분 및 장섬유의 보류도를 높이기 위해 microparticle을 이용한 보류시스템을 적용하였다. 이때 사용된 약품은 C-PAM 0.01% 및 Bentonite 0.05%를 1 : 5 비율로 혼합하여 사용하였다.
2.2.3 수초지 특성 분석
제조된 수초지는 KS M ISO 187에 따라 상대습도 50±2%, 온도 23±1℃로 조절된 항온·항습실에서 24 시간 이상 조습처리한 후 표준규격 KS M ISO 536에 의거하여 평량을 측정하였다.
광학적 특성으로서 백색도는 KS M ISO 6588-2에 의거하여 Elrepho(L&W, Sweden)를 이용하여 측정하였으며, 물리적 특성으로서 인장강도는 KS M ISO 1924-2에 의거하여 Tensile strength tester(L&W, Sweden)로 측정하였고, 제로스팬 인장강도는 KS M ISO 15361에 따라 측정(Pulmac Zero-Span TS-100) 하였다.
2.2.4 폐수의 특성 분석
2.2.4.1 전기전도도 및 pH
폐액 내 무기이온의 함량 변화를 확인하기 위해 전기전도도(ORION model 120)를 측정하였고, 표백제에 따른 폐수의 특성 변화를 확인하기 위해 pH(Orion model 1420 A)를 측정하였다.
2.2.4.2 탁도, SCODcr, Cationic demand 및 UV-spectrometer
폐수에 의한 환경부하를 평가하고자 표백처리 후 회수된 폐액을 1/10배로 희석시켜 탁도 (HACH, 2100P turbidimeter)를 측정하였다. 폐액에 존재하는 용해된 유기물질들의 화학적 산소요구량과 폐액 내에 존재하는 anionic trash를 확인하기 위해 Reactor Digestion Methods로 SCODcr(HACH, DR/2500 spectrophotometer)와 양이온 요구량(CAS)을 측정하였다. 또한, 폐액에 용존하는 리그닌의 함량을 비교하고자 각 폐액의 UV/VIS-Spectrum (Optizen POP)을 측정하여 흡광계수를 비교하였다.
3. 결과 및 고찰
3.1 표백방법에 따른 수초지의 광학적 특성 변화
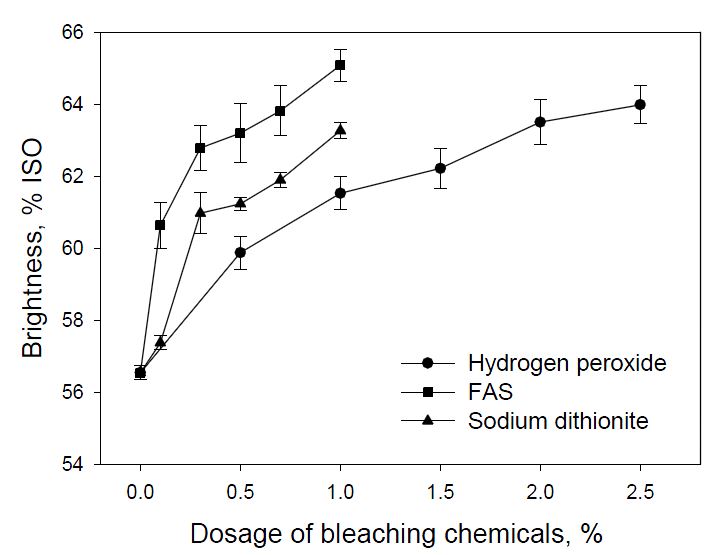
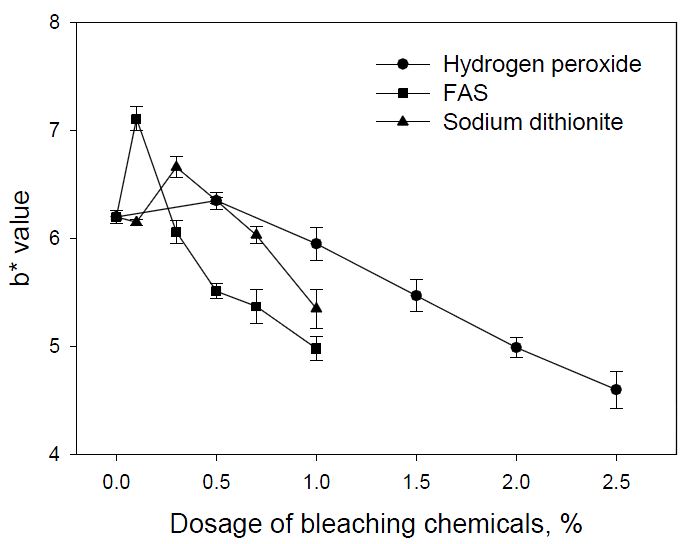
탈묵된 펄프의 광학적 특성을 개선시키기 위하여 과산화수소 (H2O2), FAS ((H2N)2CSO2) 및 차아황산나트륨 (Na2S2O4)의 첨가량을 증가시키며 표백을 실시한 결과 Fig. 1에서와 같이 표백제의 첨가량을 증가함에 따라 백색도는 상승하는 결과를 나타냈다. Fig. 1에서 산화표백제와 환원표백제의 백색도 개선 효과를 비교해 보면 환원표백제인 FAS와 차아황산나트륨이 산화표백제인 과산화수소 보다 우수한 표백 효과를 확인할 수 있었다. 이는 환원표백제들이 과산화수소를 이용한 산화제보다 펄프 내에 존재하는 리그닌과 염료들의 발색단을 효과적으로 억제시켜 발색을 비활성화 시키기 때문이다.7) 환원표백제에서 FAS와 차아황산나트륨의 표백효과를 비교해 보면 FAS의 백색도가 차아황산나트륨 보다 높은 값을 나타냈다. 이는 FAS의 sulfinate(>1100 mV) 이온이 차아황산나트륨의 dithionite (800 mV) 보다 강한 환원력을 갖기 때문에 Fig. 1에서와 같이 동일한 양의 표백제를 첨가하더라도 평균 백색도가 2%-ISO point 정도 높게 나타났다.7)Fig. 2의 결과를 살펴보면 표백제 첨가량이 증가함에 따라 b* value가 감소되는 경향이 나타났는데, 이는 DIP 내에 존재하는 TMP와 UKP와 같은 펄프에서 유발되었던 yellow 계열의 색상이 표백에 의해 감소됨에 따라 b* value가 감소된 것으로 판단된다. 각각의 표백제에 따른 백색도가 63% ISO 정도로 유사하게 나타나도록 표백제를 첨가하였을 때 b* value는 과산화수소 표백 시 4.99, FAS 5.51, 차아황산나트륨 5.35이 나타났다. 결과 값에 대한 차이는 크지 않지만 표백제에 따라 황 변화의 안정성에 있어 과산화수소가 다른 환원표백제 보다 안정적이라고 판단된다.
3.2 표백방법에 따른 수초지의 물성 변화
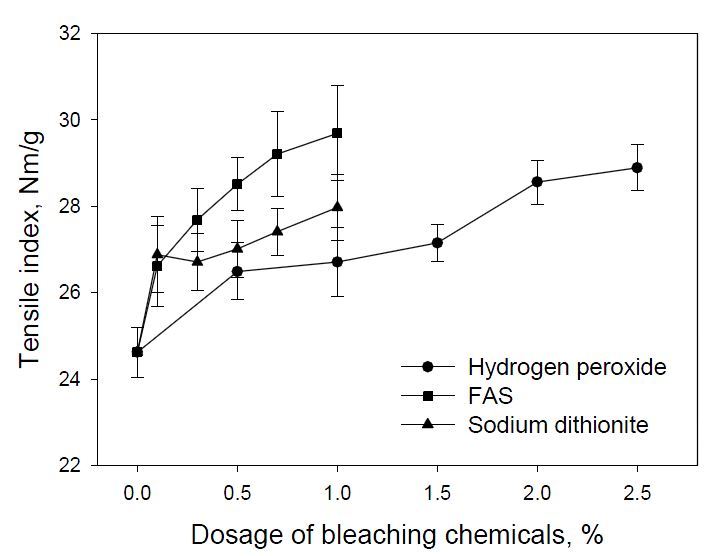
Fig. 3은 표백제 첨가량에 따른 수초지의 물성 변화를 확인하기 위해 측정한 강도적 성질의 결과이다. Fig. 3에서와 같이 표백제의 종류에 따라 인장강도 특성은 차이가 있었으며, 표백제 첨가량을 증가함에 따라 인장강도는 증가하는 경향을 나타냈다. 표백제에 따라서는 FAS 표백 시 가장 높은 인장강도가 나타났고 차아황산나트륨, 과산화수소 순으로 강도가 증가되는 것으로 나타났다. 이와 같이 표백제의 종류에 따라 인장강도 특성의 차이가 나타난 이유로서 탈묵펄프의 특성 변화가 주요 인자로 판단되며, 또한 탈묵펄프 내에 존재하는 염료가 강환원제에 의해 저분자화 되고 분해됨으로서 지필형성 과정에서 섬유간 결합력 개선에 따른 결과로 사료된다. 또한 표백 시 첨가된 가성소다에 의해 물리적 특성의 강도 변화가 유도된 것으로 판단된다. 표백 시 첨가되는 가성소다는 셀룰로오스 분자의 결정 사이에 팽윤을 일으켜 세포벽의 직경을 증가 시키면서 내강을 좁게 만들며, 섬유의 길이를 다소 감소시키는15) 특징을 갖기 때문이다. 이때, 섬유가 팽윤되어 표면에 고착된 일부분의 잉크 입자와 무기물들의 접착력이 약화되어 섬유로부터 박리되면서 섬유와 섬유 사이에 결합을 할 수 있는 면적 또한 증가하게 된다. 이와 같이 가성소다를 포함한 표백제의 첨가량이 증감됨에 따라 섬유간 결합이 증가하여 강도적 특성이 개선된 것으로 판단된다.
3.3 표백방법에 따른 폐수의 특성 변화
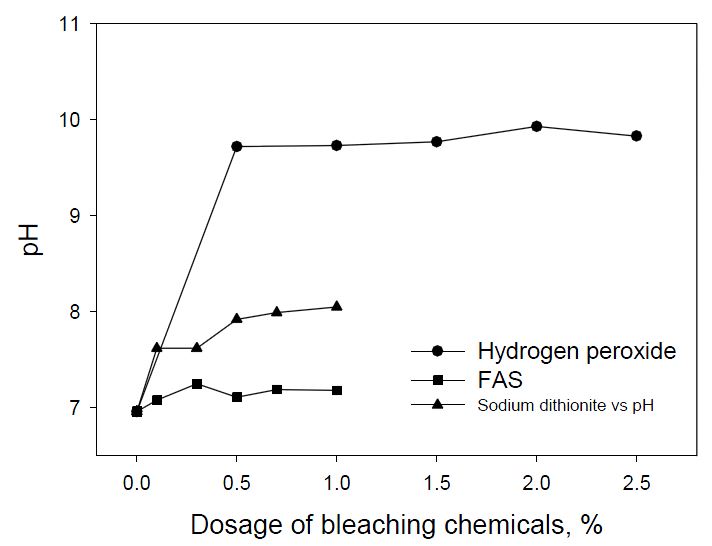
표백제의 첨가량과 종류에 따라 환경에 미치는 영향을 평가하고자 표백 후 회수된 폐수의 pH와 전기전도도를 측정하였다. Fig. 4에서와 같이 FAS를 사용하였을 경우, 표백 폐수의 pH는 약 8을 나타냈고, FAS의 경우에서는 첨가량에 따른 차이가 크게 나타나지 않았다. 이는 반응 식 [2]와 같은 반응으로 FAS의 sulfinate가 가성소다와 반응하여 강한 환원제가 만들어지고 반응 식 [3]에서와 같이 발색단이 환원되면서 생성된 요소(urea)와 아황산수소나트륨(sodium hydrogen sulfite)만 생성되어 pH 변화에 영향을 미치지 않은 것으로 판단된다.7)
차아황산나트륨의 경우 FAS와 달리 첨가량을 증가함에 따라 pH가 알칼리로 변화되는 경향이 나타났는데, 이는 차아황산나트륨 제조 시 혼합한 NaBH4와 NaHSO3에 의해 제조된 가성소다의 영향 때문으로 사료된다. 특히, NaBH4(sodium borohydride) 제조 시 식 [4]와 같이 NaBH4가 만들어지면서 부가적으로 반응 식 [5]와 같이 sodium methoxide가 물과 반응하면서 가성소다가 생성된다. 여기서 생성된 용액의 메탄올은 증발시키고 반응 식 [6]과 같이 NaHSO3가 첨가되면서 생성된 차아황산나트륨을 표백제로 사용하기 때문에 폐수에서도 알칼리성을 띄게 되는 것이며, 약품 첨가량이 증가함에 따라 알칼리성으로 변화되었다고 판단된다.7)
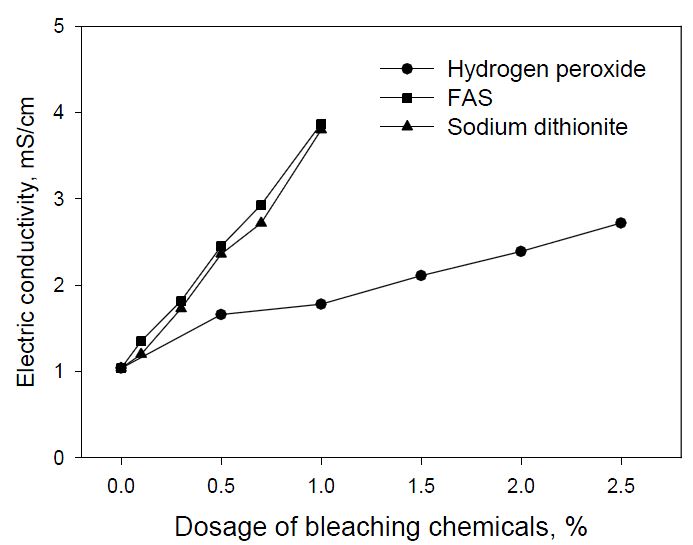
과산화수소 표백 후 회수한 폐액에서는 강알칼리 특성이 나타났는데, 이는 과산화수소 표백 시 첨가제로 첨가된 가성소다와 규산나트륨의 영향으로 판단된다. 과산화수소 표백 시 가성소다의 대부분은 perhydroxyl anion(HOO-)을 만들며 소모가 되지만, 규산나트륨은 물과 반응하여 hydroxide(HO-)를 만들어 표백 후에도 높은 알칼리 상태가 나타나게 되면서 강알칼리를 유지하도록 buffer solution 역할로 표백제의 투입량에 따른 pH의 변화가 크지 않은 것으로 나타났다. Fig. 5는 표백제에 따른 전기전도도 변화를 측정한 결과로서 환원 표백 시 표백제의 첨가량이 증가함에 따라 전기전도도가 높게 나타났고 환원표백제에 의한 결과는 유사하게 나타났다. 이처럼 유사한 결과가 나타난 이유는 환원 표백 후 발생하는 HSO3-, SO32-, HOS4- 이온들에 의한 영향이 큰 것으로 판단되며,17) 탈묵펄프 내에 존재하는 염료가 분해되면서 용해된 무기물들에 의한 높은 전기전도도가 나타난 것으로 사료된다. 과산화수소의 경우 표백 중 용출되는 일부의 리그닌, 헤미셀룰로오스, 지방산, 추출물 등의 유기물들에 의해 전기전도도가 완만하게 증가하는 경향이 나타났다.16)
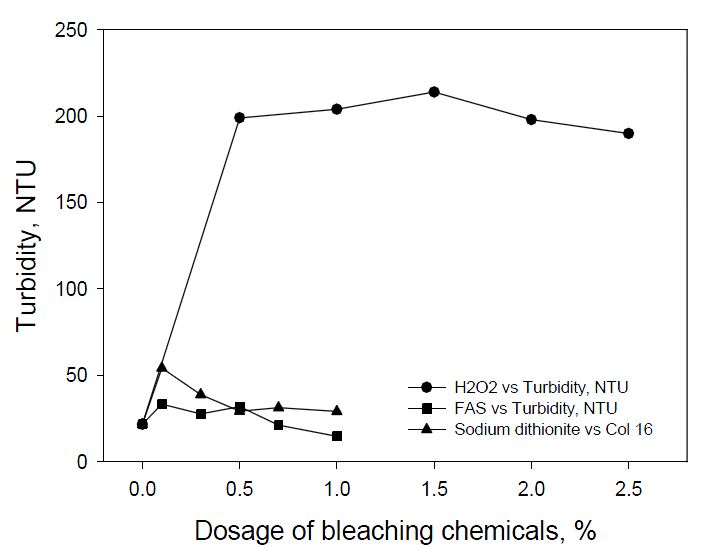
표백 폐수의 부유 또는 용존 이물질 등에 의한 탁도를 측정한 결과를 Fig. 6에 나타냈다. FAS와 차아황산나트륨을 이용한 환원표백에서 과산화수소를 이용한 산화표백보다 현저히 낮은 탁도 값을 나타냈다. 환원 표백제는 강한 환원력으로 인해 폐수에 존재하는 염료의 azo group을 hydroazo groups 또는 amine 형태로 저분자로 변화시켜 염료의 색을 부분적으로 또는 완전히 분해시킴으로써 발색의 효과를 억제하였기 때문이다.17) FAS를 이용한 폐수에서의 탁도는 표백제가 증가함에 따라 비교적 낮은 값을 나타냈는데, 이는 azo 염료가 화학 구조상 다른 발색단에 비해 쉽게 FAS에 의해 환원되기 때문이다. 특히, FAS는 강한 환원력으로 염료를 색도가 없는 aromatic amine의 형태로 분해시키는 특징을 가지고 있다.17) 반면 과산화수소의 경우, 표백 후 폐액 내에 펄프에서 용출된 리그닌, 헤미셀룰로오스, 지방산, 레진산과 같은 다량의 유기물뿐만 아니라 염료들이 그대로 남아 있어 높은 탁도 값이 나타난 것으로 사료된다.7)
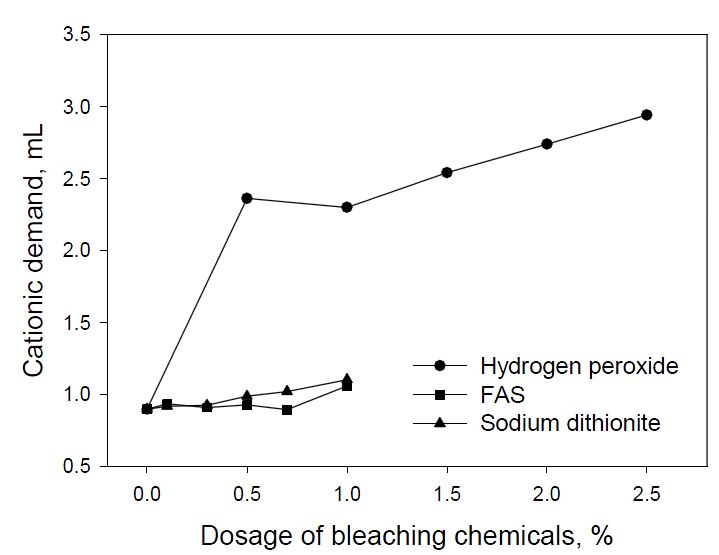
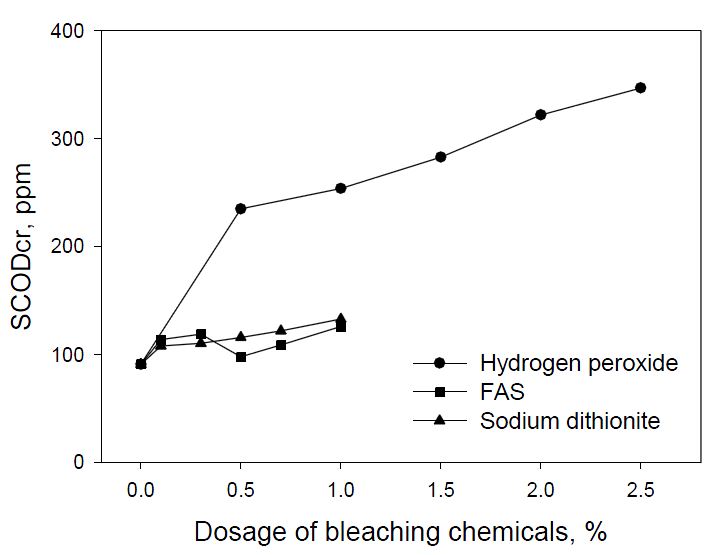
폐수에 용해된 유기물들의 양과 공정부하에 미치는 영향을 평가하기 위해 Fig. 7 및 8에서와 같이 양이온 요구량과 화학적 산소요구량을 측정하였다. Fig. 7에서 표백 전 양이온 요구량은 0.90 mL에서 과산화수소를 첨가함에 따라 증가하여 최대 2.94 mL까지 상승하였다. 반면, FAS와 차아황산나트륨을 첨가하였을 경우 양이온 요구량은 증가하였지만 각각 최대 1.06 mL, 1.10 mL로서 과산화수소에 비해 현저히 낮았다. 이와 같이 과산화수소 표백 시 양이온 요구량이 높게 나타난 것은 표백제에 의해 유기물 용출이 증가하였기 때문으로 사료된다. 이러한 거동을 확인하기 위해 Fig. 8에서와 같이 화학적 산소요구량(COD)을 측정한 결과 Fig. 7과 유사한 경향을 나타냈다. 따라서 과산화수소를 이용한 표백에서 약품 첨가량이 증가할수록 용해되는 유기물의 양이 증가되는 것을 확인 할 수 있었다. 반면 Fig. 8의 결과를 통해 환원표백 시 환원제에 의해 일부 유기물들이 용출된 것으로 사료된다.
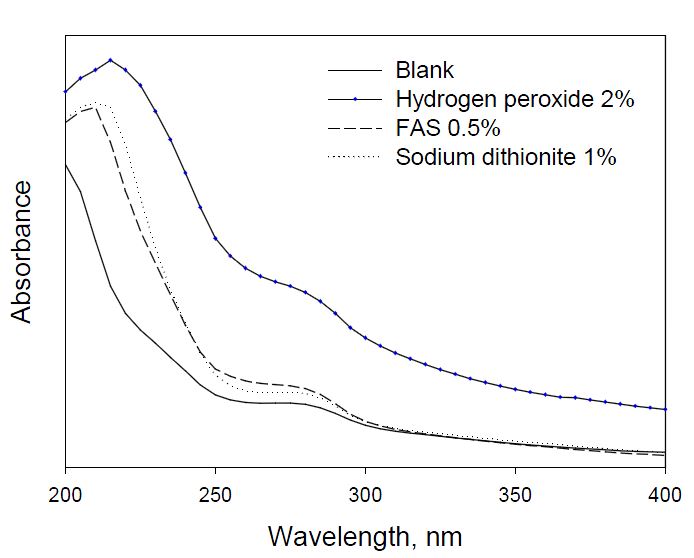
Fig. 9는 표백처리 하지 않은 탈묵펄프(백색도 56.3% ISO)를 표백제에 따라 백색도 63% ISO가 되도록 표백 시킨 후 회수된 폐수의 UV-spectrum을 나타낸 것이다. UV 280 nm 파장에서 리그닌의 주요 구조인 guaiacylglycerol-β-arylether,phenylcoumaran, pinoresinol, biphenyl, guaiacyl-α-arylether 등의 페닐프로판 또는 그 축합단위가 자외선을 흡수한다.18)Fig. 9에서 표백제에 의한 UV 흡광도를 살펴보면 과산화수소 표백 시 흡광계수가 가장 높게 나타났고, FAS와 차아황산나트륨을 이용한 환원표백에서는 과산화수소 보다 흡광계수가 낮게 나타났다. 이를 통해 환원표백을 진행하였을 때 보다 과산화수소 표백 시 일부 리그닌들이 분해되지 못한 상태로 폐액에 용출된 것으로 판단되며, 광학적 특성 변화에서와 같이 황변 현상에 안정적인 것으로 사료된다.
4. 결 론
본 연구에서는 표백제를 달리하여 탈묵펄프를 표백한 경우 나타나는 광학적·물리적 특성의 차이와 표백 후 발생 폐수의 성상 변화를 분석하였으며 그 결과는 다음과 같다.
1. 표백제에 따라 탈묵펄프를 표백한 결과 동일 첨가량 대비 FAS > Na2S2O4 > H2O2 순으로 광학적 특성이 개선되었다. 따라서, 단일 조건으로 표백할 경우 산화표백 방법보다 환원표백 방법이 적은 양의 표백제로 우수한 효과를 나타났다.
2. 물리적 특성으로서 FAS를 이용해 표백을 하였을 경우 가장 우수한 인장강도 특성을 나타냈고, 과산화수소를 이용하였을 경우 낮은 인장강도 결과를 나타냈다.
3. 표백된 폐수를 분석한 결과 과산화수소를 사용한 폐수에서 높은 pH, 탁도, COD, 양이온 요구량이 나타났지만, 전기전도도는 환원 표백제의 폐수 보다 낮은 값들이 나타났다. 따라서 과산화수소를 이용한 산화표백 시 높은 환경부하가 발생하는 것으로 판단된다.
4. FAS와 차아황산나트륨을 이용한 환원표백 시 탈묵펄프 내 잔존하는 리그닌뿐만 아니라 염료까지 분해시켜 표백이 이루어지기 때문에 과산화수소를 이용한 표백보다 낮은 탁도 값을 나타냈다. 그러나 표백 후 발생하는 황화물들에 의해 전기전도도는 높게 나타났다.
이상의 결과를 보았을 때 FAS와 차아황산나트륨을 이용한 환원표백이 과산화수소를 이용한 산화표백 보다 광학적·물리적 특성을 개선시키고, 환경부하를 감소시키는 것으로 나타났다. 하지만 환원 표백 시 황 이온들 발생시켜 또 다른 환경문제를 야기하고 있다. 따라서 환원표백으로 발생하는 황 이온들을 효과적으로 제어할 수 있는 기술이 연구된다면 보다 효율적으로 탈묵펄프를 표백할 수 있을 것으로 판단된다.