1. 서 론
에멀젼은 서로 섞이지 않는 두 액체 사이에 한 액체에 다른 액체가 콜로이드 상태로 퍼져 있는 용액이다. 두 개의 액체는 연속 용매와 용질 용매에 따라 여러 유화액의 종류를 형성한다. 에멀젼은 일반적으로 흰색을 띠는데 이것은 빛이 균일하게 산란되어 일어나는 현상이다.
에멀젼의 크기는 에멀젼화 처리에 사용되는 기계적 에너지, 계면활성제의 양, 두 가지 다른 수상과 유상의 점도의 영향을 받는다. 계면활성제를 첨가하여 에멀젼이 만들어질 때 미셀을 형성하기 위하여 사용되는 최소 계면활성제의 양을 미셀 생성 임계 농도(critical micell concentration, CMC)라고 부른다. 임계 농도 이상에서 구형의 미셀이 만들어지는데, 미셀의 모양은 계면활성제의 양, 수상과 유상의 비율에 따라 달라진다. 구형 미셀은 계면활성제의 농도가 높아지면 막대모양을 거쳐 수상층과 유상층으로 구별되는 층별 구조로 전환되기도 한다.
고 전단응력 에너지를 사용하면 입자크기를 50-500 nm로 줄일 수 있고 계면활성제, 저분자량 에멀젼 보조 안정화제를 사용하면 충돌과 분산에 의한 에멀젼의 파괴(Ostwald ripening)를 예방할 수 있다.1) 나노에멀젼은 열역학적으로 불안정하지만 에멀젼의 성분과 제조 방법에 따라 특성과 성질이 달라진다.2) 나노 에멀젼은 20-200 nm 정도의 입자크기이며 상대적으로 입도 분포도가 좁은 분포를 보인다.3) 이렇게 마이크론 크기 이하로 작아진 에멀젼은 친유성 약물의 정맥주사를 통한 유효 성분 전달에 효과적이기 때문에 약물전달 분야에서 관심이 증대되어 왔다.4) 나노에멀젼 제조 공정에서 계면활성제의 종류와 계면활성제의 첨가량이 입자크기에 영향을 미치며 계면활성제의 함유량이 17.5%일 경우 입자크기가 가장 작게 형성되었다.5)
셀룰로오스는 지구상에 가장 풍부한 천연 유기물이다. 생체 적합성이 높고, 생물학적 분해가 가능한 특성을 지니고 있어 복합 소재의 대체재로 사용이 가능하다. 셀룰로오스의 중합도(degree of polymerization; DP)는 약 10,000 정도이며 결정영역과 비결정영역이 교차 반복하는 연결되어 있는 구조이며 결정구조로 인하여 유연성과 강도적으로 우수한 성질을 나타낸다.6,7)
셀룰로오스는 글루코오스 단위로 구성된 섬유이며 이를 가공하여 수 나노 미터에서 수십 나노 미터의 폭을 갖는 물질을 만들 수 있으며 이를 나노셀룰로오스라고 정의한다. 최근 나노 셀룰로오스는 낮은 열 팽창, 높은 종횡비, 생분해성, 우수한 기계적 특성과 같은 다양한 특성을 가지고 있다. 나노셀룰로오스 특성을 바탕으로 포장, 바이오 의약, 접착제, 섬유, 전자 제품 및 자동차의 고분자 응용 분야에서 주목받고 있다.8,9)
셀룰로오스 나노섬유는 비표면적이 크기 때문에 수분 친화력이 크며 이런 성질을 화장품 보습 소재로 사용이 가능하다. 오일팜 수간의 셀룰로오스 나노섬유의 수분 유지력을 측정하여 화장품 보습제 특성을 분석하였으며,10) 목질계 자원으로 셀룰로오스를 추출하는 방법에 따라 셀룰로오스 나노섬유의 수분 유지력의 차이가 있다.11) 셀룰로오스 나노섬유의 특징적인 점탄성 성질을 화장품에 응용할 수도 있다. 셀룰로오스 나노섬유 현탁액의 레올러지 성질을 체계적으로 분류하였으며12) 이런 성질을 기반으로 동적상태에서 점도가 낮고 정적상태에 점도 높은 제형을 요구하는 화장품에 적용할 수 있다.
본 연구에서는 식품 공업에서 pickering 에멀젼화제로 사용가능성이 증가하고 있는 셀룰로오스 나노섬유를 화장품의 에멀젼 공정에 첨가하여 효능이 향상된 화장품 조성을 확인하고자 하였다. 기존 호모믹서로 만들어진 에센스에 1) 고압균질기 처리로 만든 나노 에멀젼 2) 셀룰로오스 나노섬유를 첨가하여 새롭게 만든 나노 에멀젼 3) 셀룰로오스 나노섬유 첨가와 고압균질기 작업으로 만든 나노 에멀젼을 각각 제조하여 화장품 제형 적용 가능성을 확인하고자 하였다.
2. 재료 및 방법
2.1 공시 재료
셀룰로오스 나노섬유를 제조하기 위한 원료는 무림P&P로부터 제공받은 활엽수 표백크라프트 펄프(Hardwood Bleached Kraft Pulp)를 사용하였다. 카르복시메틸화 반응에 사용한 시약은 수산화나트륨(96.0%, NaOH, 삼전화학), 염화아세트산 (98.0%, ClCH2COO-Na+, 삼전화학), 에탄올(95.0%, C2H5OH, 삼전화학)을 사용하였다. 나노 에멀젼에 사용한 에센스는 화이트코스팜(주)에서 제공받아 사용하였다.
2.2 실험 방법
2.2.1 셀룰로오스 나노섬유 제조13)
셀룰로오스 나노섬유를 제조하기 위해 활엽수 표백 크라프트 펄프에 카르복시메틸화 전처리를 실시하였다. 반응이 완료된 펄프는 흡인여과방법으로 세척하여 셀룰로오스 나노섬유 제조에 사용하였다.
셀룰로오스 나노섬유는 그라인더(Supermasscolloider; MKZA10-15Ⅳ, Masuko Sangyo, Japan)와 고압균질기(high pressure homogenizer; Panda plus, GEA, Italy)를 혼합사용하여 제조하였다. 전처리된 펄프를 1.5%(w/w)로 희석한 후 디스크(MKG-C 120#, Masuko Sangyo, Japan) 회전속도 1,000±60 rpm, 디스크 간격 200-250 μm 조건으로 그라인더를 총 3회 통과시켰다. 그라인더를 통과 후 800±50 bar 조건으로 고압균질기를 총 4회 통과시켜 셀룰로오스 나노섬유를 제조하였다.
2.2.2 에멀젼 처리
2.2.2.1 호모믹서를 사용한 에멀젼 제조
제공된 에센스를 교반하기 위하여 T 25 digital ULTRA-TURRAX (IKA, Germany)를 사용하였다. 셀룰로오스 나노섬유를 첨가한 경우 교반전에 셀룰로오스 나노섬유를 2.0% 첨가하였다(대조군-에센스의 교반, 비교군-셀룰로오스 나노섬유를 첨가후 교반하여 셀룰로오스 나노섬유의 호모믹서에서 교반효과 확인).
2.2.2.2 나노 에멀젼 제조
에센스의 나노 에멀젼화를 위해 고압균질기를 사용하였다. 제공받은 마스크팩 에센스에 균질기(Homogenizer, IKA, Germany)를 사용하여 8,000 rpm에서 충분히 분산시켰다. 분산된 에센스를 고압균질기(High-Pressure Homogenizer, Panda plus, GEA, Italy)에 500 bar로 총 3회 통과시켜 나노 에멀젼으로 제조하였다. 셀룰로오스 나노섬유를 첨가한 경우 균질기 처리 단계 이전에 첨가하였고 사용한 셀룰로오스 나노 섬유는 1.0%(w/w) 현탁액을 사용하였다(대조군: 기존 에센스의 나노 에멀젼화, 비교군-나노에멀젼화 공정에 셀룰로오스 나노섬유를 첨가하여 나노에멀젼공정에서 셀룰로오스 나노섬유의 효과를 확인).
2.2.3 분석
2.2.3.1 TEM 분석
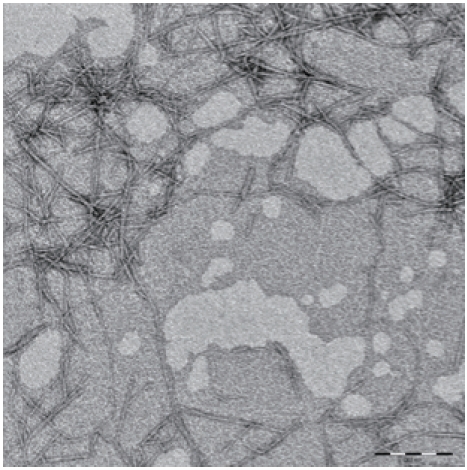
나노 셀룰로오스의 크기 측정을 위해 분산과 지지막 종류에 따른 투과전자현미경의 대면적 이미지를 확인하고자 하였다. 에너지 여과 투과전자현미경(Energy Filtering-Transmission Electron Microscopy, EF-TEM, 120 kV, Libra120, Carl Zeiss, Germany)을 이용해 glow discharge 처리를 25초간 15 mA에서 처리한 후 제조된 셀룰로오스 나노 피브릴 입자 간 상호작용을 최소화하기 위해 0.001%로 희석하였고, glow discharge 처리된 그리드 위에 고정 후 Uranyl acetate를 사용하여 음성염색을 실시하였다. 샘플링 후 바이오투과전자현미경(120 kV, Talos L120C, FEI, Czech)을 이용하여 8,500 배율에서 촬영된 대면적 이미지로 CNF의 크기를 측정하였다.
2.2.3.2 나노입도분석기 분석
제조된 나노에멀젼의 입자크기 분석을 위해 나노 입도분석을 실시하였다. 분석을 위해 나노에멀젼을 데시게이터에 넣은 후 진공펌프로 감압하여 탈기(degassing)를 8시간 실시하여 나노에멀젼 내 기포를 제거하였다. 기포가 제거된 나노에멀젼을 나노 입도분석기(Dynamic Light Scattering Spectrophotometer DLS-7000, Otsuka Electronics Co., Ltd. Japan)를 사용하여 분석을 실시하였으며, 나노 입도분석 조건은 분산매를 물로 설정한 후 30초 동안 입자 크기를 측정한 후 총 5회 반복하여 입자 크기를 분석하였다.
2.2.3.3 에멀젼 안정화도 측정
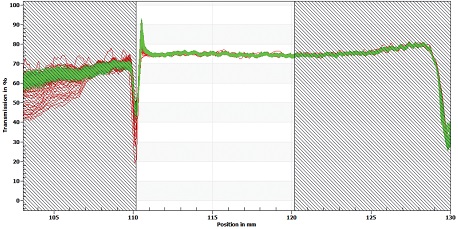
제조된 4가지 에멀젼의 안정화도를 분석하기 위하여 LUMiSizer® (LUM GmbH, Berlin, Germany)를 사용하였다. 제조된 에멀젼의 점도가 너무 높아 분석에 적합하지 않아, 증류수를 사용하여 농도를 1:1로 희석하여 측정하였다. 시료를 test tube에 넣고 4000 rpm의 속도로 50분간 회전시키면서 시료에 근적외선(Near IR light)을 10초 간격으로 투과시키고, 이때 투과된 빛의 세기변화(곡선의 기울기)를 시료의 분산 안정성을 측정하였다.
3. 결과 및 고찰
3.1 셀룰로오스 나노 섬유의 형태와 특성
본 연구에 사용한 셀룰로오스 나노섬유를 투과전자현미경으로 관찰하였다. 셀룰로오스 나노섬유의 폭은 5.3±2.0 nm의 분포를 보였으며 길이는 850±240 nm 이었다(Fig. 1).
3.2 셀룰로오스 나노섬유 첨가가 균질기 작업에서 에멀젼의 크기에 미치는 영향
선형의 셀룰로오스 나노섬유 고분자가 균질기 작업에서 에멀젼 입자크기에 영향을 미칠 것으로 생각하고 일반 호모믹서와 나노입자화 고압균질기에 각각 첨가하여 첨가한 것과 첨가하지 않은 것을 비교 분석하였다.
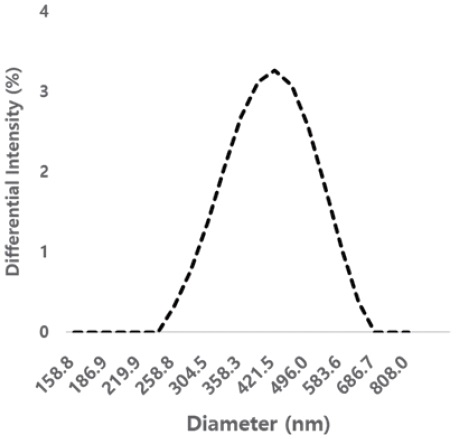
Dynamic Light Scattering를 사용하여 에멀젼의 입자크기를 측정하였다. 호모믹서를 사용한 교반으로 제조되어 분양받은 에멀젼의 크기는 422 nm이었지만 (Fig. 2) 셀룰로오스 나노섬유를 첨가하여 호모믹서로 교반한 에멀젼의 입자크기는 115 nm로 (Fig. 3) 셀룰로오스 나노섬유 첨가에 의해 평균 에멀젼 입자 크기가 감소된 것을 확인하였다. 교반 과정에서 선형 셀룰로오스 나노섬유가 에멀젼의 유동에 장애가 되어 에멀젼의 절단 현상이 일어난 것으로 추정된다.
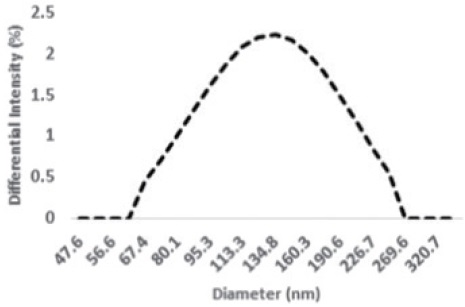
Fig. 3.
Particle size distribution of emulsion from homo-mixer with cellulose nanofiber (SA3) (average: 114.7±17.5 nm).
고압균질기를 사용한 교반에서 에멀젼의 크기는 138 nm이었으며(Fig. 4) 셀룰로오스 나노섬유를 첨가한 경우 16 nm의 평균 에멀젼 입자 크기를 나타내었다(Fig. 5). 호모믹서에 비하여 고압 균질기 작업을 한 것이 에멀젼의 입자 크기가 작았으며 이런 경향은 셀룰로오스 나노섬유를 첨가한 경우 더욱 뚜렷하게 나타났다.
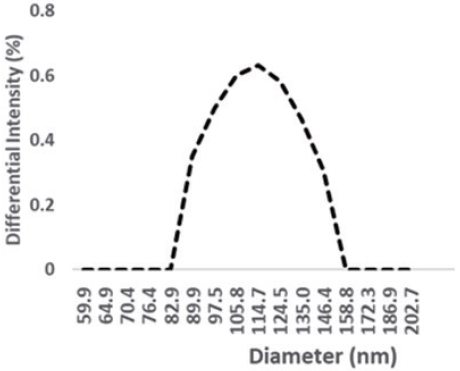
Fig. 4.
Particle size distribution of emulsion from high-pressure homogenizer (SA2) (average: 137.9±10.5 nm).
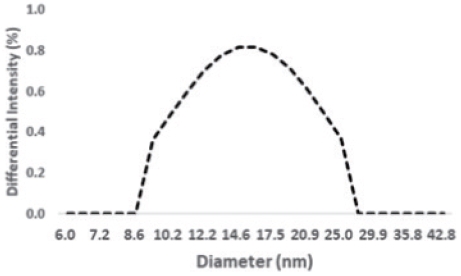
Fig. 5.
Particle size distribution of emulsion from high-pressure homogenizer with cellulose nanofiber (SA4) (average: 15.9±1.5 nm).
Wang 등은 식용등급 비온성 계면활성제를 사용한 에멀젼 입자 크기 조절에서 계면활성제의 종류와 첨가량으로 입자 크기조절이 가능하였으며 입자크기가 평균 50 nm 이하로 까지 만들 수 있었고 보고하였다.14) 이런 계면활성제를 사용한 에멀젼의 크기 조절은 계면활성제의 사용양이 많다는 단점이 있다. 나노 에멀젼의 장점은 유효물질 피부 전달을 위하여 에멀젼 입자크기가 작아지면 경계면에서 표면장력이 줄어들어 균일하게 퍼지며, 침투 능력이 향상된다. 또한 매우 작은 입자들은 브라운 운동을 활발하게 할 수 있어 중력에 의한 침강을 극복할 수 있다. 이런 현상은 크리밍이나 침강현상이 화장품의 유통기한 내에 일어나지 않게 한다. 또한 입자 크기가 작아지면 입자 간 응집도 예방할 수 있으며 상이 분리되지 않고 잘 분산되어 있게 유지시킨다. 또한 작아진 입자들은 효과적으로 유효성분을 피부에 전달시킬 수 있다.
에멀젼의 크기가 200 nm 이하인 나노 에멀젼은 여러 분야에 응용되고 있으며 다양한 장점을 가지고 있다, 콜로이드 입자의 장기 안정성이 향상되며 친수성이나 소수성 약물 전달물질의 가용화 능력이 향상되며 이로 인하여 치료 약물의 안정성이 향상된다. 또한 피부나 점막을 통한 전달 능력이 향상된다.15)
용해가 어려운 경구제 약품에서 나노입자 제형으로 변형시켜 약품의 전달력을 향상시킬 수 있다. 나노 현탁액제, 지방이나 고분자를 사용하는 나노 전달체 등의 기술이 적용되었다.16) 마이크론 단위 이하의 에멀젼 크림 제형을 통한 diazepam의 피부 전달 실험에서 피부전달력이 유상입자의 크기에 의존하였으며 고압균질기 사용하는 입자 크기가 현저하게 감소하였고 피부전달력이 급격하게 향상되었다.17) 유효 성분의 피부전달에서 수상 기반이나 유상 기반 에멀젼에 여부, 에멀젼 입자의 크기, 에멀젼화제뿐만 아니라 계면 구조(미셀, 액정)가 피부 및 경피 흡수에 영향을 미친다.18) 이런 피부 및 경피 흡수의 영향을 바탕으로 화장품 분야에 적용한 제품들이 설계되었다.
3.3 에멀젼 입자 분산 안정화도 측정
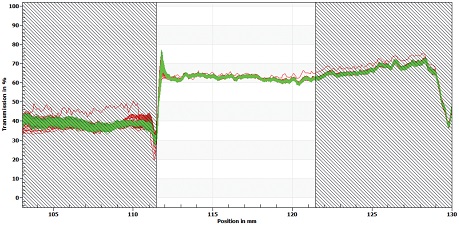
LUMiSizer analysis에 의한 분산 안정화도 측정은 시료에 근적외선을 조사하여 흡광되고 투과된 빛의 양(transmission)을 측정하여 분리되는 과정이 일어나는 물질의 분포를 확인하는 것이다 본 연구에서는 각각 만들어진 에멀젼의 안정화도를 4,000 rpm의 원심분리 조건에서 가라앉거나(sedimentation) 또는 뜨는 (creaming) 현상을 측정하여 얻어진 결과로 안정화 정도를 비교하였다. 각 시료의 측정값은 Fig. 6, 7, 8, 9에 제공하였고 이 측정으로부터 계산한 불안정화 지수(instability index)를 Fig. 10에 정리 비교하였다.
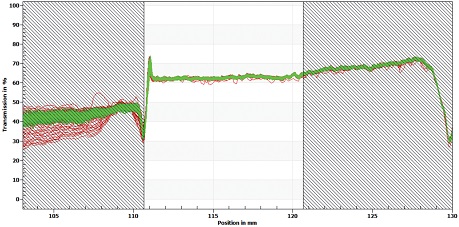
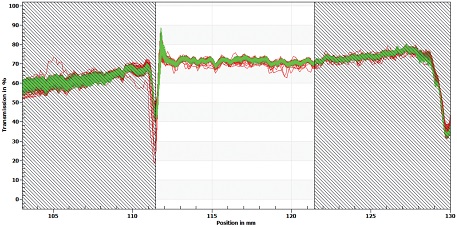
Fig. 9.
Emulsion stability of SA4 (emulsion from high-pressure homogenizer with cellulose nanofibril) by LUMiSizer analysis.
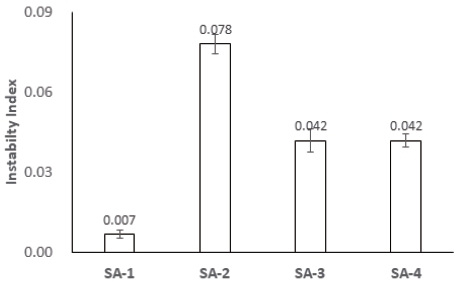
Fig. 10.
Instability index of 4 different emulsion products.
(1-2: Emulsion from homomixer (SA1),
2-2: Emulsion from high pressure homogenizer (SA2),3-3: Emulsion from homomixer with cellulose nanofibril (SA3),4-2: Emulsion from high pressure homogenizer with cellulose nanofibril (SA4))각 시료에 10초마다 빛을 조사하여 측정한 결과, 시료에서 크리밍이나 침강이 발생하지 않아 에멀젼은 안정한 상태인 것으로 생각된다. 하지만, 투과된 빛의 양을 나타내는 그래프에서 SA2가 시간에 따른 편차가 가장 크게 나타났고(Fig. 7), SA3(셀룰로오스 나노섬유 첨가와 homo-mixer 처리)과 SA4(셀룰로오스 나노섬유 첨가와 고압균질기 처리)에서는 구간의 편차가 작게 나타났다(각각 Fig. 8, Fig. 9). 이런 결과로 볼 때 셀룰로오스 나노섬유가 에멀젼의 물리적 안정성에 기여하는 것으로 판단된다.
불안정화 지수를 보여주는 Fig. 10에서 고압균질기를 사용하여 만든 에멀젼(SA2)의 수치가 가장 높았으나, 셀룰로오스 나노섬유를 첨가한 시료 SA4의 불안정화 지수는 0.042로 안정화도를 높였으며, 이는 셀룰로오스 나노섬유 첨가에 의한 점탄성의 증가와 부분적인 Pickering 에멀젼화에 의한 것으로 생각된다. 점탄성의 증가로 인한 단단해진 네트워크가 입자의 분산속도를 감소시켜 에멀젼의 안정화도를 증가시킨다.19) 이런 현상은 에멀젼에 실리카를 첨가하여 에멀젼의 입자크기와 연속상의 점탄성 성질을 개질하여 에멀젼의 안정화도를 향상시킨 경우20)와 유사한 경향을 보인다. 셀룰로오스 나노섬유를 첨가하여 입자의 크기를 감소시킨 경우 (SA1 vs SA3) 불안정화도가 증가하였으며 이것은 계면활성제의 양이 충분하지 않은 상태에서 입자크기의 감소 때문으로 판단된다.
4. 결 론
균질화 작업에서 셀룰로오스 나노섬유의 첨가가 입자크기에 미치는 영향을 탐색하였다. 호모 믹서를 사용하여 균질화한 에멀젼의 입자크기는 421 nm이었고 고압균질기를 사용한 균질화 과정에서 입자크기는 138 nm로 입자 크기의 감소를 확인하였다. 셀룰로오스 나노섬유를 첨가한 경우 호모믹서 균질화 작업에서 입자 크기가 118 nm 이었고 고압균질기를 사용하는 균질화 작업에서 입자 크기가 15.9 nm로 급격한 입자 크기 감소를 확인하였다.
호모믹서를 사용하여 균질화한 에멀젼(입자크기 421 nm)이 안정화도가 가장 높았다. 고압균질기를 사용하여 에멀젼의 크기를 감소시킨(입자크기 138 nm) 경우 안정화도가 가장 낮았지만 셀룰로오스 나노섬유를 첨가한(입자크기 15.9 nm) 경우 상대적으로 안정하였다. 따라서 셀룰로오스 나노섬유를 첨가하고 고압균질기로 균질화 작업을 할 경우 에멀젼의 입자크기를 피부 전달에 맞게 조절할 수 있을 뿐 아니라 에멀젼의 안정화도도 셀룰로오스 나노섬유 첨가에 의하여 향상되기 때문에 제약이나 화장품 분야에서 유효성분을 효과적으로 전달하기 위한 기술로 사용이 가능할 것으로 생각된다.