1. 서 론
펄프·제지 산업 및 목질계 바이오매스를 활용하는 산업의 부산물로 발생하는 리그닌(Lignin)은 셀룰로오스(Cellulose), 헤미셀룰로오스(Hemicellulose)와 함께 목재를 구성하는 주성분으로 수종에 따라 차이가 있으나 대략 15-40% 정도의 비중을 차지하고 있다.1,2) 이렇게 발생하는 리그닌은 전 세계적으로 연간 5-7천만 톤으로 리그닌의 고부가가치화를 위한 연구 목적으로 활용되는 리그닌은 2% 미만이며, 대부분은 단순 소각을 통한 제지공정의 에너지원으로 활용되고 있다.3)
리그닌은 페닐 프로판(C6-C3) 전구체들이 탄소-탄소 공유결합과 에테르 결합을 통하여 3차원 무정형의 거대한 분자구조를 형성하게 된다.4-6) 이렇게 형성된 리그닌은 전처리 공정에 따라 다양한 화학적 작용기를 지니게 되며, 대표적인 화학적 작용기는 메톡실기(-OCH3), 카보닐기, 지방족 수산기, 페놀성 수산기 등이 있다.7) 그 중 페놀성 수산기는 대표적인 수소 공여체(Hydrogen donor)로 벤젠 고리의 π 전자와 상호작용하여 비편재화된 자유 라디칼을 생성하는 과정을 통해 강력한 항산화 특성을 갖는다.8-10) 또한, 리그닌은 벤젠 고리를 포함하는 공액계 시스템으로 이루어져있기 때문에 발색단을 가지고 있고, 특정 자외선의 파장을 흡수할 수 있는 자외선 차단 기능을 지니고 있다.10-12) 최근에는 이러한 리그닌의 항산화 특성 및 자외선 차단 특성을 필름 등에 응용하는 연구가 진행되고 있다.11,13,14)
Poly(vinyl alcohol) (PVA)는 비닐에스테르 계열의 고분자를 비누화시켜 제조되는 수산기를 포함하는 선형 고분자로 수용성을 지니는 생분해성 고분자이다. 특히 투명성, 내산소 투과성, 내용제성, 내유성 등 다양한 장점을 갖고 있어 편광 및 포장용 필름 등에 사용되고 있다.15) 하지만 포장용 필름에 요구되는 자외선 차단 및 항산화 특성의 한계가 존재하였으며 이러한 특성들을 개선시키고자 다양한 물질을 혼합한 복합체를 제조하고, 자외선 차단 및 항산화 특성을 부여하는 연구가 진행되고 있다.16-18) Yang 등19)은 PVA, 키토산, 리그닌 나노 입자를 기반으로 하는 복합 필름을 제조하여 분석한 결과, 리그닌 나노 입자를 첨가한 필름에서 인장강도와 영률이 향상되었으며, 높은 자외선 차단 특성과 항산화 효과, 항균성 등이 확인되었다고 보고하였다.
본 연구에서는 항산화 특성 및 UV 차단 특성이 우수한 리그닌에 페놀성 수산기가 풍부한 카테콜계의 화학물질인 3,4-dihydroxybenzylamine (DHBA)를 합성하여 UV 차단 및 항산화 특성이 향상된 EKL-DHBA 제조를 통한 고부가가치의 리그닌 기반 소재를 연구하고자 하였다. FT-IR, 1H NMR, XPS, 31P NMR 분석을 통한 특성 분석 및 물리적 특성 분석인 GPC, TGA 분석을 수행하였다. 제조된 EKL-DHBA의 첨가량을 다르게 하여 PVA 용액과 혼합한 복합 필름을 제조하였고, EKL-DHBA/PVA 복합 필름의 항산화 특성 및 UV 차단 특성, 기계적 특성 분석을 통하여 리그닌 기반 소재로써 필름에 대한 응용 가능성을 확인하고자 하였다.
2. 재료 및 방법
2.1 공시재료
EKL-DHBA 제조를 위하여 M사에서 활엽수 크라프트 리그닌(Kraft lignin, KL)을 분양받아 사용하였다. 실험에 사용된 시약으로는 Sigma-Aldrich (USA)의 epichlorohydrin (ECH, >99%), 3,4-dihydroxybenzylamine hydrobromide (DHBA, 98%)와 Daejung Chemical (Korea)의 N,N-dimethylformamide (DMF, 99.5%), potassium carbonate anhydrous (K2CO3, 99.5%)를 구매하여 사용하였다. DMF의 경우 Sigma-Aldrich (USA)의 molecular sieve 3Å (4-8 mesh)으로 수분을 제거한 무수 상태로 사용하였으며, 필름 제조에는 점도 49.8 cPs, 검화도 87.5 mol%인 polyvinyl alcohol 2,000 (PVA)을 Daejung Chemical (Korea)에서 구매하여 사용하였다. 증류수(deionized water, DW)는 3차 증류수기(RO-180, Human, Korea)로 제조하여 사용하였다. 구매한 모든 약품은 추가 정제 없이 사용되었다.
2.2 실험방법
2.2.1 EKL 제조
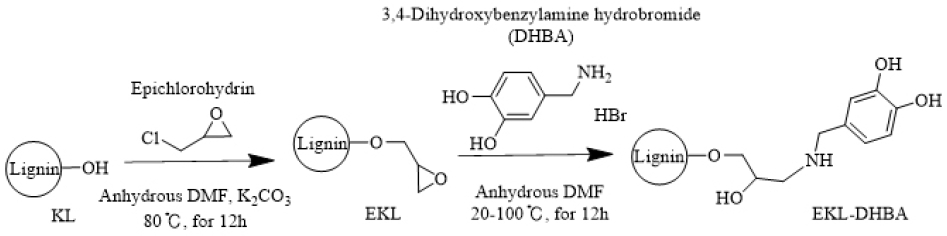
KL에 DHBA를 합성한 EKL-DHBA 제조 시 반응 사이트를 만들어주고자 리그닌의 수산기를 에폭사이드로 치환한 epoxy kraft lignin (EKL)을 제조하였다. 제조 방법은 Table 1의 조건으로 Fig. 1과 같이 제조하였다. 250 mL 둥근 플라스크에 KL 1 g과 K2CO3 0.765 g를 넣은 다음 ECH를 Table 1의 조건과 같이 투입하고 분산시켰다. 그다음 무수 DMF 40 mL를 첨가하여 용해한 후 교반 가열기(MR Hei-Tec, Heidolph, Korea)에서 80℃ 조건으로 12시간 동안 반응시켰다. 반응 후 EKL 용액의 회수는 원심분리기(MF 550, Hanil, Korea)를 이용하였다. 반응 후 혼합물을 2000 rpm으로 5분간 원심분리를 진행하였고, 상등액 부분은 회수하여 감압농축기(N-1110, EYELA, Japan)로 70℃ 조건에서 농축하여 잔여 DMF를 제거하였다. 그리고 증류수 300 mL를 넣고 초음파 세척기(JAC-5020, KODO, Korea)를 이용해 분산시킨 후 nylon membrane filter (직경 90 mm, 공극 직경 0.2 µm, Whatman)를 이용해서 미반응 ECH와 DMF를 제거하였다. 회수한 EKL은 동결건조기(FDCF-12006, OP-ERON, Korea)를 이용하여 파우더 형태로 EKL을 회수하였다.
2.2.2 EKL-DHBA 제조
EKL에 DHBA를 합성한 EKL-DHBA는 Table 2의 반응 조건에 따라 Fig. 1과 같이 제조하였다. 최적 조건으로 확인된 EKL과 DHBA를 250 mL 둥근 플라스크에 Table 2의 조건과 같이 투입한 다음 무수 DMF 30 mL를 첨가하였다. 그리고 초음파 세척기를 이용하여 용해시킨 후 각 조건의 반응온도로 설정된 교반 가열기에서 12시간 동안 반응시켰다. 반응 후 2000 rpm에서 원심분리를 5분간 수행하였다. 회수된 상등액을 감압농축기로 농축하여 DMF를 제거하였으며, 100 mL의 증류수를 첨가하고 농축하는 것을 2번 반복하여 잔여 DMF를 제거하였다. DMF가 제거된 EKL-DHBA는 300 mL의 증류수를 넣어 초음파 세척기를 통하여 증류수에 분산시킨 다음 nylon membrane filter (직경 47 mm, 공극 직경 0.2 µm, HYUNDAI MICRO Co., LTD, Korea)로 여과하였고, 미반응 DHBA 및 잔여 약품을 제거하기 위하여 1 L의 증류수를 이용하여 세척을 진행한 후 동결건조기를 이용하여 파우더 형태의 EKL-DHBA를 회수하였다.
2.2.3 EKL-DHBA/PVA 복합 필름 제조
최적 조건으로 확인된 EKL-DHBA의 항산화 특성과 UV 차단 특성 확인 및 첨가량에 따른 필름의 기계적 특성을 평가하기 위하여 Table 3의 조건으로 EKL-DHBA/PVA 혼합 용액 및 필름을 제조하였다. 500 mL 둥근 플라스크에 PVA 15 g와 증류수 285 g를 투입한 다음 90℃ 조건의 교반 가열기에서 3시간 동안 용해하여 5 wt% PVA 용액을 제조하였다. 그리고 PVA 첨가량 대비 EKL-DHBA의 첨가량(0%, 0.2%, 0.4%, 0.6%, 0.8%, 1.0%)을 다르게 하여 5 mL의 무수 DMF에 용해 후 PVA 용액과 혼합하여 EKL-DHBA/PVA 용액을 제조하였다. EKL-DHBA/PVA 복합 필름은 용매 캐스팅 방법으로 petri dish (90 mm×15 mm) 에 6 g을 도포 후 30℃ 조건에서 2일간 건조하여 회수하였다. 또한, 리그닌과 EKL-DHBA와의 항산화 특성과 UV 차단 특성을 비교하기 위하여 KL의 에탄올 용해분만 회수한 에탄올 용해 리그닌(Ethanol soluble lignin, EL)을 20 mL 에탄올에 용해한 다음 PVA와 혼합하여 용액 및 필름을 제조하였다. EL의 첨가량은 EKL-DHBA와 동일하게 진행하였다.
2.2.4 물리·화학적 특성 분석
KL, EKL, EKL-DHBA의 화학적 특성 분석을 위하여 FT-IR, 및 1H NMR, XPS 분석 방법을 실시했으며, FT-IR 및 1H NMR, XPS 분석조건은 다음과 같다. FT-IR은 PerkinElmer (USA) 사의 attenuated total reflectance attachment (ATR)가 장착된 Frontier 모델을 사용하여 4000 cm-1부터 400 cm-1의 범위에서 각 시료 당 256번의 스캔을 실시하였다. 1H NMR 분석은 600 MHz NMR (FT-NMR 600MHz spectrometer, Bruker Avance Ⅱ 600, Bruker, USA)를 이용했으며, NMR solvent (DMSO-d6, 0.75 mL)에 각각의 시료 20 mg을 용해 시킨 다음 128회 스캔하여 분석하였다. XPS 분석은 Thermo Scientific (U.K) 사의 K Alpha + 모델로 분석을 진행하였다. 조사범위는 400 µm를 200 eV와 50 eV의 pass energy로 분석하였고 Binding energy의 calibration은 C1s (284.8 eV)으로 진행되었다.
물리적 특성 분석은 GPC 및 TGA 분석 방법을 실시하였다. 리그닌 샘플의 분자량을 분석하기 위하여 분자량 분석(Gel Permeation Chromatography, GPC)를 진행했으며, 각 시료를 1 mg씩 정량하여 HPLC DMF (99.8%, DaeJung, Korea) 1 mL에 용해 후 SPD-20A (UV/Vis detector, Shimadzu, Japan), RID-20A (Refractive index, Shimadzu, Japan) 검출기가 장착된 CBM-20A (Shimadzu, Japan)로 측정하였다. 이때 컬럼은 오븐 온도 70℃에서 한 개의 agilent PLgel mixed-C (300×7.5 mm, 5 µm)와 agilent PLgel mixed-D (300×7.5 mm, 5 µm), agilent PLgel mixed-E (300×7.5 mm, 3 µm)를 연결하여 분석하였다. UV 검출기의 파장은 280 nm, injection volume은 100 µL로 설정한 뒤 DMF를 이동상으로 하여 1.0 mL/min의 조건 하에 측정을 진행했다. 분자량에 대한 검량선 작성은 1,480에서 1,233,000 g/mol 범위의 polystyrene standard를 이용하여 작성된 검량선을 통해 각 시료의 분자량 분포를 분석하였다. KL, EKL, EKL-DHBA의 열분해 거동 (TGA) 확인하기 위하여 열중량 분석기(Thermogravimetric analyzer, SDT Q600, TA Instrument, USA)를 이용했으며, 분석조건은 시료를 상온에서부터 10℃/min의 승온 속도로 700℃까지 가열하였고 flowing gas는 N2를 이용하였다.
2.2.5 수산기 함량 분석
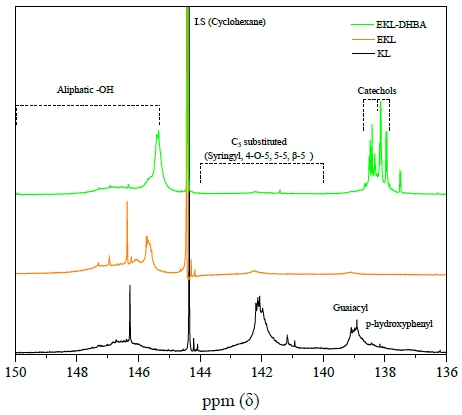
KL 및 EKL, EKL-DHBA의 phenolic hydroxyl 그룹과 aliphatic hydroxyl 그룹의 함량 분석을 위하여 FT-NMR 600MHz spectrometer (Bruker Avance Neo 600, Bruker, USA)를 이용했으며, Alessandro. G 등20)의 분석 방법에 따라 샘플을 제조하여 31P NMR 분석하였다. 분석 프로그램은 Mestrenova를 사용했으며, Internal standard인 cyclohexane이 나타나는 144.5-144.2 ppm 영역을 1로 설정한 후 150-145 ppm 영역의 aliphatic hydroxyl 그룹 및 143.1-141.3 (Syringyl), 139.5-137.8 (Guaiacyl), 137.5-136.0 (p-hydroxyphenyl) ppm 영역을 적분하여 다음 Eq. (1)에 따라 hydroxyl group의 함량을 계산하였다.21,22)
여기서 IC = Internal standard의 농도(mg/mL), Ia = Internal standard의 실제 첨가량(mL), CMW = cyclohexanol의 분자량(g/mol), SA = 각 영역의 적분 값, SW = 실제 사용한 각 시료의 질량(g)을 의미한다.
2.2.6 광학적 특성 분석
첨가량을 다르게 하여 제조한 EKL-DHBA/PVA 필름의 광 투과도를 측정하기 위하여 분광 광도계(UV-Vis spectrophotometer, X-ma 3000 PC, Human, Korea)를 이용하였다. 분석범위는 400-700 nm 범위를 분석하였으며, 광 투과도를 측정하기 위하여 550 nm의 파장 값을 평가하였다.
2.2.7 항산화 특성 분석
EKL-DHBA 및 EL의 항산화 특성을 분석하고자 분광 광도계를 이용했으며, An 등23)의 분석 방법을 참고하였다. 먼저 2,2-diphenyl-1-picrylhydrazyl (DPPH) 용액을 제조하기 위하여 DPPH 3 mg을 메탄올 50 mL에 용해하여 DPPH 용액을 제조하였다. 그리고 5배 희석한 EKL-DHBA/PVA 용액 1 mL를 DPPH 용액 1 mL와 15 mL 원심분리 용기에 담은 후 알루미늄 호일로 겉면을 감싸 빛을 차단하고 30분 동안 25℃, 200 rpm의 조건으로 incubated shaker (IST-4075R, JEIO tech, Korea)에서 반응시켰다. 반응 후에는 517 nm의 측정값을 다음 Eq. (2)를 통해 계산하여 DPPH radical scavenging capacity (RSC, %)를 분석하였다. EL/PVA 혼합 용액 역시 동일한 방법으로 분석하였다.
여기서 A0 = EKL-DHBA 및 EL 용매 1 mL + DPPH 용액 1 mL, As = EKL-DHBA/PVA 및 EL 혼합 용액 1 mL + DPPH 용액 1 mL, Ab = EKL-DHBA/PVA 및 EL 혼합 용액 1 mL + Methanol 1 mL을 의미한다.
3. 결과 및 고찰
3.1 EKL 특성 분석
3.1.1 물리·화학적 특성 분석
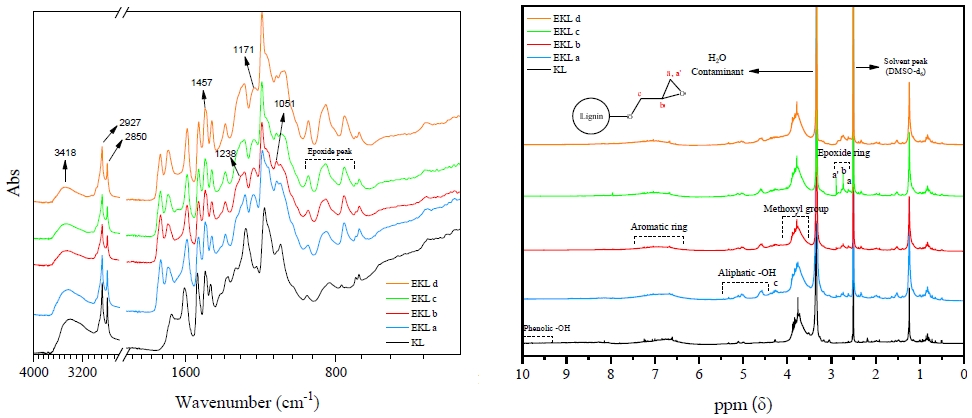
KL에 DHBA를 합성하기 위한 반응 사이트를 만들고자 ECH를 표 1의 조건에 따라 첨가하여 리그닌의 수산기가 에폭사이드 작용기로 치환된 EKL을 제조하였다. Fig. 2는 KL과 EKL 샘플들의 FT-IR 및 1H NMR 스펙트럼이다. FT-IR 스펙트럼을 통해 KL과 ECH를 반응시킨 후 에폭사이드 작용기와 관련된 908 cm-1 oxirang 피크가 나타났으며, 첨가량이 증가할수록 피크가 증가하는 것을 확인할 수 있었다.24) 또한, KL의 수산기가 에폭사이드로 치환되면서 3418 cm-1에 할당된 –OH 피크가 감소했으며, 2927, 2850 cm-1에 해당되는 C-H 피크와 1238 및 1171 cm-1에 할당된 C-O-C 피크가 증가하였다. 그리고 치환된 에폭사이드 작용기의 링 구조가 개열되면서 1457 cm-1의 methylene 피크 및 1051 cm-1와 1021 cm-1의 C-O 피크가 증가하는 것으로 나타났다.25,26) 추가로 1795 및 1730 cm-1에서 나타난 C=O 관련 피크는 유기용매인 DMF의 사용으로 기존의 NaOH 수용액에서의 반응보다 유기적인 반응성이 증가하여 발생한 부반응으로 사료된다.27,28)
1H NMR 스펙트럼에서는 10-9.4 ppm에서 나타나던 페놀성 수산기의 피크가 사라졌으며, 2.85-2.61 ppm 범위에서 에폭사이드 작용기와 관련된 피크가 나타났다.29) 또한, 에폭사이드 링 구조의 개열에 의해 형성된 것으로 사료되는 4.34-4.20 ppm 및 4.67-4.51 ppm의 지방족 수산기의 피크를 확인할 수 있었다.30-32)
XPS 분석결과에서 Fig. 3(a)와 같이 C1s (284,4 eV) 및 O1s (532 eV)에 해당하는 두 개의 주요 피크가 나타났으며, KL과 ECH의 반응으로 EKL의 산소 함량이 크게 증가한 것으로 나타났다. Fig. 3(b)-3(e)는 KL과 EKL의 C1s와 O1s 코어 스펙트럼을 각각의 피크로 피팅한 것으로 Fig. 3(b)-3(c)에서는 KL의 수산기에 에폭사이드 작용기를 치환한 후에 286.18 eV에 할당된 C-O 피크의 면적이 크게 증가하였으며, 284.54 eV에서 나타난 C-C/C=C 피크의 면적이 상대적으로 감소하는 것으로 나타났다. 또한, 부반응에 의해 형성된 것으로 사료되는 C=O (287.60 eV)피크의 증가가 확인되었다.33,34) O1s 코어 레벨 스펙트럼에서는 C-O (532.08 eV)피크 면적의 증가가 확인되었으며, 부반응으로 인한 C=O (531.83 eV)피크의 증가 역시 확인되었다. 그에 반해 C-OH (532.08 eV)피크는 상대적으로 감소하는 것으로 나타났다(Fig. 3(d)-3(e)).35)
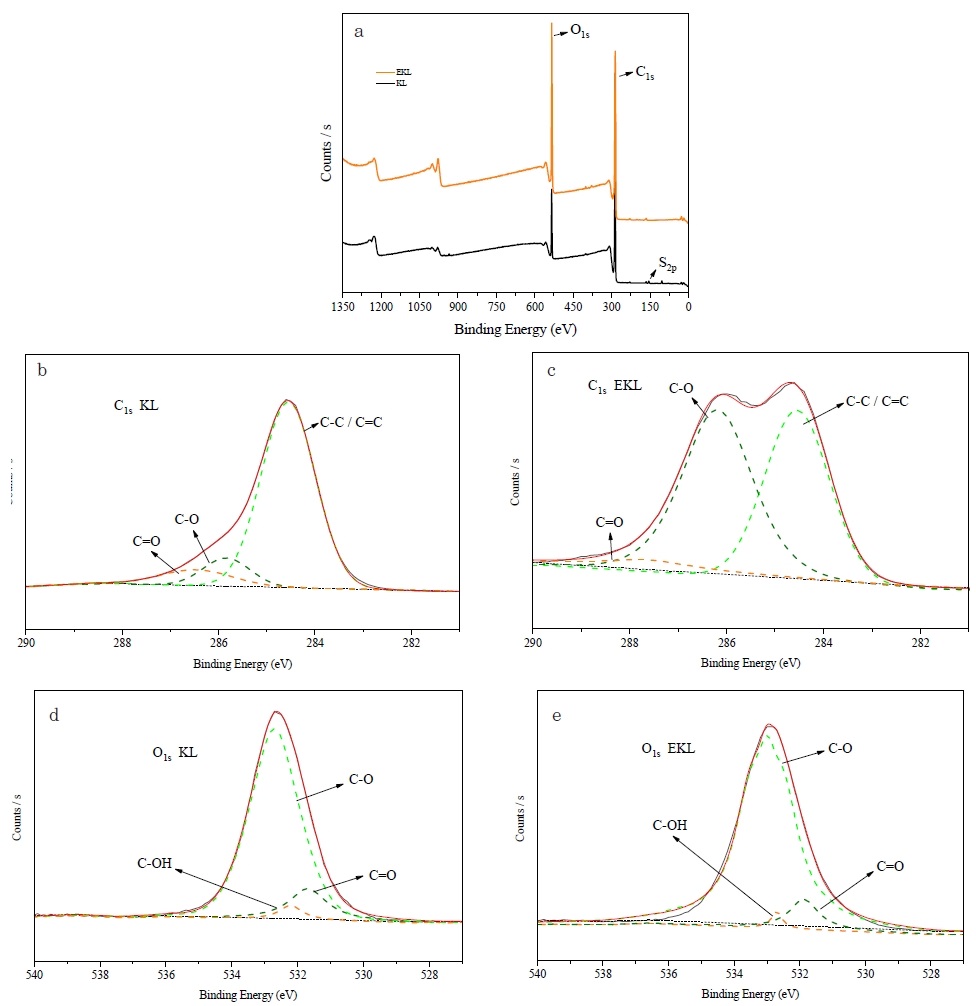
Fig. 3.
(a) XPS survey scan spectra of KL and EKL; (b, c) C1s core-level spectra of KL and EKL; (d, e) O1s core-level spectra of KL and EKL.
GPC 분석결과 ECH의 첨가량이 증가할수록 수-평균 분자량 및 질량-평균 분자량의 증가하여 KL 대비 수-평균 분자량은 최대 1.9배, 질량-평균 분자량은 6.17배 증가한 것으로 나타났다(Table 4). 또한, TGA 분석결과를 통하여 분자량의 증가에 따른 열적 안정성의 증가하여 최대 48℃가 증가하는 것으로 나타났다. 이는 KL에 epoxy group이 도입됨에 따라 일부 리그닌을 가교 결합을 형성하게 되고 거대 축합구조를 유도하였기 때문에 열적 안정성이 상당히 증가된 것으로 사료된다.
3.1.2 수산기 함량 분석
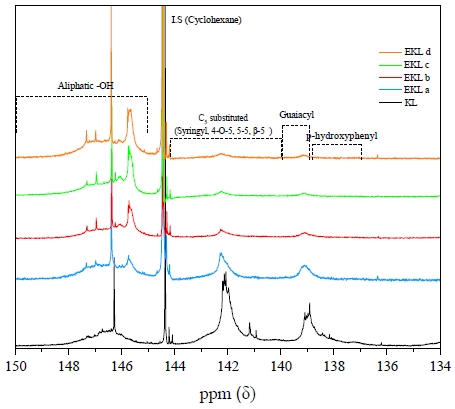
KL과 EKL 샘플은 31P NMR을 통하여 수산기 함량 분석을 수행하였다. Fig. 4와 Table 5는 31P NMR 분석결과로 ECH 첨가량이 증가함에 따라 KL에 존재하는 페놀성 수산기인 syringyl, guaiacyl, ρ-hydroxyphenyl의 피크 및 함량이 점점 감소하는 것을 확인할 수 있었으며, 치환된 에폭사이드 링의 개열로 145.82-145.40 ppm 범위에서 새로운 지방족 수산기 피크와 함량이 증가하였다.21,22) 이러한 결과를 바탕으로 화학구조 분석에서 에폭사이드 작용기의 피크가 강하게 나타났으며, 페놀성 수산기의 함량이 낮은 EKL c가 최적 제조조건으로 사료된다.
Table 5.
Hydroxyl group content of KL and EKLs
3.2 EKL-DHBA 특성 분석
3.2.1 물리·화학적 특성 분석
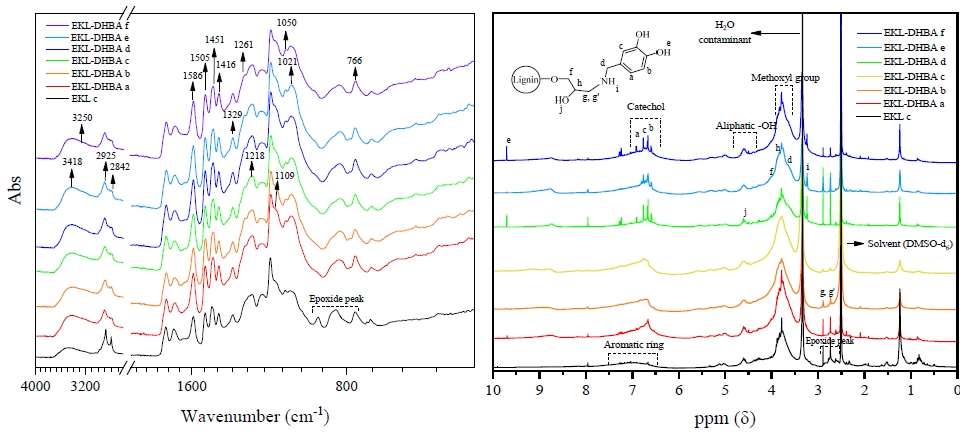
최적 조건으로 선정된 EKL c와 DHBA를 합성하여 EKL-DHBA를 제조하였으며, Fig. 5는 FT-IR 스펙트럼과 1H NMR 스펙트럼을 나타냈다. FT-IR에서는 아민기 및 페놀성 수산기를 지닌 DHBA와의 합성으로 908 cm-1 oxirang 피크가 사라졌으며, 에폭사이드 링의 개열로 3418 cm-1에서의 –OH 피크, 2925 및 2842 cm-1의 C-H 피크, 1451 cm-1 methylene 피크, 1050 cm-1 및 1020 cm-1에서의 C-O 피크가 증가하는 것으로 나타났다. 또한, 페놀성 수산기와 관련된 피크로는 1586, 1505 cm-1 aromatic ring 피크, 1416 cm-1 aromatic ring C-H 피크가 증가하였으며, 또한, 1329 cm-1 G ring C-O 피크와 1261 cm-1 S ring의 C-O 피크가 나타났다. 아민기와 관련해서는 3250 cm-1 –NH 피크, 1218, 1109 cm-1 C-N 피크, 766 cm-1 N-H wagging 피크가 확인되었다.25)
1H NMR에서는 9.71 (e) ppm의 페놀성 수산기 피크와 6.91 (a), 6.76 (c), 6.64 (b) ppm의 aromatic ring 피크, 3.24 (i) ppm의 아민기 피크를 확인할 수 있었다.41,42) 또한, 에폭사이드 링 구조의 개열로 2.74 ppm의 에폭사이드 피크가 사라졌으며, 4.63-4.54 (j) ppm의 지방족 수산기 피크의 증가와 3.98-3.92 (f), 3.86 (h), 2.89, 2.73 (g, g’) ppm의 알킬 체인과 관련된 피크들이 확인되었다.38,39)
Fig. 6(a)는 EKL-DHBA e의 XPS 분석결과 중 표면 원소함량을 분석한 결과로 C1s (284.4 eV), O1s (532 eV)의 피크 및 N1s (399 eV), Br3d (69.22 eV), 두 개의 피크가 추가로 나타났다. N1s 피크의 경우 DHBA의 아민기에 기인된 피크로 사료되며, Br3d 피크는 양성자화된 아민기에 Br-이 염 형태로 존재하는 것으로 사료된다. Fig. 6(b)-6(d)는 C1s 및 O1s, N1s의 코어 레벨 스펙트럼을 각 피크로 피팅한 것으로 Fig. 6(b)에선 새로운 C-N (286.03 eV)피크가 나타났으며, aromatic ring에 의한 C-C / C=C (284.52 eV)피크의 증가를 확인할 수 있었다. 반면 C=O (287.83 eV)피크 및 C-O (286.22 eV)피크는 감소한 것으로 나타났고, 이는 새로 나타난 C-N 피크 및 C-C / C=C 피크의 증가에 따른 상대적인 감소로 사료된다.33,34,40)Fig. 6(c)의 O1s 코어 스펙트럼에서는 DHBA의 페놀성 수산기 및 에폭사이드 링의 개열로 C-OH (532.62 eV)피크 증가가 나타났으며, 상대적으로 C=O (531.84 eV), C-O (533.27 eV)피크가 감소한 것으로 사료된다.35)Fig. 6(d)의 N1s 코어 레벨 스펙트럼에서는 C-N (398.95 eV)피크, –NHR (400.21 eV) 및 –N+H2R (401.69 eV)피크가 나타났다. –N+H2R (401.69 eV)피크의 경우 DHBA에 포함된 HBr에 의하여 반응 시 산성 조건이 형성되어 –NHR 구조가 양성자화 된 것으로 사료된다.40,42,43) 결과적으로 C1s에서의 새로운 C-N 피크 형성 및 N1s에서의 –N+H2R, –NHR, C-N 피크 형성을 통하여 EKL-DHBA의 합성이 성공한 것으로 사료된다.
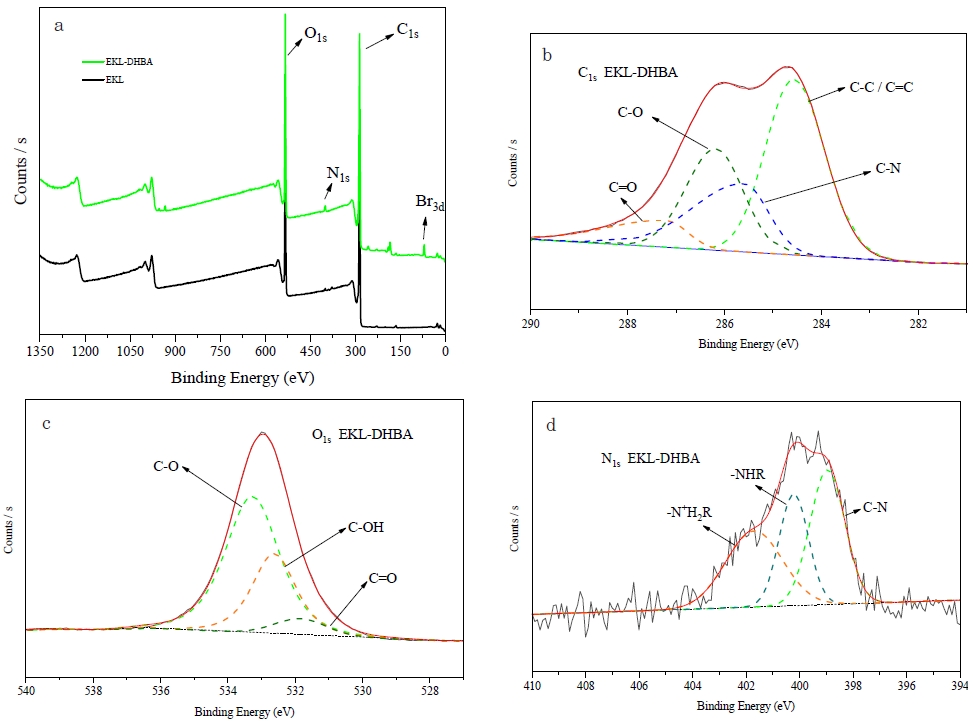
Fig. 6.
(a) XPS survey scan spectra of EKL and EKL-DHBA; (b) C1s core-level spectra of EKL-DHBA; (c) O1s core-level spectra of EKL-DHBA; (d) N1s core-level spectra of EKL-DHBA.
Table 6은 Table 2의 조건에 따라 제조한 EKL-DHBA의 수율, GPC 분석, TGA 분석결과를 정리한 것으로 20-100℃ 범위의 온도 조건 중 80℃에서 가장 높은 수율을 보였으며, 80℃ 조건에서 DHBA 첨가량을 0.1 g과 0.2 g으로 조절한 EKL-DHBA d와 EKL-DHBA e에서는 차이가 없는 것으로 나타났다. GPC 분석결과, EKL c와 EKL-DHBA 샘플들의 수-평균 분자량은 큰 차이가 없었으나 질량- 평균 분자량에서 반응온도 증가에 따른 분자량이 증가하는 경향을 확인하였다. TGA를 통한 최대 열분해 온도 또한 분자량 증가에 따라 16-23℃ 향상되는 것으로 나타났다.
Table 6.
Yield, molecular weight, and maximum thermal degradation temperatures of EKL c and EKL-DHBAs
3.2.2 수산기 함량 분석
EKL에 DHBA를 합성한 후 페놀성 수산기의 변화를 확인하고자 31P NMR 분석을 하였다. Fig. 7과 Table 7는 31P NMR 분석결과로 DHBA의 카테콜 구조와 관련된 피크가 p-hydroxyphenyl 영역인 140.2-137.8 ppm에서 나타났으며, 해당 영역에서의 함량이 0 mmol/g인 EKL 대비 EKL-DHBA에서는 약 1 mmol/g의 함량을 나타내었다.21,22) 따라서 수율이 높았던 80℃ 조건 중 화학구조 분석에서 카테콜 구조에 관련된 피크가 나타났으며, 페놀성 수산기의 함량이 가장 높았던 EKL-DHBA e가 최적 조건으로 선정되었다.
Table 7.
Hydroxyl group content of EKL c and EKL-DHBAs
3.3 EKL-DHBA/PVA 복합 필름 특성 분석
3.3.1 광학적 특성 분석
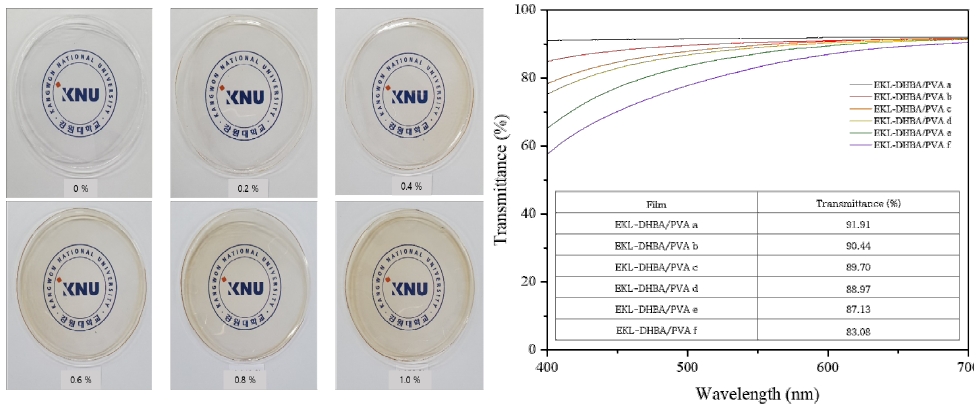
Fig. 8은 필름의 투명도 및 550 nm 파장에서의 광 투과도 분석결과이다. 필름의 투명도를 육안으로 확인하였을 때 순수한 PVA 필름인 EKL-DHBA/PVA a의 경우 로고 확인에 문제가 없었으며, EKL-DHBA 첨가량이 1 wt%인 EKL-DHBA/PVA f 필름은 옅은 갈색을 나타내었으나 로고 확인에는 문제가 없었다. 하지만 광 투과도 분석결과 EKL-DHBA a는 91.91%의 투과도를 보이는 반면 EKL-DHBA 첨가량이 0.2 wt%씩 증가할수록 약 1-2%의 투과도가 감소하였고 EKL-DHBA/PVA f 필름에서는 83.08%로 확인되어 8.83% 감소하는 것으로 나타났다.
3.3.2 항산화 특성 분석
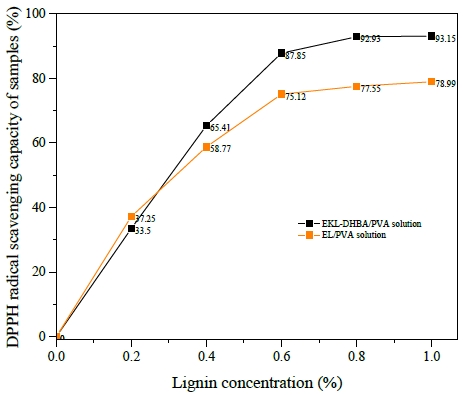
KL에 DHBA를 합성하여 제조한 EKL-DHBA와 EL의 항산화 특성을 비교 분석하고자 하였으며, Fig. 9는 그 결과를 나타낸 것이다. EKL-DHBA의 첨가량이 0.2 wt%의 경우 같은 양의 EL을 첨가한 용액보다 낮은 DPPH 소거 정도를 나타내었으나 첨가량이 증가할수록 EKL-DHBA를 첨가한 용액의 항산화 특성이 높게 나타났으며, 결과적으로 1 wt%를 첨가한 지점에서 93.15%의 DPPH 소거 정도를 보여 EL보다 14.16% 높은 항산화 효과를 나타내었다. 이를 통하여 카테콜 구조의 도입을 통한 KL의 항산화 특성을 향상시킬 수 있는 것으로 사료된다.
3.3.3 UV 차단 특성 분석
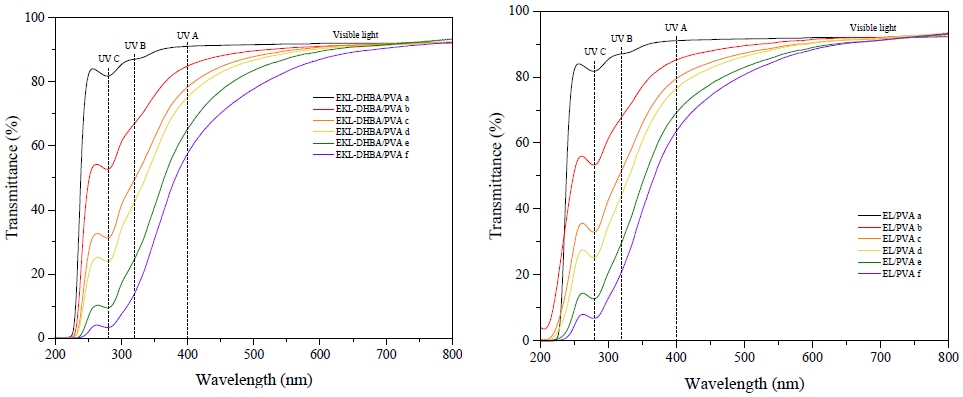
EKL-DHBA 및 EL을 혼합한 PVA 필름의 UV 차단 특성을 분석하고자 하였으며, Fig. 10은 200-800 nm 범위의 자외선-가시광선 영역을 분석한 결과이다. EKL-DHBA 및 EL의 첨가량이 증가할수록 필름의 광 투과도가 감소하는 것을 확인할 수 있었다. 특히 인체에 악영향을 주는 UV-A (320-400 nm), UV-B (280-320 nm)영역에서 1 wt%의 EKL-DHBA/PVA f 필름의 투과율은 57.55-13.88%, 13.88-3.25%이고, EL/PVA f 필름의 투과율은 63.51-21.38% 및 21.38-6.75%으로 확인되었다. 따라서 EKL-DHBA/PVA f 필름이 EL/PVA f 필름보다 더 낮은 투과율을 보임으로써 UV 차단 특성이 향상된 것으로 판단된다. 또한, Zhang 등44)이 제조한 나노 사이즈의 hemp hurd 목분 5 wt%를 첨가한 PVA 필름과 10 wt%의 TiO2를 첨가한 PVA 필름의 투과율을 비교한 것에 따르면 UV-A의 범위 중 345-400 nm에서 약 90-70%의 투과율을 보여주는 TiO2 필름 대비 5% hemp hurd/PVA 복합 필름은 70-61%의 투과율을 나타냈다고 하였는데, EKL-DHBA 필름의 경우 57.55-13.88%로 더 우수한 UV-A 차단 특성을 보여주었다. 이러한 결과를 통하여 EKL-DHBA의 UV 차단 특성이 TiO2와 비교하여도 크게 떨어지지 않음을 확인할 수 있었으며, UV 차단 특성의 향상 이유는 KL에 DHBA를 도입함으로써 UV를 흡수할 수 있는 컨쥬게이트된 시스템이 증가했기 때문으로 사료된다.10-12)
4. 결 론
본 연구에서는 펄프·제지 산업의 부산물로 발생하는 크라프트 리그닌의 항산화 및 UV 차단 특성이 향상된 고부가가치 소재화를 위하여 두 단계 반응으로 DHBA가 치환된 리그닌을 제조하였다. 리그닌에 DHBA의 도입은 화학적 특성 분석(FT-IR, 1H NMR 및 XPS) 및 물리적 특성 분석(TGA, GPC), 31P NMR 분석을 통하여 EKL-DHBA가 성공적으로 제조되었다고 판단된다. 제조된 EKL-DHBA의 향상된 항산화 및 UV 차단 특성 확인 및 첨가량에 따른 기계적 특성을 확인하기 위하여 EKL-DHBA/PVA 복합필름을 제조하였다. 항산화 특성 분석결과에서는 EKL-DHBA의 첨가량의 증가에 따른 항산화 특성의 증가를 확인하였고, 최대 첨가량인 1.0%에서는 78.99%의 DPPH free radical 소거 효율을 보여준 EL/PVA 용액보다 14.16% 향상된 93.15%를 나타내는 것을 확인하였다. 필름의 UV 차단 특성 분석결과, EKL-DHBA/PVA f 필름은 UV-A 영역에서 57.55-13.88%의 투과율을 나타내었고, UV-B 영역에서 13.88-3.25%의 투과율을 나타내었으며, EL보다 EKL-DHBA가 UV 차단 특성이 높은 것을 확인할 수 있었다. 따라서 항산화 및 UV 차단 특성을 지닌 EKL-DHBA은 복합 재료의 첨가제로서 큰 잠재력을 기대할 수 있고, 리그닌 기반 바이오 신소재 활용성을 높이는 계기가 될 수 있을 것으로 판단된다.