1. 서 론
나노셀룰로오스는 셀룰로오스를 물리, 화학, 생물학적 처리 방법을 통해 나노단위로 가공한 것을 말한다. 나노셀룰로오스는 제조 방법에 의해 구분되며, 물리적 처리에 의한 셀룰로오스 나노피브릴, 화학적 산 가수분해에 의한 셀룰로오스 나노크리스탈, 박테리아에 의해 합성된 박테리아 셀룰로오스 등으로 분류된다.1-3) 나노단위로 가공된 셀룰로오스는 종횡비와 비표면적이 커 강도와 탄성계수가 높으며, 치수 안전성, 친환경성 등의 장점을 가진 물질로 주목받고 있다.4-7)
나노셀룰로오스는 비표면적이 커짐에 따라 물과 수소결합 능력이 증가하여 건조가 매우 어려울 뿐만 아니라 건조과정에서 나노셀룰로오스 간 수소결합에 의해 응집이 발생한다. 이렇게 응집되어 건조된 나노셀룰로오스는 나노화 과정에서 증가된 비표면적이 감소하고, 이 때문에 나노셀룰로오스의 우수한 성질이 감소한다. 나노셀룰로오스의 건조 문제를 해결하기 위해 분무 건조 방법과, 동결 건조 방법이 고안되었다.8-10) 하지만 두 가지 방법 모두 건조과정에서 나노셀룰로오스 입자가 일부 응집되며, 건조 전의 나노셀룰로오스가 가지는 물성을 완전히 회복하지 못한다. 위의 건조 방법의 문제점을 해결하기 위해 나노셀룰로오스를 코팅하여 건조하는 방법이 고안되었다. 코팅제로 계면활성제, 당류가 사용되며, 이러한 물질이 나노셀룰로오스 입자를 둘러싸고, 건조 과정에서 나노셀룰로오스 간 응집되는 것을 방해한다.11,12)
나노셀룰로오스를 활용하기 위해 위처럼 많은 연구가 진행된 반면, 나노셀룰로오스를 건조하지 않고 활용하는 방법에 대해 연구도 진행되고 있다. 건조되지 않은 나노셀룰로오스 현탁액은 점탄성이 우수하고, 수분 친화력이 높아 수분 유지력이 좋다. 이러한 특성을 가진 나노셀룰로오스 현탁액은 화장품, 페인트, 시멘트 등에 사용된다.13,14)
나노셀룰로오스 현탁액은 일반적으로 물에 분산된 상태로 사용하여 미생물에 의해 쉽게 오염될 수 있다. 특히 공기 중에는 셀룰로오스를 분해하여 영양원으로 삼는 고초균, 검은 곰팡이 등의 미생물이 있기 때문에 쉽게 오염된다.15,16)
나노셀룰로오스는 셀룰로오스를 잘라 나노단위로 제조된 물질이기 때문에 셀룰로오스에 비해 더 쉽게 오염될 수 있다. 이러한 특징 때문에 현탁액을 무균 상태로 제조한다고 해도 작업 중 잠깐의 공기 노출에 의해 오염될 수 있다. 나노셀룰로오스 현탁액이 셀룰로오스 분해 미생물에 의해 오염될 경우 급격한 점도 저하 문제가 발생할 수 있으며, 특히 나노셀룰로오스를 현탁액으로 사용하고자 할 때 주요 물성인 점탄성이 매우 크게 감소한다.17)
본 연구에서는 나노셀룰로오스 현탁액이 세균에 의해 오염되었을 때, 발생하는 물성 저하를 점도를 통해 측정하였다. 그리고 나노셀룰로오스 현탁액의 보존성 향상을 위해 보존제를 첨가하였을 때, 미생물 오염 방지 효과를 확인하고자 한다.
2. 재료 및 방법
2.1 공시재료
나노셀룰로오스 제조에 사용한 펄프는 M사의 활엽수 표백 크라프트 펄프를 사용하였으며, 카르복시메틸화에 사용한 시약은 수산화나트륨, 염화아세트산, 에탄올을 사용하였다. 미생물 오염 방지를 위한 보존제로는 페녹시에탄올, 1,2-헥산디올, 아지드나트륨을 사용하였다.
2.2 실험 방법
2.2.1 카르복시메틸화 전처리
나노셀룰로오스를 제조하기 이전 전처리로 카르복시메틸화 처리를 하였다. 카르복시메틸화 전처리는 펄프 100.0 g에 수산화나트륨 19.7 g이 용해된 에탄올 2 L을 혼합하여 상온에서 두 시간 이상 방치하였다. 방치된 펄프에 염화아세트산 21.7 g이 용해된 에탄올 500 mL를 혼합하여 70℃에서 두 시간 반응시켜 카르복시메틸화를 실시하였다. 반응이 종료된 펄프는 에탄올을 제거한 후 아세트산과 증류수를 사용하여 pH 6-7이 되도록 중화, 세척한 후 나노셀룰로오스 제조에 사용하였다.
2.2.2 나노셀룰로오스 제조
카르복시메틸화 전처리된 펄프를 1%(w/w)로 희석 후 고압균질기를 통과시켜 나노셀룰로오스를 제조하였다. 나노셀룰로오스 제조에 사용한 고압균질기(PANDA PLUS, GEA, Italy)의 사용 조건은 최초 100 bar에서 1회 통과 이후 2회 통과부터는 600 bar로 압력을 조절하였다. 최종 통과 횟수는 최소 통과횟수를 포함하여 7회 통과시켜 셀룰로오스 나노피브릴을 제조하였다.
미생물 오염 방지를 위한 첨가제가 포함된 나노셀룰로오스는 각 보존제를 0.4, 0.8, 1.2, 1.6%(w/w)를 첨가한 후 위 제조방법으로 제조하였다.
2.2.3 오염 미생물 배양액 제조
나노셀룰로오스 오염 미생물로 S. xylosus(Staphylococcus xylosus, KCCM 40887)와 B. subtilis(Bacillus subtilis, KCCM 11316)을 한국미생물보존센터에서 분양받아 사용하였다. 생육배지는 보통 배지(beef extract 30.0 g/L, peptone 5.0 g/L)를 사용하였으며, 30℃ 진탕 배양기에서 하루 동안 배양하였다. 하루 동안 배양된 S. xylosus와 B. subtilis 배양액 5.0 mL을 취해 새로운 nutrient 배지 50 mL에 분주한 후 하루 동안 배양하여 나노셀룰로오스 현탁액에 분주할 배양액을 제조하였다.
2.2.4 나노셀룰로오스 현탁액 내 오염 미생물 배양
나노셀룰로오스 현탁액의 미생물에 대한 오염을 확인하기 위해 나노셀룰로오스 현탁액에 오염미생물 배양액을 접종 후 배양하였다. 나노셀룰로오스 현탁액을 100 mL 삼각플라스크에 20.0 g을 넣은 후 고압멸균기로 121℃, 15분간 멸균을 실시하였다. 멸균된 나노셀룰로오스 현탁액에 S. xylosus와 B. subtilis 배양액 1 mL를 접종한 후 25℃ 진탕 배양기에서 3일간 배양하였다. 보존제가 첨가된 나노셀룰로오스 현탁액도 같은 방법을 반복하여 실시하였다.
2.2.5 오염된 나노셀룰로오스 현탁액의 미생물 검출
나노셀룰로오스 현탁액의 미생물 오염 여부를 확인하기 위해 미생물이 배양된 나노셀룰로오스 현탁액을 고체배지에 도말하여 확인하였다. 사용된 고체배지는 보통 한천배지를 사용하였다. 오염된 나노셀룰로오스 현탁액 1 mL를 고채배지에 도말하고, 후 25℃ 진탕 배양기에 24시간 배양 후 배양된 미생물의 콜로니를 확인하여 오염 여부를 확인하였다.
2.2.6 투과전자현미경 분석
카르복시메틸화 전처리된 활엽수 표백 크라프트 펄프로 제조된 나노피브릴의 크기를 분석하기 위하여 투과전자현미경 분석을 실시하였다. 분석하기 위한 그리드 제조 방법은 나노피브릴을 0.01%(w/w)로 희석한 후 300 mesh 카본그리드에 위치시킨 후 아세트산 우라늄으로 음영염색을 하여 관찰용 샘플을 제조하였다. 투과전자현미경(Libra 120, Carl Zeiss, Germany) 관찰 조건은 가속전압 120 kV에서 관찰하였으며, 나노피브릴 섬유 50개의 폭 크기를 측정하여 분석하였다.
2.2.7 오염된 나노셀룰로오스의 점도 측정
나노셀룰로오스 현탁액의 물성과 미생물 오염에 따른 물성 저하를 측정하기 위해 레오미터를 사용하여 점도 측정하였다. 점도측정기(MCR 102, Anton Paar, Austria) 사용조건은 측정 툴은 D-PP 25를 사용하여 나노셀룰로오스 현탁액의 점도를 측정하였다.
3.결과 및 고찰
3.1 제조된 나노셀룰로오스의 미생물 오염 특성
카르복시메틸화 전처리된 활엽수 표백 크라프트 펄프로 제조된 나노셀룰로오스의 폭 크기를 측정하기 위해 투과전자현미경 분석 결과를 Fig. 1에 나타내었다. 투과전자현미경을 통해 폭 크기를 확인한 결과 3.2-7.7 nm(평균 4.8 nm)의 크기를 갖는 나노셀룰로오스가 제조된 것을 확인하였다.
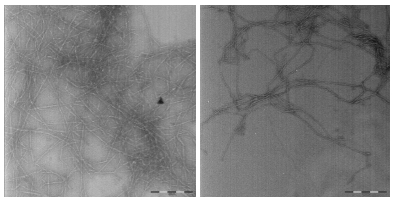
Fig. 1.
Transmission electron microscopy image of nanocellulose (scale bar: 200 nm).
나노셀룰로오스 현탁액에 S. xylosus와 B. subtilis 배양액을 접종하여 나노셀룰로오스 현탁액을 오염시킨 후 점도를 측정한 결과를 Fig. 2에 나타내었다. 제조된 나노셀룰로오스의 점도는 8,321 mPa·s로 확인 되었으며, S. xylosus와 B. subtilis에 의해 오염된 나노셀룰로오스 현탁액의 점도는 크게 감소하였다. 나노셀룰로오스 현탁액의 점도가 감소하는 원인 중 미생물에 의한 점도 감소 효과는 미생물이 분비하는 셀룰로오스 분해 효소에 의한 효과이다. 때문에 두 세균 배양액을 나노셀룰로오스 현탁액에 접종하였을 때, 세균에 의한 나노셀룰로오스의 분해가 발생하였으며, 이로 인해 나노셀룰로오스 현탁액의 점도가 크게 감소한 것으로 판단된다.
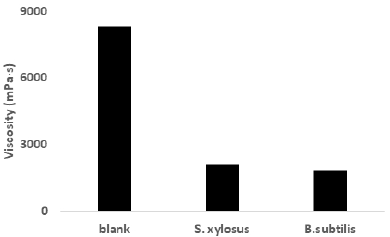
Fig. 2.
Viscosity of contaminated nanocellulose by bacteria.
B. subtilis는 일반적으로 셀룰로오스 분해 효소를 생산하는 세균으로 알려져 있으며, 셀룰로오스를 분해하는 효소를 생산하는 세균으로도 사용된다.18)S. xylosus의 경우 일반적인 셀룰로오스 분해 미생물은 아니지만 탄수화물을 영양원으로 하는 병원성 세균이다.19)B. subtilis의 경우 셀룰라아제를 가지고 있기 때문에 나노셀룰로오스 현탁액에 접종되었을 때, 셀룰라아제에 의한 나노셀룰로오스 분해가 진행된 것으로 판단된다. S. xylosus의 경우 B. subtilis처럼 셀룰라아제 활성이 높지 않지만 셀룰라아제를 가지고 있어 B. subtilis와 같이 나노셀룰로오스 분해에 의해 점도 저하를 발생시킨 것으로 판단된다.
3.2 페녹시에탄올이 첨가된 나노셀룰로오스의 미생물 오염 특성
페녹시에탄올이 첨가된 나노셀룰로오스 현탁액의 오염여부를 확인한 결과를 Table 1에 나타내었다. 고체배지에 배양한 미생물의 콜로니는 생균수 측정이 가능한 30개 이상의 콜로니가 확인되었을 때, 양성으로 표시하였으며, 페녹시에탄올을 0.4% 첨가하였을 때, 고체배지에서 대부분 유의미한 콜로니 수가 확인되었다. 0.8%가 첨가되었을 때, S. xylosus의 경우에는 콜로니 수가 줄어드는 것이 확인되었지만, B. subtilis의 경우에는 0.4%를 첨가하였을 때와 비슷하게 확인되었다. 페녹시에탄올을 1.2% 이상 첨가하였을 때 두 미생물 모두 콜로니 수가 감소하였으며, 1.8%가 첨가되었을 때에는 10개 이하의 콜로니만 확인되었다.
Table 1.
Microbial contamination of nanocellulose with phenoxyethanol
| | S. xylosus | B. subtilis |
|---|
| Blank | +++ | +++ |
| Phenoxyethanol | 0.4% | ++- | ++- |
| 0.8% | +-- | ++- |
| 1.2% | --- | --- |
| 1.8% | --- | --- |
페녹시에탄올은 의료, 화장품용으로 사용되는 방부제로 그람 음성균, 그람 양성균, 진균, 효모에 대해서 항균 또는 생육을 억제하는 것으로 알려져 있다. 페녹시에탄올은 주로 세포막을 파괴하여 세포 내 물질 누출을 제어하지 못하도록 하여 항균능력을 발휘한다.20,21) 특히 박테리아의 경우 TCA회로의 효소 억제를 통해 항균능력을 발휘한다. 이러한 이유로 나노셀룰로오스 현탁액에 페녹시에탄올이 첨가될 경우와의 생장을 억제하여 결과적으로 나노셀룰로오스를 분해하는 효소를 분비하지 못하도록 한다.
페녹시에탄올이 첨가된 나노셀룰로오스 현탁액의 오염 후 잔류하는 점도 측정 결과를 Fig. 3에 나타내었다. 점도 측정결과 B. subtilis가 S. xylosus보다 더 크게 점도가 감소한 것으로 확인 되었다. 특히 S. xylosus의 경우에는 페녹시에탄올이 1.2% 이상 첨가된 경우 Table 1에 나타난 결 과와 같이 나노셀룰로오스가 분해되지 않는 것으로 판단된다. 하지만 S. xylosus의 경우 Table 1에서 오염이 확인되지 않았지만 점도 측정 결과 일부 분해되어 점도가 감소한 것으로 판단된다. 두 결과로 미루어볼 때, 보존제로 페녹시에탄올을 1.2% 이상 첨가하여 나노셀룰로오스 현탁액을 제조할 경우 두 미생물 오염을 방지할 것으로 판단된다.
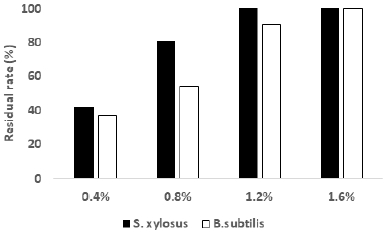
Fig. 3.
Viscosity residual rate of contaminated nanocellulose with phenoxyethanol by S. xylosus and B. subtilis.
3.3 1,2-헥산디올이 첨가된 나노셀룰로오스 현탁액의 미생물 오염 특성
1,2-헥산디올이 첨가된 나노셀룰로오스 현탁액의 오염여부를 확인한 결과를 Table 2에 나타내었다. 1,2-헥산디올이 첨가된 나노셀룰로오스 현탁액에서는 모든 농도에서 미생물 오염이 확인되었다. 특히 페녹시에탄올은 1.2% 이상 첨가될 경우 미생물 오염이 확인되지 않는 반면, 1,2-헥산디올의 경우 1.8%를 첨가한 경우에도 미생물 오염이 확인되었다.
Table 2.
Microbial contamination of nanocellulose with 1,2-hexanediol
| | S. xylosus | B. subtilis |
|---|
| Blank | +++ | +++ |
| 1,2 Hexanediol | 0.4% | +++ | +++ |
| 0.8% | +++ | ++- |
| 1.2% | ++- | ++- |
| 1.8% | +-- | +-- |
1,2-헥산디올이 첨가된 나노셀룰로오스 현탁액의 오염 후 잔류하는 점도 측정 결과를 Fig. 4에 나타내었다. 점도 측정결과 S. xylosus가 B. subtilis보다 더 크게 점도가 감소한 것으로 확인 되었다. 페녹시에탄올이 첨가된 나노셀룰로오스 현탁액의 오염 후 점도 측정결과를 비교 했을 때, S. xylosus의 경우 더 분해된 것이 확인 되었으며, B. subtilis의 경우에는 잔류하는 점도가 높게 확인되었다. 1,2-헥산디올이 1.2% 이상 나노셀룰로오스 현탁액에 첨가되었을 때, B. subtilis의 경우 오염은 확인되지만 보존제에 의해 나노셀룰로오스 분해에 어려움이 있는 것으로 판단된다. 하지만 S. xylosus의 경우 B. subtilis보다 보존제에 의한 영향을 적게 받아 점도가 더 크게 감소한 것으로 판단된다.
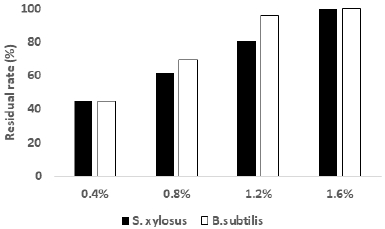
Fig. 4.
Viscosity residual rate of contaminated nanocellulose with 1,2 hexanediol by S. xylosus and B. subtilis.
1,2-헥산디올은 1,2-알칸디올계 화합물로, 알칸디올계 화합물이 세균 등의 미생물에 대해 항균력을 보이는 이유는 세균의 세포막 형성과정을 방해하기 때문으로 알려져 있다. 이전 연구에서 세균에 대해 1,2-헥산디올의 방부력을 측정한 결과 첨가 농도에 따라 균의 성장을 억제하였으나, 완전히 균이 성장을 억제하지 못하는 것이 확인된 바 있다.22) 또한 세균에 따라서 균의 성장에 대해 매우 약한 억제력을 보이기도 한다. 이 때문에 1,2-헥산디올은 단독으로 사용하여 항균능력을 발휘하는 것보다 다른 보존제와 함께 사용하여 그 능력을 극대화하는 것이 연구되고 있다.23) 이러한 연구 결과를 바탕으로 본 연구의 결과에서도 완전한 균 성장 억제력을 보이지 않았으며, 1,2-헥산디올을 1.6% 첨가하였을 때 오염은 있으나, 점도 저하를 방지할 수 있었다.
3.4 아지드나트륨이 첨가된 나노셀룰로오스 현탁액의 미생물 오염 특성
아지드나트륨이 첨가된 나노셀룰로오스 현탁액의 오염여부를 확인한 결과를 Table 3에 나타낸 결과 아지드나트륨이 첨가된 모든 나노셀룰로오스 현탁액에서 미생물 오염이 확인되었다. 이는 1,2-헥산디올과 마찬가지로 두 미생물이 아지드나트륨에 대해 큰 저해를 받지 않기 때문으로 판단된다.
Table 3.
Microbial contamination of nanocellulose with sodium azide
| | S. xylosus | B. subtilis |
|---|
| Blank | +++ | +++ |
| Sodium azide | 0.4% | +++ | +++ |
| 0.8% | ++- | ++- |
| 1.2% | ++- | ++- |
| 1.8% | +-- | +-- |
아지드나트륨은 질소 3개가 이중결합으로 연결되어 있는 질소 화합물로 생물에 대해 독성 물질이며, 박테리아의 유전자 변이를 일으켜 세균을 제거한다.24) 하지만 페녹시에탄올과 1,2-헥산디올과 다르게 인체에 대해 유해성이 보고된 바 있으며, 이 때문에 일부 세균을 제거하는 데 사용되는 용도 외에 화장품 등의 용도로 사용되지 않는다. 아지드나트륨은 특히 효소당화 공정에서 오염을 방지하기 위한 방부제로 사용된다. 하지만 아지드나트륨의 독성으로 인해 당화용액을 발효하는 과정에서 저해요소로 작용하여 효소당화 연구에만 사용되고 있다.25) 아지드나트륨은 세균을 제거하는 데 사용되지만, 그 효과는 미생물의 종류에 따라 크게 달라진다. 특히 진균을 제거하는 용도로는 적합하지 않다는 보고가 있으며, 세균 중에서도 아지드나트륨에 의해 억제되지 않는 세균도 많다. 이러한 연구결과를 바탕으로 본 실험에 사용된 세균은 아지드나트륨에의해 성장이 억제된 것이 확인되었지만, 그 효과는 1,2-헥산디올과 비슷하게 확인되었다. 때문에 1,2-헥산디올처럼 아지드나트륨은 단독으로 사용되는 것이 아닌 다른 보존제와 함께 사용되어야 하는 것으로 판단된다.
아지드나트륨이 첨가된 나노셀룰로오스 현탁액의 오염 후 잔류하는 점도 측정 결과를 Fig. 5에 나타낸 결과 S. xylosus와 B. subtilis 모두 점도가 감소하였고 그 정도는 비슷한 수준으로 감소하였다. 앞에서 사용한 페녹시에탄올과 1,2-헥산디올은 낮은 농도가 첨가되었을 때, 미생물 오염에 의한 점도 저하가 컸다. 하지만 농도가 증가함에 따라 오염에 의한 점도 감소가 적거나 확인되지 않았다. 하지만 아지드나트륨을 첨가한 나노셀룰로오스 현탁액의 경우 다른 보존제를 첨가한 경우보다 점도가 감소하였으며, 1.6%를 첨가한 경우에도 10% 이상 점도가 감소하였다. 아지드나트륨을 첨가하는 경우 보존제를 첨가하지 않은 나노셀룰로오스 현탁액에 비해 점도 감소 수준이 낮지만, 다른 보존제에 비해 미생물 오염을 방지하는데 어려운 것으로 판단된다. 특히 1,2-헥산디올의 경우 S. xylosus의 경우에만 1,2-헥산디올에 영향을 덜 받는 것으로 확인되었으나, 두 미생물 모두 아지드나트륨에 대해 다른 두 보존제보다 보존 능력이 떨어지는 것으로 판단된다.
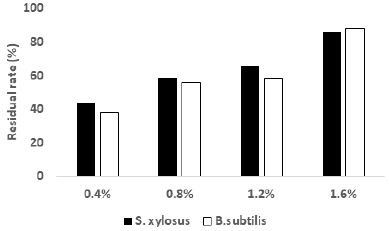
Fig. 5.
Viscosity residual rate of contaminated nanocellulose with sodium azide by S. xylosus and B. subtilis.
4. 결 론
본 연구에서는 나노셀룰로오스 현탁액의 미생물 오염에 의한 물성 저하와 이를 방지하기 위해 보존제를 사용하여 미생물 오염을 방지하고자 하였다. 나노셀룰로오스 현탁액을 보존제 없이 미생물 오염에 노출하게 되면 점도적 특성이 매우 저하되는 것이 확인됐으며, 이를 방지하기 위해 보존제가 필요하다.
보존제를 첨가한 나노셀룰로오스 현탁액을 미생물 오염에 노출시켰을 때, 가장 효과가 좋은 것은 페녹시에탄올로 확인되었으며, 1,2-헥산디올, 아지드나트륨 순으로 보존 효과가 우수하였다. 페녹시에탄올의 경우 1.2% 이상 첨가된 경우 미생물에 의한 점도 저하 문제를 확인할 수 없었다. 1,2-헥산디올, 아지드나트륨을 보존제로 사용한 경우 1.6% 농도로 첨가하였을 때, 미생물에 의한 오염을 방지하기 위해서는 보존제 함량을 1.6% 이상 첨가해야 할 것으로 판단된다.
Acknowledgements
이 논문은 2017년도 정부(교육부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업임(No. NRF-2016R1D1A1A09916310).
Literature Cited
J. Y. Lee, C. H. Kim, E. H. Kim, T. U. Park, J. P. Jeun and S. Y. Kim, Journal of Korea TAPPI,
Evaluation of electron beam irradiation as new pretreatment for cellulose nanofibril production,
48(4); 99-106 (2016)
Lee, J. Y., Kim, C. H., Kim, E. H., Park, T. U., Jeun, J. P., and Kim, S. Y., Evaluation of electron beam irradiation as new pretreatment for cellulose nanofibril production, Journal of Korea TAPPI 48(4):99-106 (2016).
10.7584/jktappi.2016.08.48.4.99N. Lavoine, I. Desloges, A. Dufresne and J. Bras, Carbohydrate Polymers,
Microfibrillated cellulose - Its barrier properties and application in cellulosic materials: A review,
90(2); 735-764 (2012)
Lavoine, N., Desloges, I., Dufresne, A., and Bras, J., Microfibrillated cellulose - Its barrier properties and application in cellulosic materials: A review, Carbohydrate Polymers 90(2): 735-764 (2012).
10.1016/j.carbpol.2012.05.026A. Šturcová, G. R. Davies and S. J. Eichhorn, Biomacromolecules,
Elastic modulus and stress-transfer properties of tunicate cellulose whiskers,
6(2); 1055-1061 (2005)
Šturcová, A., Davies, G. R., and Eichhorn, S. J., Elastic modulus and stress-transfer properties of tunicate cellulose whiskers, Biomacromolecules 6(2):1055-1061 (2005).
A. Bhatnagar and M. Sain, Journal of Reinforced Plastics and Composites,
Processing of cellulose nanofiberreinforced composites,
24(12); 1259-1268 (2005)
Bhatnagar, A. and Sain, M., Processing of cellulose nanofiberreinforced composites, Journal of Reinforced Plastics and Composites 24(12): 1259-1268 (2005).
10.1177/0731684405049864M. C. Li, Q. Wu, K. Song, S. Lee, Y. Qing and Y. Wu, ACS Sustainable Chemistry & Engineering,
Cellulose nanoparticles: Structure-morphology-rheology relationships,
3(5); 821-832 (2015)
Li, M. C., Wu, Q., Song, K., Lee, S., Qing, Y., and Wu, Y., Cellulose nanoparticles: Structure-morphology-rheology relationships, ACS Sustainable Chemistry & Engineering 3(5):821-832 (2015).
10.1021/acssuschemeng.5b00144M. Jorfi and E. J. Foster, Journal of Applied Polymer,
Recent advances in nanocellulose for biomedical applications,
132(14); 41719 (2015)
Jorfi, M. and Foster, E. J., Recent advances in nanocellulose for biomedical applications, Journal of Applied Polymer 132(14):41719 (2015).
10.1002/app.41719L. Berglund, A. K. Mohanty, M. Misra and L. Drzal (ed.), Cellulose-based nanocomposites; 807-832, In Natural Fibers, Biopolymers and Biocomposites, Boca Raton, Florida. CRC Press. (2005)
Berglund, L., Cellulose-based nanocomposites, In Natural Fibers, Biopolymers and Biocomposites, Mohanty, A. K., Misra, M., and Drzal, L. (ed.), CRC Press, Boca Raton, Florida, pp. 807- 832 (2005).
Y. Peng, D. J. Gardner and Y. Han, Cellulose,
Drying cellulose nanofibrils: In search of a suitable method,
19(1); 91-102 (2012)
Peng, Y., Gardner, D. J., and Han, Y., Drying cellulose nanofibrils: In search of a suitable method, Cellulose 19(1):91-102 (2012).
10.1007/s10570-011-9630-zR. J. Moon, A. Martini, J. Nairn, J. Simonsen and J. Youngblood, Chemical Society Reviews,
Cellulose nanomaterials review: Structure, properties and nanocomposites,
40(7); 3941-3994 (2011)
Moon, R. J., Martini, A., Nairn, J., Simonsen, J., and Youngblood, J., Cellulose nanomaterials review: Structure, properties and nanocomposites, Chemical Society Reviews 40(7): 3941-3994 (2011).
10.1039/c0cs00108bR. Kolakovic, T. Laaksonen, L. Peltonen, A. Laukkanen and J. Hirvonen, International Journal of Pharmaceutics,
Spray dried nanofibrillar cellulose microparticles for sustained drug release,
430(1); 47-55 (2012)
Kolakovic, R., Laaksonen, T., Peltonen, L., Laukkanen, A., and Hirvonen, J., Spray dried nanofibrillar cellulose microparticles for sustained drug release, International Journal of Pharmaceutics 430(1):47-55 (2012).
10.1016/j.ijpharm.2012.03.031N. Butchosa and Q. Zhou, Cellulose,
Water redispersible cellulose nanofibrils adsorbed with carboxymethyl cellulose,
21(6); 4349-4358 (2014)
Butchosa, N. and Zhou, Q., Water redispersible cellulose nanofibrils adsorbed with carboxymethyl cellulose, Cellulose 21(6):4349-4358 (2014).
10.1007/s10570-014-0452-7C. Eyholzer, A. Borges de Couraça, F. Duc, P. E. Bourban, P. Tingaut, T. Zimmermann and K. Oksman, Biomacromolecules,
Biocomposite hydrogels with carboxymethylated, nanofibrillated cellulose powder for replacement of the nucleus pulposus,
12(5); 1419-1427 (2011)
Eyholzer, C., Borges de Couraça, A., Duc, F., Bourban, P. E., Tingaut, P., Zimmermann, T., and Oksman, K., Biocomposite hydrogels with carboxymethylated, nanofibrillated cellulose powder for replacement of the nucleus pulposus, Biomacromolecules 12(5):1419-1427 (2011).
10.1021/bm101131bJ. A. Shatkin, T. H. Wegner, E. T. Bilek and J. Cowie, Tappi Journal,
Market projections of cellulose nanomaterial-enabled products (Part 1): Applications,
13(5); 9-16 (2014)
Shatkin, J. A., Wegner, T. H., Bilek, E. T., and Cowie, J., Market projections of cellulose nanomaterial-enabled products (Part 1): Applications, Tappi Journal 13(5):9-16 (2014).
J. Cowie, E. T. Bilek, T. H. Wegner and J. A. Shatkin, Tappi Journal,
Market projections of cellulose nanomaterial-enabled products (Part 2): Volume estimates,
13(6); 57-69 (2014)
Cowie, J., Bilek, E. T., Wegner, T. H., and Shatkin, J. A., Market projections of cellulose nanomaterial-enabled products (Part 2): Volume estimates, Tappi Journal 13(6):57-69 (2014).
J. G. Wijman, P. P. de Leeuw, R. Moezelaar, M. H. Zwietering and T. Abee, Applied and Environmental Microbiology,
Air-liquid interface biofilms of Bacillus cereus: Formation, sporulation, and dispersion,
73(5); 1481-1488 (2007)
Wijman, J. G., de Leeuw, P. P., Moezelaar, R., Zwietering, M. H., and Abee, T., Air-liquid interface biofilms of Bacillus cereus: Formation, sporulation, and dispersion, Applied and Environmental Microbiology 73(5):1481-1488 (2007).
10.1128/aem.01781-06K. Huttunen, A. Hyvärinen, A. Nevalainen, H. Komulainen and M. R. Hirvonen, Environmental Health Perspectives,
Production of proinflammatory mediators by indoor air bacteria and fungal spores in mouse and human cell lines,
111(1); 85-92 (2003)
Huttunen, K., Hyvärinen, A., Nevalainen, A., Komulainen, H., and Hirvonen, M. R., Production of proinflammatory mediators by indoor air bacteria and fungal spores in mouse and human cell lines, Environmental Health Perspectives 111(1):85-92 (2003).
10.1289/ehp.5478L. E. Berghem and L. G. Pettersson, European Journal of Biochemistry,
The mechanism of enzymatic cellulose degradation: Purification of a cellulolytic enzyme from Trichoderma viride active on highly ordered cellulose,
37(1); 21-30 (1973)
Berghem, L. E. and Pettersson, L. G., The mechanism of enzymatic cellulose degradation: Purification of a cellulolytic enzyme from Trichoderma viride active on highly ordered cellulose, European Journal of Biochemistry 37(1): 21-30 (1973).
10.1111/j.1432-1033.1973.tb02952.xW. Li, W. W. Zhang, M. M. Yang and Y. L. Chen, Molecular Biotechnology,
Cloning of the thermostable cellulase gene from newly isolated Bacillus subtilis and its expression in Escherichia coli,
40(2); 195-201 (2008)
Li, W., Zhang, W. W., Yang, M. M., and Chen, Y. L., Cloning of the thermostable cellulase gene from newly isolated Bacillus subtilis and its expression in Escherichia coli, Molecular Biotechnology 40(2):195-201 (2008).
10.1007/s12033-008-9079-yZ. Pourramezan, G. R. Ghezelbash, B. Romani, S. Ziaei and A. Hedayatkhah, Microbiology,
Screening and identification of newly isolated cellulose-degrading bacteria from the gut of xylophagous termite Microcerotermes diversus (Silvestri),
81(6); 736-742 (2012)
Pourramezan, Z., Ghezelbash, G. R., Romani, B., Ziaei, S., and Hedayatkhah, A., Screening and identification of newly isolated cellulose-degrading bacteria from the gut of xylophagous termite Microcerotermes diversus (Silvestri), Microbiology 81(6):736-742 (2012).
10.1134/s0026261712060124P. Gilbert, E. G. Beveridge and P. B. Crone, Microbios,
Effect of phenoxyethanol on the permeability of Escherichia coli NCTC 5933 to inorganic ions,
19(75); 17-26 (1977)
Gilbert, P., Beveridge, E. G., and Crone, P. B., Effect of phenoxyethanol on the permeability of Escherichia coli NCTC 5933 to inorganic ions, Microbios 19(75):17-26 (1977).
P. Gilbert, G. Beveridge and P. B. Crone, The Journal of Pharmacy and Pharmacology,
The action of phenoxyethanol upon respiration and dehydrogenase enzyme systems in Escherichia coli [proceedings],
28; 51 (1976)
Gilbert, P., Beveridge, G., and Crone, P. B., The action of phenoxyethanol upon respiration and dehydrogenase enzyme systems in Escherichia coli [proceedings], The Journal of Pharmacy and Pharmacology 28:51 (1976).
E.-Y. Choi, Kor. J. Aesthet Cosmetol,
Effect of phenoxyethanol and alkane diol mixture on the anti-microbial activity and antiseptic ability in cosmetics,
13(2); 213-220 (2015)
Choi, E.-Y., Effect of phenoxyethanol and alkane diol mixture on the anti-microbial activity and antiseptic ability in cosmetics, Kor. J. Aesthet Cosmetol. 13(2):213-220 (2015).
S. J. Hwang, S. Park, J. K. Hwang and J. G. Pan, Letters in Applied Microbiology,
Food-grade antimicrobials potentiate the antibacterial activity of 1, 2-hexanediol,
60(5); 431-439 (2015)
Hwang, S. J., Park, S., Hwang, J. K., and Pan, J. G., Food-grade antimicrobials potentiate the antibacterial activity of 1, 2-hexanediol, Letters in Applied Microbiology 60(5):431-439 (2015).
10.1111/lam.12398J. A. Jones, J. R. Starkey and A. Kleinhofs, Mutation Research/Genetic Toxicology,
Toxicity and mutagenicity of sodium azide in mammalian cell cultures,
77(3); 293-299 (1980)
Jones, J. A., Starkey, J. R., and Kleinhofs, A., Toxicity and mutagenicity of sodium azide in mammalian cell cultures, Mutation Research/Genetic Toxicology 77(3):293-299 (1980).
10.1016/0165-1218(80)90064-6Y. W. Nam, J. E. Kim, J. Cho, S. P. Chung, H. S. Lee and E. C. Kim, Journal of the Korean Society of Clinical Toxicology,
A lethal case of sodium azide ingestion,
6(1); 49-51 (2008)
Nam, Y. W., Kim, J. E., Cho, J., Chung, S. P., Lee, H. S., and Kim, E. C., A lethal case of sodium azide ingestion, Journal of the Korean Society of Clinical Toxicology 6(1):49-51 (2008).
M. F. Ibrahim, S. Abd-Aziz, M. E. M. Yusoff, L. Y. Phang and M. A. Hassan, Renewable Energy,
Simultaneous enzymatic saccharification and ABE fermentation using pretreated oil palm empty fruit bunch as substrate to produce butanol and hydrogen as biofuel,
77; 447-455 (2015)
Ibrahim, M. F., Abd-Aziz, S., Yusoff, M. E. M., Phang, L. Y., and Hassan, M. A., Simultaneous enzymatic saccharification and ABE fermentation using pretreated oil palm empty fruit bunch as substrate to produce butanol and hydrogen as biofuel, Renewable Energy 77: 447-455 (2015).
10.1016/j.renene.2014.12.047








