1. 서 론
리그닌은 자연계에 존재하는 유기고분자 중 셀룰로오스 다음으로 풍부하며 지속가능한 자원이다.1) 식물세포 내에 리그닌은 수종에 따라 차이는 있으나 약 20-40%의 비율로 존재하며 coniferyl, sinapyl, 그리고 p-coumaryl alcohol의 단위체를 기반으로 3차원의 매우 복잡한 구조를 가지고 있는 무정형 고분자 물질이다.1,2) 2017년 Orbisresearch3)에서 발간한 “Global Lignin Products Market-Trends and Forecasts 2017” 보고서에 따르면, 세계적으로 7,000만 톤의 리그닌이 펄핑과정 중 부산물로서 발생하나 대부분은 에너지 생산 또는 매립을 통해 처리되고 약 2-3%만이 다른 용도를 위해 사용된다.
최근 석유계 자원의 고갈현상과 함께 환경적 규제가 강화됨에 따라 석유계 자원으로부터 유래된 oil, 화학약품, 고분자 등과 같은 제품의 대체자원 개발에 대한 관심이 급증하고 있다. C6-C3 phenylpropane 기반의 리그닌은 석유계 자원으로부터 유래된 페놀성 고분자를 대체할 수 있는 물질로서 주목받고 있으며 리그닌의 고도활용을 위한 연구가 다방면에서 진행되고 있다. 석유를 대체하기 위한 연구로서 Cheng 등4)은 리그닌을 이용한 biofuel 개발을 진행하였고 Qin 등5)은 sulfonated alkali lignin을 graft중합하였을 때 기존에 coal-water slurry의 분산제로 사용되었던 naphthalene sulfonate보다 우수한 특성을 나타냈다고 보고하였다. 또한 Ferry 등6)은 lignin과 polybutylene succinate를 중합하여 flame retardant로서 활용하고자 하였으며, Abu-Dalo 등7)은 금속의 부식억제제로서 리그닌을 이용하는 연구를 수행하였다.
리그닌의 고도활용을 위해서 각각의 활용분야에 적합한 리그닌을 선택하는 것은 매우 중요하다. 왜냐하면 리그닌을 구성하고 있는 단위체의 함량이나 구조 및 물리·화학적 특성이 리그닌을 부산물로서 생산하는 전처리 방법에 따라 상이해질 수 있기 때문이다.2) 리그닌을 생산하는 대표적인 전처리 방법으로는 화학펄핑, 생물학적 처리, steam explosion, 이온성 액체, 공융용매, 초임계 처리 등이 있다.8) 크라프트 펄핑은 대표적인 펄프제조방법으로 펄핑 시 발생하는 리그닌이 전 세계적으로 생산되는 리그닌의 85%를 차지하고 있다.9) 그러나 증해 중 2차 변성이 발생하여 다분자성이 높고 분리 및 정제가 복잡하여 다른 용도로의 활용이 쉽지 않은 실정이다.9) Steam explosion은 물리적 힘과 화학적인 효과를 동시에 사용하는 방법으로 에너지비용이 낮고 친환경적이며 재활용비용이 발생하지 않는 장점이 있으나8) digestion이 불완전하고10) 반응 중에 repolymerization을 수반하여 불균일한 구조의 리그닌을 생성한다고 보고된 바 있다.11,12) 초임계수를 이용한 바이오매스의 전처리는 처리시간이 짧고 toxicity가 낮은 방법으로 처리과정 중 리그닌의 β-O-4 결합이 파괴되는 것으로 알려져 있다.13) 앞서 언급한 바와 같이 전처리방법에 따라 리그닌의 변화가 다양한 방식으로 발생하기 때문에 각각의 전처리에 의해 제조된 리그닌을 효율적으로 활용하기 위해서는 여러 종류의 리그닌에 대한 특성규명이 명확하게 이뤄져야 한다.
따라서 본 연구에서는 일차적으로 활엽수 크라프트 리그닌, 억새 steam-explosion 리그닌, 초임계당화 잔사 리그닌, 상업용 크라프트 리그닌 등 4가지 종류의 리그닌에 대해 thermogravimetric(TG), derivative thermogravimetric(DTG), differential scanning calorimetry(DSC) 등의 열적 특성을 분석하고 분자량, syringyl/guaiacyl 비율(S/G ratio), 작용기의 분포 등 구조적, 화학적 특성을 파악하고자 하였다.
2. 재료 및 방법
2.1 실험재료
2.1.1 리그닌
각각의 전처리방법에 따라 추출된 리그닌의 특성을 파악하기 위하여 활엽수 크라프트 리그닌(L1), 억새 steam-explosion 리그닌(L3), 상업용 크라프트 리그닌(L4) 등을 A, B, C사로부터 분양받아 사용하였으며 초임계 당화 잔사 리그닌(L2)은 국립산림과학원의 연속식 초임계 당화장치를 이용해 신갈나무 목분을 처리한 후 남은 잔사로부터 추출하여 분석에 사용하였다.
2.1.2 시약
실험에 사용된 pyridine(99.5%), acetic anhydride (98.0%), tetrahydrofuran(THF, 99.5%) 등은 Daejung Chemicals로부터 구입하였으며 CDCl3(99.8%), hydriodic acid(99.95%), ethyl iodide(99%), pentane (99%) 등은 Sigma-aldrich사의 제품을 사용하였다.
2.2 실험방법
2.2.1 아세틸레이션
분자량, proton nuclear magnetic resonance(1H-NMR) 분석 등을 위해 각 리그닌의 아세틸레이션을 진행하였다. 약 100 mg의 리그닌을 2 mL의 pyridine에 용해한 후 acetic anhydride 2 mL를 첨가하고 상온 하에서 12시간 동안 교반하였다. 12시간 반응 후에, 아세틸화 반응물을 200 mL의 얼음이 첨가된 증류수에 교반하면서 천천히 한 방울씩 첨가하여 리그닌의 뭉침현상을 방지하면서 증류수에 침전시켰다. 이후 증류수 내에 침전된 리그닌을 직경 47 mm, 공극 직경 0.45 µm의 nylon membrane filter를 이용해 여과하고 차가운 탈이온수로 세척한 후 동결건조기(FDCF-12006, OPERON)에서 동결건조하여 분석에 사용하였다. 분석 시 Fourier transform infrared(FT-IR) 분석을 통해 아세틸레이션 여부를 확인한 후에 각 분석을 실시하였다.
2.2.2 분자량 분석
각 리그닌의 분자량 분포를 확인하기 위하여 아세틸레이션된 리그닌 1 mg을 THF 1 mL에 용해한 후 gel permeation chromatography(GPC, Shimadzu, UV and RI detectors)를 이용해 분석하였다. GPC column은 PLgel 5 µm mixed-C, -D, 그리고 PLgel 3 µm mixed-E를 순차적으로 연결하여 분석에 사용하였으며 oven 온도는 40℃로 설정하였다. UV 검출기의 파장은 280 nm, injection volume은 100 µL로 설정하였고 THF를 이동상으로 하여 1 mL/min의 조건으로 흘려주었다. 분자량에 대한 검량선 작성은 1,480에서 1,233,000 g/mol범위의 polystyrene standard를 이용하였으며 작성된 검량선을 통해 각 리그닌의 분자량 분포를 분석하였다.
2.2.3 화학적 구조 분석
FT-IR 분석은 PerkinElmer사의 attenuated total reflectance attachment(ATR)가 장착된 Frontier 모델을 이용하여 각 시료당 256번의 스캔을 실시하였다.
Phenolic hydroxyl 그룹과 aliphatic hydroxyl 그룹 함량을 파악하기 위해 Bruker사의 FT-NMR 600 MHz spectrometer(Bruker Avance Ⅱ 600)를 이용하여 1H-NMR 분석을 실시하였다. 아세틸레이션된 리그닌 시료당 스캔수는 300 K 조건에서 128회 실시하였으며 acquisition time 1.3초, 90° pulse, relaxation delay 7초의 조건으로 분석을 수행하였다. 4.0-3.5 ppm 영역의 methoxyl region을 1로 설정하여 2.4-2.2, 2.2-1.8 ppm 영역의 phenolic hydroxyl, aliphatic hydroxyl 그룹의 적분을 실시하였으며 정량분석된 methoxyl group의 값을 기준으로 각 hydroxyl group의 정량값을 다음 식에 의해 산출하였다.
Hydroxyl group(mmol/g)=Methoxyl group(mmol/g)×Integral value of hydroxyl group
2.2.4 Methoxyl 그룹 함량 분석
Methoxyl 그룹은 gas chromatography/flame ionization detector(GC/FID)를 이용하였으며 박 등14)의 방법에 기초하였다. 30 mg의 리그닌을 정량한 후 4 mL의 hydriodic acid와 함께 바이얼에 투입하고 130℃의 oil bath에서 30분간 반응시켰다. 반응 중 5분 간격으로 흔들어 주었으며 반응 후 얼음물에서 냉각하였다. 냉각된 용액에 내부표준물질로 200 µL의 ethyl iodide(300 mg/mL pentane)를 첨가하고 3 mL의 pentane을 추가적으로 투입하였다. 전체 용액을 충분히 교반한 후 다시 얼음물에서 냉각하고 상분리된 용액에서 pentane상에 속하는 부분을 분취하여 GC/FID에서 분석을 실시하였다. 분석에 사용된 GC는 Agilent사의 7890B모델을 사용하였으며 DB-624 column(30 m×0.25 mm i.d.)을 이용하였다. Injector와 detector 온도는 200, 230℃로 설정하였으며 Oven의 온도 조건은 40℃에서 5분간 유지한 후 분당 10℃의 속도로 180℃까지 가열하였다. 이동상은 질소를 이용하였으며 flow rate은 1.1 mL/min, split ratio는 1/120으로 설정하였다.
2.2.5 S/G ratio 분석
각 리그닌별 구성성분과 S/G ratio를 파악하기 위해 pyrolysis gas chromatography/mass spectrometer(Py-GC/MS) 분석을 실시하였다. Pyrolyzer는 Frontier lab의 Oy-2020iD, GC와 MS는 Agilent사의 5975C, 7890A 모델을 사용하였으며 column은 DB-5MS(30 m×0.25 mm×0.25 µm)를 이용하였다. 0.5 mg의 시료를 비활성화된 SUS 컵에 담고 550℃에서 열분해한 후 열분해한 가스를 GC/MS로 주입하여 분석을 실시하였다. Column flow는 0.7 mL/min, split ratio는 1/70으로 설정하였다. Oven 온도 조건은 40℃에서 5분간 유지한 후 분당 10℃의 속도로 310℃까지 상승시키고 동일온도에서 10분간 유지하였다.
2.2.6 열분석
각 리그닌의 열적 특성을 파악하기 위해 thermogravimetric analyzer(TGA 8000, PerkinElmer)와 Differential scanning calorimetry(DSC Q2000, TA Instrument)를 이용하여 분석을 실시하였다. TGA 분석 시 리그닌 1 mg을 분당 20℃의 승온속도로 650℃까지 가열하였으며 sample gas는 Helium을 이용하였다. DSC 분석은 약 2 mg의 리그닌을 이용해 첫 스캔 시 분당 10℃의 속도로 상온에서 105℃까지 승온시킨 후 다시 20℃까지 동일한 속도로 냉각하고 두 번째 스캔을 분당 5℃의 승온속도로 180℃까지 수행하였다. 세 번째 스캔은 두 번째 스캔과 동일한 조건으로 설정하였으며 두 번째 스캔으로부터 얻은 DSC thermogram을 통해 유리전이온도를 분석하였다.
3. 결과 및 고찰
3.1 분자량 분포
리그닌의 제조방법에 따른 분자량 분포를 확인하고자 GPC 분석을 실시하였으며 그 결과를 Table 1과 Fig. 1에 나타냈다. 중량평균분자량은 리그닌의 제조방법에 따라 상이한 값을 가지는 것으로 분석되었으며 활엽수 크라프트 리그닌 L1의 중량평균분자량이 5,680 g/mol로 가장 낮게 측정되었다. 크라프트 펄핑 시 주요 리그닌 개열 반응은 반응종인 OH-, SH-에 의한 페놀성, 비페놀성 β-aryl ether 결합의 개열이며, 펄핑 중 발생하는 retro-aldol 반응은 저분자화된 리그닌의 condensation을 감소시키는 것으로 보고된 바 있다.15) 본 연구에서 사용된 활엽수 크라프트 리그닌도 크라프트 펄핑 시 발생하는 기작들의 영향에 의해 저분자화되어 낮은 분자량 범위를 나타낸 것으로 사료된다. 한편, 초임계당화법에 의해 추출된 리그닌인 L2는 L1에 비해 높은 분자량과 낮은 PDI 값을 가지는 것으로 분석되었다. 또한 L3의 분자량은 16,430 g/mol로 가장 높은 값을 나타냈으며 PDI 값도 6.8로 다른 리그닌에 비해 상대적으로 넓은 분자량 범위를 지니는 것으로 분석되었다. Robert 등16)은 steam explosion처리 시 β-O-4 결합의 파괴와 함께 C-C condensed 구조가 증가한다고 보고한 바 있으며 Jiebing 등11)과 Auxenfans 등12)은 동일처리 시 β-O-4 결합의 파괴가 repolymerization을 수반하여 분자량 분포가 넓어지고 더 불균일한 구조의 리그닌을 생성한다고 보고하였다. 따라서 L3의 높은 분자량과 PDI 값은 steam explosion 처리 시 발생한 repolymerization에 기인한 것으로 판단된다.
Table 1.
Molecular weight distributions and polydispersity index (PDI) of various lignins
| No. | Species | Mn (g/mol) | Mw (g/mol) | PDI |
|---|
| L1 | Kraft lignin (hardwood) | 1,430 | 5,680 | 4.0 |
| L2 | Supercritical water extraction lignin (hardwood) | 2,170 | 8,280 | 3.8 |
| L3 | Steam-explosion lignin (silver glass) | 2,400 | 16,430 | 6.8 |
| L4 | Commercial kraft lignin (unknown) | 2,120 | 9,460 | 4.5 |
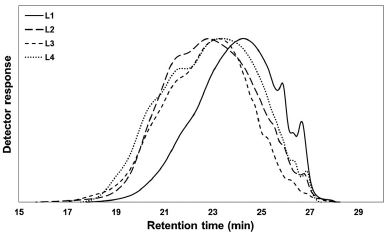
Fig. 1.
Molecular weight distribution curves of various lignins.
3.2 화학적 구조
각 리그닌의 FT-IR분석 결과를 Fig. 2에 나타냈으며 스펙트럼의 분석은 Lisperguer 등,17) Boerju 등,18) Faix19) 등의 연구에 기초하였다. 모든 리그닌의 스펙트럼은 absorbance의 차이는 있었으나 전체적으로 유사한 형태를 나타냈다. 3,600-3,000 cm-1 파장에서 hydroxyl 그룹의 OH기로부터 유래된 peak이 나타났으며 methylene 그룹과 methyl 그룹의 CH stretching이 2,850-2,830 cm-1 파장에서 나타났다. 일반적으로 2,000 cm-1 이하의 영역에서 리그닌의 IR spectrum은 다양한 작용기가 확인되기 때문에 복잡한 형태를 나타내고 이에 대한 분석이 매우 어렵다. 1,720에서 1,660 cm-1 파장에서 carbonyl 그룹의 unconjugated C=O, 1,510-1,500 cm-1 파장에서 aromatic ring band유래의 peak이 관찰되었다. 또한 Phenolic hydroxyl 그룹의 C-O stretching에 기인한 peak이 1,120-1,110 cm-1 파장에서 강하게 나타났으며, methoxyl group의 C-O deformation에서 유래된 peak이 1,030-1,020 cm-1 파장에서 확인되었다.
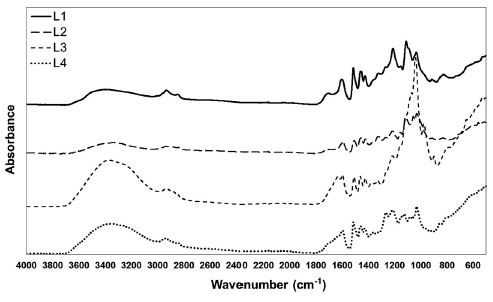
Fig. 2.
FT-IR spectra of various lignins.
3.3 작용기 분석
각 리그닌의 phenolic hydroxyl 그룹과 aliphatic hydroxyl 그룹에 대해 분석하기 위하여 1H-NMR 분석을 실시하였으며 NMR spectrum을 Fig. 3에 나타냈다. 4-3.5 ppm영역에서 methoxyl group이 나타났고 이 영역을 1로 설정한 후 2.4-2.2, 2.2-1.8 ppm 영역의 phenolic hydroxyl, aliphatic hydroxyl 그룹의 비율을 분석하였다. 또한 methoxyl 그룹을 정량하고 분석된 값을 이용하여 각 hydroxyl 그룹의 함량을 산출하였으며 각 작용기 함량에 대한 산출결과를 Table 2에 나타냈다.
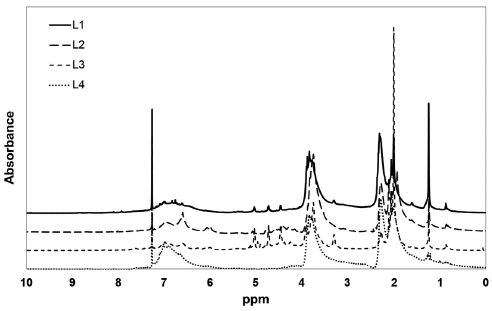
Fig. 3.
1H-NMR spectra of various lignins.
Table 2.
The contents of methoxyl and hydroxyl groups of various lignins
| Lignin | Methoxyl groups
(mmol/g) | Phenolic OH
(mmol/g) | Aliphatic OH
(mmol/g) | Total OH
(mmol/g) |
|---|
| L1 | 4.0 | 2.8 | 1.8 | 4.6 |
| L2 | 3.1 | 1.1 | 2.4 | 3.5 |
| L3 | 0.8 | 0.2 | 1.1 | 1.3 |
| L4 | 1.6 | 1.1 | 1.7 | 2.8 |
Methoxyl 그룹과 hydroxyl 그룹은 리그닌을 나타내는 특징적인 작용기이다. L1-L4의 methoxyl 그룹 함량은 4.0, 3.1, 0.8, 1.6 mmol/g으로 초본류인 억새로부터 유래된 L3이 가장 낮은 methoxyl 그룹을 함유하고 있는 것으로 분석되었다. 또한 L4의 경우 활엽수를 이용한 L1, L2에 비해 절반 이하의 methoxyl 그룹 함량을 가진 것으로 분석되었다. 초본류 리그닌은 목재에 존재하는 리그닌과 다르게 한 개의 methoxyl 그룹을 가진 guaiacyl 구조와 두 개의 methoxyl 그룹을 가진 syringyl 구조뿐만 아니라 methoxyl 그룹이 없는 hydroxyphenyl 구조를 가지기 때문에 억새로부터 추출된 리그닌인 L3의 methoxyl 그룹 함량이 가장 낮은 것으로 판단된다.12)
총 hydroxyl 그룹과 phenolic hydroxyl 그룹 함량은 methoxyl 그룹 함량과 동일한 경향을 나타냈으나 aliphatic hydroxyl 그룹은 반대 경향을 나타냈다. 일반적으로 저분자량 영역의 리그닌이 다량의 methoxyl 그룹과 phenolic hydroxyl 그룹을 함유하는 것으로 알려져 있으며14) 본 연구의 결과에서도 리그닌의 제조방법에 관계없이 동일한 경향을 얻을 수 있었다. 또한 aliphatic hydroxyl 그룹의 경우 L2에서 가장 높은 값을 나타냈으며 이는 초임계당화공정 중 리그닌의 propane side chain에 대한 공격으로 인해 다량의 aliphatic hydroxyl 그룹이 형성되었기 때문인 것으로 판단된다.13)
리그닌의 hydroxyl 그룹은 리그닌의 용해성을 증가시킴과 동시에 다양한 고분자와의 반응성도 증가시킨다.20) 따라서, 높은 hydroxyl 그룹 함량을 지닌 저분자량 영역의 리그닌이 리그닌 개질에 보다 적합하다고 할 수 있으며 본 연구에 사용된 4종의 리그닌 중 저분자 영역에 속하는 활엽수 크라프트 리그닌(L1)이 다른 리그닌에 비해 리그닌 개질에 더 알맞은 소재인 것으로 판단된다.
3.4 S/G ratio
Py-GC/MS 분석을 통해 각 리그닌의 pyrolysis products를 분석하였으며 그 결과를 Table 3에 나타냈다. L4를 제외한 리그닌 시료들의 주요 pyrolysis products로는 guaiacyl 유형의 guaiacol, 4-methylguaiacol, 4-ethylguaiacol, 4-vinylguaiacol, isoeugenol, 4-propylguaiacol, acetoguaiacone, vanillin, 4-hydroxy-3-methoxy-benzoic acid 등과 syringyl 유형의 3,4-dimethoxyphenol, 4-allylsyringol, syringylaldehyde, acetosyringone, sinapinaldehyde, 4,4’-methylenebis[2,6-dimethoxy]-phenol 등으로 분석되었다. L4의 경우 guaiacyl 유형의 리그닌은 동일하게 분석되었으나 syringyl 유형의 리그닌이 미검출됨에 따라 guaiacyl 유형의 리그닌만으로 구성된 침엽수를 원료로 사용하여 제조한 것으로 판단되며 이는 methoxyl 그룹 함량 측정결과와도 일치하는 경향이다. Rio 등21)에 따르면 침엽수 리그닌은 주로 guaiacyl 유형의 리그닌과 소량의 hydroxyphenyl 유형의 리그닌으로 구성되어 있다고 보고된 바 있다.
Table 3.
Pyrolysis products of various lignins
| Compounds | Relative distribution of pyrolysis products (%) |
|---|
| L1 | L2 | L3 | L4 |
|---|
| Phenol | 1.18 | - | - | 0.91 |
| p-Cresol | 1.67 | - | - | 3.85 |
| 3,5-Xylenol | - | - | - | 2.21 |
| Guaiacol | 5.76 | 4.45 | 4.47 | 10.54 |
| 4-Methylguaiacol | 9.81 | 5.13 | 5.13 | 24.08 |
| 4-Ethylguaiacol | 4.77 | 2.24 | 2.34 | 9.71 |
| 4-Vinylguaiacol | 5.92 | 4.88 | 4.75 | 11.85 |
| Isoeugenol | 3.57 | 3.45 | 3.41 | 12.37 |
| 4-Propylguaiacol | - | - | - | 2.35 |
| Acetoguaiacone | 1.39 | 1.47 | 1.62 | 2.82 |
| Vanillin | 1.53 | 2.52 | 2.20 | 2.54 |
| Benzoic acid, 4-hydroxy-3-methoxy- | 12.38 | 10.72 | 10.40 | 2.86 |
| 3,4-Dimethoxyphenol | 16.00 | 15.75 | 14.99 | - |
| 4-Allylsyringol | 1.27 | 14.36 | 14.52 | - |
| Syringylaldehyde | 3.18 | 6.30 | 6.16 | - |
| Acetosyringone | 2.72 | 3.59 | 3.56 | - |
| Sinapinaldehyde | - | 2.56 | 2.55 | - |
| Phenol, 4,4’-methylenebis[2,6-dimethoxy- | 3.21 | 1.13 | 1.22 | - |
| 1,2-Benzenediol, 3-methoxy- | 8.64 | 4.05 | 3.19 | - |
| 1,2-Benzenediol | - | - | - | 4.23 |
| 1,2-Benzenediol, 4-methyl- | - | - | - | 7.40 |
| Sum (G type) | 45.12 | 34.88 | 34.32 | 79.11 |
| Sum (S type) | 26.37 | 43.69 | 43.01 | - |
| Total | 74.35 | 78.57 | 77.34 | 86.08 |
| S/G ratio | 0.58 | 1.25 | 1.25 | - |
S/G ratio의 경우 L1이 0.58, L2가 1.25, L3이 1.25로 나타났다. 크라프트 펄핑 시 syringyl 유형 리그닌은 guaiacyl 유형 리그닌에 비해 쉽게 탈리그닌화되는 것으로 보고된 바 있으며22,23) 결과적으로 초임계당화공정으로부터 추출된 활엽수 리그닌(L2)에 비해 상대적으로 낮은 활엽수 크라프트 리그닌 L1의 S/G ratio는 syringyl 유형 리그닌의 탈리그닌화에 기인한 것으로 판단된다.
3.5 열적 특성
리그닌의 열분해는 리그닌 내 다양한 구조의 결합에너지에 기초하여 발생한다. 또한 리그닌의 열적 특성은 다양한 분야에 리그닌을 활용하는 데 있어 매우 중요한 요소로서 작용한다. 따라서 본 연구에서는 TG 분석을 통해 다양한 전처리방법이 리그닌의 열분해 거동과 열안정성에 미치는 영향에 대해 파악하고자 하였다.
Fig. 4는 각 리그닌에 대한 TG thermogram으로 L1의 char residue는 35%, L2-L4는 25, 26, 35%로 측정되었다. 리그닌의 열분해에 대한 주요 영향인자는 분자량과 작용기로14) methoxyl 그룹이 다량으로 존재할 경우 리그닌의 char residue는 감소하는 것으로 연구된 바 있으나 분자량에 의한 영향을 함께 고려해야만 한다.24) 또한 Jakab 등24)의 연구에 따르면 syringyl 유형 리그닌에 비해 guaiacyl 유형 리그닌의 condensation 반응이 용이하며 Tejado 등25)은 5번 탄소 위치에 methoxyl group이 없는 guaiacyl 유형 리그닌이 condensed C-C 결합을 형성할 수 있다고 보고하였다. 저분자량인 L1의 열분해는 다른 리그닌에 비해 저온에서 시작되었으나 최종 char residue는 높은 값을 나타냈다. 이는 상대적으로 높은 함량의 guaiacyl 유형 리그닌이 condensed 구조를 형성하였기 때문으로 판단된다. L2와 L3은 열분해에 있어 큰 차이를 보이지 않았으며 guaiacyl 유형 리그닌만으로 구성된 L4가 L1과 함께 가장 높은 char residue값을 나타냈다. 따라서 guaiacyl 유형 리그닌이 char residue에 주요한 영향을 미치는 것으로 보이며 크라프트 펄핑을 통해 추출된 리그닌이 다른 전처리법에 의해 추출된 리그닌에 비해 높은 열안정성을 지니는 것으로 판단된다.
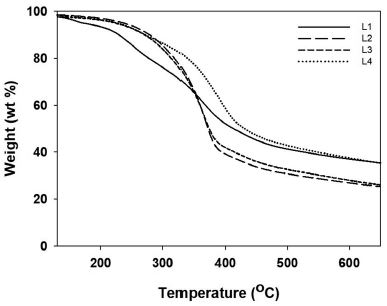
Fig. 4.
TG thermograms of various lignins.
DTG 분석은 온도변화에 따른 상대적인 무게 감소율을 계산함으로써 최대 열분해 온도를 확인할 수 있다. 각 리그닌에 대한 DTG thermogram을 Fig. 5에 나타냈으며 최대분해온도와 유리전이온도 분석결과를 Table 4에 나타냈다. 각 리그닌의 최대분해온도는 L4를 제외하고 360℃ 부근에서 형성되었으며 L4는 약 390℃로 분석되었다. Sun 등26)과 박 등14)에 따르면 리그닌의 methyl-aryl ether 결합의 파괴는 300-400℃에서 발생하고 C-C 결합구조는 370-400℃ 범위에서 파괴된다. 또한 리그닌 내에서 C-C 결합은 매우 중요한 구조이며 C-C 구조 중 aromatic ring의 다섯 번째 탄소를 포함하는 C-C 구조가 더 주도적으로 존재한다.25) Syringyl 유형 리그닌의 경우 5번 탄소위치에 methoxyl 그룹이 존재함에 따라 C-C 구조의 형성이 어렵고 5번 탄소위치에 methoxyl 그룹이 없는 guaiacyl 유형 리그닌이 C-C 구조를 형성할 수 있다.25) 따라서 guaiacyl 유형 리그닌만으로 구성된 L4가 다른 리그닌에 비해 더 많은 수의 condensed C-C 결합을 형성함에 따라 더 높은 최대분해온도를 나타낸 것으로 판단된다.
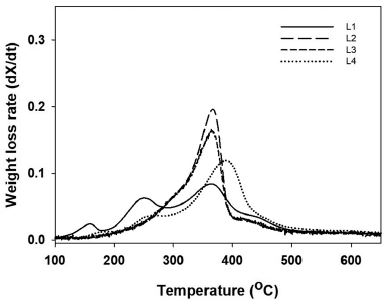
Fig. 5.
DTG thermograms of various lignins.
Table 4.
The maximum degradation and the glass transition temperature of various lignins
| L1 | L2 | L3 | L4 |
|---|
| Max. degradation temp. (℃) | 364 | 367 | 366 | 389 |
| Glass transition temp. (℃) | 124 | 119 | 123 | 174 |
DSC 결과를 바탕으로 유리전이온도의 분석을 실시하였으며 그 결과를 Table 4에 나타냈다. 일반적으로 유리전이온도는 분자량, 수분, 결정 영역 등에 의해 영향을 받는다. 4종의 리그닌 중 L1, L2, L3 등의 유리전이온도는 120℃ 부근에서 형성되었으며 L4는 174℃로 분석되었다. 이는 TGA, DTG 분석결과와 동일한 경향으로 L4를 구성하는 리그닌 유형에 의한 영향으로 판단된다. 또한 Glasser 등27)과 El Khald-Hansen 등28)의 연구에 따르면 침엽수 크라프트 리그닌의 유리전이온도가 활엽수 리그닌에 비해 높은 값을 나타내는 것으로 보고된 바 있으며 본 연구에서도 동일한 결과를 얻을 수 있었다.
4. 결 론
본 연구에서는 리그닌의 고도활용을 위해 다양한 종류의 리그닌에 대해 물리적, 화학적 분석을 실시하였으며 각 리그닌의 전처리 방법에 따른 영향을 파악하고자 하였다. 초임계당화공정에 의해 추출된 활엽수 리그닌의 경우 활엽수 크라프트 리그닌에 비해 분자량이 높았으나 상대적으로 낮은 PDI 값을 갖는 것으로 나타났으며 전체적으로 고분자량 영역의 리그닌이 높은 PDI 값을 갖는 경향을 보였다. 리그닌의 종류에 관계없이 FT-IR spectrum은 absorbance의 차이는 있었으나 전체적으로 유사한 형태를 나타냈다. Methoxyl 그룹과 phenolic hydroxyl 그룹 함량은 분자량이 클수록 적은 것으로 분석되었으며 초본류인 억새 리그닌에서 가장 낮은 함량이 나타났다. 상업용 크라프트 리그닌(L4)의 경우 guaiacyl 유형 리그닌만으로 구성된 것으로 분석되었으며 활엽수 크라프트 리그닌의 S/G ratio가 가장 낮게 측정되었다. 열분해분석 시 크라프트 펄핑으로부터 추출된 리그닌들이 더 높은 열안정성을 가지는 것으로 나타났다. 침엽수에서 추출된 상업용 크라프트 리그닌(L4)의 최대분해온도가 가장 높게 나타났으며 유리전이온도에 있어서도 다른 리그닌에 비해 매우 높은 값을 보였다. 따라서 본 연구를 통해 원료와 전처리방법이 리그닌의 특성에 미치는 영향을 확인할 수 있었으며 분석된 특성을 기반으로 적합한 용도를 개발한다면 리그닌의 활용성을 높이는 계기가 될 수 있을 것으로 판단된다.
Acknowledgements
이 논문은 2018년도 정부(교육부)의 재원으로 한국연구재단 지원을 받아 수행된 기초연구사업임(No. 2018R1A6A1A0325582).
Literature Cited
S. J. Kim, J. Kang, W. J. Youe, S. M. Lee and Y. S. Kim, Journal of Korea TAPPI,
Preparation and mechanical properties of melt-spun carbon fibers from wood tar and wood tar/kraft lignin blends,
49(5); 56-64 (2017)
Kim, S. J., Kang, J., Youe, W. J., Lee, S. M., and Kim, Y. S., Preparation and mechanical properties of melt-spun carbon fibers from wood tar and wood tar/kraft lignin blends, Journal of Korea TAPPI 49(5):56-64 (2017).
10.7584/jktappi.2017.10.49.5.56J. H. Noh, D. S. Kim and Y. J. Sung, Journal of Korea TAPPI,
The isolation of kraft lignin from black liquor during Korean red pine kraft pulping and evaluation of the isolated kraft lignin,
49(4); 170-177 (2017)
Noh, J. H., Kim, D. S., and Sung, Y. J., The isolation of kraft lignin from black liquor during Korean red pine kraft pulping and evaluation of the isolated kraft lignin, Journal of Korea TAPPI 49(4):170-177 (2017).
10.7584/jktappi.2017.08.49.4.170N. Cheng, Y. Yamamoto, K. Koda, Y. Tamai and Y. Uraki, Bioresource Technology,
Amphipathic lignin derivatives to accelerate simultaneous saccharification and fermentation of unbleached softwood pulp for bioethanol production,
173; 104-109 (2014)
Cheng, N., Yamamoto, Y., Koda, K., Tamai, Y., and Uraki, Y., Amphipathic lignin derivatives to accelerate simultaneous saccharification and fermentation of unbleached softwood pulp for bioethanol production, Bioresource Technology 173:104-109 (2014).
10.1016/j.biortech.2014.09.093Y. Qin, D. Yang, W. Guo and X. Qiu, Journal of Industrial and Engineering Chemistry,
Investigation of grafted sulfonated alkali lignin polymer as dispersant in coal-water slurry,
27; 192-200 (2015)
Qin, Y., Yang, D., Guo, W., and Qiu, X., Investigation of grafted sulfonated alkali lignin polymer as dispersant in coal-water slurry, Journal of Industrial and Engineering Chemistry 27:192-200 (2015).
10.1016/j.jiec.2014.12.034L. Ferry, G. Dorez, A. Taguet, B. Otazaghine and J. M. Lopez-Cuesta, Polymer Degradation and Stability,
Chemical modification of lignin by phosphorus molecules to improve the fire behavior of polybutylene succinate,
113; 135-143 (2015)
Ferry, L., Dorez, G., Taguet, A., Otazaghine, B., and Lopez-Cuesta, J. M., Chemical modification of lignin by phosphorus molecules to improve the fire behavior of polybutylene succinate, Polymer Degradation and Stability 113:135-143 (2015).
10.1016/j.polymdegradstab.2014.12.015M. A. Abu-Dalo, N. A. Al-Rawashdeh and A. Ababneh, Desalination,
Evaluating the performance of sulfonated kraft lignin agent as corrosion inhibitor for iron-based materials in water distribution systems,
313; 105-114 (2013)
Abu-Dalo, M. A., Al-Rawashdeh, N. A., and Ababneh, A., Evaluating the performance of sulfonated kraft lignin agent as corrosion inhibitor for iron-based materials in water distribution systems, Desalination 313:105-114 (2013).
10.1016/j.desal.2012.12.007A. K. Kumar and S. Sharma, Bioresources and bioprocessing,
Recent updates on different methods of pretreatment of lignocellulosic feedstocks: a review,
4(1); 7 (2017)
Kumar, A. K. and Sharma, S., Recent updates on different methods of pretreatment of lignocellulosic feedstocks: a review, Bioresources and bioprocessing 4(1):7 (2017).
10.1186/s40643-017-0137-9S. P. Moon, Utilization of lignin : past, present, futureIn proceeding of fall conference of KTAPPI; 34 (2013)
Moon, S. P., Utilization of lignin : past, present, future, In proceeding of fall conference of KTAPPI, p.34 (2013).
V. B. Agbor, N. Cicek, R. Sparling, A. Berlin and D. B. Levin, Biotechnology advances,
Biomass pretreatment: fundamentals toward application,
29(6); 675-685 (2011)
Agbor, V. B., Cicek, N., Sparling, R., Berlin, A., and Levin, D. B., Biomass pretreatment: fundamentals toward application, Biotechnology advances 29(6):675-685 (2011).
10.1016/j.biotechadv.2011.05.005L. Jiebing, G. Henriksson and G. Gellerstedt, Bioresource Technology,
Lignin depolymerization/repolymerization and its critical role for delignification of aspen wood by steam explosion,
98(16); 3061-3068 (2007)
Jiebing, L., Henriksson, G., and Gellerstedt, G., Lignin depolymerization/repolymerization and its critical role for delignification of aspen wood by steam explosion, Bioresource Technology 98(16):3061-3068 (2007).
T. Auxenfans, D. Crônier, B. Chabbert and G. Paës, Biotechnology for Biofuels,
Understanding the structural and chemical changes of plant biomass following steam explosion pretreatment,
10(1); 36 (2017)
Auxenfans, T., Crônier, D., Chabbert, B., and Paës, G., Understanding the structural and chemical changes of plant biomass following steam explosion pretreatment, Biotechnology for Biofuels 10(1):36 (2017).
10.1186/s13068-017-0718-zS. J. Moon, I. Y. Eom, J. Y. Kim, T. S. Kim, S. M. Lee, I. G. Choi and J. W. Choi, Bioresource Technology:,
Characterization of lignin-rich residues remaining after continuous super-critical water hydrolysis of poplar wood (Populus albaglandulosa) for conversion to fermentable sugars,
102(10); 5912-5916 (2011)
Moon, S. J., Eom, I. Y., Kim, J. Y., Kim, T. S., Lee, S. M., Choi, I. G., and Choi, J. W., Characterization of lignin-rich residues remaining after continuous super-critical water hydrolysis of poplar wood (Populus albaglandulosa) for conversion to fermentable sugars, Bioresource Technology: 102(10):5912-5916 (2011).
10.1016/j.biortech.2011.02.091S. Y. Park, J. Y. Kim, H. J. Youn and J. W. Choi, International Journal of Biological Macromolecules,
Fractionation of lignin macromolecules by sequential organic solvents systems and their characterization for further valuable applications,
106; 793-802 (2018)
Park, S. Y., Kim, J. Y., Youn, H. J., and Choi, J. W., Fractionation of lignin macromolecules by sequential organic solvents systems and their characterization for further valuable applications, International Journal of Biological Macromolecules 106:793-802 (2018).
10.1016/j.ijbiomac.2017.08.069A. Shrotri, H. Kobayashi and A. Fukuoka, Catalytic conversion of structural carbohydrates and lignin to chemicals; 59-123, In Advances in Catalysis, Academic Press. (2017)
Shrotri, A., Kobayashi, H., and Fukuoka, A., Catalytic conversion of structural carbohydrates and lignin to chemicals, In Advances in Catalysis, Academic Press, Vol.60, pp. 59-123 (2017).
10.1016/bs.acat.2017.09.002D. Robert, M. Bardet, C. Lapierre and G. Gellerstedt, Cellulose Chemistry And Technology,
Structural changes in aspen lignin during steam explosion treatment,
22; 221-230 (1988)
Robert, D., Bardet, M., Lapierre, C., and Gellerstedt, G., Structural changes in aspen lignin during steam explosion treatment, Cellulose Chemistry And Technology 22:221-230 (1988).
J. Lisperguer, P. Perez and S. Urizar, Journal of the Chilean Chemical Society,
Structure and thermal properties of lignins: characterization by infrared spectroscopy and differential scanning calorimetry,
54(4); 460-463 (2009)
Lisperguer, J., Perez, P., and Urizar, S., Structure and thermal properties of lignins: characterization by infrared spectroscopy and differential scanning calorimetry, Journal of the Chilean Chemical Society 54(4):460-463 (2009).
10.4067/s0717-97072009000400030C. G. Boeriu, D. Bravo, R. J. Gosselink and J. E. van Dam, Industrial Crops and Products,
Characterisation of structure-dependent functional properties of lignin with infrared spectroscopy,
20(2); 205-218 (2004)
Boeriu, C. G., Bravo, D., Gosselink, R. J., and van Dam, J. E., Characterisation of structure-dependent functional properties of lignin with infrared spectroscopy, Industrial Crops and Products 20(2):205-218 (2004).
10.1016/j.indcrop.2004.04.022O. Faix, Chemistry, Physics and Technology of Wood,
Classification of lignins from different botanical origins by FT-IR spectroscopy, Holzforschung-International Journal of the Biology,
45(s1); 21-28 (1991)
Faix, O., Classification of lignins from different botanical origins by FT-IR spectroscopy, Holzforschung-International Journal of the Biology, Chemistry, Physics and Technology of Wood 45(s1):21-28 (1991).
T. Saito, J. H. Perkins, F. Vautard, H. M. Meyer, J. M. Messman, B. Tolnai and A. K. Naskar, ChemSusChem,
Methanol fractionation of softwood kraft lignin: Impact on the lignin properties,
7(1); 221-228 (2014)
Saito, T., Perkins, J. H., Vautard, F., Meyer, H. M., Messman, J. M., Tolnai, B., and Naskar, A. K., Methanol fractionation of softwood kraft lignin: Impact on the lignin properties, ChemSusChem 7(1):221-228 (2014).
10.1002/cssc.201300509J. C. Rio, A. Gutiérrez, M. Hernando, P. Landín, J. Romero and Á. T. Martínez, Journal of Analytical and Applied Pyrolysis,
Determining the influence of eucalypt lignin composition in paper pulp yield using Py-GC/MS,
74(1-2); 110-115 (2005)
Rio, J. C., Gutiérrez, A., Hernando, M., Landín, P., Romero, J., and Martínez, Á. T., Determining the influence of eucalypt lignin composition in paper pulp yield using Py-GC/MS, Journal of Analytical and Applied Pyrolysis 74(1-2):110-115 (2005).
B. J. Fergus and D. A. I. Goring, Pap. Mag. Can,
Topochemistry of delignification in Kraft and neutral sulphite pulping of birch wood,
69(9); T314-T322 (1969)
Fergus, B. J. and Goring, D. A. I., Topochemistry of delignification in Kraft and neutral sulphite pulping of birch wood, Pap. Mag. Can. 69(9):T314-T322 (1969).
J. C. Rıo, A. Gutiérrez, J. Romero, M. J. Martınez and A. T. Martınez, Journal of Analytical and Applied Pyrolysis,
Identification of residual lignin markers in eucalypt kraft pulps by Py–GC/MS,
58; 425-439 (2001)
Rıo, J. C., Gutiérrez, A., Romero, J., Martınez, M. J., and Martınez, A. T., Identification of residual lignin markers in eucalypt kraft pulps by Py–GC/MS, Journal of Analytical and Applied Pyrolysis 58:425-439 (2001).
E. Jakab, O. Faix and F. Till, Journal of Analytical and Applied Pyrolysis,
Thermal decomposition of milled wood lignins studied by thermogravimetry/mass spectrometry,
40; 171-186 (1997)
Jakab, E., Faix, O., Till, F., Thermal decomposition of milled wood lignins studied by thermogravimetry/mass spectrometry, Journal of Analytical and Applied Pyrolysis 40:171-186 (1997).
A. Tejado, C. Pena, J. Labidi, J. M. Echeverria and I. Mondragon, Bioresource Technology,
Physico-chemical characterization of lignins from different sources for use in phenol-formaldehyde resin synthesis,
98(8); 1655-1663 (2007)
Tejado, A., Pena, C., Labidi, J., Echeverria, J. M., and Mondragon, I., Physico-chemical characterization of lignins from different sources for use in phenol-formaldehyde resin synthesis, Bioresource Technology 98(8):1655-1663 (2007).
10.1016/j.biortech.2006.05.042R. Sun, J. Tomkinson and G. L. Jones, Polymer Degradation and Stability,
Fractional characterization of ash-AQ lignin by successive extraction with organic solvents from oil palm EFB fibre,
68(1); 111-119 (2000)
Sun, R., Tomkinson, J., Jones, G. L., Fractional characterization of ash-AQ lignin by successive extraction with organic solvents from oil palm EFB fibre, Polymer Degradation and Stability 68(1):111-119 (2000).
10.1016/s0141-3910(99)00174-3W. G. Glasser and R. K. Jain, Chemistry, Physics and Technology of Wood,
Lignin derivatives. I. alkanoates, Holzforschung - International Journal of the Biology,
47(3); 225-233 (1993)
Glasser, W. G. and Jain, R. K., Lignin derivatives. I. alkanoates, Holzforschung - International Journal of the Biology, Chemistry, Physics and Technology of Wood 47(3):225-233 (1993).
B. El Khaldi-Hansen, M. Schulze and B. Kamm, Qualitative and quantitative analysis of lignins from different sources and isolation methods for an application as a biobased chemical resource and polymeric material; 15-44, In Analytical Techniques and Methods for Biomass, Cham. Springer. (2016)
El Khaldi-Hansen, B., Schulze, M., and Kamm, B., Qualitative and quantitative analysis of lignins from different sources and isolation methods for an application as a biobased chemical resource and polymeric material. In Analytical Techniques and Methods for Biomass, Springer, Cham, pp. 15-44 (2016).
10.1007/978-3-319-41414-0_2








