1. 서 론
석탄, 석유, 천연가스 등의 화석연료는 현대사회 발전과 더불어 그 사용량이 증가되어 왔다. 매장량이 한정되어 있는 화석연료는 사용함에 따라 고갈되어 가고 있으며 대기환경 문제 등을 일으키는 등의 문제를 가지고 있다. 따라서 이러한 화석연료를 대체할 신재생에너지에 대한 관심이 증가되고 있다. 신재생에너지는 기존 화석연료를 변환시켜 이용하거나 햇빛, 물, 지열, 바이오매스 등을 포함한 재생 가능한 에너지를 변환시켜서 이용하는 에너지를 의미한다. 우리나라는 신재생 에너지를 재생에너지(7가지)와 신에너지(4가지)로 구분하여 총 11가지 에너지를 선정하여 지속개발하고 있다. 재생에너지 중 하나인 바이오에너지는 태양광을 이용하여 광합성되는 모든 식물 및 생물 유기체(바이오매스)를 이용한 에너지를 의미한다. 바이오에너지원의 대상이 되는 바이오매스는 주로 옥수수, 보리 등의 곡물이나 나무, 사탕수수, 볏짚 등의 식물 또는 유기계 폐기물, 임업 폐기물, 축산 폐기물 등이 있다. 바이오매스를 발효 공정을 통해서 효과적으로 바이오알코올(바이오에탄올 또는 바이오부탄올)이나 바이오가스(메탄가스) 등으로 전환하여 이용할 수 있다.
특히 바이오알코올은 수송용 연료를 대체할 목적으로 사용하고 있으며 전 세계 여러 국가에서 신재생 에너지 연료혼합 의무제도(Renewable Fuel Standard)를 도입하여 휘발유에 바이오에탄올 일정 수준으로 혼합하여 사용하도록 권장하고 있다.1) ISO(International Sugar Organization)가 2012년에 발표한 전 세계 에탄올 생산량은 2001년 166억 리터에서 2011년 834억 리터로 급증하였으며 동일년도 전체의 약 87%의 양을 미국과 브라질이 생산하는 것으로 보고하였다.2) 미국과 브라질은 넓은 경작지를 바탕으로 대규모 수확이 가능한 옥수수 및 사탕수수를 바이오매스 작물로 경작하여 바이오에탄올을 생산하고 있다. 옥수수나 사탕수수 등의 전분질계 또는 당질계 원료는 복잡한 구조로 이루어져 있지 않기에 발효에 보다 용이하다는 장점이 있다. 하지만 식품 원료를 사용하기에 이러한 바이오에탄올 시장은 식량 가격 상승에 따른 불안정한 공급 및 도덕적 문제점을 가지고 있다는 단점이 있다.3) 따라서 비식용인 목질계 바이오매스에 대한 관심이 높아지고 있다.
목질계 바이오매스는 주로 셀룰로오스를 당화하여 단당의 형태로 전환한 후 이를 발효하여 바이오에탄올을 얻을 수 있다. 하지만 목질계 바이오매스는 셀룰로오스뿐만 아니라 헤미셀룰로오스와 리그닌과 함께 복잡한 구조를 가지고 있기 때문에 당화를 효율적으로 하기위해서 당화 전에 전처리가 필수적이다.4)
목질계 바이오매스를 전처리하는 방법은 산이나 염기를 통한 화학적 전처리, 물리적인 힘을 이용한 전처리, 생물학적 전처리 그리고 이러한 것들이 복합적으로 혼합되어 있는 전처리 등 매우 다양하다.5) 목질계 바이오매스는 전처리를 통해 셀룰로오스에 대한 효소의 접근성을 향상시켜 결국은 단당 생산을 높이는 것을 그 목표로 두고 있다. 알칼리 전처리도 목질계 바이오매스의 구조를 파괴할 수 있는 효과적인 화학 전처리 중 하나이다.
알칼리 전처리는 주로 수산화나트륨을 사용하며 그 처리시간, 온도 및 농도에 영향을 받아 매우 복잡하며 각기 다른 반응을 수반한다. 일반적으로 100℃ 이상의 고온과 저농도(0.5-4%) 조건에서는 필링오프 반응(peeling-off reaction)을 일으켜서 리그닌과 헤미셀룰로오스 및 셀룰로오스 사이의 에스테르 결합을 파괴하여 효과적으로 리그닌을 제거하며 일부 헤미셀룰로오스가 가수분해 되어 마찬가지로 제거된다.6,7) 비셀룰로오스인 리그닌과 일부 헤미셀룰로오스가 제거됨에 따라 셀룰로오스에 대한 접근성이 향상되어 효소 당화를 촉진시킨다. 반면에 약품의 회수가 어렵다는 단점도 존재한다. 이와 달리 100℃이하의 저온과 고농도(6-20%) 조건에서는 리그닌의 제거가 많이 발생하지 않으며 헤미셀룰로오스가 효과적으로 용해되어 제거된다.8) 또한 약품회수에 용이하다는 장점이 있다.
본 연구에서는 필링 반응이 발생하지 않는 저온 조건에서 전처리 온도 및 수산화나트륨 농도를 달리하여 헤미셀룰로오스와 리그닌의 용해가 어떠한 영향을 받는지 연구하였다. 또한 각기 다른 전처리된 굴참나무 목분의 효소당화를 통해 단당 생산에 대한 영향을 분석하였다.
2. 재료 및 방법
2.1 공시재료
굴참나무(Quercus variabilis)는 충북 제천시 한수면 송계리에 위치한 충북대학교 학술림에서 벌목하여 분쇄기(IKA사의 MF10B)를 이용하여 입자 크기 2.0 mm 이하로 분쇄 후 기건시켜 사용하였다. 가성소다는 93% 순도의 제품(Showa, Japan)을 사용하였다. 효소로는 Celluclast 1.5L과 Novozym 188(Novozyme, Denmark)을 사용하였다.
2.2 실험방법
2.2.1 알칼리 전처리
탈지된 굴참나무 목분(전건 기준)과 수산화나트륨 수용액을 1:6(w/v)의 비율로 혼합한 후 일정온도에서 4시간 동안 전처리하였다. 농도에 따른 전처리 효과를 알아보기 위해서 온도는 90℃ 로 일정하게 유지하고 수산화나트륨 수용액 농도는 4, 8, 13, 18%로 두었다. 온도에 따른 전처리 효과는 수산화나트륨 수용액 농도 13%로 일정하게 두고 45, 60, 75, 90℃로 각각 실시하였다. 전처리를 끝낸 후 글라스필터(P4, pore size)로 여과하여 수산화나트륨 수용액의 5배 정도의 증류수를 사용하여 잔류하는 약품을 제거하여 사용하였다.
2.2.2 효소당화
효소당화는 250 mL 삼각플라스크를 이용하여 50℃, 150 rpm 조건으로 진탕배양기에서 실시하였다. 삼각플라스크 내에 굴참나무 목분 12.0 g과 50 mM citrate buffer(pH 4.8) 138.0 mL을 넣고 120℃에서 15분간 멸균한 다음 효소를 첨가하여 당화하였다. 효소활성은 Whatman No.1 정량여과지를 이용하여 측정하였으며 42 FPU/mL이다. 효소로는 Celluclast 1.5L을 기질 1.0 g 당 30 FPU을 첨가하였고 Novozym 188을 Celluclast 1.5L 첨가량의 1/3 수준으로 사용하였다. 효소당화 중 당 농도를 측정하기 위해서 2, 4, 6, 8, 12, 24, 48 시간 때 2.0 mL의 샘플을 채취하여 여과하여 사용하였다.
2.2.3 발효
전처리된 굴참나무로부터 얻은 효소당화액 중 90℃에서 4, 8% 수산화나트륨 전처리된 굴참나무로부터 얻은 두 가지 효소당화액만을 발효하였다. 발효 균주로는 Saccharomyces cerevisiae를 사용하였으며 Yeast Mould(YM) broth에서 24시간 배양하여 사용하였다. 여과한 효소당화액에 영양분을 첨가하여 멸균 후 당화액의 5%에 해당되는 효모를 접종하였다. YM broth 조성은 glucose 10 g/L, peptone 5 g/L, yeast extract 3 g/L, malt extract 3 g/L 이며 영양분은 각각 yeast extract 5 g/L, peptone 5 g/L, MgSO4 1 g/L, K2HPO4 1 g/L을 첨가하였다. 발효는 30℃, 150 rpm 조건으로 진탕배양기에서 총 72시간 동안 진행하였으며 6, 12, 24, 48, 72 시간 마다 샘플을 채취하여 글루코오스 감소량 및 에탄올 생산량을 분석하였다.
2.2.4 분석
2.2.4.1 굴참목분의 화학조성 분석
굴참목분의 화학적 조성 분석을 위하여 아세톤 추출물 함량 측정(Tappi 204 om-88), 온수 추출물 함량 측정(Tappi 207 om-93), 산 불용성 및 가용성 리그닌 분석(Tappi 222 om-88과 Tappi Useful Method UM 250)을 실시하였다.
2.2.4.2 당 조성 분석 (1H-NMR)
농도 및 온도에 따른 알칼리 전처리 효과를 확인하기 위해서 알칼리 전처리 전과 후의 굴참나무 목분의 다당류 성분 변화를 1H-NMR 분석을 통해 알아보았다. 굴참나무 목분 40 mg을 24 N 황산(72%) 0.6 mL에 30℃, 1시간 동안 항온수조에서 1차 가수분해하였다. 2차 가수분해는 중수(D2O) 3.0 mL을 넣고 희석하여 100℃, 1시간 동안 실시하였다. 반응이 끝난 후 여과액을 모아서 NMR spectrometer(500H㎐, Bruker)로 분석하였다. Top spin 프로그램을 사용하여 스펙트럼 상에서의 아노머성 수소 피크를 적분하여 단당류를 정량 분석하였다.
2.2.4.3 효소당화 및 발효 공정 중 당 농도 또는 에탄올 생산량 분석
효소당화 및 발효 공정 중 시간에 따라 샘플을 채취하여 HPLC(high performance liquid chromatograph) (Shimadzu, Japan)를 이용해 샘플 내 단당류 또는 에탄올 농도를 측정하였으며 이를 통해 당화율 또는 발효율을 분석하였다. 컬럼(Aminex HPX-87H, 300 mm x 7.8 mm, Bio-Rad)과 굴절률 검출기(RID-10A, Shimadzu, Japan)를 사용하였다. 이동상으로는 50 mM 황산을 사용하였으며 온도 60℃, 유속 0.6 mL/min 조건으로 분석하였다.
3. 결과 및 고찰
3.1 전처리 농도에 따른 굴참나무 화학조성 비교
굴참나무의 화학성분은 냉·온수추출물(7.0%), 에탄올·벤젠 추출물(3.0%), 리그닌(26.0%), 다당류(67.5%)로 보고되었다.9) 본 연구에서 사용한 공시재료인 굴참나무의 화학조성은 Table 1에 나타냈다. 추출물(1.9%), 리그닌(23.1%), 다당류(75.1%) 각각 다음과 같이 나타났으며 선행 연구 결과9)와 비교하여 추출물과 리그닌이 좀 더 낮았으며 다당류는 더 높게 나타났다. 수산화나트륨 수용액의 농도를 달리한 전처리 전후 굴참나무 목분의 화학조성 및 당조성 변화를 Table 2에 나타내었다. 전처리 후 굴참나무 목분의 리그닌과 자이란이 선택적으로 제거되었으며 특히 자이란의 제거가 뚜렷하게 나타났다(Table 2). 염기 전처리 후 23.3-27.8% 정도의 리그닌이 제거되었으며 수산화나트륨 4%를 제외하고 농도가 증가함에 따라 리그닌 제거량이 약간 상승하였지만 그 차이는 매우 미비하였다. 수산화나트륨 수용액의 농도가 4%였을 때 자이란의 47.0%가 제거되었으며 8% 이상의 농도에서는 보다 많은 70.0% 이상의 자이란이 제거됨을 확인할 수 있었다. 하지만 8, 13, 18% 농도에서는 자이란 제거의 뚜렷한 차이는 나타나지 않았다. 셀룰로오스의 경우 15.2-18.4% 정도 전처리 후 제거된 것으로 나타났는데 이는 일부 저분자량의 셀룰로오스가 용해된 것으로 추정되며 농도에 따른 차이점을 나타내지는 않았다.
Table 1
The chemical composition of cork oak (raw material)
| Substance | Content (% of ODM) |
|---|---|
| Cork oak | |
| Acetone extractives | 0.6 |
| Hot-water extractives | 1.3 |
| Lignin | |
| Acid insoluble | 20.4 |
| Acid soluble | 2.7 |
| Polysaccharides | |
| Glucan | 52.7 |
| Xylan | 16.0 |
| Galactan | 3.7 |
| Mannan | 1.5 |
| Arabinan | 1.2 |
Table 2
The change of chemical compostion of cork oak which pretreated at different sodium hydroxide concentration (at 90℃)
3.2 전처리 온도에 따른 굴참나무 화학조성 비교
전처리 온도에 따른 화학조성의 변화를 확인하기 위하여 수산화나트륨 수용액의 농도를 13%로 고정한 후 온도(45, 60, 75, 90℃)를 변화시켜 전처리를 실시하였다. 전처리 온도가 증가할수록 약간씩 리그닌의 제거량이 상승하였고 이런 경향은 염기의 농도를 달리했을 경우와 비슷하였다(Table 3). 리그닌에서처럼 자이란 또한 전처리 온도가 상승할수록 더 많이 제거되었으며 90℃에서 가장 많이 용해되어 제거된 것으로 나타났다. 글루코오스 및 다른 단당들 또한 전처리 온도 상승에 따라 제거량이 조금씩 상승하는 경향을 나타내었다.
Table 3
The change of chemical compostion of cork oak which pretreated at different pretreatment temperature (13% NaOH treatment)
3.3 전처리 조건에 따른 굴참나무의 효소당화 비교
목질계 바이오매스 내 셀룰로오스를 효과적으로 효소당화하기 위해서는 다양한 영향인자들을 고려해야 한다. 그 중 리그닌 및 헤미셀룰로오스의 함량은 효소당화에 영향을 끼치는 인자 중 하나이다.10) 목질계 바이오매스 내 존재하는 리그닌 및 헤미셀룰로오스는 셀룰로오스와 결합되어 있기 때문에 셀룰라아제가 셀룰로오스에 효과적으로 흡착하는 것을 물리적으로 방해하는 요인으로 여겨지고 있다.10,11) 자이란과 리그닌의 제거에 따른 효소당화의 영향에 대한 연구를 살펴보면, 자이란과 리그닌은 둘 다 그 제거된 양이 증가할수록 효소당화를 향상시키는 것으로 알려져 있다. 하지만 자이란 제거와 리그닌 제거 중 어느 것이 더 효소당화와 밀접한 관계가 있는지는 기질 종류 및 전처리 방법에 따라 다르게 해석될 수 있다.
가장 일반적인 전처리 방법인 묽은 산 전처리는 산 조건에서 쉽게 분해되는 자이란 및 글루코만난 계열의 헤미셀룰로오스를 제거한다. 옥수수 줄기의 묽은 산 전처리 결과, 산농도 및 온도를 증가함에 따라 자이란 분해속도가 증가하였다. 또한 자이란 제거량이 증가할수록 옥수수 줄기의 효소당화율도 향상되었으며 선형에 가까운 상관관계를 나타냈다. 하지만 리그닌의 경우 산농도 및 온도를 증가하여도 20% 이상 제거하는데 한계가 발견되었고 효소당화율과도 낮은 상관관계가 나타났다.11) 목질계 바이오매스인 올리브나무에서도 유사한 결과가 나타났다. 저농도(1.4% H2SO4, w/w), 190-210℃ 고온 조건에서 묽은 산 가수분해를 진행한 결과, 목재 내 존재하는 리그닌의 분해보다는 자이란의 분해(86.5%)가 주로 일어났으며 이에 따라 효소당화율이 70% 이상에 도달했다.12) 묽은 산 전처리에서는 자이란의 제거가 리그닌의 제거보다 효소당화에 큰 영향을 끼치는 것으로 해석될 수 있다.
이와 달리 자이란 제거보다 리그닌 제거가 효소당화에 더 큰 영향을 끼친 연구도 발표되었다. 암모니아수를 이용한 침지 전처리는 바이오매스 내 존재하는 에스테르 결합을 끊어 리그닌이나 헤미셀룰로오스를 용해시켜 제거한다. 3종류의 초본류(옥수수 줄기, 담배 줄기, 대마 목부)를 암모니아수 침지 처리하여 효소당화한 결과, 자이란 제거와 효소당화율 증가는 상관관계가 낮게 나타났지만 리그닌제거는 상관관계가 크게 나타났다. 리그닌의 용출이 가장 큰 옥수수 줄기가 가장 높은 당화율을 나타냈고 리그닌 용출이 가장 작은 담배 줄기가 가장 낮은 효소당화 정도를 나타냈다.13)
이렇듯 많은 연구를 통해 자이란과 리그닌 제거가 효소당화를 촉진시킬 수 있는 주요 인자임을 알 수 있으며 본 연구에서는 알칼리 농도 및 온도를 변화하여 자이란 및 리그닌 용해 정도에 따른 효소당화 차이를 비교하였다. Fig. 1은 동일 알칼리 농도(13% NaOH, w/v)에서 온도를 45-90℃까지 변화를 주어 전처리한 굴참목분의 효소당화 나타냈다. 모든 전처리재가 미전처리재에 비해 높은 당화정도을 나타냈으며 특히 90℃ 전처리온도에서의 굴참목분이 가장 큰 당화정도를 나타냈다(Fig. 1). 이는 90℃에서 효소당화를 억제하는 물리적 요인인 리그닌(24.2%) 및 자이란(78.8%)을 가장 많이 제거하였기 때문으로 생각된다(Table 3). 하지만 다른 온도에서는 전처리에 의한 화학적 성분(리그닌, 헤미셀룰로오스)의 제거가 효소당화에 크게 영향을 끼치지 않았다. 온도 60℃가 45℃보다 전처리에 의해 30.6 %의 자이란과 2.6%의 리그닌이 더 많이 제거되었다. 하지만 효소당화는 유사한 정도로 나타났다. 또한 온도 60℃와 75℃의 화학적 성분의 제거는 유사하였지만 당화는 75℃에서 전처리된 굴참목분이 높게 나타났다.
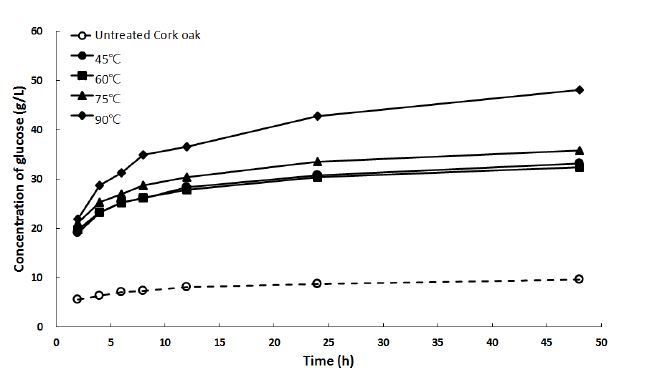
Fig. 1.
Release of glucose from pretreated cork oak after enzymatic hydrolysis with different treated temperature (at 13% NaOH).
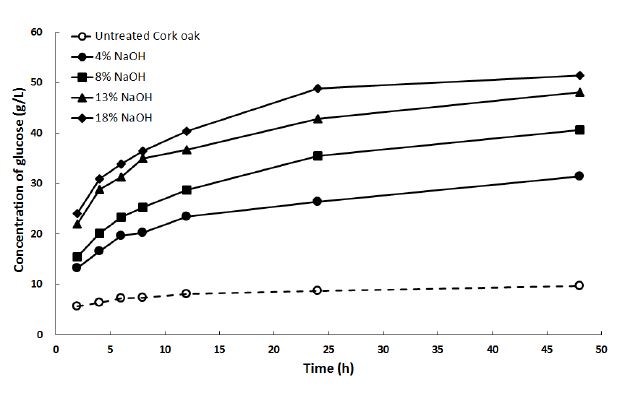
동일 전처리 온도(90℃)에서 수산화나트륨 농도를 변화시켜 전처리한 굴참목분의 효소당화 정도 Fig. 2에 나타냈다. 수산화나트륨 농도가 증가할수록 효소당화율을 증가하는 것으로 나타났다. 하지만 수산화나트륨 농도에 따른 화학적 성분 제거와 효소당화가 큰 상관관계를 나타내지는 않았다. 따라서 화학적 성분(리그닌 및 자이란)의 제거 외에 다른 물리적 요인에 의해 효소당화가 차이를 나타내는 것으로 추정된다.
염기 전처리에서 셀룰로오스의 팽윤이 발생하게 되는데 이러한 현상은 셀룰로오스의 결정화도에 영향을 끼쳐 효소당화에도 영향을 끼친다.14-16) 수산화나트륨 수용액 7%에서 전처리 온도를 바꾸어 자작나무의 효소당화를 연구한 결과 온도가 올라갈수록 결정화도가 떨어졌고, 이러한 결정화도 감소가 추후 효소당화를 촉진시키는 주요 인자라고 추정하였다.7) 따라서 본 연구에서도 온도 및 농도에 따른 결정화도와 같은 물리적 요인이 효소당화에 영향을 끼친 것으로 추정되며 추후 연구에서 보다 정확한 분석이 요구된다.
3.4 발효특성 비교
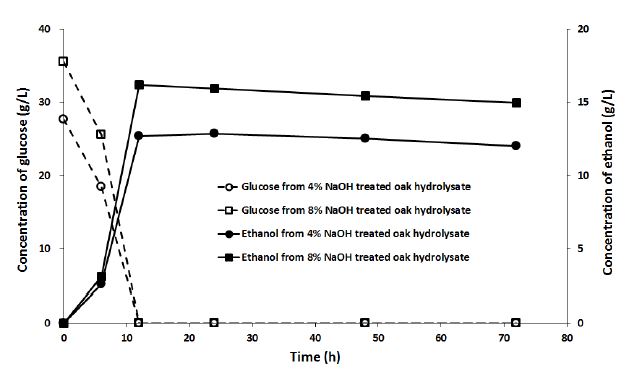
산 당화의 경우 온도, 시간, 농도에 따라서 과반응이 진행된 경우 furfural, hydroxy- methylfurfural(HMF), levulunic acid, 아세트산 등 발효저해 물질이 발생할 수 있다. 하지만 효소당화에서는 발효저해 물질이 발생하지 않는다. 따라서 본 실험에서는 효소 당화액의 발효가 용이할 것으로 가정하였으며 일부 조건에서 생성된 효소 당화액만을 발효하여 발효 특성을 확인하였다(Fig. 3). 수산화나트륨 수용액 4%와 8%를 온도 90℃에서 전처리한 굴참나무 목분으로부터 얻은 효소 당화액의 발효 특성을 나타냈다. 각기 다른 조건에서 전처리된 효소당화액은 둘 다 12시간 때 대부분의 글루코오스를 소모하여 에탄올로 전환시켰으며 최대 에탄올 농도를 나타냈다. 이론적 발효율은 12시간 때 각각 90.9%(90℃ - 4% NaOH)와 89.2%(90℃ - 8% NaOH)로 나타났다. 수산화칼슘으로 전처리된 옥수수대를 효소 당화 후 발효한 결과, 93.2%의 발효율을 나타냈다.17) 또한 분쇄 전처리된 사탕수수 찌꺼기(sugar cane bagasse)와 밀짚 효소 당화액을 발효하여 89.8, 91.8%의 이론적 발효 수율을 나타냈다.18) 다른 바이오매스와 비교하여 이론적 발효율이 비슷한 정도에 도달하는 것을 확인하였으며 에탄올 생산 원재료로써 가능성을 확인하였다.
4. 결 론
다양한 온도 및 농도에서 염기 전처리가 효소당화에 미치는 영향에 대해 연구하였다. 전처리되지 않은 굴참목분에 비해 전처리 후 효소당화가 증가하였으며 이러한 원인이 염기 전처리에 의한 리그닌 및 자이란 제거에 따른 효과라고 판단된다. 온도와 농도가 증가할수록 효소당화율이 증가하는 경향이 나타났으며 화학적 성분(리그닌, 자이란)의 제거 뿐만 아니라 물리적 요인(결정화도 등)에 영향을 받은 것으로 판단된다. 또한 일부 조건에서 얻은 효소당화액을 효과적으로 발효하여 이론적 발효율이 89% 이상을 얻을 수 있던 것으로 보아 바이오에탄올을 얻기에 적합한 방법으로 생각된다.