1. 서 론
셀룰로오스계 물질은 수 세기 동안 인류가 광범위하게 사용하여 온 물질이다. 셀룰로오스는 지구상에 가장 풍부한 천연 유기물 자원이다. 셀룰로오스는 전통적으로 면 섬유, 레이온 섬유, 제지 산업에서 활발하게 사용하여 왔다. 박테리아에 의하여 합성된 셀룰로오스는 의료영역에서 사용 가능성을 확인하기 위하여 인공 피부, 인공 혈관, 창상 치료제, 인공 장기 등 다양한 분야에서 시도되었다. 바이오 의료 영역에서 사용하기 위하여, 섬유 형태학적 특성, 고순도, 수분 유지 능력, 인장 강도, 유동성, 생체 적합성 등이 중요한 요소이다. 셀룰로오스 나노섬유는 바이오 의료 영역에서 필요로 하는 다양한 특성을 지니고 있는 소재이다.
나노공학에 의한 제품 개발과 생산이 급격하게 증가하고 있다. 이런 나노물질은 안전 문제를 야기하고 있지만 현재까지도 셀룰로오스 나노섬유에 대한 연구가 충분하게 이루어지 않고 있다. 입자 크기가 작아지면 비표면적이 커지고, 전통적인 물질(비 나노물질)보다 단위 면적당 반응성이 증가하게 된다.
천연 섬유(석면)이나 인조 섬유(생분해되지 않는 유리섬유)의 독성에 대한 연구에서 보면 이것들이 인간의 몸에서 장기간 노출될 경우 폐 섬유화와 암 유발을 증가시키는 것으로 보고된 바 있다.1) 셀룰로오스 섬유를 흡입한 경우 폐 내에서 다양한 생리적 변화(granuloma-육아종, alveolitis-이물성 폐포염, epithelial hyperplasia-상피 세포 과 형성, fibrosis-섬유화)가 일어난다.2-7) 셀룰로오스 섬유에 노출될 경우 시험관 수준의 실험에서 쥐의 대식세포(macrophages)에 영향을 미쳐 석면이나 유리섬유보다 염증 유발 물질을 분비시키는 것이 확인되었다.8) 셀룰로오스 섬유 물질은 쥐의 폐에서 분해되지 않고 유지 기간이 길었으며 이로 인하여 호흡기 관련 질병증상을 야기시켰다.9-11)
셀룰로오스 나노섬유를 다양한 산업 분야에서 활발하게 적용하려는 다양한 시도들이 보고되고 있다.12) 셀룰로오스 나노섬유를 사용하는 작업 조건에서 인체에 노출될 수 있다. 겔 상태의 셀룰로오스 나노섬유는 피부 접촉으로 전달이 가능하다. 건조된 상태의 셀룰로오스 나노섬유로 작업할 경우에는 분말이 호흡기를 통하여 폐로 전달될 수 있다. 세포 독성 시험은 독성 물질이 세포 기능에 영향을 미치는 정도를 시험관 조건에서 평가한다. 체내 방어기작이 존재하지 않는 조건에서 세포를 배양하여 분리할 수 있을 경우 세포 독성 시험법의 민감도가 높다.
셀룰로오스는 원료 물질과 관계없이 시험관 시험 결과 세포 독성이 매우 낮다.13) 하지만 셀룰로오스 섬유를 호흡기로 상당한 농도를 흡입한 경우 세포파괴가 보고되었다.10)
이번 연구에서는 셀룰로오스 나노섬유가 피부를 통하여 피부 내 조직에 전달된 후 간에서의 해독 작용과 신장에서의 배출과 관련된 세포 시험을 통하여 인체에 미치는 영향을 탐색하고자 하였다. 피부, 간, 신장 세포를 대표할 수 있는 3가지 세포를 사용하여 각 부위의 독성 가능성 여부를 탐색하였다.
2. 재료 및 방법
2.1 재료
M사의 혼합 활엽수 크라프트 펄프를 셀룰로오스 원료로 사용하였다. 또한, 카르복시메틸화 반응에 수산화나트륨, 염화 아세테이트, 에탄올을 사용하였다.
본 실험에 사용된 인간 섬유아세포주(human skin fibroblast)인 Hs68 세포, 인간 간암 세포주(human hepatoma cell line)인 HepG2 세포와 인간 신장 세포주(human embryonic kidney cell line)인 HEK293 세포는 ATCC(American Type Culture Collection, USA)에서 구입하여 사용하였다.
세포 독성 실험을 위해 사용한 fetal bovine serum(FBS), penicillin/streotomysin(P/S), Dulbecco’s modified Eagle’s(DEMM) 배지는 Gibco/BRL(USA)로부터, 0.25% trypsin EDTA는 Thermo fisher scientific(USA)에서 구입하였다. 그리고 3-(4,5-Dimethyl-2-thiazolyl)-2,5-diphenyl-2H-tetrazolium bromide(MTT)는 Sigma Aldrich Co.(USA)에서, 96 well을 포함한 세포배양 plastic culture dish들은 Nunc Inc.(USA)로부터 구입하여 사용하였다. 그 외의 모든 시약은 1급 또는 특급을 사용하였으며, 세포 배양에 필요한 기구는 Life Technologies(USA)에서 구입하여 사용하였다.
2.2 방법
2.2.1 카르복시메틸화 전처리
카르복시메틸화 전처리를 위하여 상업용 펄프 100.0 g을 에탄올 용매 1.0 L에 첨가하여 팽윤시킨 후 해리시켰다. 여기에 에탄올 1.0 L에 수산화나트륨 19.7 g을 용해시킨 후 해리된 펄프에 첨가하고 상온에서 2시간 이상 교반하여 셀룰로오스 내 수산기의 이온화 반응을 유도하였다. 수산기의 이온화가 유도된 셀룰로오스에 염화 아세테이트를 첨가하여 카르복시메틸화 반응을 유도하였으며, 원하는 치환도에 따라 다른 염화아세테이트 양을 조절하였다. 70℃에서 두 시간 반응 시킨 후 펄프 내 에탄올을 제거한 후 세척하여 셀룰로오스 나노섬유 제조의 원료로 사용하였다.
2.2.2 셀룰로오스 나노섬유 제조
카르복시메틸화 전처리된 펄프를 2.0%로 희석한 후 고압균질기(Panda Plus, GEA, Italy)를 사용하여 셀룰로오스 나노섬유를 제조하였다. 고압균질기를 사용한 1차 처리는 100 bar의 압력으로 펄프의 균질화를 시도하였다. 이후 600 bar로 압력을 높여 7회 통과시켜 셀룰로오스 나노섬유를 제조하였다.
2.2.3 세포 독성 시험
2.2.3.1 세포 배양
Hs68 세포, HepG2 세포, HEK293 세포는 10% fetal bovine serum(FBS)에 P/S penicillin(100 unit/mL), streptomycin(50 μg/mL)를 포함한 DMEM(Dulbeco’s Modified Eagle’s Media) 배지를 사용하여 37°C, 5% CO2, 95% humid air로 조절된 배양기(Thermo Scientific)에서 배양하였다. 세포는 100 mm cell culture dish 바닥에 세포가 80% 정도 자랐을 때 계대 배양하며 유지하였다.
2.2.3.2 세포 독성 시험(MTT assay)
Hs68 세포, HepG2 세포 또는 HEK293 세포를 96-well culture plate에 1×104 cells/well로 분주한 다음, 37°C, 5% CO2에서 24시간 동안 배양하였다. 24시간 후 이전 배양에 사용된 배지를 제거하고 시료인 셀룰로오스 나노섬유를 각 0.02, 0.2, 1 μg/mL의 농도별로 용해한 배지로 분주하고 37°C, 5% CO2의 배양조건에서 24시간 동안 각각 반응시켰다. 24시간 후 각 well 당 0.2% MTT용액(5 mg/ml)을 20 μL씩 첨가하여 37°C, 5% CO2 배양기에서 3시간 동안 반응시켰다. 반응 후 상등액을 모두 제거하고 생성된 formazan에 DMSO(dimethyl sulfoxide) 200 μL씩을 넣어 37°C에서 10분간 모두 용해하고 ELISA reader(Molecular Devices, USA)기기를 이용하여 570 nm에서 흡광도를 측정하였다. 세포 생존율(%)은 다음과 같은 식을 사용하여 나타내었다. 각 실험은 3번 반복 수행하였으며 흡광도를 측정한 후 세포 생존율(%)은 다음과 같은 식을 사용하여 나타내었다.
2.3 분석
2.3.1 나노입도 분석
제조된 셀룰로오스 나노섬유의 폭을 측정하기 위하여 나노입도 분석기(Nano Particle Size, Analyzer, Nanophox, Sympatec GmbH, Germany)를 사용하였다. 카르복시메틸화 전처리된 시료를 0.001%로 희석시켜 분산된 시료를 사용하였다. 나노입도분석기를 사용하여 30초 동안 10회 반복하여 입자크기의 빈도를 측정하였다.14)
2.3.2 유변학적 특성
치환도 변이가 셀룰로오스 나노섬유의 유변학적 성질이 차이를 분석하기 위하여 레오미터(Rheometer, MCR 102, Anton Paar, Austria)를 사용하였다. D-PP 25 부품을 사용하여 측정하였고, 점도 곡선과 진동수, 진폭에 따른 유변학적 특성을 분석하였다.15)
3. 결과 및 고찰
3.1 셀룰로오스 나노섬유의 형태
전처리 조건이 셀룰로오스 나노섬유의 폭에 영향을 미친다. 본 연구에서는 나노입도 분석기를 사용하여 셀룰로오스 나노섬유의 폭의 분포도를 측정하였다. 카르복시메틸화 후 치환도는 치환된 셀룰로오스를 산 가수분해 후 단당을 핵자기 공명 분석하여 치환도를 확인하였다.16) 그라인더 방법으로 작업한 후 고압균질기로 2차 가공하여 제조한 셀룰로오스 나노섬유의 치환도 0.1로 카르복시메틸화 전처리된 셀룰로오스 나노섬유의 폭은 41.8 nm임에 비하여 치환도 0.3이나 0.5로 처리된 시료는 10 nm 이하의 폭으로 확인되었다(Table 1). 치환도가 0.1인 경우 음이온 도입에 의하여 셀룰로오스 나노섬유화의 촉진이 덜 진행되었지만 치환도 0.3 이상인 경우 음이온 도입에 의한 정전기적 반발력에 의한 셀룰로오스 나노단위의 이탈이 충분하게 진행되어 치환도의 증가가 나노섬유의 폭의 감소로 더 이상 진행되지는 않은 것으로 생각된다.
Table 1.
Width of cellulose nanofibril with different carboxymethylation pretreatment
| Degree of Substitution | Width (nm) | ||
|---|---|---|---|
| X10 | X50 | X90 | |
| 0.1 | 37.4 | 41.8 | 46.4 |
| 0.3 | 8.0 | 8.7 | 9.1 |
| 0.5 | 8.6 | 8.9 | 9.5 |
카르복시메틸화 전처리 조건의 치환도를 낮은 상태, 중간 상태로 높은 상태로 처리한 경우 전처리 조건이 미치는 영향을 분석하였다. 그라인더 방법으로 나노섬유를 제조하고, 전자 현미경으로 폭을 측정한 결과, 전처리하지 않은 셀룰로오스 나노섬유의 평균 폭은 31.0 nm이었지만 전처리 정도가 낮은 경우 14.6 nm, 전처리 정도가 중간인 경우 14.7 nm와 전처리로 인한 카르복시기 도입이 높은 경우 12.3 nm로 보고되었다.17) 4차 아민 양이온화 전처리 후 만든 나노 입도 분석기로 분석한 결과, 치환도가 0.1로 전처리된 후 제조된 셀룰로오스 나노섬유의 폭은 8.1-14.1 nm 범위로 제조된 반면 치환된 0.3으로 전처리된 후 나노섬유의 폭은 3.9-9.5 nm 범위의 폭 분포로 치환도가 낮게 처리된 후 만들어진 나노섬유보다 폭이 작아진 것을 보고된 바 있다.15)
3.2 셀룰로오스 나노섬유의 점탄성
셀룰로오스의 점탄성 성질에 영향을 미치는 두 가지 요소는 입자의 크기 및 형태와 관련된 특성이고 다른 하나는 섬유 표면의 전하 상태이다. 섬유의 형태학적 요소는 길이, 폭, 피브릴화 정도, 네트워크 구조에 영향을 받는다. 표면 전하는 전처리 과정에서 셀룰로오스 나노섬유의 음이온이나 양이온 작용기를 도입하여 나노화 과정에서 사용되는 전기적 에너지를 줄이기 위하여 도입된다.
유변학적 성질은 전단응력 조건에서 측정되었으며, 시료의 농도는 2.0 wt%, 온도 25°C에서 측정하였다. 치환도 0.5로 전처리된 셀룰로오스 나노섬유의 점도가 가장 높았고, 치환도 0.3, 치환도 0.1로 치환된 셀룰로오스 나노섬유 순으로 점도 값을 보였다(Fig. 1). 치환도 0.3으로 만들어진 셀룰로오스 나노섬유의 폭이 치환도 0.5보다 작지만, 도입된 카르복시메틸기에 의한 물과 친화력 증가에 의하여 점도가 상승하는 것으로 판단된다. TEMPO-산화 전처리 후 만들어진 셀룰로오스 나노섬유의 카르복실기 함량이 250-650, 350-700 μmol/g 처리된 시료의 경우 카르복실기 함량이 높을수록 높은 점도 값을 보였다.18) 4차 아민 양이온 전처리된 셀룰로오스 나노섬유의 경우, 치환도 0.3으로 전처리된 후의 나노섬유가 치환도가 0.1로 전처리된 후 제조된 셀룰로오스 나노섬유보다 점도 값과 저장탄성계수 및 손실탄성계수가 높아, 전처리에서 도입된 양이온이나 음이온이 만들어진 셀룰로오스 나노섬유의 점탄성 성질에 영향을 미치는 것으로 생각된다.15) 카르복시메틸 전처리와 4차 아민 전처리된 셀룰로오스 나노섬유의 점탄성 성질 비교 결과 카르복시메틸화 처리된 셀룰로오스 나노섬유가 유사한 치환도 값에서 4차 아민 전처리로 처리된 셀룰로오스 나노섬유보다 동일 전단 속도에서 높은 점도 값을 보였다.15)
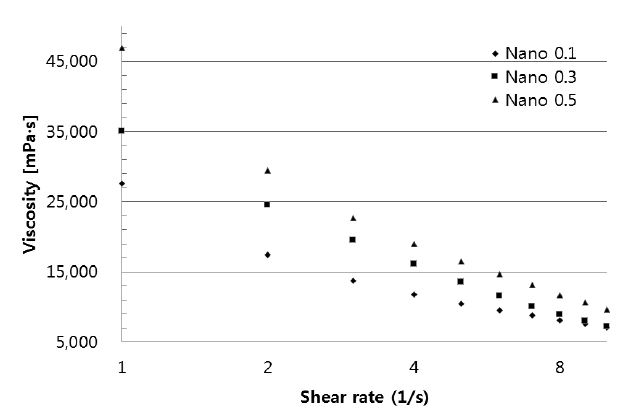
Fig. 1.
Viscosity as a function of rate for cellulose nanofibrils with differently carboxymethylated.
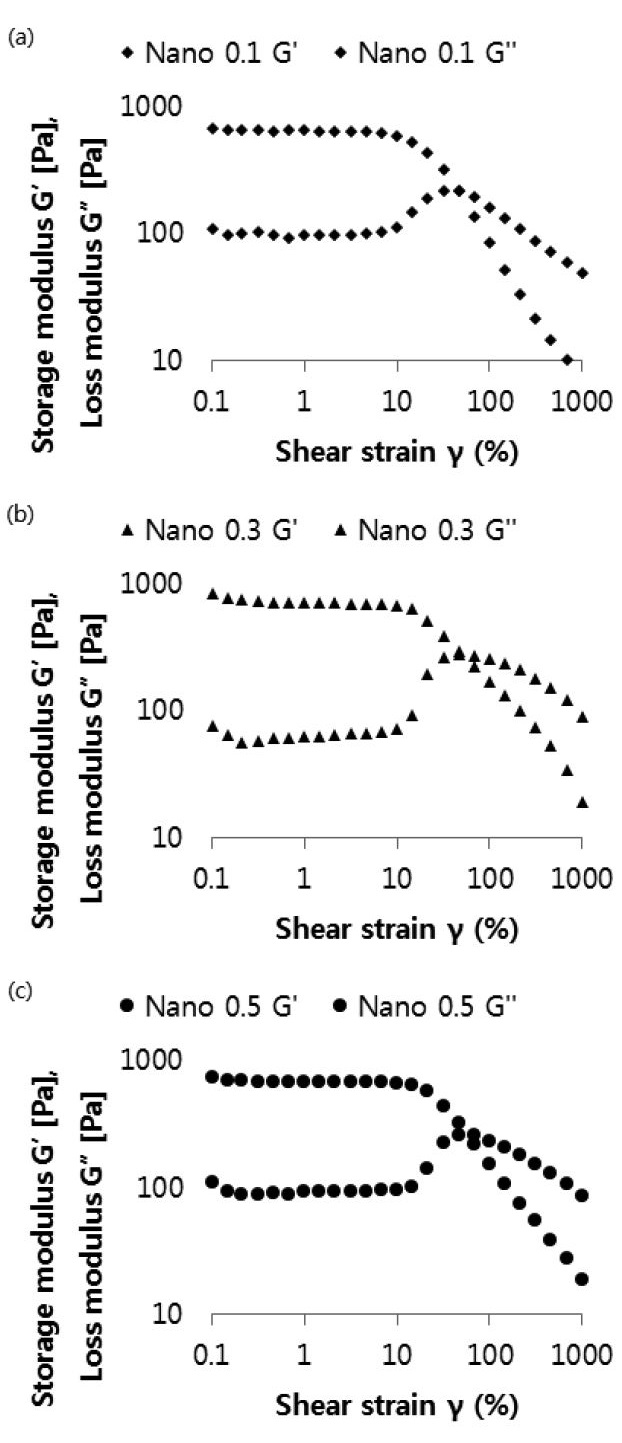
셀룰로오스 나노섬유 현탁액의 변형을 증가시키면서 진동 전단 변형(oscillating shear deformation)을 측정하였다. 전처리 치환도와 관계없이 3가지 시료 모두 비슷한 경향을 보였다(Fig. 2). 선형 점탄성 구간에서는 저장탄성계수(G’) 값이 손실탄성계수(G”) 값보다 큰 고체나 겔과 같은 성질을 보였지만 전단 변형이 50%인 영역에서 저장 탄성계수와 손실탄성계수 값이 같아지며 이후 전단변형이 증가함에 따라 손실탄성계수(G”) 값이 저장탄성계수(G’) 값보다 커지는 점성물질이나 액체 같은 성질로 전이됨을 알 수 있다. 셀룰로오스 나노섬유의 전단변형 증가에 따른 겔에서 액체로의 전이는 다른 연구자들에 의해서도 보고된 바 있다.19,20)
3.3 세포 독성
3.3.1 섬유 아세포 독성
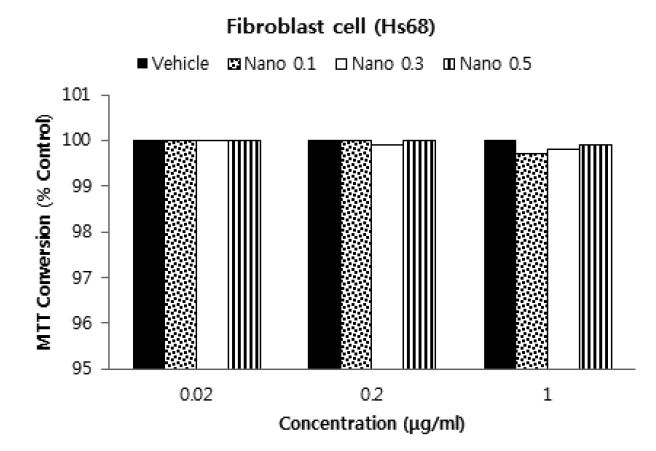
혼합 활엽수 크라프트 펄프를 카르복시메틸화 전처리 시킨 후 만들어진 셀룰로오스 나노섬유의 섬유 아세포 독성을 실시하였다. 배지 내에 전건 셀룰로오스 나노섬유 기준으로 0.02, 0.2, 1.0 mg/L를 첨가하여 세포 독성을 시험하였다. 치환도 0.5로 전처리된 셀룰로오스 나노섬유의 경우 치환도 0.1이나 0.3로 치환된 셀룰로오스 나노섬유보다 세포 생존율이 높았지만 모든 경우 99% 이상의 세포 생존율을 보이기 때문에 그 차이는 크지 않다(Fig. 3).
라디에타 소나무로 만든 셀룰로오스 나노섬유, 유칼립투스로 만든 셀룰로오스 나노섬유, 전처리를 거치지 않고 만든 것이나 TEMPO-산화 처리 후 만들어진 셀룰로오스 나노섬유, 건조하지 않은 것이나 동결 건조 후 다시 겔로 만든 셀룰로오스 나노섬유 등 다양한 셀룰로오스 나노섬유의 3T3 fibroblast cell을 이용한 세포 독성 시험에서 모두 세포 독성이 없음이 보고되었다.21) 하지만 셀룰로오스 나노섬유와 polyethyleneimine(PEI)와 가교 결합 또는 cetyl trimethylammonium bromodie (CTAB) 계면활성제와 가교결합된 것들은 세포 독성을 보였다.21)
음이온이나 양이온으로 전처리한 후 만들어진 셀룰로오스 나노섬유를 인간피부 섬유아세포(HDF)로 실시한 세포 독성 시험을 AB와 LDH 두 가지 방법으로 assay한 결과, 24시간 셀룰로오스 나노섬유 처리 후 손상 평가에서 3가지 시료 모두 세포 멤브레인의 손상을 가져오지 않았을 뿐 아니라 세포형태의 변화도 관찰되지 않았다고 보고되었다.22) 섬유 아세포 L 929세포를 사용한 또 다른 세포 독성 연구에서 셀룰로오스 나노섬유는 세포 독성이 없고 산화스트레스도 유발하지 않는다고 보고되었다.23) 또한 TEMPO-산화 전처리와 카르복시메틸화 전처리로 만들 셀룰로오스 나노섬유의 L929 cell line에 의한 세포 독성 시험 결과 원형질 막에서 LDH의 유출로 평가한 세포 독성 시험 결과 세포 독성이 없음이 보고되었다.24)
3.3.2 간세포 독성
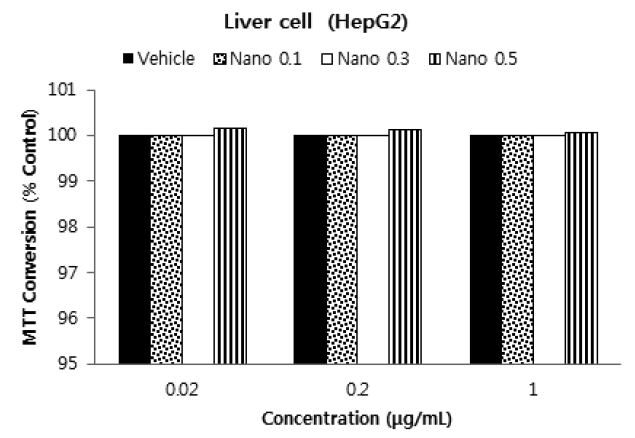
혼합 활엽수 크라프트 펄프를 카르복시메틸화 전처리시킨 후 만들어진 셀룰로오스 나노섬유의 간 세포 독성을 실시하였다. 배지 내에 전건 셀룰로오스 나노섬유 기준으로 0.02, 0.2, 1.0 mg/L를 첨가하여 세포 독성을 시험하였다. 치환도 0.5로 전처리된 셀룰로오스 나노섬유의 경우 치환도 0.1이나 0.3으로 치환된 셀룰로오스 나노섬유보다 간 세포 생존율이 높았지만 모든 경우 99% 이상의 세포 생존율을 보이기 때문에 그 차이는 크지 않다(Fig. 4).
셀룰로오스 나노섬유로 두 가지 세포주를 배양한 결과 태생기 전능세포(pluripotent cell)와 간암세포주(human hepatocellular carcinoma cell line, HepG2)의 경우, 형태나 유전자의 변형없이 잘 배양시킬 수 있음을 확인하였다.25) 셀룰로오스 나노섬유의 주입 후 3차원 지지체에 적합한 점탄성 성질을 가지며 세포 생체치환성도 높고 간세포 성분은 HepG2세포의 성장에 영향을 미치지 않았다.26) 따라서 활엽수 크라프트를 카르복시메틸화 전처리 후 만든 셀룰로오스 나노섬유는 0.02-1.0 μg/mL 농도로는 간세포에 독성을 끼치지 않는 것으로 생각된다.
3.3.3 신장 세포 독성
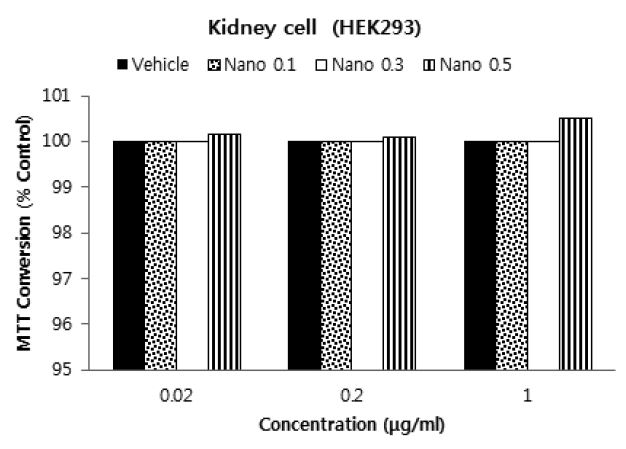
혼합 활엽수 크라프트 펄프를 카르복시메틸화 전처리 후 만들어진 셀룰로오스 나노섬유의 신장 세포 독성을 실시하였다. 배지 내에 전건 셀룰로오스 나노섬유 기준으로 0.02, 0.2, 1.0 mg/L를 첨가하여 세포 독성을 시험하였다. 치환도 0.5로 전처리된 셀룰로오스 나노섬유의 경우 치환도 0.1이나 0.3으로 치환된 셀룰로오스 나노섬유보다 신장 세포 생존율이 높았지만 모든 경우 99% 이상의 세포 생존율을 보이기 때문에 그 차이는 크지 않다(Fig. 5). 신장 세포에 대한 셀룰로오스 나노섬유의 세포 독성 관련 연구는 거의 없다. 셀룰로오스 나노결정을 가지고 인간배아 신장 세포에(human embryonic kidney cells(HEK 293)) 배양한 결과 셀룰로오스 나노결정 물질(아마 효소 처리 후 셀룰로오스 나노결정물 제조 시료)는 0.1 mg/mL의 농도에서 신장 세포 독성을 보이지 않았다.27) 본 연구와 인용연구 결과를 기반으로 저농도에서 셀룰로오스 나노물질(나노섬유와 나노결정)은 신장세포의 독성이 낮거나 없는 것으로 예상된다.