1. 서 론
2. 재료 및 방법
2.1 재료
2.2 방법
2.3 측정
3. 결과 및 고찰
3.1 비목질계 바이오매스의 유기용매 리그닌 회수율
3.2 회수 리그닌의 함량 분석
3.3 유기용매 리그닌의 주성분 분석(PCA)
3.4 유기용매 리그닌의 수산기 함량 분석
3.5 유기용매 리그닌의 항산화능 분석
4. 결 론
1. 서 론
현대 사회는 한정적인 화석연료의 매장량, 플라스틱 폐기물 문제 등 환경적 위기에 직면해 있다. 이에 대응하기 위해, 석유 기반 플라스틱의 사용량 감축을 위한 규제가 범국가적으로 전개되고 있다. 기존의 화석연료 기반의 소재에 대한 의존도를 줄임과 동시에 탄소 배출을 절감하고, 다양한 산업 규제에 대응할 수 있는 경쟁력을 가진 바이오매스의 활용을 기반으로 한 친환경 소재의 개발이 필수적인 과제로 떠오르고 있다.1,2)
리그닌은 셀룰로오스, 헤미셀룰로오스와 함께 식물의 외벽을 이루는 구성 성분 중 하나로써, 펄프화 공정을 거쳐 부산물의 형태로 얻을 수 있다. 정확한 구조가 밝혀지지 않았지만, 리그닌은 p-coumaryl, guaiacyl, syringyl 기본 전구체들이 에터(ether) 또는 C-C 결합으로 형성된 복잡한 방향족 기반의 고분자이다.3,4) 불규칙한 화학구조 및 분자량으로 인한 낮은 가공성에도 불구하고, 높은 열안정성, 항산화성, UV 차단성 및 다양한 오염물에 대한 흡착성능 등 뛰어난 기능을 지니고 있어 최근에는 리그닌을 이용한 화학제품의 기초 원료 활용, 탄소섬유 및 바이오플라스틱 제조, 유기물질 흡착 등 폭넓은 분야에서 활용하려는 연구가 활발히 진행되고 있다.5,6,7)
바이오매스로 활용 가능한 형태의 리그닌은 목재 및 비목재 식물에서 화학적 공정을 통해 추출할 수 있다. 그러나 목질계 바이오매스는 느린 생장 속도로 인해 추출 및 공급량에 한계가 있다. 반면 비목질계 바이오매스인 Corn, Straw, Kenaf, Ramie 및 Hemp 등의 작물은 목질화 정도가 낮고 높은 바이오매스 수확량, 강한 환경 적응력을 특징으로 하며, 빠른 생장 속도로 인해 향후 안정적인 공급이 가능하여 유망한 바이오매스 원료로 평가받는다.8)
본 연구에서는 비목질계 바이오매스 중에서 Ramie, Kenaf 및 Hemp를 대상으로 글리콜에테르와 산 촉매를 사용한 유기용매 공정을 이용해 리그닌을 분리 및 회수하였다. 회수한 리그닌의 화학적 구조 및 기능성 분석을 통해 추후 생분해성 고분자 복합소재, 친환경 접착제 등과 같은 바이오매스 기반의 지속 가능한 소재로의 활용 가능성을 검토하고자 하였다.
2. 재료 및 방법
2.1 재료
본 연구에서는 Ramie (충북 서천군), Hemp (경북 안동시), Kenaf (방글라데시)로 세 종류의 시료를 사용하였으며 다이텍연구원 한국친환경융합소재센터에서 제공받았다. 각 시료에 대한 기본 화학조성은 Table 1과 같다. Hemp는 hurd (속대), bast (인피)로 나누어 실험을 진행하였다. 시료는 별도의 처리 없이 50 ± 5 mm 길이로 절단하여 사용하였다(Fig. 1).
Table 1.
Chemical composition of non-woody biomass
유기용매 공정에서, 글리콜에테르(ethyl carbitol)와 황산, 수산화나트륨을, P-NMR 분석을 위한 시료의 전처리에는 피리딘, deuterated chloroform (CDCl3), 2-chloro-4,4,5,5,-tetramethyl-1,3,2-dioxaphospholane (TMDP), chromium(III) acetylacetonate (Cr(acac)3)를, 항산화능 측정에는 에탄올, 다이메틸설폭사이드(DMSO), 2,2-diphenyl-1-picrylhydrazyl (DPPH)을 사용하였다(Table 2).
Table 2.
Information on experimental reagents
2.2 방법
2.2.1 유기용매 공정
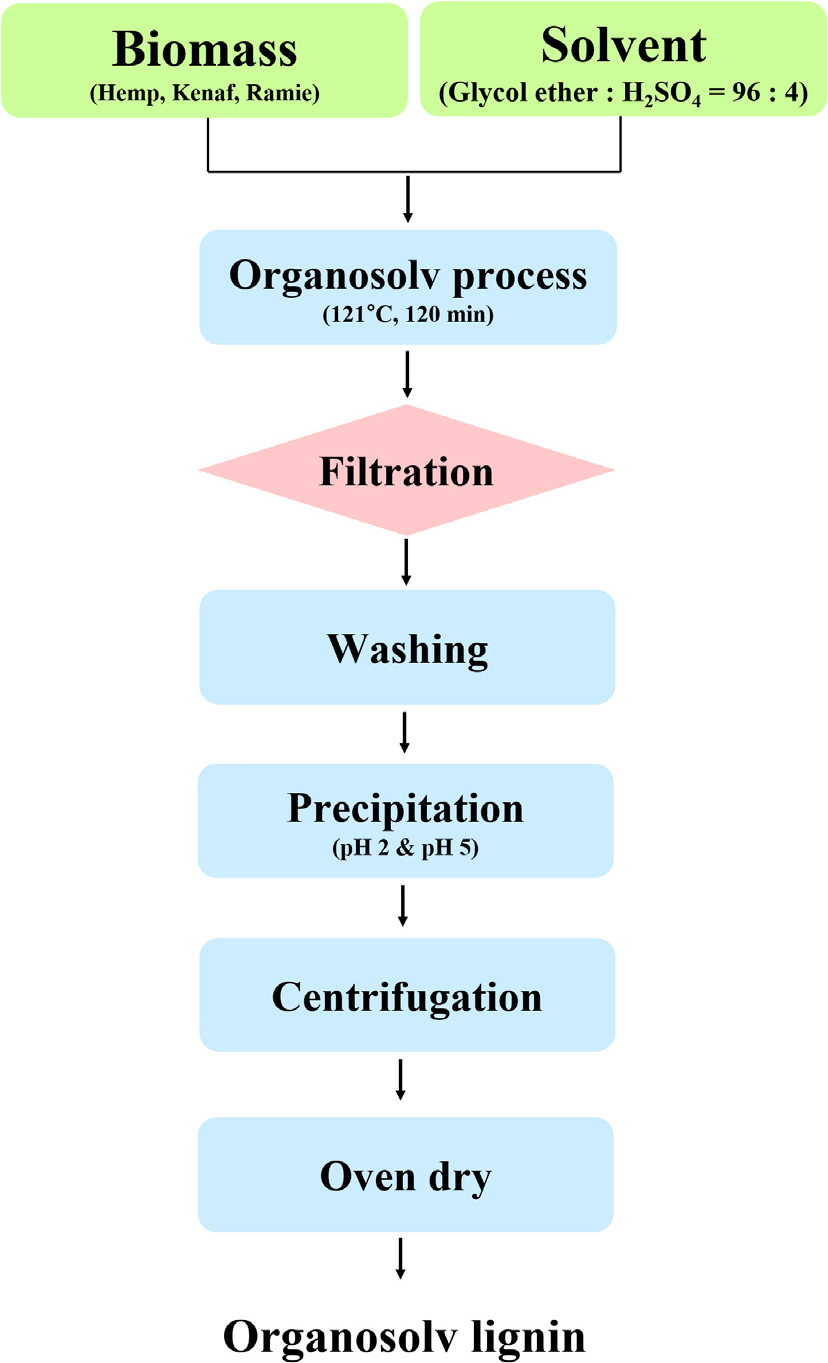
비목질계 바이오매스로부터 리그닌을 추출하는 공정은 Fig. 2와 같다. 고비점 용매인 glycol ether와 반응 촉매인 H2SO4을 사용해 공용매를 제조하였으며, 50 g의 시료를 1 : 10 (wt./wt.)의 비율로 공용매(glycol ether : H2SO4 = 96 : 4, wt./wt.)와 혼합하여 1 L의 삼각플라스크에 투입 후 24시간 동안 실온에서 침지하였다. 이후 오토클레이브(HB-506, Hanbaek Science, Korea)를 이용해 121°C에서 0.15 MPa로 2시간 동안 반응시켰다. 반응이 종료된 후 필터페이퍼(No. 2 Qualitative Filter Paper, Adventec)를 이용해 감압 여과를 실시했다. 이후 1% NaOH 수용액 및 증류수로 순차 세정하여 흑액과 펄프를 분리하였다.
2.2.2 리그닌 회수
리그닌을 회수하기 위해 NaOH를 사용하였다. 흑액을 교반하며 NaOH를 첨가하여 pH를 2 또는 5로 조절한 후, 실온에서 24시간 동안 정치시켜 리그닌의 응집을 유도하였다. 이후 원심분리기(LABOGENE 1580, Korea)를 이용하여 3,600 rpm에서 30분간 원심분리를 수행하고, 상등액과 응집된 리그닌을 분리하였다. 회수된 리그닌은 60°C의 건조기에서 24시간 동안 건조한 후 회수하였다. 남은 상등액에는 증류수를 추가하여 동일한 분리 과정을 반복함으로써 잔여 리그닌을 추가로 회수하였다.
2.3 측정
2.3.1 리그닌의 회수율과 함량 분석
리그닌의 수율은 사용한 시료의 건조중량에 대한 회수된 리그닌의 건조중량과의 비로 계산하였다. 또한 72% 황산법을 사용하는 TAPPI T 222 om-21에 의거하여 회수된 리그닌의 클라손 리그닌 함량을 정량했다.
2.3.2 주성분 분석(PCA)
각 시료에서 추출된 리그닌의 분류 특성을 확인하기 위해 IR 스펙트럼 데이터를 활용하여 주성분 분석(principal component analysis, PCA)을 수행하였다. IR 스펙트럼 데이터는 ATR-IR (Alpha-P model, Bruker Optics, Germany)을 이용해 4,000–400 cm-1의 측정영역에서 수집하였다. 또한 한 시료당 24회의 반복 스캔을 통해 평균값을 도출하였다. 획득한 IR 스펙트럼 데이터는 CAMO Software의 UnscramblerⓇ Ver. 9.8 (CAMO Software Inc., USA)을 이용하여 5차식 및 2차 미분 전처리 과정을 거친 후, 주성분 분석에 활용되었다. 주성분 분석 결과로 도출된 score plot, loading 값, 그리고 2차 미분 데이터를 이용하여 리그닌의 분류 특성에 대한 비교 분석을 실시하였다.
2.3.3 유기용매 리그닌의 수산기 함량 분석
Ramie, Kenaf, Hemp (bast) 및 Hemp (hurd)에서 회수한 리그닌의 수산기 정량을 위해 Meng 등9)의 방법을 참고하여 31P-NMR (phosphorus-31 nuclear magnetic resonance spectroscopy) 분석하였다. 시료는 TMDP로 전처리하여 인산화 후 FT-NMR 500 MHz (Avance Neo 500, Bruker, Germany)를 이용해 함량을 측정하였다. 분석 시 Mestrenova를 사용하였고 내부 표준물질인 NHND의 피크가 나타나는 152 ppm의 integration index를 1로 설정하였다. 이를 기준으로 다른 signal이 나타나는 영역의 면적비를 구하였다. 페놀기가 나타나는 영역은 세분화하여 syringyl & condensed hydroxyl, guaiacyl, p-hydroxyphenyl의 면적비를 계산하였다. 계산된 면적비는 다음 Eq. [1]에 따라 수산기의 함량으로 계산되었다.
여기서, 는 수산기의 면적비, 는 NHND의 면적비를 의미한다.
2.3.4 항산화 특성 분석
Ramie, Kenaf, Hemp (bast) 및 Hemp (hurd) 리그닌의 항산화 특성의 분석을 위해 Gordobil 등10)의 방법을 참고하여 U-Vis spectrophotometer (GENESYS 180, Thermo Fisher, USA)를 이용하여 분석하였다. 10 mL 유리 바이알에 제조된 농도별로 공용매(EtOH/DMSO = 19 : 1)에 용해된 리그닌 용액 2.75 mL를 0.2 mM DPPH 용액 0.75 mL와 혼합 후 빛으로 인한 라디칼의 분해를 차단하기 위해 알루미늄 호일로 바이알 겉면을 감싸 1시간 동안 상온에서 반응시켰다. 반응 후에는 512 nm의 값을 측정한 후 Eq. [2]를 통해 계산하여 radical scavenging ability (RSA, %)를 분석하였으며, 농도별로 측정된 RSA는 선형회귀법을 통해 half maximal inhibitory concentration (IC50, mg/mL)을 계산하였다. 모든 리그닌 시료의 항산화능은 동일한 방법으로 측정하였다.
여기서, 는 DPPH의 초기 흡광도(nm), 는 DPPH의 1시간 후 흡광도(nm)를 의미한다.
3. 결과 및 고찰
3.1 비목질계 바이오매스의 유기용매 리그닌 회수율
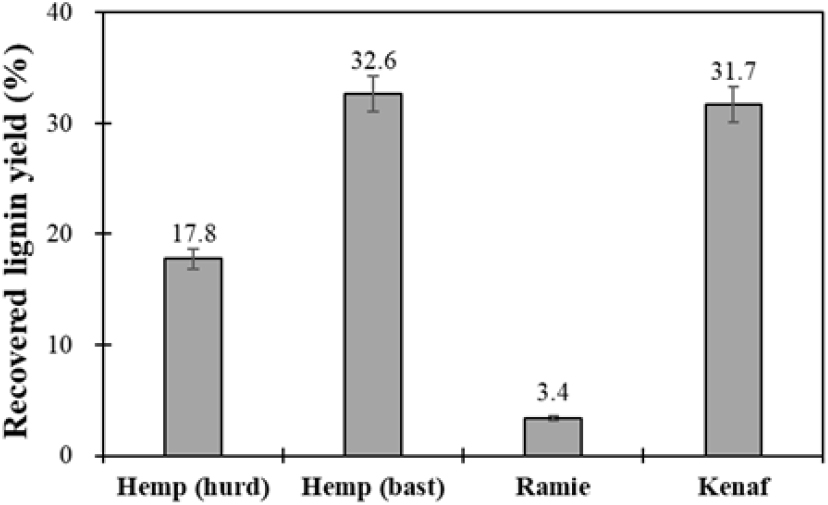
유기용매 공정에서 사용한 glycol ether는 높은 비점을 가져 증류를 통해 회수가 가능하며 기존의 에탄올 기반 공정보다 경제성이 우수하고 환경친화적이라는 장점이 있다.11) 본 연구에서는 비목질계 바이오매스인 Hemp, Kenaf, Ramie를 대상으로 유기용매 공정을 통해 회수된 리그닌의 회수율을 분석하였으며 그 결과는 Fig. 3과 같다. Hemp (bast)에서 32.6%, Kenaf에서 31.7%의 높은 리그닌 수율을 달성했으며, Hemp (hurd)는 17.8%, Ramie는 3.4%의 수율을 보였다. 이러한 차이는 각 바이오매스의 화학적 조성과 밀접한 관련이 있는 것으로 추측되며 Ramie의 낮은 수율은 효소 또는 기계적 전처리를 병행하면 개선될 수 있을 것으로 판단된다.12)
3.2 회수 리그닌의 함량 분석
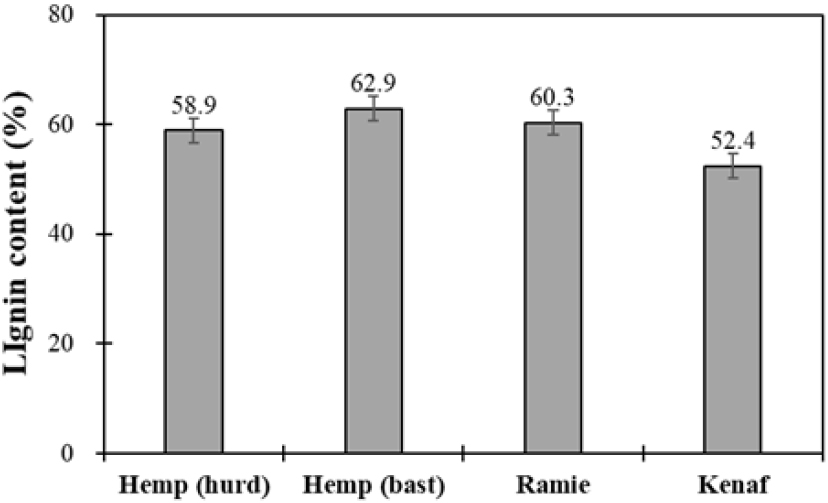
회수된 리그닌 시료에서 다시 산 불용성 리그닌을 측정한 결과는 Fig. 4와 같다. Hemp (hurd)에서 58.9%, Hemp (bast)에서 62.9%, Ramie에서 60.3%, Kenaf에서 52.4%로 나타났다. 이는 추출 리그닌 시료를 대상으로 한 분리·회수한 후 다시 클라손 리그닌의 함량을 평가한 값으로, glycol ether를 이용한 유기용매 공정이 초기 추출 단계에서부터 리그닌의 구조를 보존하여 산 처리 시 가수분해되지 않는 불용성 분획을 효과적으로 확보했음을 의미한다.13) 특히, Hemp와 Ramie의 높은 불용성 분획은 glycol ether와 황산 혼합용매 처리 중 β-O-4 결합 구조 유지가 우수했음을 반영하며,14) Kenaf의 상대적으로 낮은 비율은 분리 과정 중 일부 저분자 분획이 산 처리로 용출된 결과로 추측된다. 이처럼 리그닌 시료에서 직접 클라손 리그닌을 측정함으로써, 공정 후 리그닌의 열적·화학적 안정성과 고분자 특성 유지 가능성을 보다 정확히 평가할 수 있으며, 향후 바이오 리파이너리 공정에서 고부가가치 리그닌의 활용에 기초 자료로 활용될 수 있다.
3.3 유기용매 리그닌의 주성분 분석(PCA)
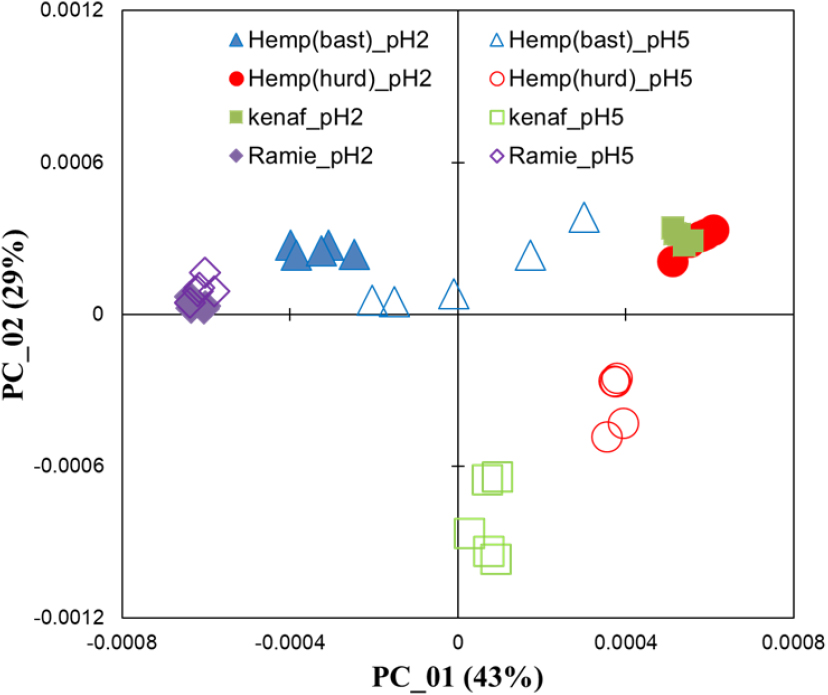
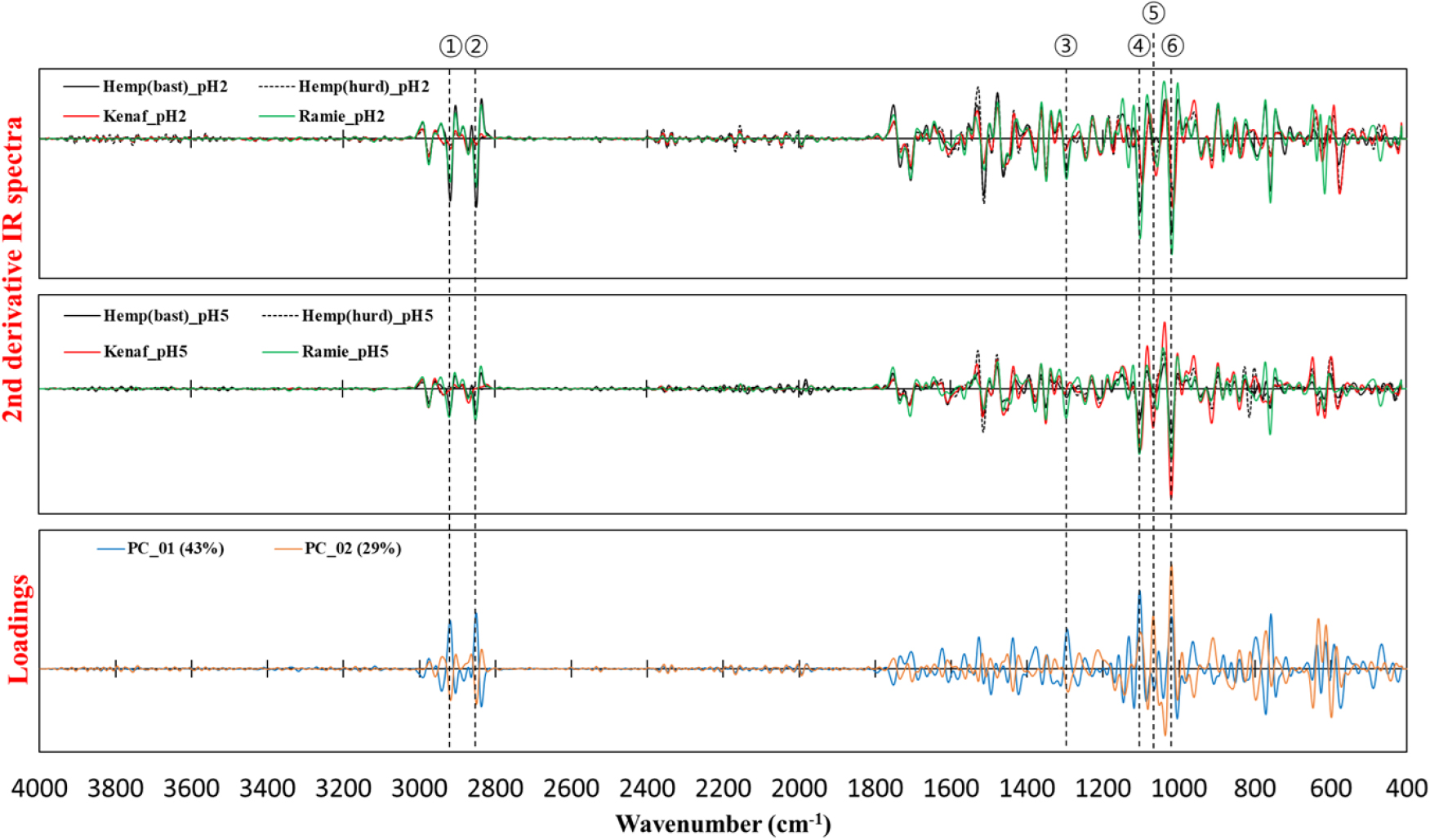
pH 2와 pH 5의 조건으로 회수한 비목질계 바이오매스 유기용매 리그닌의 분류 특성을 확인하기 위해서 리그닌의 IR 스펙트럼을 5차 다항식 및 2차 미분 전처리 후 주성분 분석을 실시하여 Fig. 5와 같은 Score plot을 얻었다. PC_01, PC_02와 같이 표기된 백분율은 ‘explained variance’로 총분산 중에서 해당 주성분을 설명할 수 있는 분산의 양을 의미한다.15) 따라서 PC_01이 전체 분산의 43%, PC_02가 29%를 차지한다고 설명할 수 있다. PC_01의 음(-)의 영역에는 Ramie와 Hemp (bast)에서 회수된 리그닌이 분포하고 양(+)의 영역의 경우 Hemp (hurd) 및 Kenaf에서 회수한 리그닌이 들이 분포하며 이들이 각각 클러스터를 이루며 어느 정도 분류가 된 모습을 확인할 수 있다. PC_02의 경우 음의 영역에는 pH 5로 조절하여 회수한 Kenaf와 Hemp (hurd) 리그닌이 있으며, 양의 영역에는 나머지 리그닌들이 위치하고 있다.
PCA score plot으로부터 분류가 확인된 IR 스펙트럼의 피크를 추적하기 위해 2차 미분 스펙트럼과 PC_01, PC_02의 적재값(loadings)이 큰 피크들을 Fig. 6에 나타내었다. 여기서 언급되는 로딩값이란 PCA에서 생성한 변수 PC_01, PC_02에 대하여 기존의 2차 미분 스펙트럼이 얼마나 영향을 미치는지 나타내는 지표이다.16)
로딩값에서 분류에 결정적인 영향을 미치는 6개의 주요 피크들이 확인되었으며 Table 3에 나타내었다. PC_01에 영향을 미친 4개의 주요 피크는 다음과 같다. 2,918 cm-1과 2,848 cm-1에서 관찰되는 피크는 C-H 비대칭 및 대칭 stretching 진동으로, 셀룰로오스 또는 헤미셀룰로오스 내 methylene group의 특성 피크에 해당한다.17,18) 1,293 cm-1 피크는 리그닌에서 기인한 C-O stretching 진동으로, 페놀성 방향족 구조의 흡수대에서 나타나는 피크로 해석되어 진다.19) 1,106 cm-1 파장의 피크의 경우 셀룰로오스의 글루코오스 단위간 에터(ether) 결합에 기인한 것으로 확인되었다.20) PC_02에서는 2개의 주요 피크가 분류에 기여하였다. 1,066 cm-1의 경우 셀룰로오스 안의 -CH 결합 및 C-O stretching 진동과 관련된 피크이며,21) 1,022 cm-1의 피크는 셀룰로오스 안의 C-O 에테르 결합 또는 리그닌의 메톡시기(-OCH3)에서 유래하는 복합적 특성을 나타낸다.22) 따라서 주성분 분석을 통해 얻은 PC_01과 PC_02를 로딩값과 2차 미분 IR 스펙트럼을 비교해 보았을 때, 회수된 리그닌은 방향족 구조의 형태와 다당류 성분의 잔존 함량에 따라 분류되는 것으로 추측된다.
Table 3.
Assignment of main IR absorption peaks by PCA of recovered lignin
3.4 유기용매 리그닌의 수산기 함량 분석
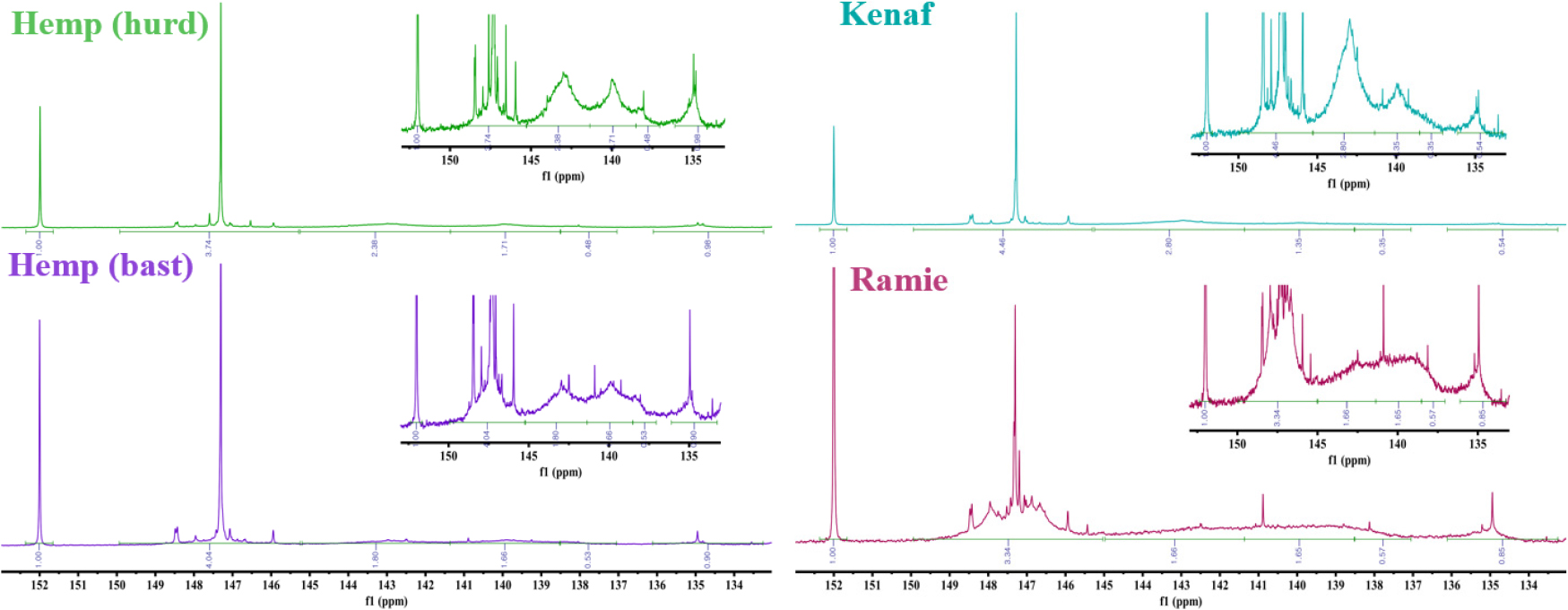
Ramie, Kenaf, Hemp (bast) 및 Hemp (hurd)으로부터 추출한 리그닌의 31P-NMR 분석을 실시하였다. 분석 결과는 Fig. 7에 나타냈다. 149.9–145.3 ppm은 지방족 수산기, 133.2–136.2 ppm은 카복시성 수산기, 137–145.3 ppm은 페놀성 수산기의 존재를 보여준다. 특히 페놀성 수산기의 경우, 구아이아실기, 시링길기, ρ-하이드록시페닐기 및 축합형 수산기의 영역으로 나누어진다. 분류된 스펙트럼의 영역별 수산기 함량을 산출하기 위해 영역별 Integral index를 구하였으며, 계산된 작용기의 함량 값은 Table 4에 나타냈다.
Table 4.
Functional group concentrations in recovered lignin derived from non-woody biomass
모든 회수 리그닌은 3–4 mmol/g의 수산기를 함유하고 있다. Hemp (hurd)와 Kenaf에서 추출한 리그닌의 경우 3.709 mmol/g 및 3.693 mmol/g으로 높게 나타났다. 반면 Hemp (bast)와 Ramie에서 추출한 리그닌은 3.450 mmol/g 및 3.245 mmol/g으로 다소 낮게 나타났다. 총 수산기 함량이 높다는 것은 추후 에스터화(esterification), 카복실화(caboxylation) 등 다양한 화학적 개질 반응의 여지가 높다는 것으로 해석할 수 있다. 따라서, Hemp (hurd)와 Kenaf에서 추출한 리그닌이 개질 소재로서의 추후 활용 가능성이 더 높다고 판단된다.
항산화능에 직접적으로 관여하는 페놀성 수산기의 경우, Hemp (hurd)와 Kenaf에서 추출한 리그닌이 1.825 mmol/g, 1.759 mmol/g으로 높은 수치를 보인다. 반면 Ramie와 Hemp (bast)에서 추출한 리그닌은 1.560 mmol/g, 1.542 mmol/g으로 다소 낮은 수치를 나타내었다. 이 결과로 미루어보아, Hemp (hurd)와 Kenaf에서 추출한 리그닌이 항산화성이 가장 우수할 것으로 예측된다.
추가적으로, 리그닌의 반복단위인 구아이아실기, 시링길기 및 축합형 수산기의 함량 부분에서 큰 차이를 볼 수 있었다. Hemp (bast)와 Ramie에서 추출한 리그닌은 0.6 mmol/g 대의 수치를 보였으나, Kenaf와 Hemp (hurd)에서 추출한 리그닌은 0.9–1 mmol/g 대의 상대적으로 높은 수치를 관찰하였다. 시링길기 및 축합형 수산기는 steric hindrance가 높은 메톡시기가 페놀에 연결된 형태이기 때문에 함량이 많을수록 같은 조건에서 상대적으로 낮은 화학적 반응성을 보이게 된다.23) 따라서, Hemp (bast)와 Ramie 보다는 Hemp (hurd)와 Kenaf에서 추출한 리그닌이 개질 및 응용에 유리할 것으로 판단된다.
결과적으로, 원료에 따라 회수 리그닌 내 존재하는 수산기별 함량은 뚜렷한 차이를 보였으며, 이는 비목질계 바이오매스 리그닌 구조 및 조성 차이에 의한 것으로 사료된다.
3.5 유기용매 리그닌의 항산화능 분석
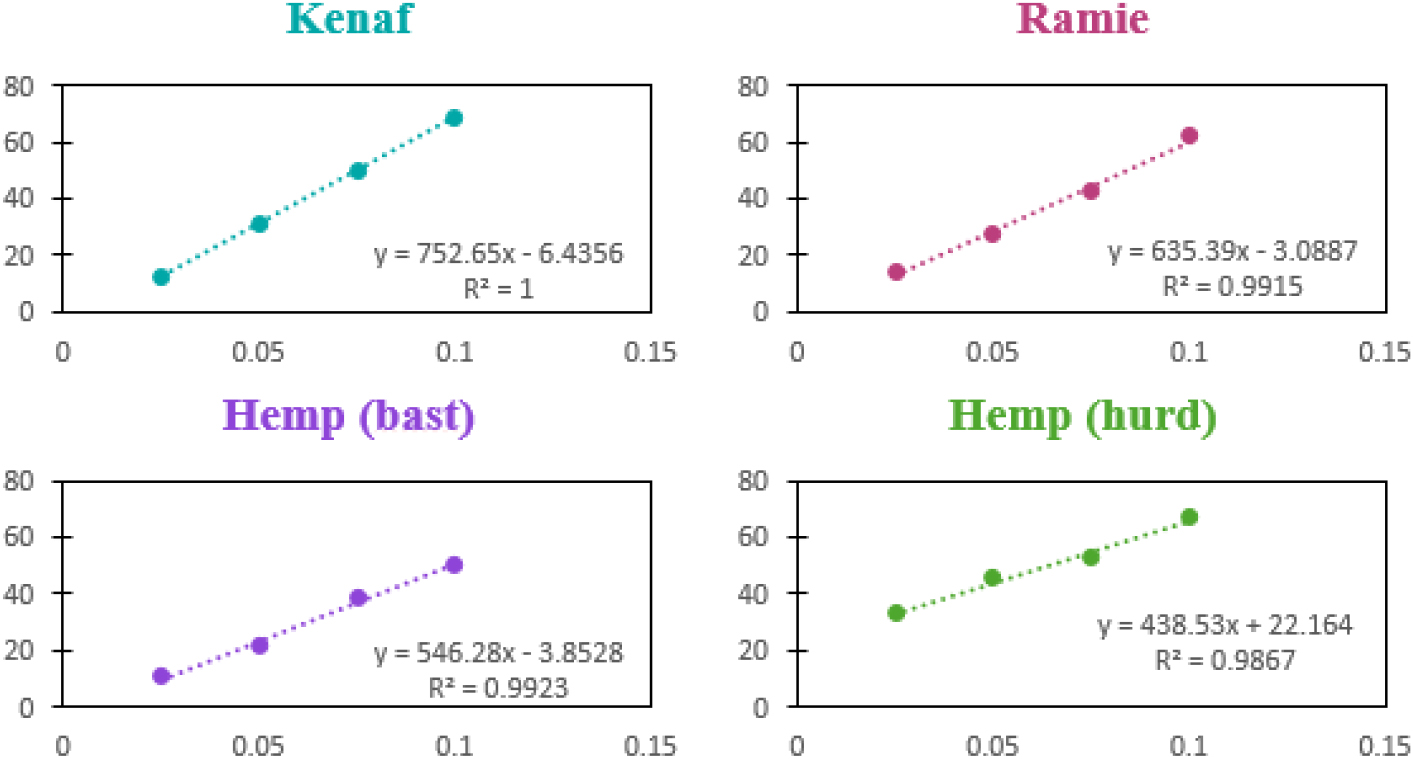
Ramie, Kenaf, Hemp (bast) 및 Hemp (hurd)으로부터 추출한 리그닌의 항산화능을 분석하였다. 선형회귀법을 이용하여 x축은 농도, y축은 RSA (%)인 일차방정식을 산출하였으며 Fig. 8에 나타내었다. 그림과 같이, 각 시료의 일차방정식은 0.98을 초과하는 높은 결정계수(R2)를 나타내며 선형 모델의 타당성을 확인할 수 있었다. 따라서, 구간 내의 추정값은 신뢰할 수 있는 값임을 알 수 있다. 이를 근거로 50%의 RSA를 갖는 리그닌의 농도인 IC50을 산출하여 Table 5에 나타내었다. IC50은 항산화 성능이 50%를 발현할 때의 용액의 농도를 나타내는 값으로, 이 수치가 낮을수록 항산화능이 뛰어나다는 의미를 가진다. IC50값을 살펴보면, Hemp (hurd)에서 추출한 리그닌이 0.064 mg/mL로 가장 낮은 수치를 보였고, Kenaf 추출 리그닌이 0.075 mg/mL, Ramie 추출 리그닌이 0.084 mg/mL 그리고 Hemp (bast) 추출 리그닌이 0.099 mg/mL 순의 높은 수치를 나타내었다. 이러한 결과는 Zhu 등24)의 보고와 일치하며, 리그닌의 페놀성 수산기 함량과 IC50 수치는 반비례함을 확인할 수 있다. 반면 지방족 수산기 및 카복시성 수산기 등의 다른 작용기 함량과는 뚜렷한 상관계를 확인하기 어려웠으며, 이는 페놀성 수산기가 항산화 발현에 더 직접적으로 관여함을 간접적으로 확인할 수 있지만 향후 기타 작용기의 항산화능 발현 기여 정도를 정량적으로 규명하기 위한 추가연구가 필요하다고 판단된다.
Table 5.
The radical scavenging activity (RSA) according to the concentration of recovered lignin and IC50 value
4. 결 론
본 연구에서는 비목질계 바이오매스로부터 glycol ether 기반 유기용매 공정을 적용해 리그닌을 추출하고 그 특성을 분석하였다. Hemp (bast)와 Kenaf는 각각 32.6%, 31.7%의 높은 리그닌 회수율을 보였으며, Ramie 리그닌의 회수율은 3.4%로 가장 낮았다. 추출된 리그닌 내에 존재하는 클라손 리그닌 함량은 Hemp (bast)에서 62.9%로 가장 높은 수치를 보였다. 주성분 분석을 통해 각 바이오매스에 따라 방향족 구조의 형태와 다당류 잔존량 등의 차이가 나타나는 것으로 보인다. 31P-NMR 분석 결과, 리그닌의 작용기 조성은 원료 식물에 따라 다소 차이를 보이며, 특히 Hemp (hurd)에서 추출한 리그닌은 3.709 mmol/g의 가장 많은 수산기 함량과 0.064 mg/mL의 가장 낮은 IC50값을 가져 뛰어난 항산화 활성을 보였다.
본 연구는 화석연료 기반의 플라스틱을 대체하기 위한 바이오매스 소재의 적용 가능성을 확인하는 기초 연구이다. 화석연료의 의존도를 낮추고 지속 가능한 바이오매스 기반 친환경 소재 개발에 기여할 수 있는 기초자료로 충분히 활용될 수 있을 것으로 예상되며, 후속 연구를 통해 플라스틱 대체 소재로의 적용 실험을 진행하고자 한다.