1. 서 론
2. 셀룰로오스/나노셀룰로오스 소재의 구조적·물리적 특성과 장점
2.1 셀룰로오스와 나노셀룰로오스의 구조적 특성
2.2 셀룰로오스 및 나노셀룰로오스의 물리적 특성
2.3 약물전달시스템(DDS)에 응용하기 좋은 장점
3. 퇴행성 뇌질환에서 셀룰로오스 기반 DDS 응용 사례
3.1 알츠하이머병(Alzheimer’s disease)에서의 응용
3.2 파킨슨병(Parkinson’s disease)에서의 응용
3.3 헌팅턴병(Huntington’s disease)에서의 응용
3.4 ALS 및 기타 신경변성질환에서의 응용
4. 셀룰로오스의 위치와 한계
5. 셀룰로오스 DDS의 전망
6. 결론 및 제안
1. 서 론
퇴행성 뇌질환(neurodegenerative diseases)은 고령화에 따라 빠르게 증가하는 대표적 난치성 질환군으로, 알츠하이머병(Alzheimer’s disease, AD), 파킨슨병(Parkinson’s disease, PD), 헌팅턴병(Huntington’s disease, HD), 근위축성 측삭경화증(amyotrophic lateral sclerosis, ALS) 등이 포함된다. 이들 질환은 단백질 응집, 신경염증, 산화 스트레스, 시냅스 소실, 신경세포 사멸 등 공통된 병태생리를 보이며, 일단 발병하면 진행을 역전시키기 어려워 장기적인 인지 및 운동 기능 저하를 유발한다[1,2,3]. 다양한 소분자·항체·핵산 기반 치료제의 후보들이 개발되고 있음에도 불구하고 임상으로의 전환 비율이 낮은 중요한 이유 중 하나는, 혈–뇌 장벽(blood–brain barrier, BBB)이 외부에서 투여된 약물의 뇌 내 도달을 강하게 제한하기 때문이다[4,5]. BBB는 대부분의 친수성 소분자와 고분자·단백질·핵산 기반 치료제를 차단하므로, 약물 자체의 효능뿐만 아니라 적절한 약물전달시스템(drug delivery system, DDS)을 통해 BBB를 극복하거나 우회하는 전략이 필수적이다[6].
이를 위해 리포솜(liposomes), 합성 고분자 나노입자(polymeric nanoparticles), 무기 나노입자(inorganic nanoparticles), 세포 유래 외소포체(extracellular vesicles) 등 다양한 DDS가 개발되어, 표면 리간드 결합을 통한 수용체 매개 세포통과(receptor-mediated transcytosis), 폴리에틸렌글리콜(polyethylene glycol, PEG) 코팅을 통한 장순환 등을 중심으로 뇌 표적화가 시도되고 있다[7]. 그러나 이들 시스템은 합성 지질·고분자에 크게 의존하여 장기 독성·체내 축적 가능성, 복잡한 제조 공정과 비용, 환경 지속가능성 측면에서 한계를 가진다. 또한 특정 치료제의 경우 기존 DDS로는 안정성, 방출 제어, 뇌 표적화 효율을 동시에 만족시키기 어렵다는 보고도 있다. 이러한 배경에서 재생 가능한 바이오매스(biomass)에서 유래하며 본질적으로 생체적합성과 생분해성이 높은 셀룰로오스(cellulose) 및 나노셀룰로오스(nanocellulose)가 기존 DDS를 보완할 수 있는 새로운 플랫폼 소재로 주목받고 있다. 셀룰로오스는 β-(1→4)-D-glucopyranose가 선형으로 연결된 다당류로, 높은 결정성과 수소결합 네트워크에 기반한 우수한 기계적 강도와 유연성을 가지며, 셀룰로오스 나노크리스탈(cellulose nanocrystal, CNC), 나노피브릴(cellulose nanofibril, CNF), 박테리아 셀룰로오스(bacterial cellulose, BC)와 같은 나노셀룰로오스는 높은 비표면적과 3차원 네트워크 구조를 통해 약물 및 생체분자와의 상호작용을 정밀하게 조절할 수 있는 플랫폼을 제공한다.
또한 셀룰로오스 사슬의 풍부한 하이드록실기(-OH)는 카르복실기, 아민기, 실란기 등 다양한 기능성 그룹으로 변환이 가능하여, 표면 전하, 친·소수성, 리간드 결합 능력을 조절함으로써 약물 로딩과 방출 프로필을 설계할 수 있다. 이러한 특성 덕분에 셀룰로오스는 나노입자, 하이드로겔, 필름, 에어로겔, 3차원 스캐폴드 등 다양한 형태의 DDS 매트릭스로 가공되어, 비강–뇌 경로(nose-to-brain)를 이용한 파킨슨병 모델의 도파민성 약물 전달, 경구 제형을 통한 알츠하이머병 모델에서의 아밀로이드 베타(Aβ) 감소 및 신경염증 완화, 헌팅턴병·ALS에서의 병리 단백질 응집 억제, 신경 조직공학 스캐폴드를 통한 뇌 조직 재생 지원 등으로 응용되고 있다[8]. 그럼에도 셀룰로오스 기반 DDS는 BBB 통과 최적화, 소수성 약물 로딩 한계, 콜로이드·저장 안정성, 제조 공정의 표준화 및 규제 불확실성 등 여러 과제를 안고 있다. 본 논문에서는 이러한 점을 고려하여, 셀룰로오스 및 나노셀룰로오스 기반 DDS의 구조적·기능적 특성을 파악하고, 주요 퇴행성 뇌질환별 응용 사례, 기존 DDS와 비교한 위치 및 한계, 그리고 향후 설계 전략과 임상 응용 전망을 중심으로 그 응용과 전략을 종합적으로 고찰하고자 한다.
2. 셀룰로오스/나노셀룰로오스 소재의 구조적·물리적 특성과 장점
셀룰로오스와 나노셀룰로오스는 구조적·물리적 특성이 우수하고, DDS 구축에 유리한 여러 장점을 동시에 지니고 있어 다양한 생의학·재료 분야에서 활발히 연구되고 있다. 특히, 풍부한 자원 기반의 재생 가능한 바이오폴리머이면서도 기계적 강도, 표면 특성, 생체적합성 및 생분해성을 고루 갖추고 있어, 퇴행성 뇌질환과 같은 만성질환을 대상으로 하는 지속형 DDS 매트릭스로서 높은 잠재력을 보여준다.
2.1 셀룰로오스와 나노셀룰로오스의 구조적 특성
셀룰로오스는 β-(1→4)-D-glucopyranose 단위가 선형으로 중합된 고분자 다당류로, 사슬 내·사슬 간 강한 수소결합과 높은 결정성을 특징으로 한다[9]. 이러한 구조적 특성은 미시적으로는 결정 영역과 비결정 영역이 교차하는 계층적 구조를 형성하고, 거시적으로는 3차원 네트워크 구조를 이루게 하여, 탁월한 기계적 강도와 동시에 적절한 유연성을 부여한다. 이와 같은 강인한 분자 간 상호작용과 네트워크 구조는 기계적 안정성과 형태 유지가 중요한 DDS 매트릭스 설계에 유리한 기반을 제공한다.
나노셀룰로오스는 셀룰로오스를 물리적 또는 화학적 처리(고전단 처리, 기계적 분쇄, 화학적 전처리 등)를 통해 나노 크기의 피브릴 또는 결정으로 분리한 소재로, 마이크로미터의 벌크(bulk) 셀룰로오스와 동일한 화학 구조를 가지나, 약 100 nm 이하의 나노미터 스케일로 분산 가능한 섬유·결정·네트워크 형태로 존재하는 경우를 말한다. 즉, 화학식은 동일하지만 크기 스케일과 비표면적, 장폭비(high aspect ratio) 및 형상(섬유/막대/네트워크)의 차이를 기준으로 셀룰로오스와 나노셀룰로오스를 나눌 수 있다. 대표적인 나노셀룰로오스는 셀룰로오스 나노피브릴(CNF)과 셀룰로오스 나노크리스탈(CNC), 박테리아 셀룰로오스(BC)가 있다. CNF는 직경 수십 나노미터 수준의 높은 장폭비를 가진 피브릴이 얽힌 네트워크 구조를 형성하며, CNC는 상대적으로 짧고 막대형(rod-like)의 나노결정 형태로 높은 결정성과 강성을 지닌다[10](Table 1). 이들 나노셀룰로오스는 셀룰로오스에 비해 매우 높은 비표면적을 갖고, 조밀하면서도 연속적인 3차원 네트워크를 형성할 수 있어 외부 분자와의 상호작용에 특히 유리하다. 또한 이러한 구조적 특징은 약물의 흡착 및 담지, 그리고 DDS 내에서의 확산 및 방출을 정밀하게 설계하는 데 직접적으로 활용될 수 있다. 특히 CNF는 높은 장폭비와 연속적인 피브릴 네트워크로 인해 하이드로겔·에어로겔 형성 능력이 우수하여, 점탄성이 요구되는 주사형 겔 제형이나 점막 접착성이 중요한 비강 내 DDS에서 약물의 국소범위에서 체류하는 시간을 연장하여 지속적인 약물 방출에 유리하다[11,12]. 반면 CNC는 상대적으로 짧고 강성이 높은 막대형 나노결정이므로, 안정한 콜로이드 분산과 정밀한 입자 크기 제어가 가능해 전신 투여용 나노입자 또는 복합 나노입자의 코어 소재로 활용하기 적합하고, 표면 기능화를 통해 BBB 표적 리간드 부착이나 전하 조절을 구현하기 용이하다[13]. BC는 고순도 나노피브릴이 치밀한 3차원 네트워크를 이루고 있어 강도가 우수하고 수분을 보유하는 능력이 뛰어나므로, 뇌손상 부위나 신경조직 결손 부위에 적용하는 국소 스캐폴드형 DDS에서 약물 전달과 동시에 물리적 지지체 및 세포 부착 기질을 돕는 역할을 수행할 수 있다[14,15]. 이와 같이 CNF, CNC, BC의 형태적, 물리적 차이는 투여 경로(전신/국소/비강), 요구되는 방출 양상(급속/지속), 표적 조직(뇌/점막/손상 조직)에 따라 서로 다른 최적 설계 전략을 제공하며, DDS를 질환 및 제형 특성에 맞게 맞춤형으로 설계하는 데 중요한 설계 인자로 작용한다.
Table 1.
Structural and physicochemical characteristics of cellulose/nanocellulose materials and DDS-relevant advantages
2.2 셀룰로오스 및 나노셀룰로오스의 물리적 특성
셀룰로오스 및 나노셀룰로오스의 대표적인 물리적 특성으로는 높은 기계적 강도, 열적 안정성, 생분해성, 그리고 친환경성을 들 수 있다[16]. 셀룰로오스 기반 재료는 3차원 수소결합 네트워크를 통해 우수한 인장강도와 탄성률을 나타내며, 이는 필름, 하이드로겔, 에어로젤, 스캐폴드 등의 형상으로 가공되었을 때도 유지된다[17]. 특히 나노셀룰로오스를 기반으로 제조된 나노종이(nanopaper)나 하이드로겔은 치밀한 네트워크 구조를 형성하여 기계적 성질과 내수성이 크게 향상되며, 구조적 안정성이 요구되는 생체용 DDS 매트릭스로 적합하다.
또한, 나노셀룰로오스는 매우 높은 비표면적과 특이적인 메쉬(mesh)/와이어(wire) 구조를 갖기 때문에, 용질 및 생체분자와의 상호작용이 용이하다[18]. 이러한 높은 비표면적은 단순 물리흡착뿐 아니라, 표면 개질을 통한 화학적 결합, 이온성 상호작용 등을 통한 기능성을 조절 가능하게 하고, 이를 통해 복합소재로 활용될 경우 매트릭스 재료의 기계적·열적·장벽 특성을 크게 개선할 수 있다. 생분해성 및 친환경성 역시 셀룰로오스 기반 소재의 중요한 장점으로, 체내에서 분해·배출이 가능한 DDS 플랫폼을 설계할 수 있으며, 환경 부담이 적은 지속가능한 바이오 소재로서의 활용가치가 높다.
2.3 약물전달시스템(DDS)에 응용하기 좋은 장점
나노셀룰로오스는 높은 생체적합성, 생분해성, 비독성, 우수한 분산성, 그리고 높은 비표면적을 동시에 갖추고 있어 DDS 응용에 특히 적합한 소재로 주목받고 있다. 이러한 특성으로 인해 나노셀룰로오스는 다양한 약물(소분자 약물, 펩타이드, 단백질, 핵산 등)을 흡착 또는 운반하기 용이하며, 약물이 매트릭스 내부 또는 표면에 균일하게 분산될 수 있어 제어방출형(controlled release system) DDS의 매트릭스로 이상적이다[19].
셀룰로오스 사슬은 풍부한 하이드록실기(-OH)를 포함하고 있어, 카복실기 도입, 양이온화, 고분자 그래프트(grafting) 등 다양한 화학적 유도체화가 가능하다[20]. 이러한 표면 기능성 개질과 구조적 다양성 덕분에 약물과의 물리·화학적 결합(수소결합, 정전기적 상호작용, 공유결합 등)을 쉽게 설계할 수 있으며, 이를 통해 약물의 결합량, 방출 속도, 용출 특성, 나아가 약동학적 프로파일을 정밀하게 조절할 수 있다. 예를 들어, 표면 전하를 조절하여 양이온성/음이온성 약물과의 상호작용을 최적화하거나, 특정 pH 또는 효소 환경에서 결합이 선택적으로 해리되도록 설계함으로써 표적 부위에서의 약물 방출을 유도할 수 있다. 더불어, 셀룰로오스 및 나노셀룰로오스는 고강도·내구성을 기반으로 다양한 형상으로 가공이 가능하다[21]. 필름, 하이드로겔, 나노피브릴 매트, 스폰지, 마이크로/나노비드 등 여러 형태의 DDS 플랫폼으로 구현할 수 있으며, 이는 경구, 주사, 국소, 비강 등 다양한 투여 경로와 요구 물성을 만족시키는 데 큰 장점이 된다. 이러한 형상 다양성은 표면적·공극 구조·기계적 안정성 등 DDS 설계에 중요한 인자를 세밀하게 조절할 수 있게 해 주며, 복합 고분자나 무기 나노입자와의 조합을 통해 기능성을 추가적으로 부여할 수 있다.
뿐만 아니라, 셀룰로오스 기반 DDS는 BBB를 통과하거나 우회하기 위한 설계 측면에서도 뛰어난 이점을 가진다. 카르복시메틸 셀룰로오스(carboxymethyl cellulose, CMC)나 CNF와 같이 점액점착성이 우수한 셀룰로오스 유도체는 비강 점막에 장시간 부착되어 약물의 국소 체류 시간을 크게 연장시킬 수 있으며, 이를 통해 후각신경·삼차신경을 따라 직접 뇌로 이동하는 비강–뇌 경로를 리포솜·고분자 나노입자보다 효율적으로 활용할 수 있다[22]. 비강 투여 전임상 연구에서 CMC계열의 나노입자 또는 젤 제형은 동일 약물의 단순 용액 대비 뇌/혈장 농도비와 뇌 내 AUC (area under curve)가 유의하게 상승하는 것으로 보고되었으며, 일부 경우에는 유사 크기의 PEG-PLGA 나노입자와 비교하여도 뇌 축적 효율에서 크게 뒤지지 않는 것으로 나타난다[23]. 이는 전신 순환을 거쳐 BBB를 통과해야 하는 리포솜·고분자 나노입자와 달리, 셀룰로오스 기반 비강 DDS가 비강–뇌 직접 경로를 활용함으로써 상대적으로 낮은 전신 노출과 충분한 뇌 내 농도를 확보할 수 있음을 시사한다. 또한 셀룰로오스·나노셀룰로오스 기반 하이드로겔이나 스캐폴드는 뇌실 내 혹은 뇌손상 부위에 국소 주입·이식하여 약물을 장기간 방출하는 뇌 인접(depot) 제형으로 설계할 수 있어, BBB를 직접 관통시키기보다는 BBB 안쪽 또는 바로 인접한 공간에서 농도 구배를 형성함으로써 효과적으로 약물의 일정한 농도를 유지할 수 있도록 한다[24,25]. 이러한 국소 depot 전략은 리포솜·고분자 나노입자의 전신 투여에 비해 BBB 투과율(%) 자체는 낮더라도, 표적 영역에서의 실질적인 노출 시간과 농도 측면에서 경쟁력 있는 치료 지표를 보일 수 있다는 점에서 의미가 있다. 더불어 나노셀룰로오스 표면에 transferrin, LDL receptor ligand, peptide ligand와 같은 BBB 수용체 표적 리간드를 고밀도로 다중 결합시키면, 기존 고분자 나노입자와 유사한 수용체 매개 세포통과 전략을 적용할 수 있으며, 친수성 셀룰로오스 껍질은 혈중 단백질의 비특이적 흡착(opsonization)을 줄여 RES (망상내피계)에 의한 제거를 지연시키고, 결과적으로 순환 시간 연장과 BBB 접근 가능성을 간접적으로 향상시킬 수 있다[26,27]. 이러한 메커니즘적 관점에서 볼 때, 셀룰로오스 기반 비강 DDS는 비강–뇌 경로 및 국소 depot 제형, 표면 수화층에 의한 안정성 향상 등을 통해 뇌 노출을 최적화하는 플랫폼으로 활용될 수 있다.
종합하면, 셀룰로오스와 나노셀룰로오스는 기계적 강도, 네트워크 형성 능력, 높은 비표면적과 기능화 가능성, 그리고 생체적합성과 생분해성을 동시에 갖추고 있을 뿐만 아니라, 비강–뇌 경로 및 국소 뇌 인접 제형을 활용한 BBB 우회 설계에 강점을 지닌다. 이러한 특성은 퇴행성 뇌질환을 포함한 다양한 질환에서의 첨단 약물전달시스템 설계에 있어 셀룰로오스 기반 DDS를 기존 리포솜·고분자 나노입자를 보완하거나, 특정 투여 경로에서는 대체할 수 있는 유망한 바이오 기반 플랫폼으로 평가될 수 있다(Table 2).
Table 2.
Comparative features of major brain-targeted DDS platforms
3. 퇴행성 뇌질환에서 셀룰로오스 기반 DDS 응용 사례
퇴행성 뇌질환을 대상으로 한 셀룰로오스 기반 약물전달시스템의 응용은 아직 초기 단계이지만, 알츠하이머병, 파킨슨병, 헌팅턴병, ALS 등 다양한 질환에서 점차 그 사례가 축적되고 있다. 특히 셀룰로오스 유도체의 경구 제형, 비강 내 점막접착 나노입자, 단백질 응집을 표적하는 트레할로스 기반 시스템, 신경 조직공학용 하이드로겔 스캐폴드 등은 각 질환의 병태생리에 맞추어 특화된 전달 전략을(Fig. 1) 제시하며 그 사례를 Table 3에 나타냈다.
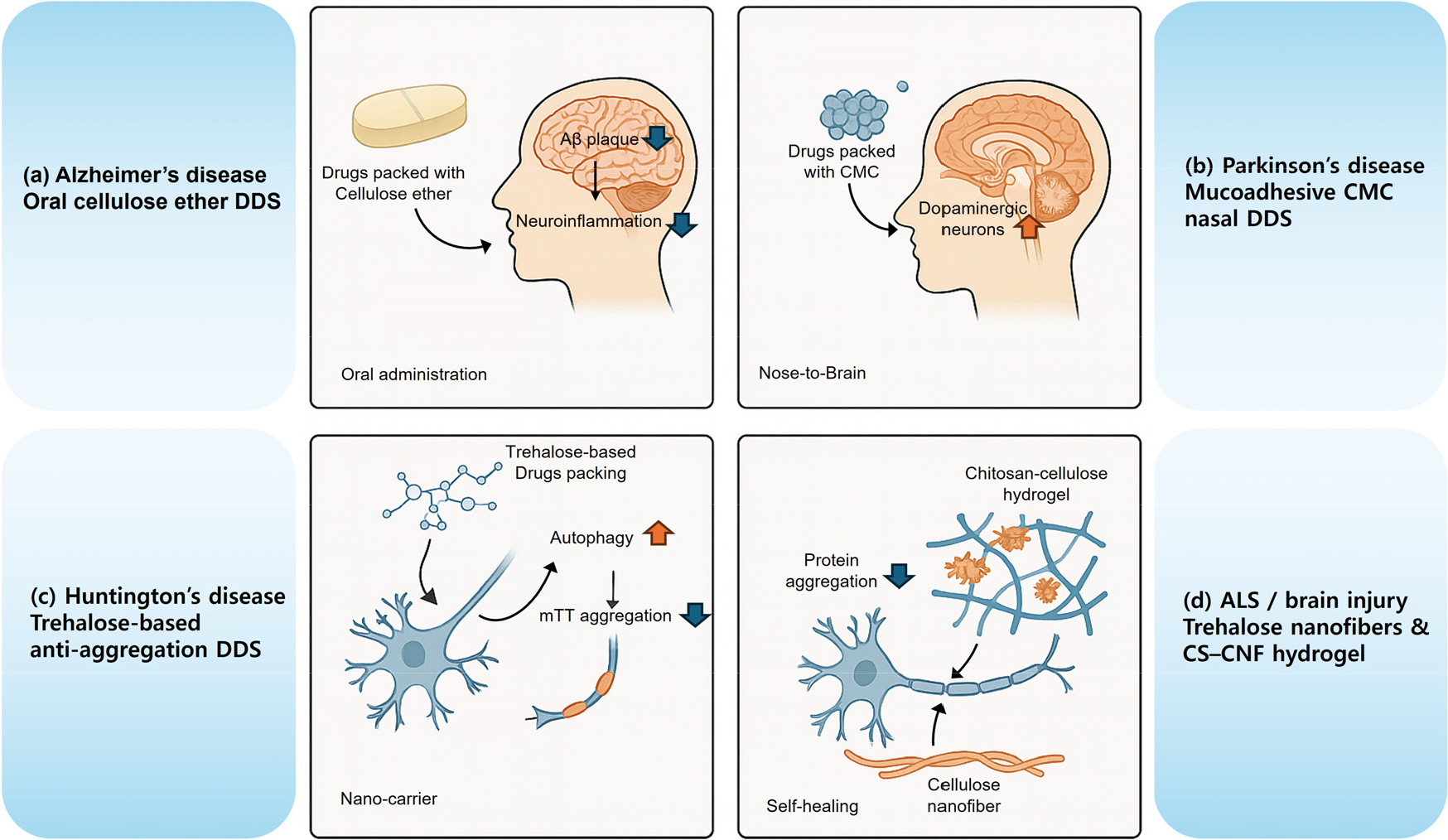
Fig. 1.
Representative applications of cellulose-based DDS according to disease and administration route. (a) Oral cellulose ether formulations modulate amyloid-β pathology and neuroinflammation in Alzheimer’s disease. (b) Mucoadhesive carboxymethyl cellulose (CMC)-based nasal nanocrystals deliver dopaminergic agents to the striatum via the nose-to-brain pathway in Parkinson’s disease. (c) Trehalose-based systems interfere with mutant huntingtin aggregation and activate autophagy in Huntington’s disease. (d) Trehalose-coated nanofibers and chitosan–cellulose nanofibril hydrogels trap pathological proteins and support neural tissue repair in ALS and brain injury models.
Table 3.
Representative cellulose-based DDS applications in neurodegenerative diseases
3.1 알츠하이머병(Alzheimer’s disease)에서의 응용
알츠하이머병(AD)은 아밀로이드 베타(amyloid-β, Aβ) 올리고머와 플라크 축적, 그에 따른 신경염증과 시냅스 소실이 핵심 병인으로 제시되는 대표적인 퇴행성 뇌질환이다[28]. 셀룰로오스 기반 DDS는 이러한 병태생리를 조절하기 위해 주로 두 가지 측면에서 접근하고 있다. 하나는 Aβ 생성·응집·제거에 직접 관여하는 치료제의 뇌 전달을 강화하는 방향이고, 다른 하나는 염증·교세포 활성 등 미세 환경을 동시에 조절하는 다중 타깃 전략이다.
카르복시메틸 셀룰로오스(CMC) 기반 나노입자는 치료제의 뇌 전달을 강화하는 전략을 구현하기 위한 대표적인 플랫폼 중 하나이다. CMC로 코팅된 자성 나노입자(Fe3O4@CMC)에 도파민을 로딩한 시스템은 알츠하이머병 관련 인지 기능 저하와 도파민성 신호 이상을 동시에 겨냥한 예로, 인간 유래 뇌미세혈관 내피세포(human lung microvascular endothelial cell, HLMVE)를 이용한 생체외 BBB 모델에서 나노입자의 흡수 및 투과가 확인되었다[29]. 이 연구를 통해 CMC로 코팅된 나노입자는 24–48시간 노출 후에도 세포 독성이 보고되지 않았으며, 음전하를 띠는 CMC의 표면 특성이 내피세포 표면 수용체 및 양전하 영역과 정전기적으로 상호작용함으로써, 수용체 매개 세포내 섭취와 전이를 촉진하는 것으로 생각되었다. 이러한 결과는 셀룰로오스 유도체가 단순한 부형제를 넘어 BBB를 통과하는 나노캐리어로 기능할 수 있음을 시사한다.
한편, 셀룰로오스 에테르(cellulose ether, CE; 예: TC-5RW)를 이용한 경구 제형은 Aβ 병리를 직접 조절하는 치료제로 다중 타깃 전략의 대표적 물질로 제안되고 있다. 5XFAD 트렌스제닉 마우스 모델에서 CE를 단회 또는 주 1회 경구 투여한 연구에서는, 공간기억 및 인지 기능의 유의한 개선과 함께 뇌 내 Aβ 올리고머 및 플라크 부담이 현저히 감소한 것으로 보고되었다[8]. 더 나아가 CE 투여는 성상세포증(astrogliosis)과 미세아교세포증(microgliosis)을 완화시키고, 신경염증 매개 인자인 glia maturation factor-β (GMFβ)의 발현을 조절함으로써, 단백질 축적과 염증 반응을 동시에 완화하는 효과를 보여준다[8]. 일부 전임상 연구에서는 단일 투여 후 뇌 내 Aβ 농도가 50–60% 정도 감소하고, 이러한 효과가 수개월 이상 지속되는 결과도 제시되며, 셀룰로오스 유도체가 약물 전달 매트릭스를 넘어 AD 병태 자체를 조절하는 활성 물질로 기능할 수 있다는 가능성을 나타낸다[8].
요약하면, AD에서 셀룰로오스 기반 DDS는 CMC 코팅 나노입자를 통한 약물의 BBB 전달 강화와, CE를 활용한 Aβ 병리 및 신경염증의 직접 조절이라는 두 축에서 응용되고 있으며, 인지 기능 개선과 병리 단백질 감소를 동시에 달성할 수 있는 잠재력을 보여주고 있다.
3.2 파킨슨병(Parkinson’s disease)에서의 응용
파킨슨병(PD)은 중뇌 흑질(substantia nigra)의 도파민성 뉴런 소실과 선조체(striatum) 도파민 결핍을 특징으로 하며, 운동 증상의 조절을 위해 도파민 작용제(agonist) 등의 반복 투여가 필수적이다. 셀룰로오스 기반 DDS는 이러한 PD 치료에서 주로 비강–뇌 경로를 활용하여, BBB를 우회하면서도 도파민계 약물을 표적 부위에 효율적으로 전달하는 전략에 집중하고 있다.
비강내 투여를 이용한 한 예로, 락토페린-PEG-PLGA 나노입자(lactoferrin-PEG-PLGA nanoparticles, Lf-NPs)에 로티고틴을 로딩한 시스템이 보고되어 있다[30]. 비록 나노입자의 핵심 매트릭스는 합성 고분자이지만, 셀룰로오스 및 다당류 기반 DDS 연구와 밀접하게 연계되는 전략으로, 비강내 투여 후 약 4시간에서 뇌 내 형광 신호가 최대에 도달하여 약 48시간에 걸쳐 로티고틴의 81.3%가 지속적으로 방출되는 제어방출 특성이 관찰되며, 나노입자는 뇌 전체로 분포하되 특히 PD 병변의 중심인 선조체 부위에 선택적으로 농축되는 특징을 보였다[30]. 이는 비강–뇌 경로와 락토페린 수용체 매개 흡수가 결합한 결과로, 향후 셀룰로오스 나노소재와의 하이브리드화 가능성을 보여주는 사례로 볼 수 있다. 실제로 CMC의 우수한 점액접착성(mucosal adhesion)은 비강 상피 표면에서의 체류 시간을 연장하고 또한 서서히 방출된다[22]. 이들은 비강내 투여를 활용한 CMC 기반 DDS가 전신 부작용은 줄이면서 삼차신경과 후각신경을 따라 뇌로의 직접 이동을 촉진하여 선조체 및 흑질에 충분한 도파민성 자극을 제공할 수 있는 비침습적 플랫폼으로 사용될 수 있는 가능성을 나타낸다. 결과적으로, PD에서 셀룰로오스 기반 DDS는 비강 점막에서의 점액접착성과 장기 체류, 비강–뇌 경로를 통한 직접 뇌 전달이라는 특성을 활용하여, 도파민 작용제의 표적 전달과 지속 방출을 달성하는 방향으로 활용되고 있으며, 침습성이 낮으면서도 고효율 뇌 표적화를 가능하게 하는 플랫폼으로서 의미 있는 가능성을 제시하고 있다.
3.3 헌팅턴병(Huntington’s disease)에서의 응용
헌팅턴병(HD)은 CAG 반복 확장에 의해 생성되는 돌연변이 헌팅틴(mutant huntingtin, mHTT) 단백질의 응집과 축적이 핵심 병인으로 여겨지는 유전성 신경변성질환이다[31,32]. 따라서 HD 치료에서는 병리 단백질의 응집을 억제하거나 이미 형성된 응집체를 제거하는 전략이 중요하며, 셀룰로오스 및 관련 다당류 기반 DDS는 이러한 단백질 응집 조절에 초점을 맞춰 개발되고 있다.
트레할로스(trehalose) 유도체인 TR-066을 활용한 시스템은 HD에서 셀룰로오스·다당류 기반 DDS의 대표적인 사례이다. 트레할로스는 자연계에 존재하는 이당류로, 단백질 구조를 안정화하고 비정상적인 응집을 억제하며, 동시에 자가포식(autophagy)을 활성화하는 특성이 알려져 있다[33,34]. TR-066 기반 DDS는 BBB를 통과해 뇌에 도달한 뒤, mHTT 응집체를 직접 제거하고 새로운 응집 형성을 억제하도록 설계되었다. 헌팅턴병 유전자 변형 마우스 모델에서 TR-066 단회 투여만으로도 운동 기능 및 행동 지표의 개선과 생존 기간의 연장이 관찰되었으며, 이는 단백질 응집체 제거 메커니즘이 실제 질환 진행을 지연시키거나 부분적으로 역전시킬 수 있음을 시사한다[34].
향후에는 트레할로스 유도체와 안티센스 올리고핵산(antisense oligonucleotide, ASO), siRNA 등의 유전자 치료제를 셀룰로오스 기반 나노캐리어에 동시 탑재하여, mHTT 발현 억제와 응집체 제거를 병행하는 복합 전략이 유망할 것으로 전망된다[35,36]. 이 경우 셀룰로오스 나노소재는 유전물질과 소분자 응집 억제제를 동시에 수행하는 다기능 매트릭스로 활용될 수 있으며, 표면 기능화를 통해 BBB 수용체 매개 통과와 특정 신경세포에 대한 표적화를 동시에 추구하는 방향으로 발전할 수 있다. 즉 HD에서 셀룰로오스 기반 DDS는 “단백질 응집질환”을 겨냥한 플랫폼으로서, 병인 단백질의 생성·응집·제거를 다층적으로 조절하는 치료 전략의 한 축을 형성할 잠재력을 지니고 있다.
3.4 ALS 및 기타 신경변성질환에서의 응용
근위축성 측삭경화증(ALS)을 포함한 기타 신경변성질환에서는, 병리 단백질의 축적과 신경염증, 산화 스트레스 등이 복합적으로 작용하여 운동 뉴런을 포함한 다양한 신경세포의 점진적 소실을 유발한다[37,38]. 이들 질환에서 셀룰로오스 및 트레할로스 기반 DDS는 주로 병리 단백질을 물리적으로 포획(trapping)하거나, 응집·독성화를 억제하는 조기 개입 플랫폼으로서 제안되고 있다. 트레할로스 코팅 나노피브릴은 이러한 전략의 한 예로, 아밀로이드 베타, 알파-시누클레인(α-synuclein) 등 다양한 병리 단백질을 표면에서 포획하여 신경세포와의 직접적인 상호작용을 차단하는 기능을 수행한다[39]. 셀룰로오스 나노피브릴 또는 기타 나노피브릴 매트릭스를 기반으로 한 이러한 시스템은, 신경세포 주변 미세환경에서 생성·분비되는 독성 응집체를 선택적으로 흡착함으로써, 세포막 손상과 미토콘드리아 기능 저하, 시냅스 독성을 완화하는 데 기여할 수 있다. 특히 ALS와 같이 질환 초기에는 임상 증상이 뚜렷하지 않지만, 병리 단백질 축적은 이미 진행되고 있는 경우, 트레할로스 코팅 나노피브릴과 같은 시스템은 증상 발현 이전 또는 초기 단계에서 병리 과정에 개입하는 예방·조기 치료 플랫폼으로 활용 가능하다. 더불어, 키토산-셀룰로오스 나노피브릴(chitosan cellulose nanofiber, CS-CNF) 복합 하이드로겔과 같은 셀룰로오스 기반 스캐폴드는 ALS 및 기타 신경변성질환에서 손상된 신경회로의 재구성을 돕는 조직공학적 보조 플랫폼으로도 적용 가능하다. CS-CNF 하이드로겔은 0.09 wt% 수준의 CNF를 포함하는 조성에서 신경줄기세포의 생존과 분화를 효과적으로 지지하며, 알데하이드 또는 케톤이 반응해 생성되는 결합인 Schiff base 결합을 통한 자가치유(self-healing) 네트워크가 뇌 조직의 미세변형 환경에 유연하게 적응할 수 있는 특성을 제공한다[40]. 얼룩말 뇌손상 모델에서 관찰된 신경 재생 향상 효과는, 이러한 스캐폴드가 약물 전달과 조직 재생을 동시에 수행할 수 있는 복합 플랫폼으로 확장될 수 있음을 보여준다[40].
이와 같이 ALS 및 기타 신경변성질환에서 셀룰로오스 기반 DDS는 병리 단백질 포획 및 응집 억제, 산화 스트레스 완화, 신경 조직 재생 지지 등 다양한 메커니즘을 통해 질환 진행을 지연시키고 신경 보호 효과를 제공할 수 있는 잠재력을 지니고 있으며, 질환 초기 개입 및 재생 치료가 강조되는 미래 치료 전략에서 중요한 도구로 자리잡을 가능성이 크다.
4. 셀룰로오스의 위치와 한계
퇴행성 뇌질환 치료를 위한 DDS 분야에서 셀룰로오스 기반 시스템은 현재 주류 기술이라기보다는 보조적이고 대체적인 플랫폼으로 자리하고 있다. 임상 및 상용화 측면에서 뇌 표적화 DDS의 중심을 이루는 기술은 여전히 리포솜, 리포솜 유래 나노입자, 합성 고분자 나노입자, 무기 나노입자, 세포 유래 외소포체등이며, 이들 플랫폼은 수십 년에 걸친 전임상·임상 데이터와 규제 선례를 축적해 왔다. 반면 셀룰로오스 기반 DDS는 전임상 및 일부 초기 임상 단계 연구가 진행되고 있는 수준으로, 뇌 표적화 전달에서 ‘선발 플랫폼’으로 인정받고 있지는 못하다. 그럼에도 셀룰로오스는 높은 생체적합성과 낮은 독성, 바이오매스 기반의 지속가능성, 그리고 표면 개질의 용이성과 같은 장점 덕분에 기존 플랫폼을 보완하는 재료로서 의미 있는 위치를 점하고 있다. 특히 비강내 투여나 국소 뇌 내 주입과 같이 BBB를 부분적으로 우회할 수 있는 투여 경로에서는, 셀룰로오스 기반 시스템이 리포솜 등과 유사한 수준의 효능을 보이거나 점액접착성, 기계적 안정성 측면에서 경쟁력을 갖는 사례도 보고되고 있다[24].
그러나 셀룰로오스 기반 DDS가 퇴행성 뇌질환 영역에서 주류 기술로 도약하기 위해서는 해결해야 할 구조적·기술적 한계가 여전히 남아있다. 가장 근본적인 한계는 BBB 통과 능력이다. BBB는 소분자 치료제의 대부분과 대분자 제제를 차단하는 강력한 물리·기능적 장벽으로, 지질 이중층 구조를 갖는 리포솜은 세포막과의 유사성 덕분에 비교적 높은 투과 효율을 보이는 반면, 셀룰로오스 기반 나노입자는 기본적으로 친수성 고분자이기 때문에 수동 확산에 의존하기 어렵고, BBB를 자발적으로 통과하기 위한 물리화학적 프로파일이 상대적으로 불리하다[29,41]. 양이온성 리포솜은 정상 BBB에서도 일정 수준의 축적을 보이고, BBB가 손상된 상태에서는 뇌 내 농도가 수 배 이상 증가하는 것으로 알려져 있지만, 셀룰로오스 나노입자는 그러한 수준의 수동·능동 투과를 일관되게 보여주지 못하고 있다[29,42,43]. 수용체 매개 통과(receptor-mediated transcytosis, RMT)를 활용하기 위한 표면 리간드 도입 역시 이론적으로는 가능하나, 리포솜·고분자 나노입자에 비해 리간드 배향, 결합 안정성, 표적 효율에 대한 축적된 데이터가 부족하여, 아직은 연구 단계에서의 가능성에 머무르고 있다.
약물 로딩 및 용해도 측면에서도 구조적 제약이 존재한다. 셀룰로오스와 그 유도체(CMC, HPMC 등)는 친수성이 매우 높은 고분자로, 도파민 유사체, 스테로이드, 지질친화성 항산화제와 같이 소수성 특성이 강한 신경계 약물을 고용량으로 탑재하기가 쉽지 않다. 리포솜의 경우 지질 이중층과 수상 내부를 동시에 활용하여 소수성·친수성 약물을 모두 수용할 수 있으며, 소수성 약물에 대해 80–90% 수준의 캡슐화 효율(encapsulation efficiency)과 10–20 wt% 이상의 약물 함량을 달성한 보고도 다수 존재한다[44,45]. 반면, 표면 개질을 적용하지 않은 셀룰로오스 또는 나노셀룰로오스 기반 캐리어는 일반적으로 소수성 약물 로딩이 1–5 wt% 이하에 머무는 경우가 많고, 계면활성제 또는 소수성 작용기를 도입해도 리포솜 수준의 고함량 로딩까지 도달하기는 쉽지 않다[46,47]. 예를 들어, 수산기 일부를 양이온성 계면활성제로 개질한 CNC 시스템에서 소수성 약물의 로딩은 약 38 mg g-1 (약 3.8 wt%) 수준으로 보고되어, 고부하 리포좀 제형에 비해 여전히 낮은 편이다. CMC의 경우, 고염분·산성 환경에서 용해도가 감소하고, 뇌척수액(cerebrospinal fluid, CSF)의 이온 강도와 pH 조건에서도 응집이 유발될 수 있어, 비강내 또는 뇌실 내 투여 시 제형의 장기 안정성과 약물 가용성을 동시에 만족시키기 어렵다는 문제가 있다[46,47]. 더불어 산업 등급 CMC는 치환도(degree of substitution, DS) 편차와 낮은 순도로 인해 의약 용도로 직접 사용하기 어려우며, 의약 등급 CMC는 비용이 높고 배치(batch) 간 품질을 엄격히 관리해야 하므로, 대규모 생산과 규제 승인 과정에서 부담 요인이 된다.
입자 크기와 형상, 콜로이드 안정성 역시 중요한 제약 요소이다. BBB 통과를 위한 최적 나노입자 크기는 여러 리뷰에서 대략 10–100 nm 범위가 가장 유리한 것으로 제시되고 있으며, 특히 50–100 nm 구간에서 내피세포 부착과 조직 내 확산 사이의 균형이 가장 잘 맞는 것으로 보고된다[48]. 구형에 가까운 리포솜·고분자 나노입자는 이 범위로 입자 크기를 비교적 정밀하게 조절할 수 있는 반면, 셀룰로오스 CNC는 막대형 입자, CNF는 직경 수 나노미터에서 수십 나노미터, 길이는 수 마이크로미터에 이르는 장섬유 구조를 가지므로, 동일한 수의 크기에서라도 실제 혈류역학적 거동과 BBB 투과 양상이 크게 달라질 수 있다. 특히 CNF와 같이 긴 섬유 구조는 구형 입자에 비해 체내 분포와 조직 축적을 정량적으로 예측하기 어렵고, 사구체 여과(glomerular filtration)의 효과적인 직경 컷오프(수 nm 수준)와 비교할 때, 여과보다는 간·비장 등에서 대사되거나 장기에 축적될 가능성이 존재한다[49,50]. 또한 셀룰로오스 나노입자는 표면 전하 감소나 이온 강도 변화에 민감하여 수용액에서 응집·침전되기 쉬우며, PEG 코팅을 적용해도 장기간 저장 또는 생리적 이온 강도 조건에서 완전한 콜로이드 안정성을 확보하기는 쉽지 않다는 보고가 많다[51]. 이와 같은 물리적 불안정성은 제형의 재현성과 스케일업 시 품질 일관성을 저하시킬 뿐 아니라, in vivo 투여 후 분포·제거 거동의 예측 가능성도 떨어뜨리는 요인이 된다.
BBB 자체가 갖는 효소 장벽 역시 셀룰로오스 DDS에 불리하게 작용할 수 있다. BBB를 구성하는 내피세포와 주변 미세환경은 다양한 가수분해 효소와 단백질분해효소를 풍부하게 포함하고 있으며, 셀룰로오스의 β-글루코시드 결합은 특정 글루코시드 분해효소에 의해 부분적으로 분해될 수 있다[52,53]. 특히 당화(glycation)나 기타 화학 수식이 도입된 셀룰로오스 유도체는, CSF 내 효소 및 활성산소 환경에 노출되었을 때 캐리어의 예기치 않은 가수분해, 약물의 조기 방출, 또는 네트워크 구조를 붕괴할 가능성이 있다[54,55]. 반면 인지질 이중층 구조를 갖는 리포솜은 동일 조건에서 상대적으로 높은 구조적 안정성을 유지하며 내부 약물을 보호할 수 있는 것으로 보고되며, 효소 장벽 측면에서 보다 유리한 플랫폼으로 평가된다[45]. BBB 내피세포의 주요 약물 배출 시스템인 P-글라이코프로틴(P-glycoprotein, P-gp)은 중추신경계 약물을 세포 외로 역수송하여 뇌 내 약물농도를 감소시키는데, 셀룰로오스 기반 DDS가 수용체 매개 경로를 충분히 활용하지 못할 경우, 캐리어와 약물이 모두 P-gp의 영향을 받아 효율적인 뇌 축적을 달성하기 어렵다[56,57]. 리포솜 및 고분자 나노입자에서는 비타민 E 유도체인 TPGS (d-α-Tocopheryl polyethylene glycol 1000 succinate) 등의 P-gp 억제제를 통합하여 경구 흡수 또는 BBB 투과를 2–3배 이상 증가시킨 사례가 다수 보고되고 있으나, 셀룰로오스 플랫폼에서 이러한 P-gp 억제 전략을 체계적으로 구현한 예는 아직 제한적이며, 이는 향후 설계 측면에서 개선해야 할 중요한 과제로 남아 있다.
대량 생산·표준화와 멸균·저장 과정에서도 해결해야할 부분이 있다. 나노셀룰로오스의 구조와 표면 특성은 산 가수분해, 효소 처리, 기계적 분쇄 조건 및 원료 목질 소재와 전처리에 따라 크게 달라져 산업 규모에서 일관성을 확보하기 어렵고, 고압 균질화·초음파·효소 공정은 에너지 집약적이어서 스케일업에 대한 경제성을 고려해야 한다. 자외선·감마선·에틸렌옥사이드 멸균은 나노구조를 손상시킬 수 있으며, 동결건조 후 재수화 과정에서의 불가역적 응집도 제형 안정성과 유통·보관·사용 편의성을 제한하는 요소이다. 더불어 셀룰로오스 기반 DDS는 퇴행성 뇌질환을 대상으로 한 임상 1–3상 시험이 거의 보고되지 않았고, 대부분 동물 모델 수준의 전임상 연구에 머물러 있어 장기 in vivo 데이터와 임상 근거가 매우 부족하다. 체내 흡수·분포·대사·배설(absorption, distribution, metabolism, and excretion, ADME), 반복 투여 시 면역 반응 및 장기 축적 가능성에 대한 정량적 정보가 충분치 않아 임상 용량 설정과 투여 간격 최적화, 장기 안전성 예측에 어려움이 따르며, 다양한 적응증에서 임상 경험이 축적된 리포솜·고분자 나노입자와 비교할 때 상당한 격차가 여전히 존재한다.
이러한 점들을 종합하면, 현 시점에서 셀룰로오스 기반 DDS는 퇴행성 뇌질환 치료에서 리포솜과 고분자 나노입자를 대체하는 “주류 플랫폼”이라기보다는, 특정 투여 경로와 응용 분야에서 장점을 발휘하는 보완적·지속가능한 플랫폼으로 위치하고 있다고 볼 수 있다. 특히 비강 내 투여, 국소 뇌손상 부위 재생, 신경 조직공학 스캐폴드와 같이 셀룰로오스의 기계적 안정성과 생체적합성, 친환경성이 직접적인 장점으로 작용하는 영역에서 그 활용 가능성이 크다. 향후 표면 기능화 기술의 고도화, 다층 복합 구조 설계(예: 리포솜 코팅 셀룰로오스, 하이브리드 키메라 입자), 보다 균일한 구형 나노입자 제조 기술, 그리고 나노셀룰로오스에 대한 규제 프레임의 명확화가 이루어진다면, 셀룰로오스 기반 DDS는 퇴행성 뇌질환 치료에서 보다 중심적인 역할을 수행할 잠재력을 지니고 있다.
5. 셀룰로오스 DDS의 전망
셀룰로오스 기반 DDS은 현재 퇴행성 뇌질환 치료에서 리포솜이나 고분자 나노입자와 같은 주류 플랫폼을 대체하기보다는, 이들을 보완하는 지속가능한 고생체적합 소재로서의 가능성에 주목받고 있다. 재생 가능한 바이오매스에서 유래한 셀룰로오스는 높은 생체적합성과 낮은 독성, 풍부한 하이드록실기를 이용한 표면 개질의 용이성, 다양한 물리적 형상(나노입자, 하이드로겔, 필름, 에어로겔, 3차원 스캐폴드)으로의 가공 가능성 등 기존 플랫폼이 가지기 어려운 장점을 지닌다. 향후 셀룰로오스 합성에 대한 문제점을 보완한다면 BBB 통과 효율, 소수성 약물 로딩, 효소 안정성 등 현재 셀룰로오스 DDS의 구조적 한계가 극복될 것으로 생각된다. 4절에서 한계로 지적하였듯이, 셀룰로오스 기반 DDS의 중요한 과제 중 하나는 친수성 골격으로 인해 소수성 약물 로딩이 제한적이라는 점이다. 이에 대해 최근에는 셀룰로오스 표면을 부분적으로 소수화하여 양친매성(amphiphilic) 구조를 부여함으로써, 소수성 약물의 용해도와 적재 효율을 동시에 향상시키려는 시도가 활발히 이루어지고 있다. 예를 들어, 지방산, 방향족 아실기, 알킬 사슬 등을 에스터화 또는 우레탄 결합 형태로 도입하여 셀룰로오스 사슬 일부를 소수성 블록으로 전환하면, 수용액에서 스스로 나노입자·미셀을 형성하면서 소수성 약물을 내부에 포획하는 구조를 형성할 수 있다[58,59]. 또 다른 접근으로는 폴리락트산(polylactic acid, PLA), 폴리카프로락톤(polycaprolactone, PCL)과 같은 생분해성 소수성 고분자를 셀룰로오스에 그래프트(graft)하여 블록 공중합체 유사 구조를 만들고, 이를 이용해 자가조립 나노입자 또는 코어–셸(core–shell) 구조를 형성함으로써 약물 적재량과 안정성을 동시에 높이는 전략이 보고되고 있다[60,61]. 더불어, 친수성 셀룰로오스 골격에 소수성 치환기와 함께 시클로덱스트린(cyclodextrin) 모티프를 도입하여, 포접복합체 형성 능력과 나노셀룰로오스의 네트워크 형성을 결합한 하이브리드 시스템도 연구되고 있다[62,63]. 이러한 표면 개질 및 하이브리드 설계는 셀룰로오스의 본래 생체적합성과 생분해성을 유지하면서도, 기존 리포솜·고분자 나노입자 수준에 근접하는 소수성 약물 로딩 능력을 확보하려는 방향으로 발전하고 있으며, 향후 퇴행성 뇌질환에서 사용되는 지질친화성 항산화제, 스테로이드, 도파민계 약물 등에 대한 적용성이 클 것으로 기대된다.
또한 셀룰로오스 DDS의 공정 기술과 규제·표준화 측면이 개선된다면, 장기적으로는 알츠하이머병, 파킨슨병, 헌팅턴병, ALS와 같이 장기간 반복 투여와 삶의 질 관리가 중요한 질환에서 셀룰로오스 기반 DDS가 저독성·장기 지속 방출·비침습적 투여 경로(비강, 피하, 국소) 등에 최적화된 지속가능한 고기능 플랫폼으로 자리잡을 수 있을 것으로 생각되며, 환경·윤리적 측면까지 고려한 차세대 뇌질환 치료 기술로서 전략적 가치를 가질 것으로 기대된다.
6. 결론 및 제안
본 논문에서는 셀룰로오스 및 나노셀룰로오스 기반 DDS를 중심으로, 퇴행성 뇌질환 치료에서의 응용 가능성과 한계를 질환별 사례와 플랫폼 특성의 관점에서 고찰하였다. 셀룰로오스는 재생 가능한 바이오매스에서 유래하는 고생체적합 소재로서, 높은 기계적 강도와 생분해성, 풍부한 표면 하이드록실기를 통한 기능화 용이성을 동시에 갖추고 있다. 이러한 특성은 나노입자, 하이드로겔, 필름, 에어로겔, 3차원 스캐폴드 등 다양한 형태의 DDS 매트릭스를 구현할 수 있게 하며, 특히 비강–뇌 투여 경로, 국소 주입, 조직공학 기반 재생 치료와 결합될 때 기존 리포솜·고분자 나노입자 시스템이 제공하기 어려운 독자적인 장점을 부여한다. 알츠하이머병, 파킨슨병, 헌팅턴병, ALS를 대상으로 한 전임상 연구들에서 셀룰로오스 유도체는 아밀로이드 베타 축적 감소, 도파민 신호 회복, 병리 단백질 응집 억제, 신경세포 생존 및 조직 재생 촉진 등 다양한 수준에서 유의한 치료 효과를 보여 왔으며, 이는 셀룰로오스 기반 DDS가 단순한 약물 운반체를 넘어 병태생리 조절과 미세환경 재구성을 동시에 겨냥할 수 있는 플랫폼으로 기능할 수 있음을 시사한다.
그러나 셀룰로오스 기반 DDS는 퇴행성 뇌질환 치료에서 아직 리포솜·고분자 나노입자와 같은 선발 플랫폼을 대체할 수 있는 단계에는 이르지 못하였으며, BBB 통과에 최적화된 입자 크기와 형상 제어, 친수성으로 인한 소수성 약물 로딩 한계, 콜로이드 및 저장 안정성, 제조 공정의 표준화와 규제 수용성 등은 여전히 개선 여지가 큰 영역이다. 이러한 부분들은 한계이자 동시에 기술 발전의 명확한 목표로 볼 수 있으며, 본 논문에서 논의한 표면 기능화 화학의 정교화, 리포솜·고분자 나노입자·세포 유래 베지클과의 하이브리드 설계, 신경 조직공학 스캐폴드와의 통합, 공정 및 품질 관리의 표준화 전략은 각각 이러한 난제를 직접적으로 겨냥하고 있다. 예를 들어, 양친매성 셀룰로오스 유도체 설계와 소수성 블록/시클로덱스트린 모티프 도입은 소수성 약물 로딩 부족 문제를 보완하는 것을 목표로 하며, 하이브리드·다층 구조는 셀룰로오스의 기계적·재생적 장점과 기존 플랫폼의 BBB 표적성·고함량 로딩 능력을 결합하여 구조적 제약을 상호 보완할 수 있는 가능성을 제시한다. 또한, 신경 조직공학 스캐폴드와의 통합은 기존 DDS가 충분히 다루지 못했던 구조적 뇌손상과 회로 수준의 결손을 대상으로, 약물전달과 조직 재생을 동시에 해결하고자 하는 전략이며, 공정·규제 표준화는 배치 간 변동성과 규제 불확실성을 줄여 실제 임상 적용으로 이어지기 위한 필수 기반을 제공한다.
향후 연구에서는 이러한 전략들을 구체화하기 위해, 개별 사례 연구를 넘어 구조–활성 상관관계에 기반한 설계 원리를 확립하고, 질환별·투여 경로별 최적화 전략을 정량적으로 도출하는 전임상 연구가 필요하다. 특히 리포솜·고분자 나노입자와의 head-to-head 비교를 통해 BBB 투과 효율, 뇌/혈장 농도비, 약동학·약력학(PK/PD) 지표를 체계적으로 비교하는 실험적 데이터, 반복 투여 및 장기 노출에서의 안전성·축적 가능성을 평가하는 in vivo 연구, 그리고 사람을 대상으로 한 초기 임상 시험을 통해 셀룰로오스 기반 DDS의 실제 임상적 유용성을 검증하는 작업이 중요하다. 이러한 실험적·임상적 공백을 긍정적으로 채워 나간다면, 셀룰로오스 및 나노셀룰로오스 기반 DDS는 퇴행성 뇌질환에서 약물 전달과 조직 재생을 동시에 추구하는 지속가능한 고기능 플랫폼으로 도약할 수 있을 것이며, 궁극적으로 뇌질환 치료 패러다임 전환에 실질적으로 기여할 수 있는 잠재력이 크다고 판단된다.




