1. 서 론
리그노셀룰로오스 바이오매스는 자연에서 얻을 수 있는 가장 풍부한 자원의 일종으로 가수분해 공정을 거쳐 환원당을 생산하는 원료로 이용이 가능하다.1) 이렇게 얻어진 당은 연료, 소재, 화학 물질을 생산하는 주요 원료로서 유용한 화학기반물질로 활용된다.2) 가수분해 방법은 셀룰로오스 섬유를 분해하기 위한 공급원에 따라 산 가수분해와 효소 가수분해로 분류된다.3) 효소 가수분해는 공정 조건이 보다 온화하고 환경 친화적이며 높은 당 수율 등의 장점을 가지고 있다. 그러나 효소 가수분해 공정에서는 리그노셀룰로오스 바이오매스가 본래 가지고 있는 고유의 저항성 때문에 효소 당화가 저해된다.4)
효소 당화 공정의 합리적인 생산성을 위하여 당화에 앞서 전처리 공정이 요구된다. 전처리 공정은 방법에 따라 물리적, 화학적, 생물학적 방법으로 구분된다. 다양한 전처리 방법에 의해 바이오매스의 구조적, 화학적 변화가 발생하고 그 결과 효소의 접근성 및 활성이 높아짐에 따라 당화 효율성이 향상된다.5) 이러한 이유로 리그노셀룰로오스 바이오매스의 효율적인 효소 당화를 위해서는 전처리 공정이 필수적이지만, 전처리를 위한 적지 않은 에너지, 화학물질, 수자원 사용은 생산단계에서 자본과 비용의 많은 부분을 차지한다.6)
전처리 방법에 대한 연구와 함께 효소 당화 공정의 효율 향상을 위한 연구 또한 꾸준히 진행되었다. 그 중에서도 효소 당화의 상당한 비용을 차지하는 효소의 사용량을 줄이기 위하여 효소의 개발과 활성 증대와 같은 연구가 활발히 진행되었다.7)
효소의 활성을 증가시키기 위한 방법의 일종으로 계면활성제의 활용이 연구되었다.8) 계면활성제는 일반적으로 친수성인 머리부분과 소수성인 꼬리부분으로 구성된 양친매성 유기화합물이다. 계면활성제는 친수성인 머리부분의 이온적 특성에 따라 음이온성, 양이온성, 비이온성 및 양성 이온성(또는 양쪽성)의 네 가지로 분류된다. 계면활성제는 자체가 가지고 있는 양친매성 때문에 소수성과 친수성 물질 사이의 표면 장력을 낮추어 잘 섞이게 하는 역할을 한다. 세제, 분산제, 유화제, 습윤제 등이 계면활성제의 성질을 이용한 물질에 속한다.9)
계면활성제는 화학 공정을 이용하여 합성된 합성 계면활성제와 미생물 등을 통해 생합성된 바이오 계면활성제로 나뉜다.10) 합성 계면활성제 중에서도 생분해성, 재생 가능성, 생체 적합성 등의 기능을 갖추기 위하여 천연물질을 원료로 사용하고 친환경적 공정으로 생산한 친환경 계면활성제는 석유계 합성 계면활성제와 구분된다.11)
환경문제에 대한 인식이 중요해지면서 석유계 합성 계면활성제와 관련하여 원료 및 생산공정의 유독성 및 생산된 계면활성제의 환경 저항성 등과 관련된 환경 문제가 지난 수십 년 동안 제기되어 왔다. 최근에는 석유계 합성 계면활성제의 사용을 억제하기 위하여 바이오 계면활성제 혹은 친환경 계면활성제에 대한 개발과 적용에 대한 연구가 활발히 진행되고 있다.11,12) 마찬가지로 효소 당화 효율 증대를 위한 계면활성제 사용 연구는 주로 석유계 합성 계면활성제에 관한 것이었지만 지금은 바이오 계면활성제의 활용 가능성이 많이 연구되고 있다.13,14)
본 연구에서 효소 당화 효율 증대를 위해 사용될 po-tassium cocoyl glycinate(PCG)는 코코넛 오일과 아미노산을 합성하여 만들어지는 친환경 계면활성제의 일종이다. PCG는 화학적 합성에 의해 만들 수 있어 바이오 계면활성제보다 생산비용이 적고 생분해성, 생체 적합성 등의 친환경성 또한 가지고 있어 석유계 합성 계면활성제 또는 바이오 계면활성제를 대체하여 효소 당화 공정에 활용이 용이할 것으로 사료된다.15-17) 하지만 석유계 합성 계면활성제와 바이오 계면활성제에 비하여 효소 당화를 위한 PCG의 활용 연구에 대한 정보가 거의 없다. 따라서 본 연구에서는 PCG를 첨가한 효소 당화 실험을 통해 PCG와 당화 수율 향상 관계를 확인하고 PCG의 석유계 합성 계면활성제 대체가능성을 확인하고자 한다.
2. 재료 및 방법
2.1 공시 재료
활엽수 대표 수종의 하나인 백합나무(Liriodendron tulipifera L.)를 사용하였다. 시료를 직경 1.0 mm의 공극을 통과하도록 분쇄하고 공기 중에 건조 후 사용하였다.
2.2 분석방법
공시 재료의 화학적 조성 분석을 위하여 아세톤 추출물 함량 측정(TAPPI 204 om-88), 끓는 물 추출물 함량 측정(TAPPI 207 om-93), 산 불용성 및 가용성 리그닌 분석(TAPPI 222 om-88 and TAPPI Useful Method UM 250) 방법을 사용하여 분석하였다.18)
공시 재료의 탄수화물 조성을 비교하기 위해 1H-NMR 분석을 실시하였다. 시료에 72% 황산을 이용하여 30°C에서 한 시간 동안 1차 가수분해 후, 중수(D2O)를 넣어 희석한 후 100°C에서 한 시간 동안 2차 가수분해를 실시하였다. 가수분해 후 rhamnose를 표준 물질로 첨가하였고, 여과 과정을 거쳐 여과액을 모아 Bruker사의 AVANCE NMR spectrometer(500 MHz) 기기를 이용하여 분석하였다. NMR 스펙트럼 상의 아노머성 수소 피크를 적분하여 탄수화물 조성을 분석하였다.7)
효소 당화 공정 중 당 생산량을 측정하기 위해서 High Performance Liquid Chromatography(HPLC, Shi-madzu, Japan)를 이용하여 분석하였다. 컬럼으로는 Aminex-HPX-87H(300 mm×7.8 mm, Bio-Rad), 검출기는 굴절률검출기(refractive index detector, RID-10A, Shinmadzu, Japan)를 사용하였다. 이동상으로는 5.0 mM 황산을 사용하였으며 이동속도 0.6 mL/min으로 고정하였다. 컬럼의 온도는 60°C로 유지하였다.
2.3 전처리
삼각 플라스크 안에 백합나무 목분과 NaOH 용액을 1:10의 비율로 넣고 멸균기를 이용하여 121°C에서 60분간 반응시켰다. NaOH 용액은 0.1%, 1.0%, 10.0%의 세 가지 다른 농도로 하여 전처리에 사용되었다. 반응 종료 후 온도가 80°C 이하로 내려가면 필터를 이용하여 고형분을 물로 충분히 세척하여 중화시킨다. 세척 후 기건시키고 효소 당화 전 시료의 전건 무게를 계산하기 위하여 수분 함량을 측정하였다.
2.4 효소 당화
전처리된 목분 10.0 g(전건무게)을 0.05 M의 아세테이트 완충액(sodium acetate buffer)과 1:20의 비율로 섞고 PCG 양을 0%, 0.003%, 0.03%, 0.15%, 0.3%(v/v of buffer)로 달리하여 효소 당화를 실시하였다. 효소 당화를 위해 사용된 효소는 CTect2(Novozyme)로 시료 전건무게 1.0 g 당 15.0 FPU를 사용하였다. 반응시간 2, 4, 6, 24, 48, 72시간이 되는 시점에 당화 수율 분석을 위한 샘플을 채취하고 HPLC를 이용하여 글루코오스와 자일로오스 함량을 측정하였다. 글루코오스와 자일로오스 농도를 합하여 생산된 당의 총 함량으로 결과에 표시하였다.
3. 결과 및 고찰
백합나무의 구성성분을 분석한 결과를 Fig. 1에 나타내었다. 글루코오스, 자일로오스 그리고 리그닌이 주요 구성성분으로 나타났고 각각 47.7%, 16.2%, 23.1%의 함량을 보였다. 그 외에도 갈락토오스(3.0%)와 만노오스(3.2%) 같은 미량의 당이 포함되어 있었다. 추출물의 경우 아세톤 추출물은 전체 시료의 1.0%를 그리고 열수 추출물은 5.9%로 분석되었다.
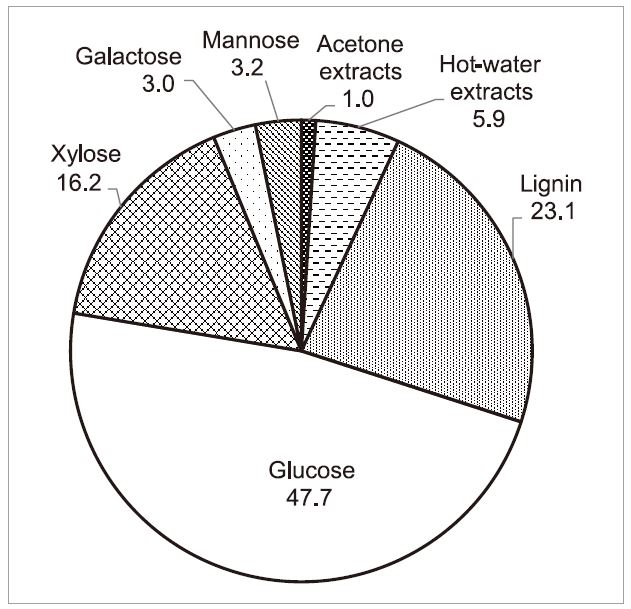
Fig. 1.
Chemical compositions of yellow poplar as a percentage of raw material.
백합나무의 당화 수율에 영향을 미치는 전처리 효과를 확인한 결과를 Fig. 2에 나타내었다. 세 가지 다른 농도(0.1%, 1.0%, 10.0%)의 NaOH 용액을 이용한 전처리 후 당화를 거쳐 생산된 최대 총 당량은 각각 2.3(±0.2), 20.1(±0.5), 20.8(±0.1) g/L으로 확인되었다. 효소 당화에 대한 전처리의 효과가 가장 긍정적인 결과는 10.0%의 NaOH 용액을 쓴 경우에서 나타났으나 1.0% NaOH 용액을 이용한 전처리 시료를 당화한 결과와 큰 차이가 없는 것으로 확인되었다. 따라서 결과를 바탕으로 효소 당화에 PCG를 사용하지 않은 경우에는 전처리에 필요한 NaOH 용액의 농도는 1.0%로도 충분한 것으로 사료된다.
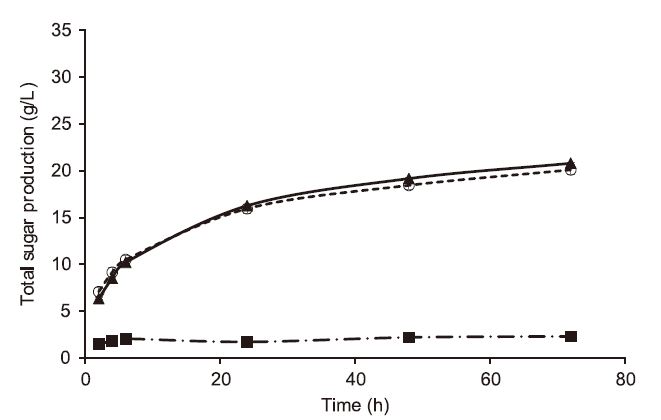
Fig. 2.
Total sugar production from yellow poplar pretreated under the different concentration of NaOH solution of 10.0% (▲, solid), 1.0% (○, square dot) and 0.01% (■, long dash dot).
NaOH 용액(10.0%)으로 전처리된 백합나무의 당화 공정에 PCG를 첨가하여 당화 수율 변화를 관찰하였다. 최대 당 생산량은 0.003%, 0.03%, 0.15%, 0.3%의 PCG가 첨가된 가수분해에서 72시간 후에 각각 27.7(±2.1), 31.8(±0.5), 30.7(±0.2), 28.5(±0.2) g/L로 나타났다(Fig. 3). PCG를 0.03% 첨가한 경우에 당 생산량이 가장 높았는데 PCG를 사용하지 않은 경우(20.8 g/L)보다 최대 11 g/L만큼 증가하였다.
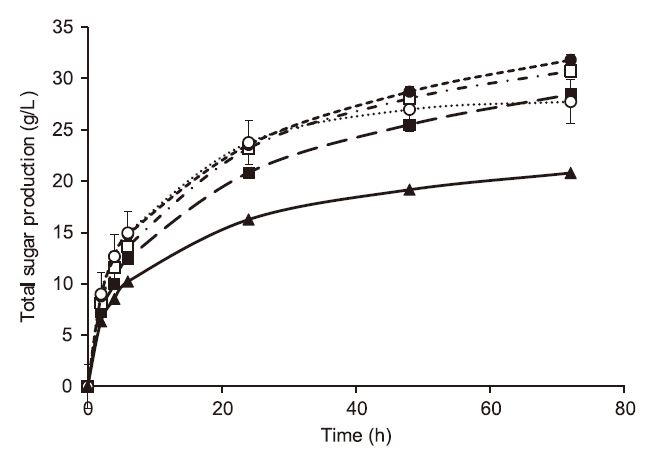
Fig. 3.
Effects of diverse concentration of PCG on the total sugar production of yellow poplar pretreated by 10.0% NaOH. Control (▲, solid), PCG 0.003% (○, round dot), PCG 0.03% (●, square dot), PCG 0.15% (□, dash dot), PCG 0.3% (■, dash long line).
NaOH 용액 1.0%로 전처리한 백합나무에 위와 동일한 농도의 PCG를 첨가하여 효소 당화를 실시한 후의 결과를 Fig. 4에 표시하였다. 최대 당 생산량은 각각 0.003%, 0.03%, 0.15%, 0.3%의 PCG 농도에서 19.2(±1.4), 25.7(±0.8), 25.3(±0.4), 22.8(±0.2) g/L로 나타났다. 10.0% NaOH 용액으로 전처리된 시료의 가수분해 실험 결과와 마찬가지로 PCG의 농도가 0.03%일 때 가장 높은 당 생산량을 보였고 그 다음으로 0.15%의 PCG 첨가 실험군이 그 뒤를 따르는 공통점을 보였다. 1.0% NaOH 전처리 시료의 경우 대조군(20.1 g/L)과 비교하였을 때 대략 5.6 g/L의 최대 당 생산량이 증가하는 것으로 확인되었다.
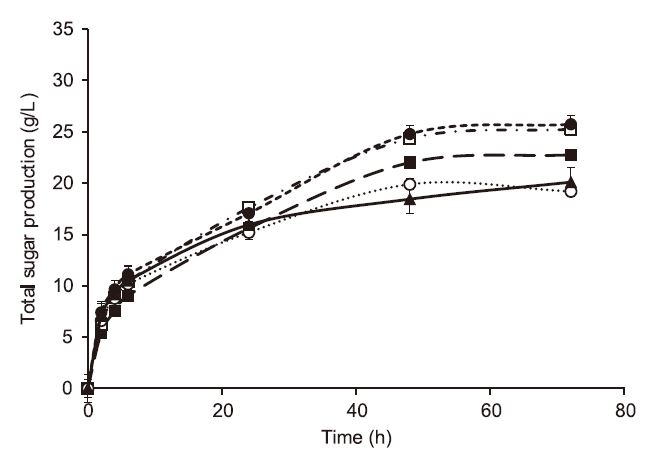
Fig. 4.
Effects of diverse concentration of PCG on the total sugar production of yellow poplar pretreated by 1.0% NaOH. Control (▲, solid), PCG 0.003% (○, round dot), PCG 0.03% (●, square dot), PCG 0.15% (□, dash dot), PCG 0.3% (■, dash long line).
공시재료를 0.1% NaOH 용액으로 전처리한 후 효소 당화를 실시한 결과를 Fig. 5에 나타내었다. 최대 당 생산량은 각각 0.003%, 0.03%, 0.15, 0.3%의 PCG 농도에서 3.4(±0.3), 7.7(±0.1), 7.4(±0.1), 3.8(±0.1) g/L로 나타났다. 위에서 언급된 1.0%와 10.0%의 NaOH 농도에서 전처리된 시료와 비교하여 0.1% NaOH 용액으로 전처리된 시료는 당의 총 생산량이 상당히 적었다. PCG를 첨가한 경우에도 0.1% NaOH 전처리된 시료의 총 당 생산량은 다른 두 전처리 조건의 실험에 비하여 낮게 나타났다. 따라서, 동일한 전처리 조건(121°C, 1 h)에서 0.1%의 NaOH 용액은 전처리 효과를 얻기에는 농도가 현저히 낮다고 판단된다. 0.1% NaOH 전처리 시료의 최대 당 생산량은 1.0%와 10.0% NaOH 전처리 시료와 마찬가지로 0.03%와 0.15%에서 가장 높게 나타났다.
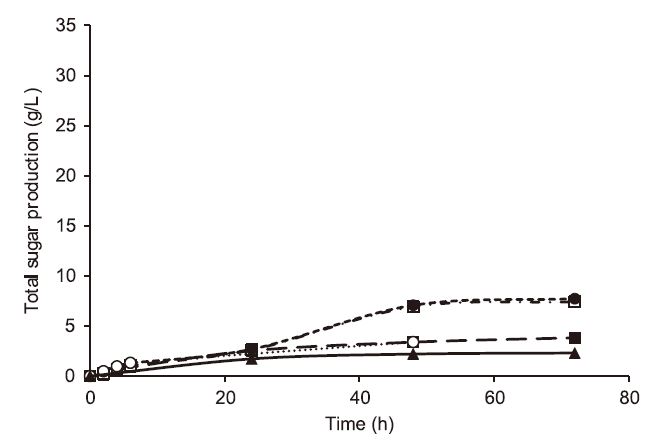
Fig. 5.
Effects of diverse concentration of PCG on the total sugar production of yellow poplar pretreated by 0.1% NaOH. Control (▲, solid), PCG 0.003% (○, round dot), PCG 0.03% (●, square dot), PCG 0.15% (□, dash dot), PCG 0.3% (■, dash long line).
실험 결과를 종합해볼 때 효소 가수분해에 대한 PCG의 효과가 상당히 흥미로운 특징들을 보였다. PCG의 최적 농도는 전처리 조건과 상관없이 일정한 것이 첫 번째 특징으로, PCG를 0.03%의 일정 농도로 첨가하는 경우에 가장 높은 당화 수율을 보이고 있는데 이는 모든 전처리 조건에서 동일하다. 두 번째 특징은 PCG와 전처리 조건의 상호작용으로 1.0%와 10.0%의 NaOH 용액으로 전처리한 시료의 대조군에서는 당 수율이 크게 차이가 없었지만 PCG를 첨가함에 따라 10.0% NaOH 용액으로 전처리된 시료의 당 수율이 1.0% NaOH 용액으로 전처리된 시료보다 확연하게 높게 나타났다. 이러한 결과들을 바탕으로 PCG는 효소의 활성도를 높이는 독립적인 기작을 일으키기도 하지만 이와 동시에 특정 조건에서 발생하는 전처리 효과와 관련된 상호작용을 통하여 효소 당화의 효율을 향상시키는 것으로 사료된다.
PCG가 효소 당화를 향상시키는 기작에 대해 이해하기 위해서 기존의 연구들에서 제시된 가설들을 살펴볼 필요가 있다. 계면활성제가 당화 수율을 증대시키는 기작에 대하여 알려진 가설들은 다음과 같다. (1) 계면 활성제가 기질 구조를 변경하고 효소에 보다 쉽게 접근 할 수 있게 만든다.19-21) (2) 계면 활성제는 효소를 안정화시키고 가수 분해 동안 변성을 방지한다.20,22) (3) 계면 활성제는 기질과 효소 사이의 긍정적인 상호 작용을 증가시킨다.8,20,23) (4) 계면 활성제는 효소의 비생산적 흡착을 감소시킨다.8,24,25)
당화 수율이 일정한 PCG 농도에서 최대치를 보이는 독립적인 기작은 위의 가설들 중 가설 (2)와 연관성이 높은 것으로 보인다. 기작 (2)를 제외한 나머지 가설들(1, 3, 4)은 PCG와 기질 사이의 직접적인 상호작용을 전제로 설명이 가능하다. 따라서 NaOH 전처리를 통하여 기질의 변화가 있을 경우에 PCG의 최적 농도에도 영향을 미치게 된다. 실제로 NaOH를 이용한 전처리의 경우에 기질의 헤미셀룰로오스와 연결된 구성성분의 가교결합이 끊어지게 되어 리그닌과 탄수화물 사이의 결합이 분리된다. 또한, 기질의 팽윤, 공극과 내부 표면적 증가, 결정화도 감소 등의 구조 변화도 일어난다.26) 예를 들어 기작 (4)-효소의 비생산적 흡착 감소는 비이온성 계면활성제의 주요 기작으로 리그닌 함량에 따라 최적 요구량이 달라진다.27) 따라서, 가수분해를 위한 PCG의 최적 농도가 일정한 이유가 PCG에 의한 효소의 안정화 및 변성 방지 기작에 의한 것이라는 가설에 타당성을 부여할 수 있다.
PCG와 전처리 조건에 따른 상호관계는 조금 더 복잡한 기작의 설명이 필요하다. 10.0% NaOH 전처리 조건이 1.0% NaOH 전처리 조건에 비해 PCG의 작용 효과를 더 증대시키는 현상은 다음의 전제 조건이 따른다. PCG에 대한 기질의 직접적인 영향을 배제하고, PCG와 효소의 상호작용과 함께 전처리에 의한 기질의 변화 사이에서 연관성을 밝혀야 한다. 가능한 가설로는 PCG가 효소를 분산시키고 입자 크기를 작게 하는 것과 전처리 과정이 시료의 공극 및 내부 표면적을 증대시킴으로써 작아진 효소의 섬유소에 대한 접근성이 향상되는 것이다. 당화 효소는 대략 20 nm에서 70 nm의 크기를 가지고 있다고 보고되었다.28) 하지만 실제로 당화 과정에서 완충액 속의 효소는 입자 크기가 큰 상태로 존재하며 당화 효소의 크기가 250 nm로 측정된 연구 보고도 있다.25) 10.0% NaOH 전처리는 두 가지 현상이 모두 충분히 일어나는 반면에 1.0% NaOH 전처리는 시료의 공극과 표면적 증대 효과가 상대적으로 부족하여 보다 낮은 수율 향상을 보이는 결과에 대하여 설명이 가능하게 된다.
본 연구의 PCG를 이용한 당화 수율 향상 결과는 기존에 보고된 석유계 합성 계면활성제를 이용한 당화 연구와 비슷하거나 더 나은 긍정적인 결과를 보였다.8,24,25,29) 같은 음이온성 계열의 sodium dodecyl sulfate(SDS)와 양이온성의 cetyl trimethyl ammonium bromide(CTAB)는 바이오매스의 당화 수율에 영향을 주지 않거나 오히려 감소시킨다고 보고되었다.8,24,29) 그리고 Tween 20, Tween 80, Triton X-100, PEG 등과 같은 비이온성 계면활성제는 당화 수율 향상에 긍정적인 효과가 PCG와 비슷하게 나타났다.8,24,29)
효소 당화 수율 향상을 위한 PCG의 사용은 친환경적인 목적으로 연구되어온 바이오 계면활성제와 비교도 가능하다. Rhamnolipid는 최근에 가장 많이 연구된 바이오 계면활성제의 일종으로 밀짚, 볏짚 등의 다양한 바이오매스의 가수분해 공정에 활용되었다.14,30) 볏짚의 가수분해 과정에서 rhamnolipid를 첨가한 연구에서 당 생산량이 15.2% 향상되어다는 연구 결과가 있다.31) 사용된 시료와 계면활성제의 종류가 달라 본 실험과 직접적인 비교는 불가능하지만 본 실험에서 최대 당 생산량 증가율은 대략 52.3%로 rhamnolipid보다 높게 나타났다. Helle (1993) 등은 sophorolipid, rhamnolipid, bacitracin 등의 다양한 바이오 계면활성제를 셀룰로오스 가수분해 실험에 활용하고 Tween 80와 비교하여 비슷한 수율 향상 효과를 보임을 확인하였다.19) 천연물의 인공 합성을 통하여 생산되는 PCG는 미생물을 이용하여 생산되는 바이오 계면활성제보다 생산성이 높고 가수분해의 수율 향상에 대한 긍정적인 효과를 나타내기 때문에 산업에 대한 적용 가능성이 더 높을 것으로 사료된다.
본 연구의 효소 당화를 위한 PCG의 사용 연구 결과, PCG의 활용은 석유계 합성 계면활성제를 대체하는 방안으로 매우 긍정적으로 고려될 수 있다. 또한 환경보호 및 가수분해 수율 향상 효과가 바이오 계면활성제에도 뒤쳐지지 않으며 가수분해 산물의 낮은 독성은 생화학적 변환 공정에 장점으로 작용할 수 있다.
4. 결 론
백합나무 목분을 0.1%, 1.0%, 10.0% NaOH 용액으로 1:20의 비율로 121°C에서 60분간 전처리한 결과, 총 당 생산량은 전처리에 사용된 NaOH용액의 농도에 비례하여 각각 2.3 g/L, 20.1 g/L, 20.8 g/L 순으로 나타났다. NaOH 0.1%는 전처리 효과를 발현하기에 부족한 양이었으나 1.0%와 10.0%의 NaOH로 전처리된 시료의 경우 당 생산량이 비슷한 수준으로 상당히 향상되었다. PCG를 이용한 효소 당화 실험 결과, 모든 전처리 시료에서 PCG를 0.03% 첨가한 경우 당화 향상 효과가 가장 높게 나타나고 그 뒤로 0.15%의 PCG 사용이 높게 나타나는 일관성을 보였다. 0.03%의 PCG 첨가는 0.1%, 1.0%, 10.0% NaOH 전처리 시료의 총 당 생산량을 최대 7.7 g/L, 25.7 g/L, 31.8 g/L로 향상시켰다. PCG는 효소의 안정화 및 변성 방지를 통하여 효소의 활성을 향상시키는 기작을 가지고 있고 이러한 기작은 시료와는 반응하지 않는 독립적인 기작으로 사료된다. 또한 10.0% NaOH 전처리 시료의 수율 향상이 1.0% NaOH 전처리 시료의 수율 향상보다 높은 이유는 PCG에 의한 효소의 변화와 전처리에 의한 시료의 변화가 맞물려 발생한 것으로 사료된다. PCG에 의하여 효소가 분산되고 입자 크기가 감소함과 동시에 전처리에 의한 시료의 공극 및 내부 표면적 증가가 서로 상호작용한 결과로 더 높은 당화 수율을 설명할 수 있다. 효소 당화 공정에 대한 PCG의 활용은 수율 향상과 친환경적 측면에서 기존에 사용되어온 석유계 합성 계면활성제의 대체가 가능하다.
Acknowledgements
이 논문은 2015년도 충북대학교 학술연구지원사업의 교내연구비 지원에 의하여 연구되었습니다
Literature Cited
E. Sjostrom, (Ed.). Wood Chemistry: Fundamentals and Applications, Elsevier. (2013)
Sjostrom, E., Wood Chemistry: Fundamentals and Applications, (Ed.), Elsevier (2013)
B. Kamm and M. Kamm, Applied microbiology and biotechnology,
Principles of biorefineries,
64(2); 137-145 (2004)
Kamm, B. and Kamm, M., Principles of biorefineries, Applied microbiology and biotechnology 64(2):137-145 (2004)
10.1007/s00253-003-1537-7J. Iranmahboob, F. Nadim and S. Monemi, Biomass and Bioenergy,
Optimizing acid-hydrolysis: a critical step for production of ethanol from mixed wood chips,
22(5); 401-404 (2002)
Iranmahboob, J., Nadim, F., and Monemi, S., Optimizing acid-hydrolysis: a critical step for production of ethanol from mixed wood chips, Biomass and Bioenergy 22(5):401-404 (2002)
10.1016/s0961-9534(02)00016-8J. D. DeMartini, S. Pattathil, J. S. Miller, H. Li, M. G. Hahn and C. E. Wyman, Energy & Environmental Science,
Investigating plant cell wall components that affect biomass recalcitrance in poplar and switchgrass,
6(3); 898-909 (2013)
DeMartini, J. D., Pattathil, S., Miller, J. S., Li, H., Hahn, M. G., and Wyman, C. E., Investigating plant cell wall components that affect biomass recalcitrance in poplar and switchgrass, Energy & Environmental Science 6(3):898-909 (2013)
10.1039/c3ee23801fL. da Costa Sousa, S. P. Chundawat, V. Balan and B. E. Dale, Current opinion in biotechnology,
‘Cradle-to-grave’ assessment of existing lignocellulose pretreatment technologies,
20(3); 339-347 (2009)
da Costa Sousa, L., Chundawat, S. P., Balan, V., and Dale, B. E., ‘Cradle-to-grave’ assessment of existing lignocellulose pretreatment technologies, Current opinion in biotechnology 20(3):339-347 (2009)
10.1016/j.copbio.2009.05.003B. Yang and C. E. Wyman, Bioproducts and Biorefining,
Pretreatment: the key to unlocking low-cost cellulosic ethanol, Biofuels,
2(1); 26-40 (2008)
Yang, B. and Wyman, C. E., Pretreatment: the key to unlocking low-cost cellulosic ethanol, Biofuels, Bioproducts and Biorefining 2(1):26- 40 (2008)
Y.-H. P. Zhang, M. E. Himmel and J. R. Mielenz, Biotechnology advances,
Outlook for cellulase improvement: screening and selection strategies,
24(5); 452-481 (2006)
Zhang, Y.-H. P., Himmel, M. E., and Mielenz, J. R., Outlook for cellulase improvement: screening and selection strategies, Biotechnology advances 24(5):452-481 (2006)
T. Eriksson, J. Börjesson and F. Tjerneld, Enzyme and Microbial Technology,
Mechanism of surfactant effect in enzymatic hydrolysis of lignocellulose,
31(3); 353-364 (2002)
Eriksson, T., Börjesson, J., and Tjerneld, F., Mechanism of surfactant effect in enzymatic hydrolysis of lignocellulose, Enzyme and Microbial Technology 31(3):353-364 (2002)
10.1016/s0141-0229(02)00134-5J. B. Kristensen, Enzymatic hydrolysis of lignocellulose: substrate interactions and high solids loadings, Department of Forest and Landscape, University of Copenhagen. (2009))
Kristensen, J. B., Enzymatic hydrolysis of lignocellulose: substrate interactions and high solids loadings, Department of Forest and Landscape, University of Copenhagen (2009)
O. Pornsunthorntawee, P. Wongpanit, S. Chavadej, M. Abe and R. Rujiravanit, Bioresource Technology,
Structural and physicochemical characterization of crude biosurfactant produced by Pseudomonas aeruginosa SP4 isolated from petroleum-contaminated soil,
99(6); 1589-1595 (2008)
Pornsunthorntawee, O., Wongpanit, P., Chavadej, S., Abe, M., and Rujiravanit, R., Structural and physicochemical characterization of crude biosurfactant produced by Pseudomonas aeruginosa SP4 isolated from petroleum-contaminated soil, Bioresource Technology 99(6): 1589-1595 (2008)
10.1016/j.biortech.2007.04.020L. Pinheiro, C. Faustino and (Ed.) R. Najjar, Amino Acid-Based Surfactants for Biomedical Applications, Application and Characterization of Surfactants, InTech. (2017)
Pinheiro, L. and Faustino, C., Amino Acid- Based Surfactants for Biomedical Applications, Application and Characterization of Surfactants, Najjar, R. (Ed.), InTech (2017)
G. O. Reznik, P. Vishwanath, M. A. Pynn, J. M. Sitnik, J. J. Todd, J. Wu, Y. Jiang, B. G. Keenan, A. B. Castle and R. F. Haskell, Applied microbiology and biotechnology,
Use of sustainable chemistry to produce an acyl amino acid surfactant,
86(5); 1387-1397 (2010)
Reznik, G. O., Vishwanath, P., Pynn, M. A., Sitnik, J. M., Todd, J. J., Wu, J., Jiang, Y., Keenan, B. G., Castle, A. B., and Haskell, R. F., Use of sustainable chemistry to produce an acyl amino acid surfactant, Applied microbiology and biotechnology 86(5):1387-1397 (2010)
10.1007/s00253-009-2431-8K. Luo, Q. Ye, X. Yi, Q. Yang, X.-m. Li, H.-b. Chen, X. Liu and G.-m. Zeng, Applied microbiology and biotechnology,
Hydrolysis and acidification of waste-activated sludge in the presence of biosurfactant rhamnolipid: effect of pH,
97(12); 5597-5604 (2013)
Luo, K., Ye, Q., Yi, X., Yang, Q., Li, X.-m., Chen, H.-b., Liu, X., and Zeng, G.-m., Hydrolysis and acidification of waste-activated sludge in the presence of biosurfactant rhamnolipid: effect of pH, Applied microbiology and biotechnology 97(12):5597-5604 (2013)
10.1007/s00253-012-4378-4H.-Y. Wang, B.-Q. Fan, C.-H. Li, S. Liu and M. Li, Bioresource Technology,
Effects of rhamnolipid on the cellulase and xylanase in hydrolysis of wheat straw,
102(11); 6515-6521 (2011)
Wang, H.-Y., Fan, B.-Q., Li, C.-H., Liu, S., and Li, M., Effects of rhamnolipid on the cellulase and xylanase in hydrolysis of wheat straw, Bioresource Technology 102(11):6515- 6521 (2011)
10.1016/j.biortech.2011.02.102Y. Li, Synthesis and physicochemical study of novel amino acid based surfacants, Department of Chemical and Biological Engineering, Chalmers University of Technology. (2012)
Li, Y., Synthesis and physicochemical study of novel amino acid based surfacants, Department of Chemical and Biological Engineering, Chalmers University of Technology (2012)
G. Zhang, B. Xu, F. Han, Y. Zhou, H. Liu, Y. Li, L. Cui, T. Tan and N. Wang, American Journal of Analytical Chemistry,
Green synthesis, composition analysis and surface active properties of sodium cocoyl glycinate,
4(09); 445 (2013)
Zhang, G., Xu, B., Han, F., Zhou, Y., Liu, H., Li, Y., Cui, L., Tan, T., and Wang, N., Green synthesis, composition analysis and surface active properties of sodium cocoyl glycinate, American Journal of Analytical Chemistry 4(09):445 (2013)
10.4236/ajac.2013.49056R. S. Makkar, S. S. Cameotra and I. M. Banat, AMB express,
Advances in utilization of renewable substrates for biosurfactant production,
1(1); 5 (2011)
Makkar, R. S., Cameotra, S. S., and Banat, I. M., Advances in utilization of renewable substrates for biosurfactant production, AMB express 1(1):5 (2011)
10.1186/2191-0855-1-5J.-S. Lee, W.-Y. Song and S.-J. Shin, Journal of Korea TAPPI,
Soda and Soda-AQ Pulps Properties from African Tulip Tree,
47(5); 85-90 (2015)
Lee, J.-S., Song, W.-Y., and Shin, S.-J., Soda and Soda-AQ Pulps Properties from African Tulip Tree, Journal of Korea TAPPI 47(5):85-90 (2015)
10.7584/ktappi.2015.47.5.085S. S. Helle, S. J. Duff and D. G. Cooper, Biotechnology and Bioengineering,
Effect of surfactants on cellulose hydrolysis,
42(5); 611-617 (1993)
Helle, S. S., Duff, S. J., and Cooper, D. G., Effect of surfactants on cellulose hydrolysis, Biotechnology and Bioengineering 42(5):611- 617 (1993)
10.1002/bit.260420509W. E. Kaar and M. T. Holtzapple, Biotechnology and Bioengineering,
Benefits from Tween during enzymic hydrolysis of corn stover,
59(4); 419-427 (1998)
Kaar, W. E. and Holtzapple, M. T., Benefits from Tween during enzymic hydrolysis of corn stover, Biotechnology and Bioengineering 59(4):419-427 (1998)
10.1002/(sici)1097-0290(19980820)59:4<419::aid-bit4>3.3.co;2-9D.-J. Seo, H. Fujita and A. Sakoda, Bioresource Technology,
Structural changes of lignocelluloses by a nonionic surfactant, Tween 20, and their effects on cellulase adsorption and saccharification,
102(20); 9605-9612 (2011)
Seo, D.-J., Fujita, H., and Sakoda, A., Structural changes of lignocelluloses by a nonionic surfactant, Tween 20, and their effects on cellulase adsorption and saccharification, Bioresource Technology 102(20):9605-9612 (2011)
10.1016/j.biortech.2011.07.034M. Kim, S. Lee, D. D. Ryu and E. Reese, Enzyme and Microbial Technology,
Surface deactivation of cellulase and its prevention,
4(2); :99-103 (1982 )
Kim, M., Lee, S., Ryu, D. D., and Reese, E., Surface deactivation of cellulase and its prevention, Enzyme and Microbial Technology 4(2):99-103 (1982)
10.1016/0141-0229(82)90090-4M. Malmsten and J. M. Alstine, J of Colloid and Interface Science,
Adsorption of poly (ethylene glycol) amphiphiles to form coatings which inhibit protein adsorption,
177(2); 502-512 (1996)
Malmsten, M. and Van Alstine, J. M., Adsorption of poly (ethylene glycol) amphiphiles to form coatings which inhibit protein adsorption, J of Colloid and Interface Science 177(2): 502-512 (1996)
10.1006/jcis.1996.0064B. C. Min, B. Bhayani, V. Jampana and B. Ramarao, Bioresources and Bioprocessing,
Enhancement of the enzymatic hydrolysis of fines from recycled paper mill waste rejects,
2(1); 1-10 (2015)
Min, B. C., Bhayani, B., Jampana, V., and Ramarao, B., Enhancement of the enzymatic hydrolysis of fines from recycled paper mill waste rejects, Bioresources and Bioprocessing 2(1):1-10 (2015)
10.1186/s40643-015-0068-2B. C. Min and B. V. Ramarao, Bioprocess and biosystems engineering,
Mechanisms of the inhibition of enzymatic hydrolysis of waste pulp fibers by calcium carbonate and the influence of nonionic surfactant for mitigation,
40(6); 799-806 (2017)
Min, B. C. and Ramarao, B. V., Mechanisms of the inhibition of enzymatic hydrolysis of waste pulp fibers by calcium carbonate and the influence of nonionic surfactant for mitigation, Bioprocess and biosystems engineering 40(6): 799-806 (2017)
10.1007/s00449-017-1745-7Y. Sun and J. Cheng, Bioresource Technology,
Hydrolysis of lignocellulosic materials for ethanol production: a review,
83(1); 1-11 (2002)
Sun, Y. and Cheng, J., Hydrolysis of lignocellulosic materials for ethanol production: a review, Bioresource Technology 83(1):1-11 (2002)
10.1016/s0960-8524(01)00212-7B. Min, Enzymatic Hydrolysis of Cellulosic Fibers in Paper Mill Waste, State University of New York College of Environmental Science and Forestry. (2017)
Min, B., Enzymatic Hydrolysis of Cellulosic Fibers in Paper Mill Waste, State University of New York College of Environmental Science and Forestry (2017)
E. Cowling and T. Kirk, Properties of cellulose and lignocellulosic materials as substrates for enzymatic conversion processes (1976)
Cowling, E. and Kirk, T., Properties of cellulose and lignocellulosic materials as substrates for enzymatic conversion processes, (1976)
R. Gupta, K. K. Sharma and R. C. Kuhad, Bioresource Technology,
Separate hydrolysis and fermentation (SHF) of Prosopis juliflora, a woody substrate, for the production of cellulosic ethanol by Saccharomyces cerevisiae and Pichia stipitis-NCIM 3498,
100(3); 1214-1220 (2009)
Gupta, R., Sharma, K. K., and Kuhad, R. C., Separate hydrolysis and fermentation (SHF) of Prosopis juliflora, a woody substrate, for the production of cellulosic ethanol by Saccharomyces cerevisiae and Pichia stipitis-NCIM 3498, Bioresource Technology 100(3):1214- 1220 (2009)
10.1016/j.biortech.2008.08.033Q. Zhang, G. He, J. Wang, W. Cai and Y. Xu, Applied Energy,
Mechanisms of the stimulatory effects of rhamnolipid biosurfactant on rice straw hydrolysis,
86; S233-S237 (2009)
Zhang, Q., He, G., Wang, J., Cai, W., and Xu, Y., Mechanisms of the stimulatory effects of rhamnolipid biosurfactant on rice straw hydrolysis, Applied Energy 86:S233-S237 (2009)
10.1016/j.apenergy.2009.04.030Q. Zhang, G. He, J. Wang, W. Cai and Y. Xu, Biomass and Bioenergy,
Two-stage co-hydrolysis of rice straw by Trichoderma reesei ZM4-F3 and Pseudomonas aeruginosa BSZ-07,
33(10); 1464-1468 (2009)
Zhang, Q., He, G., Wang, J., Cai, W., and Xu, Y., Two-stage co-hydrolysis of rice straw by Trichoderma reesei ZM4-F3 and Pseudomonas aeruginosa BSZ-07, Biomass and Bioenergy 33(10):1464-1468 (2009).
10.1016/j.biombioe.2009.06.012








