1. 서 론
리그닌(Lignin)은 셀룰로오스(cellulose), 헤미셀룰로오스(hemicellulose)와 함께 식물을 구성하는 3대 주성분으로 식물의 세포벽을 구성하고 있다.1) 리그닌 부산물들은 다양한 전처리 방법에 따라 다양한 화학구조 조성을 지니고 있는데 이 중 크라프트 펄핑(Kraft pulping) 공정에서 발생하는 크라프트 흑액(black liquor)을 무기산 또는 이산화탄소를 이용하여 중화, 산성화했을 때 발생하는 침전물들을 세척 및 회수한 크라프트 리그닌(Kraft lignin)이 가장 큰 비중을 차지하고 있다. 기존의 펄프·제지 산업에서는 이 리그닌을 회수하여 소재 등으로 활용하는 것보다는 대부분 소각시켜 제지공정을 운영하는 에너지원으로 사용해 왔으나2,3) 최근 들어, 목질계 바이오매스 성분 중 셀룰로오스 및 헤미셀룰로오스와 같은 탄수화물 성분들을 활용한 바이오에탄올 등 바이오 액체연료 제조에 관한 연구가 많아지면서 목질계 바이오매스를 이용한 바이오 연료의 문제점인 생산비용을 보존 받고자 바이오 연료 제조 시 발생하는 리그닌 부산물의 고부가가치 소재 및 약품화 연구에 관한 관심이 증가하는 실정이다.4-6)
리그닌은 재생 가능한 천연고분자로 C6-C3의 페닐 프로판 구조를 갖는 ρ–coumaryl alcohol (H), guaiacyl alcohol (G), sinapyl alcohol (S) 세 가지 종류의 단위체들이 에테르 결합인 β-O-4, α-O-4, 4-O-5 등과 탄소-탄소의 공유결합인 β-5, 5-5, β-1, β-β 등의 복잡한 결합으로 무정형의 3차원 고분자 구조를 구성하고 있다. 리그닌의 작용기로는 메톡실기(-OCH3), 페놀성 수산기, 지방족 수산기 등을 포함한 다양한 화학적 작용기가 포함되어 있으며, 증해 과정 중에 리그닌이 분해 및 화학적으로 개질되어 분자량의 분포가 넓어져 균일한 분자량과 구조를 갖는 리그닌으로 분리 및 정제가 어려운 점이 있어 특정 소재로써 활용하기에는 쉽지 않은 실정이다.7-9)
하지만 이러한 리그닌 이용 한계에도 불구하고 리그닌의 기본 구조가 석유계 폐놀성 자원과 유사하고 가격이 저렴하며 생분해성과 가장 중요한 점인 지속 가능한 친환경적 자원이라는 장점이 있기에 리그닌의 균일한 성분추출 및 다양한 소재화를 위한 연구가 진행되고 있다.10-12) 예를 들어, 리그닌을 균일한 소재로써 만들기 위해 Choi 등13)은 리그닌을 여러 유기용매에 용해시켜 특정 성분으로의 균일한 분리에 관한 연구를 수행했으며 Seo 등14)은 여러 전처리를 통해 리그닌의 개질 및 특성을 파악하고자 했다. 또한, 대표적인 전도성 고분자인 폴리아닐린(polyaniline)과 리그닌을 이용한 복합체를 제조하여 리그닌 입자 표면을 중심으로 폴리아닐린 입자가 형성되는 것을 확인했고 이것이 기존 리그닌보다 향상된 전기·화학적 특성을 나타내는 것을 확인했다. 그럼에도 불구하고 다양한 리그닌 기반 공중합체들은 물과 유기용매에 대한 용해성이 낮아서 다양한 신소재 적용에 어려움이 있다.12)
따라서 본 연구에서는 물과 유기용매에 대한 용해성이 향상된 리그닌 기반 공중합체를 제조하고자 수용성의 특성을 지닌 전도성 고분자 poly(m-aminobenzenesulfonic acid) (PABS)를 리그닌과 그라프팅(grafting) 공중합시켜 리그닌 기반 PABS 공중합체를 제조하여 고부가가치 리그닌 기반 신소재로써 활용성을 높이고자 했다. 또한, FT-IR 및 EA 원소분석을 통해 리그닌 기반 PABS 공중합체의 화학적 구조 특성 분석과 GPC 분자량 크기 분석, TGA 열적 특성 분석으로 물리적 특성을 분석하여 향후 리그닌 기반 신소재로의 고도활용을 위한 기초연구 자료로 활용하고자 하였다.
2. 재료 및 방법
2.1 공시재료
M 사에서 제공한 활엽수 크라프트 리그닌(KL) 중 20 g을 2 L의 메탄올에 용해 후 미용해분은 filter paper (직경 90 mm, Chmlab, Spain)로 여과/분리하여 제거하고 용해분은 감압농축기(rotary evaporator, N-1110, EYELA, Japan)를 이용하여 농축하였다. 농축한 용해분을 20 mL 1,4-dioxane에 용해한 다음 3 L의 증류수에 첨가 후 filter paper를 이용하여 여과/분리하였으며 미용해분을 회수하여 동결건조기(FDCF-12006, OPERON, Korea)를 이용하여 대략 10 g의 정제된 메탄올 용해 리그닌(methanol soluble lignin, ML)을 회수하여 리그닌 기반 전도성 공중합체 제조에 사용하였다. 리그닌 기반 전도성 공중합체 제조 실험에는 Sigma-Adrich 사의 aniline (≧99.5%), triphosgene, ammonium persulfate (APS, ≧98%), m-amino benzene sulfonic acid (ABS, 97%)와 대정화금 사의 acetone (99.5%), hydrochloric acid (HCl, 70%), methanol (99.5%), 1,4-dioxane (99.5%), ethyl acetate (99.5%), tetrahydrofurananhydrous (THF, 99.5%), N, N-diisopropylethylamine (DIPEA), N, N-Dimethylformamaid (DMF)을 구입하여 사용하였으며, 3차 증류수기(Human RO-180, Human, Korea)로 제조한 탈 이온수(deionized water)를 사용하였다.
2.2 실험방법
2.2.1 전도성 고분자 [Poly(m-aminobenzenesulfonic acid)] (PABS) 제조
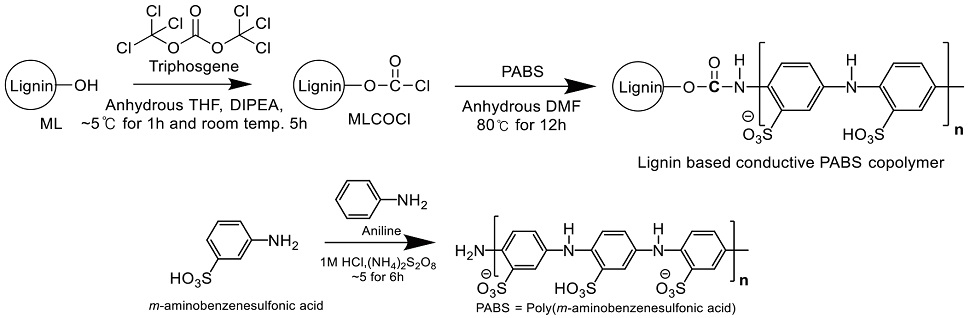
전도성 고분자 [Poly(m-aminobenzenesulfonic acid), PABS] 제조는 이전 연구에서 제조하였던 방법에 따라 Fig. 1과 Table 1의 반응조건에 따라 합성하였다.15) 먼저 1M 농도의 HCl 30 mL와 0.86 g의 ABS를 250 mL의 둥근바닥 플라스크에 넣고 60℃의 water bath와 초음파 세척기(JAC-5020, KODO, Japan)를 이용해 투명해질 때까지 용해한다. 그리고 0-5℃의 water bath에서 5분간 교반 후 개시제로 aniline을 0.99 mmol을 넣었으며, 투입 후 5분간 교반을 진행했다. 다음으로 산화제인 APS를 15 mL 투입한 다음 6시간 동안 반응을 시켰다. 반응 후, 감압농축기(rotary evaporator, N-1110, EYELA, Japan)를 이용해 농축시켜 crude PABS를 회수하였다. PABS의 정제과정으로는 먼저 과량의 acetone으로 용해한 다음 filter paper (직경 90 mm, Chmlab, Spain)로 여과/분리하여 미용해분을 회수하였으며, 회수분을 다시 증류수 100 mL에 용해시켜 미용해분을 nylon membrane filter (직경 90 mm, 공극 직경 0.2 μm, Whatman)를 이용하여 여과/제거하였다. 용해분에 존재하는 저분자량의 PABS와 잔존 약품 제거는 dialysis bag (Spectra/por® 6 dialysis membrane Pre-wetted RC tubing, MWCO 1,000, Spectrum, USA)을 이용하여 72시간 투석을 진행하였다. dialysis bag 내부의 수용성 PABS는 동결건조기(FDCF-12006, OPERON, Korea)를 사용하여 파우더 형태의 PABS로 회수하였다.
2.2.2 염화 에스테르 리그닌(MLCOCl) 제조
PABS를 리그닌에 그라프팅 공중합시켜 리그닌 기반 전도성 공중합체를 제조하기 위해서 먼저 리그닌에 전도성 고분자가 중합될 위치를 만들고자 리그닌의 수산기를 염화 에스테르(–COCl) 관능기로 치환한 염화 에스테르화 리그닌(MLCOCl)을 제조하였다. 최적 제조조건 확인을 위해 Table 2와 같이 triphosgene의 첨가량을 다르게 했으며, Park 등16)의 실험방법을 응용하여 Fig. 1과 같이 제조하였다. 먼저 250 mL의 둥근바닥 플라스크에 0.5 g의 ML과 30 mL의 무수 THF를 넣어 용해한 다음 ice water bath에서 10분 정도 교반하면서 온도를 ~5℃로 낮추었다. 반응온도가 ~5℃로 낮아진 것을 확인한 다음 DIPEA를 0.66 mmol 넣고 1분간 교반을 진행한 다음 triphosgene을 Table 2에 따라 투입하여 ~5℃의 ice water bath에서 1시간 반응시킨 다음 꺼내어 상온에서 5시간을 반응시켜 주었다. 반응혼합물에서 MLCOCl 정제는 100 mL의 ethyl acetate를 이용하여 분별 깔때기로 총 3회 반복 추출했으며, 추출한 ethyl acetate를 감압농축기를 이용해 농축하여 crude MLCOCl를 회수하였다. 그리고 탈 이온수에 crude MLCOCl를 초음파 세척기로 분산시킨 후, nylon membrane filter를 이용해서 정제된 MLCOCl를 동결건조기를 사용하여 파우더 형태의 MLCOCl를 회수하였다.
2.2.3 리그닌 기반 전도성 공중합체(MLCOCl-g-PABS) 제조
위에서 제조한 PABS를 MLCOCl에 그라프팅 공중합 시킨 리그닌 기반 공중합체 제조(MLCOCl-g-PABS)는 Fig. 1 및 Table 3에 나온 반응조건과 같이 실시하였다. 먼저 최적 조건으로 확인된 MLCOCl C와 PABS를 Table 3의 조건과 같이 투입비를 3:1로 하여 250 mL의 둥근 플라스크에 용매인 무수 DMF 30 mL와 같이 넣어준 다음 초음파 세척기를 이용해 용해한 다음 80℃의 oil bath에서 12시간 동안 교반 및 반응을 시켰다. 반응 후, 용매인 DMF를 감압농축기를 이용하여 제거 후 증류수 200 mL를 넣어 다시 재농축하면서 잔존 DMF를 제거하였다. 농축 후 원심분리기(MF550, Hanil, Korea)로 1회 증류수 400 mL를 첨가하고 총 4번 반복하여 증류수 용해분(MLCOCl-g-PABS-Sol)과 미용해분(MLCOCl-g-PABS-In)을 분리하였다. MLCOCl-g-PABS-Sol은 분리 과정에서 섞인 MLCOCl-g-PABS-In을 제거하고자 nylon membrane filter를 이용해 추가 여과/분리 과정을 거쳤다. 여과된 MLCOCl-g-PABS-Sol은 농축과정을 거쳐 동결건조기를 이용해 파우더 형태의 시료로 회수하였고, MLCOCl-g-PABS-In의 경우 충분히 얼린 다음 동결건조기를 이용해 파우더 형태로 회수하였다.
2.2.4 화학적 및 물리적 특성 분석
PABS, MLCOCl, MLCOCl-g-PABS의 화학구조 분석을 위해 1H NMR 및 FT-IR 분석방법을 실시하였다. 1H NMR 분석은 Bruker 사의 FT-NMR 600 MHz spectrometer (Bruker Avance Ⅱ 600)를 이용했으며 시료 당 스캔을 128회 실시했다. PABS의 경우 물에 대한 용해성이 높아 시료 20 mg을 NMR solvent D2O 0.6 mL에 용해시켜 분석하였다. FT-IR 분석은 PABS, MLCOCl 및 MLCOCl-g-PABS의 다양한 작용기를 확인하기 위해서 각 시료당 256번의 스캔을 실시하였고, Perkin-Elmer (USA) 사의 attenuated total reflectance attachment (ATR)가 장착된 Frontier 모델을 이용하였다.
PABS, MLCOCl, MLCOCl-g-PABS의 C, H, N 및 S의 원소함량 분석은 열전도도 검출기가 장착된 Elemetal Analyzer (frash EA 1112, USA)로 분석하였다. 표준물질은 [2,5-Bis(5-tert-butyl-2-benzo-axazol-2-yl), BBOT]를 사용하여 분석하였다.
PABS, MLCOCl 및 MLCOCl-g-PABS-In, Sol의 분자량 분석(GPC)은 각 시료를 1 mg씩 정량하여 DMF 1 mL에 녹여 SPD-20A (UV/Vis detector, Shimadzu, Japan), RID-20A (Refractive index, Shimadzu, Japan) 검출기가 장착된 CBM-20A (Shimadzu, Japan)로 측정하였다. 이때 컬럼은 70℃에서 한 개의 agilent PLgel mixed-C (300×7.5 mm, 5 μm)와 agilent PLgel mixed-D (300×7.5 mm, 5 μm), agilent PLgel mixed-E (300×7.5 mm, 3 μm)를 연결하여 분석했으며 oven 온도는 70℃로 설정했다. UV 검출기의 파장은 280 nm, injection volume은 100 μL로 설정한 뒤 DMF를 이동상으로 하여 1 mL/min의 조건으로 흘려주어 측정을 진행했다. 분자량에 대한 검량선 작성은 1,480에서 1,233,000 g/mol 범위의 polystyrene standard를 이용하여 작성된 검량선을 통해 각 시료의 분자량 분포를 분석하였다.
PABS, MLCOCl, MLCOCl-g-PABS의 열분해 거동을 파악하기 위해서 열중량 분석기(Thermogravimetric analyzer, SDT Q600, TA Instrument, USA)를 이용하여 분석하였다. 분석조건으로는 각 시료 10 mg을 20℃/min의 승온 속도로 700℃까지 가열하였고 flowing gas는 N2를 이용하였다.
3. 결과 및 고찰
3.1 전도성 고분자 Poly(m-aminobenzenesulfonic acid) (PABS)의 제조
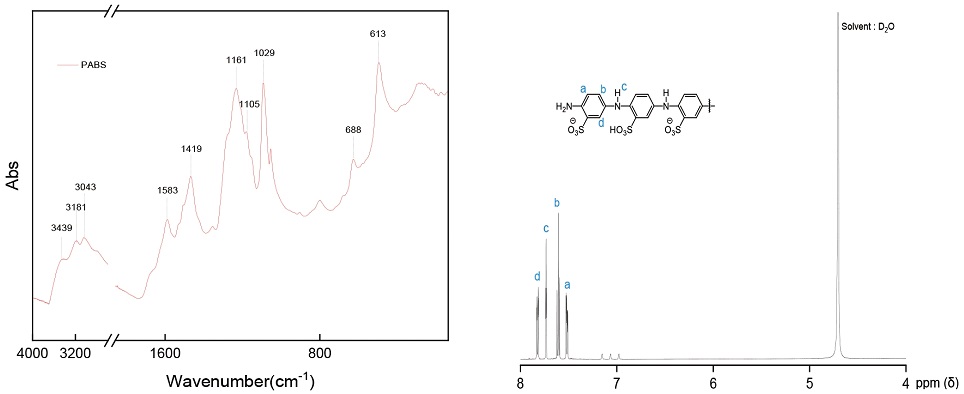
일반적으로 전도성 고분자들은 물뿐만 아니라, 유기용매에도 잘 용해되지 않는 문제점을 갖는 것으로 알려져 있다. 이러한 전도성 고분자의 불용해성은 Fig. 1에 나왔듯이 설폰산기를 지니고 있는 ABS를 모노머로 전도성 고분자를 제조하여 물 및 여러 유기용매에 대한 용해성을 증가시키고자 했으며, 또한 ABS 모노머만 중합시킬 경우 고분자 중합 반응이 잘 일어나지 않기 때문에 고분자 중합 개시제로 aniline을 소량 첨가해 전도성 고분자인 PABS를 제조할 수 있었다.17)Fig. 2는 PABS의 1H NMR 및 FT-IR 스펙트럼으로 1H NMR 스펙트럼을 통하여 전도성 고분자의 벤젠링에 있는 7.6-7.3 ppm의 수소 시그널과 아민기의 수소 시그널을 확인하였으며 FT-IR 분석을 통하여 고분자 중합 원료인 ABS에 존재하는 작용기인 aromatic ring, 설폰산기 및 아민기와 관련된 피크인 3439 cm-1 –OH 피크와 3181 cm-1 –NH의 피크, 3043 cm-1 aromatic ring의 C-H stretching 피크, 1583 cm-1 quinoid ring 피크를 확인할 수 있었다. 또한, 설폰산기의 신축 및 굽힘 진동과 관련있는 1419 cm-1 O-H bending 피크, 1161, 1029 cm-1 S=O stretching 피크, 1105 cm-1 aromatic C-N stretching 피크 688 cm-1 S-O stretching, 613 cm-1 C-S stretching 피크들을 확인하면서 이전 연구에서 제조한 PABS의 1H NMR, FT-IR 결과와 크게 차이가 없는 것으로 나타났다.15) 수평균 분자량은 약 2,000 g/mol 증가한 17,400 g/mol인 것으로 나타났으며 PABS의 원소 조성 함량 분석결과 PABS의 질소(N) 및 황(S)의 함량이 이전과 같이 높은 것을 확인할 수 있었다. 열 분해온도는 298℃에서 분해되는 열적 특성을 지닌 것으로 나타났다(Table 4). 이처럼 1H NMR 및 FT-IR을 이용한 화학구조 분석 결과와 EA 및 GPC 분자량 크기 분석, TGA 분석을 통해서 수용성 특성을 지닌 전도성 고분자 PABS가 잘 제조된 것으로 보인다.
3.2 염화 에스테르 리그닌(MLCOCl) 제조
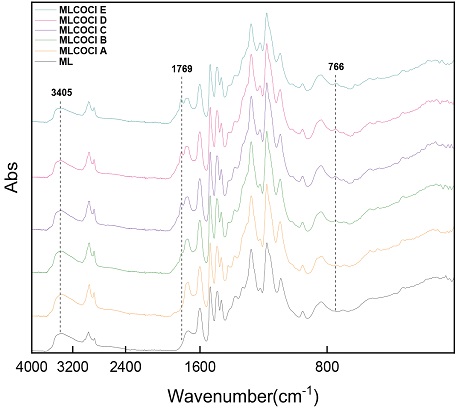
리그닌에 전도성 고분자인 PABS을 중합시키기 위해서 리그닌에 염화 에스테르 작용기를 Fig. 1과 같이 치환했으며 MLCOCl의 화학구조 분석을 위해 FT-IR 분석을 실시하였다. FT-IR 분석결과 triphosgene의 첨가량이 증가할수록 메탄올 용해 리그닌(ML)에 더 많은 염화 에스테르 작용기가 붙어 3405 cm-1 –OH 피크의 감소와 1769 cm-1 C=O stretching 피크, 766 cm-1 C-Cl bending 피크가 증가하는 것을 확인할 수 있었다. 그러나 triphosgene의 첨가량이 소량인 MLCOCl A에서는 해당 피크가 잘 나타나지 않았으며, MLCOCl C보다 더 많은 양의 약품 첨가는 결과적으로 큰 차이가 없는 것으로 판단된다(Fig. 3). 따라서 염화 에스테르 리그닌의 최적 제조조건은 MLCOCl C이며, 염화 에스테르 작용기로 치환한 리그닌 유도체가 잘 합성된 것으로 사료된다.18,19)
3.3 리그닌 기반 전도성 PABS 공중합체(MLCOCl-g-PABS) 제조
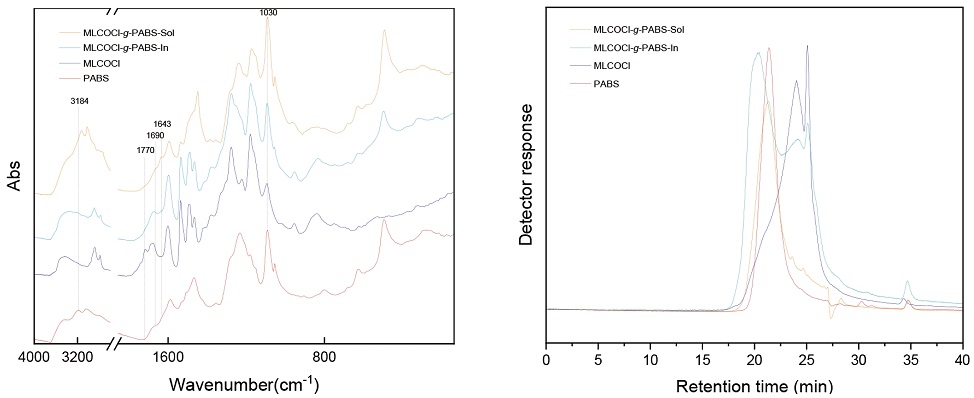
위에서 합성한 PABS와 MLCOCl의 공중합체는 Table 3에 나와 있듯이 MLCOCl과 PABS의 함량을 다르게 하여 제조했으며, 공중합체를 증류수로 MLCOCl-g-PABS-Sol과 MLCOCl-g-PABS-In으로 분리하여 분석했다. 공중합체의 수율은 Table 5와 같이 0.35 g의 MLCOCl-g-PABS-In과 0.04 g의 MLCOCl-g-PABS-Sol가 회수되었으며, 이는 공중합 반응 후, PABS가 MLCOCl에 그라프트 중합되어 대부분 MLCOCl-g-PABS-In으로 제조된 것으로 판단된다. FT-IR 분석결과로는 MLCOCl-g-PABS-In과 MLCOCl-g-PABS-Sol 모두에서 염화 에스테르 작용기에 의해 나타나던 1769 cm-1 C=O stretching 피크가 사라졌으며, 1690, 1640 cm-1 amide에 의해 나타나는 C=O stretching 피크가 나타난 것을 확인할 수 있었다.20) 또한, PABS와 결합한 미량의 저분자량을 갖는 MLCOCl의 영향으로 MLCOCl-g-PABS-Sol의 1030 cm-1 C-O 피크가 증가한 것을 확인할 수 있었다. GPC 분석으로는 MLCOCl-g-PABS-In의 경우 수평균 분자량은 9,400 g/mol, 질량 평균 분자량 값은 19,900 g/mol으로 나타났으며, MLCOCl-g-PABS-Sol의 경우 수평균 분자량이 14,900 g/mol, 질량평균 분자량은 20,100 g/mol인 것으로 확인되었다. 특히 Fig. 4를 통하여 MLCOCl-g-PABS-In의 경우에는 MLCOCl, PABS 보다 큰 부분이 형성된 것을 확인하면서 공중합체가 성공적으로 형성되었다고 사료되며, MLCOCl-g-PABS-Sol의 경우도 PABS 대비 약간 증가한 부분을 통하여 저분자량의 MLCOCl과 결합된 PABS 공중합체에 의한 결과로 사료된다.
Table 5.
Molecular weight, element content and thermal degradation temp. of MLCOCl, MLCOCl-g-PABS-In and MLCOCl-g-PABS-Sol
TGA 분석결과에서는 380℃의 열분해 온도를 가지는 MLCOCl 대비 MLCOCl-g-PABS-In의 열분해 온도가 30℃ 증가하는 것을 확인할 수 있었다(Table 5). 이는 그라프트 공중합을 통해 증가한 분자량에 의한 것으로 사료된다. EA 분석에서는 MLCOCl 대비 MLCOCl-g-PABS-In에서 공중합 후 질소(N)는 약 3.2배, 황(S)은 약 5.5배 함량이 증가한 것을 확인할 수 있었으며, MLCOCl-g-PABS-Sol에서는 미량의 질소 함량 및 1.8배의 황 함량의 감소와 산소(O) 함량의 큰 증가를 확인할 수 있었다. 이는 MLCOCl-g-PABS-In의 경우 PABS가 공중합 되어 PABS를 구성하는 질소 및 황의 성분이 영향을 준 것으로 보이며, MLCOCl-g-PABS-Sol의 경우 질소(N) 및 황(S)의 함량은 PABS와 유사하지만, 산소(O)의 함량이 다소 높게 나타났던 것으로 사료된다
4. 결 론
본 연구에서는 펄프·제지 산업에서 발생하는 부산물인 크라프트 리그닌의 물리·화학적 특성을 개선하여 기능성 신소재로 사용하고자 리그닌 기반 전도성 고분자인 MLCOCl-g-PABS를 제조하여 화학적 구조 및 물리적 특성을 분석하였다. FT-IR을 통한 화학구조 분석과 GPC 분석을 통하여 PABS의 방향족 아민기 및 설폰산기를 확인할 수 있었으며, 수평균 분자량이 17,400 g/mol로 나타나 성공적으로 합성되었음을 확인하였다. 최종적으로 리그닌과 PABS를 그라프팅 공중합하여 제조한 공중합체를 수용성 용해분과 미용해분으로 분리하여 물리·화학적 특성을 분석한 결과 미용해분의 수율이 상대적으로 높은 것으로 나타났으며, 화학구조 분석 및 GPC 분자량 분석을 통하여 미용해분에서 리그닌 및 PABS 유래 작용기들이 모두 나타나는 것을 확인하였고 분자량이 MLCOCl보다 크게 증가된 것으로 나타났다. 이러한 결과를 종합해 볼 때, 미용해분이 리그닌과 PABS의 공중합을 통하여 MLCOCl-g-PABS 공중합체로써 성공적으로 제조된 것으로 사료되며, 불용성 MLCOCl-g-PABS 공중합체의 TGA 분석결과 리그닌 대비 열분해 온도가 30℃ 증가하는 것으로 보아 이는 PABS가 리그닌에 공중합되어 MLCOCl-g-PABS 공중합체의 분자량이 증가되어 열 안정성이 향상된 것으로 사료된다. 따라서 본 연구를 통해 크라프트 리그닌의 PABS와의 공중합으로 리그닌의 특성을 개질할 수 있음을 확인함과 동시에 향후 리그닌의 고도활용을 위한 기초연구 자료로 활용할 수 있을 것으로 사료된다.