1. 서 론
바이오매스 유래의 셀룰로오스는 매년 백억 톤 이상이 생성되는 천연 유기물 고분자이다. 그 중 약 10억 톤이 종이, 섬유, 재료, 화학 산업에서 이용된다.1) 글루코오스 베타 1-4 결합으로 이루어진 셀룰로오스는 원료 및 가공방법에 따라 다형체(polymorphs)로 구성되어 있고, 그 내부는 elementary fibril로 이루어져 있다.2) 이러한 elementary fibril은 크기 및 물리·화학적 성상에 따라 나노피브릴(nanofibrillated cellulose), 나노결정(nanocrystalline cellulose), 마이크로피브릴(microfibrillated cellulose) 및 마이크로결정(microcrystalline cellulose) 셀룰로오스 등으로 분류할 수 있다.3) 또한 바이오매스 세포벽 내에는 셀룰로오스 이외에도 구성성분인 헤미셀룰로오스 및 리그닌이 서로 네트워크를 형성하여 이러한 구성성분들의 결정화도, 입도, 표면적, 헤미셀룰로오스의 존재 양식, 리그닌 함유량, 세포벽에 지리학적 존재위치, 리그닌의 세부구조(subunit)의 비율, 리그닌-탄수화물 복합체(lignin-carbohydrate complex)의 함유량 및 결합양식(phenyl glycoside, benzyl ester, 혹은 benzyl ether)의 유무에 따라 구성성분을 추출·분리 시 반응저해물질(recalcitrant moiety)로 작용할 수 있다.4-7)
대량생산과 대량소비로 대변되는 산업경제체제에서 소형화, 국지화 및 다양성으로 대변되는 바이오 경제로의 패러다임의 변화와 더불어 바이오매스 자원으로부터 4차 산업형 원천 바이오 소재(bio-derived chemicals) 개발의 관심이 증대되고 있다. 기존의 펄프·제지산업 및 섬유산업에서는 대부분의 리그닌과 헤미셀룰로오스를 증해·표백과정 등으로 제거한 후 셀룰로오스를 추출·분리하여 종이 혹은 비스코레이온 생산 원료로 사용하고 있다. 이러한 공정을 통해 바이오자원의 4차 산업형 원천 바이오 소재로서 가치화(valorization)되지 않는 비율은 바이오매스 중량투입 대비 약 30-50%로 사료된다. 가능한 많은 양의 리그닌 및 헤미셀룰로오스를 고분자 소재로 전환하기 위해 다양한 바이오매스 전처리 기술이 개발되고 있다.8-11) 이러한 바이오매스 전환 기술 중 유기용제·촉매를 이용한 탈리그닌화 기술은 기존의 제거기술에 비해 간단하면서 짧은 반응시간으로 리그닌을 선택적으로 제거할 수 있다. 또한 에너지 소비가 적으면서 소형화가 가능하고 반응시간이 짧아 생산량(throughput)에 영향을 주지 않아 주생산물인 리그노-셀룰로오스를 다양한 소재로서 사용할 수 있을 것이라 판단된다.12)
다양한 산업 소재로서의 리그노-셀룰로오스의 가능성을 탐구하기 위해, 소나무 목분과 유칼립투스 목분을 이용하여 glycol ether 용매와 산 촉매 하에서 마이크로파 처리를 통해 얻어진 잔류물의 특성비교 및 용해용제에 대한 용해성을 평가하였다.13) 반응정도(severity)에 따라 잔류물의 수율 및 잔존 리그닌 함량의 조절이 가능하였지만, 잔존 리그닌 함유량이 많은 침엽수 유래 잔류물의 경우 용해용제인 urea/NaOH 수용액에 대한 용해성이 높지 않아 다양한 소재로서의 변환이 어려울 것으로 판단되었다.
따라서, 본 연구에서는 국내산 소나무를 원료로 하여 LAS(low temperature, atmospheric pressure and short reaction time) 펄프화법14)을 이용하여 LAS 미세 잔류물을 제조한 후, 아염소산을 이용하여 미세 잔류물 내 잔존 리그닌의 함량을 인위적으로 조절하여 잔존 리그닌 함량에 따른 용해용제에 대한 용해성을 평가하고자 하였다.
2. 재료 및 방법
2.1 공시재료
2.1.1 재료
본 연구에서 사용된 목재 시편은 함수율이 9.1%인 국내산 소나무(Pinus densiflora)이며 실험실용 햄머밀을 이용하여 분말화하여 사용하였다. 분말화한 시료는 40-80 mesh로 분급하여 에탄올-벤젠 혼합용액(1:2, v/v)으로 24시간 동안 추출하여 탈지 목분을 제조하였다. 탈지 목분을 이용하여 LAS 미세 잔류물 제조 원료로 사용하였다. 용해도 측정 실험의 대조구로 microcrystalline cellulose(Avicel PH-101, Fluka Co.)를 사용하였다.
2.1.2 시약
본 연구에서 사용된 고비점 용제(HBPS)12)는 끊는점이 약 197℃이고, 순도 98.0%인 glycol ether 용매(pure grade, Sigma Aldrich Co.)를 사용하였고, LAS 펄프화를 위한 촉매로는 순도 95.0%인 황산(extra pure grade, Daejung Chemicals & Metals, Korea)을 사용하였다.
2.2 실험방법
2.2.1 LAS 펄프화
탈지된 40-80 mesh 시료의 LAS 펄프화는 이전 연구15)에서 소개한 방법을 개조하여 실험을 진행하였다. 5 g의 시료에 glycol ether와 황산 혼합시약을 1:2(w/v)로 투입하였다. 사용된 혼합시약은 glycol ether 용매에 대하여 2.0%(v/v)로 촉매인 황산을 첨가하여 제조하였다. 가압이 되지 않는 상태에서 펄프화를 진행하기 위해 감압기의 씰(seal)을 제거한 후 목분과 증해액을 둥근 유리플라스크에 넣고 오일 bath를 사용하여 반응 온도를 110±5℃로 설정하였다. 일정한 반응 온도를 부여하기 위해 시료가 들어 있는 반응 용기가 충분히 오일 bath에 잠기게 하고, 또한 100 rpm으로 일정하게 회전하도록 조절하였다. 반응 종료 후 0.5 N NaOH 수용액 500 mL를 사용하여 감압 하에서 세척을 한 후, 여과물이 중성이 될 때까지 증류수로 세척을 실시하였다. 여과 후에 생성된 미세 잔류물 시료는 기건 시킨 후 105±3℃의 건조 오븐에서 24시간 이상 건조하였다.
2.2.2 LAS 미세 잔류물의 아염소산 처리
LAS 펄프화법으로 제조된 LAS 미세 잔류물의 잔존 리그닌 함량을 조절하기 위해 아염소산화법으로 탈리그닌을 진행하였다. 아염소산 반응시간에 따른 잔존 리그닌 함량에 대한 검량선을 구축하기 위해 전건 기준 1 g의 LAS 미세 잔류물과 증류수 60 mL를 혼합한 뒤, 0.1 g의 아염소산나트륨(pure grade, Daejung Chemicals & Metals)과 0.02 mL의 빙초산(extra pure grade, Duksan, Korea)을 첨가하였다. 70℃에서 중탕을 하여 1 시간 단위로 지속적으로 0.1 g의 아염소산나트륨과 0.02 mL의 빙초산을 투입하였다. 반응 종료 후 증류수를 이용하여 감압 하에서 세척 여과하여 기건 시킨 후 105±3℃의 건조 오븐에서 24시간 이상 건조하였다.
2.2.3 측정
LAS 펄프화 반응 및 아염소산 처리 전후의 중량을 측정하여 미세 잔류물 시료 혹은 아염소산 처리된 LAS 미세 잔류물의 수율을 계산하였다. 잔존 리그닌 함량은 TAPPI T 222의 방법에 따라 Klason lignin법을 적용하여 측정하였다. 조성 당 분석은 alditol acetate법16)을 적용하였다. GC 측정 시, 사용한 컬럼은 Rxi-5ms Fused Silica column(30 m length×250 μm I.d, 0.25 μm film thickness)이고 Detecter는 FID(Flame Ionization Detector)를 사용하였다. 초기 온도는 150℃이며 분당 5℃씩 상승하도록 설정하였고 detection 온도는 250℃, 시간은 5분으로 설정해 GC 측정을 실시하였다. 개별적인 조성 당 성분의 함유량은 총 당 함량에 대한 비율로 계산하였다. TAPPI T 230 om-08에 의거해 제조된 시료의 점도를 측정하였다. 용해용제에 녹지 않는 불용해 물질의 형태적 특성을 알아보기 위해 광학현미경(BX 50, Olympus Optical Co. Ltd., Japan)을 사용하여 관찰하였다.
2.2.4 Urea/NaOH 수용액에 대한 용해도 측정
미세 잔류물 시료 혹은 아염소산 처리된 미세 잔류물 시료의 용해용제에 대한 용해도를 측정하기 위해 urea/NaOH/water(12 wt%/7 wt%/81 wt%)의 용해용제에 0.5%의 농도로 분산시킨 후, 분산된 현탁액을 -20±5℃ 냉동기에 약 12시간 냉동 후, 상온에서 voltex mixer(G-560, Scientific Industries Inc., USA)를 이용해 5분간 교반하면서 반응시켰다. 이 과정을 MCC가 완전히 용해되어 투명한 용액을 얻을 때까지 반복 진행하였고(4회) 이 4회의 freezing-thawing 기준을 사용하여 미세 잔류물 혹은 아염소산 처리된 시료의 용해도를 평가하였다. Freezing-thawing 4회를 거친 용액을 10,000 rpm에서 10분 동안 원심분리(A32010, LaboGene, Korea)하여 상등액을 분리하였다. 용해되지 않은 물질은 용해용제로 3번 세척 후, 증류수로 여과물이 중성이 될 때까지 충분히 세척해 주었다. 세척이 끝난 불용해 물질은 48시간 동안 동결 건조(TFD5505, ilShinBioBase, Korea)한 후 용해율을 측정하였다. 사용한 전건 무게 대비 불용해 물질의 전건 무게의 역산을 이용하여 용해율을 측정하였다.
3. 결과 및 고찰
3.1 아염소산 처리에 따른 미세 잔류물의 잔존 리그닌
용해용제로 실험에 사용된 urea/NaOH 수용액으로 침·활엽수의 마이크로파 화학적 분산에 의한 미세 잔류물에 대한 용해도를 평가한 연구결과13)에서 잔존 리그닌 함유량에 따른 용해도의 차이를 보였다. 활엽수 유래의 잔류물의 경우 잔존 리그닌 함량이 약 9% 이하일 때, urea/NaOH 수용액에 대한 용해도가 약 50%에서 80%이상으로 급격히 증가를 보이는 반면에 침엽수의 경우에는 잔류물의 잔존 리그닌의 함량이 14-17% 기점에서 용해율이 70% 이상으로 증가하는 경향을 보였다. 이러한 현상은 침엽수 유래 잔류물의 경우 잔존 리그닌의 함량이 용해도를 지배하는 주요한 영향인자로 판단된다.
본 실험에서는 침엽수 유래의 LAS 미세 잔류물을 이용하여 기존의 실험과 유사한 조건 즉, 액비(2:1 HBPS:침엽수 목분), 2% 황산촉매 첨가, 110℃ 반응온도 및 120분 반응시간을 이용하여 잔존 리그닌 함유량이 13%인 침엽수 LAS 미세 잔류물(수율 52.3%)을 제조하였다. LAS 미세 잔류물의 urea/NaOH/water 용해용제에 대한 용해도를 증가시키기 위해 잔존 리그닌의 함량을 조절함으로서 잔존 리그닌 함유량에 따른 사용된 용해용제에 대한 용해도를 평가하고자 하였다. 미세 잔류물의 잔존 리그닌 함량을 3.0%, 6.0% 및 9.0%로 조절하기 위해 온화한 조건에서 잔존 리그닌 함량을 제어할 수 있는 아염소산법을 본 실험의 탈리그닌 방법으로 적용하였다.
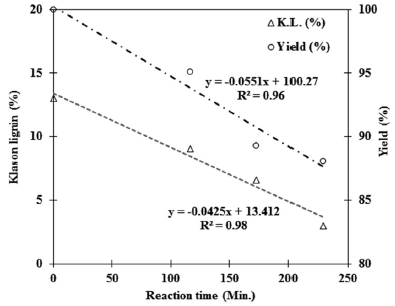
잔존 리그닌 함유량이 3.0%, 6.0% 및 9.0%인 LAS 미세화 잔류물을 얻기 위해 아염소산 처리에 따른 탈리그닌율을 검토하여 Fig. 1에서 보는 바와 같이 아염소산 처리시간에 따른 수율 및 잔존 리그닌 함량에 대한 검량선을 구축하였다. 아염소산 처리 반응시간에 비례하여 탈리그닌 수율 및 잔존 리그닌 함유량이 직선적인 비례 관계(R2 값이 모두 0.96 이상)를 나타냈으며, 구축된 검량선에 의거 3.0% 잔존 리그닌 함유량을 가진 시료는 229분, 6.0%의 경우는 173분, 9.0%의 경우는 117분의 반응시간이 필요하였다. 이때, 예측되는 잔류물의 수율은 각각 88.1%, 89.3% 및 95.1%이었다.
3.2 탈리그닌 처리된 시료의 용해성 평가
Table 1은 검량된 아염소산 반응시간으로 탈리그닌 된 잔유물의 결과를 표시하였다. 처리조건에 따라 모두 86% 이상의 수율을 얻었으며, 아염소산으로 탈리그닌화 시킴으로써 잔존 리그닌 함량이 3.0%, 6.5% 및 9.0%인 시료를 조제하였다. MCC를 대조구로 사용하여 탈리그닌 처리된 시료들과 13.0% 잔존 리그닌 함유량을 가진 LAS 미세화 잔류물의 용해도를 평가하였다.
Table 1.
Sample preparation for dissolution
| Target Klason lignin (%) | Reaction time (min) | Actual Klason lignin (%) | Yield (%) |
|---|---|---|---|
| 3.0 | 229 | 3.0±0.1 | 88.0±2.1 |
| 6.0 | 173 | 6.5±0.2 | 89.2±3.1 |
| 9.0 | 117 | 9.0±0.1 | 95.0±1.2 |
| 13.0 | 0 | 13.0±0.1 | 99.0±1.1 |
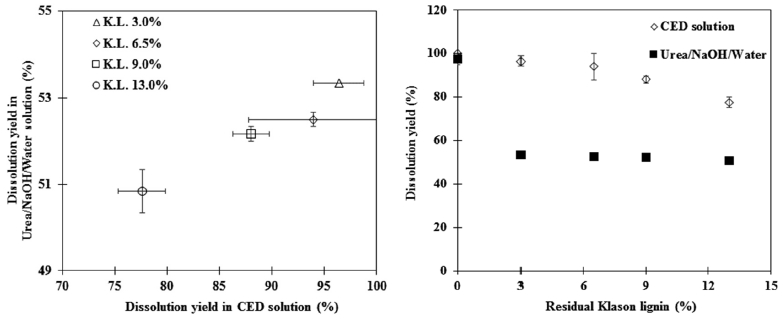
Fig. 2는 CED 용액과 urea/NaOH 수용액의 용해율에 대한 관계를 나타내었다. 침엽수 유래 잔류물의 잔존 리그닌 함유량이 많은 경우 CED 용액에 대한 용해율이 낮았던 이전의 연구결과에 비해13) 아염소산 처리에 의해 잔존 리그닌 함유량을 조절함에 따라 CED 용액에 대한 용해도는 증가하였다. 시료 중 잔존 리그닌의 함유량이 많은 경우에는 잔존 리그닌의 불용해성으로 인해 중합도 측정 시 불용분이 모세관 점도계(capillary viscometer)의 유체 통로를 막음으로써 많은 문제점을 야기하였다. 하지만, 본 연구에서 적용한 방법 즉, 아염소산으로 잔존 리그닌 양을 조절함에 따라 CED 용액에 대한 용해율이 증가하였다. 따라서 CED 용액에 최소 75% 이상의 용해율을 얻었고, 불용분에 대한 농도 보정(원심분리 등의 방법으로 분리·분급) 후, 중합도 측정치를 구하였다. 이러한 방법으로 측정한 중합도를 Fig. 3에 나타내었다.
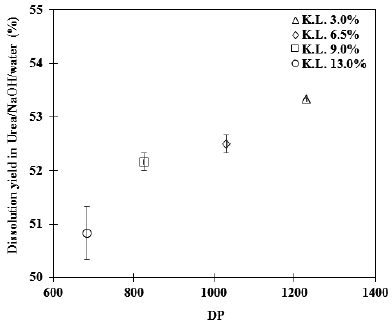
대조구로 사용한 MCC의 경우 CED 용액에 대해 100% 용해되었고, 중합도는 112이었다. LAS 미세화 잔류물(13% Klason lignin 함유량)의 경우 중합도는 633이었다. 하지만, 탈리그닌이 진행됨에 따라 미세 잔류물의 중합도는 점진적으로 증가하였다. 잔존 리그닌의 함유량이 6.5% 이하일 경우에 중합도는 약 1,000 이상으로 증가를 하였다. 이는 헤미셀룰로오스의 중합도가 셀룰로오스에 비해 상대적으로 낮기 때문에18) 비교적 헤미셀룰로오스가 많이 함유된 시료의 경우(13%의 Klason lignin 미세 잔류물) 측정 중합도가 낮게 나타났다고 판단된다. Urea/NaOH 수용액에 대한 용해율은 잔존 리그닌을 제거함에 따라 다소 증가하는 경향을 보이지만, 10%의 탈리그닌 제거율(13% 잔존 리그닌을 함유한 LAS 미세 잔류물 대비 3% 잔존 리그닌 함유 잔류물)에 비해 단지 2.5%의 미미한 용해 증가율을 나타내었다. 이러한 이유는 Fig. 3에서 보는 바와 같이 탈리그닌 처리에 따른 중합도의 상대치가 증가했기 때문이라 판단된다. 중합도 증가와 더불어 Table 2에서와 같이 목분에 비해 LAS 펄프화법에 의해 이미 많은 양의 헤미셀룰로오스가 계외로 용출됨으로써 마이크로피브릴의 재결합으로 인해 용해용제가 세포벽에 대한 접근성(accessibility)이 감소되었기 때문이라 판단된다.17)
Table 2.
Relative neutral sugar content in samples
| Samples | Klason lignin (%) | Total sugar (%) | Relative neutral sugar content (%) | ||||
|---|---|---|---|---|---|---|---|
| Glu. | Man. | Gal. | Xyl. | Ara. | |||
| Wood powder | 29.7 | 57.5 | 70.2 | 17.8 | 3.4 | 7.0 | 1.6 |
| LAS micronized pulp (13% K.L.) | 13.0 | 83.9 | 89.4 | 5.9 | 1.5 | 2.3 | 1.0 |
Fig. 4는 시료를 0.5% 농도로 용해용제에 용해한 후 원심분리를 통해 불용분을 제거하여 얻은 용액(Fig. 4의 왼쪽)과 그 불용분을 동결건조를 시켜 분리한 불용분(Fig. 4의 오른쪽)이다. 잔존 리그닌 함유량이 증가함에 따라 용해액의 색깔이 진한 갈색을 띠고 이에 반해 잔존 리그닌이 없는 MCC의 경우는 투명하다. 또한 불용분 잔사의 경우에도 비슷한 경향을 띠고 있다. 여기서 흥미로운 점은 MCC를 녹인 용해액은 시간이 지나감에 따라 용해된 입자가 서로 재결합함으로써 불투명한 색상을 띠고 3-4일 후에는 겔화(gelation)가 진행되었다. 하지만, 리그닌을 함유하고 있는 용해액의 경우에는 몇 개월이 지나더라도 MCC와 같은 겔화 혹은 상분리(phase separation) 현상을 관측할 수 없었다. 이는 용해용제에 녹아 있는 리그닌이 셀룰로오스의 재결합을 방지하기 때문이라 판단된다.

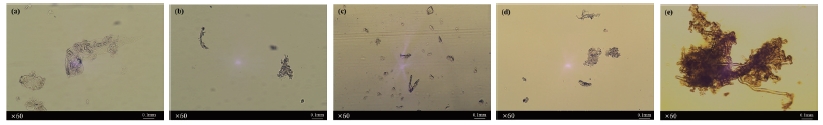
Fig. 4.
Micrographs of 0.5% dissolved urea/NaOH/water solution (left) and insoluble moiety captured by a combination of centrifugation and freezing drying (right) (a: 13% K.L., b: 9.0% K.L., c: 6.5% K.L., d: 3.0% K.L., e: MCC).
Fig. 5는 원심분리와 동결건조를 통하여 얻어진 불용성 물질을 현미경으로 관찰한 결과이다. 잔존 리그닌이 없는 MCC의 경우에는 불용성 물질은 투명하고 무정형이었다. 하지만 리그닌이 3% 함유된 시료의 경우(Fig. 5b), 불용성 물질의 일부는 피브릴 형태(길이 약 170 μm)가 관찰되었고, 리그닌의 함량이 13%인 경우(Fig. 5e) 상대적으로 긴 피브릴이 다발형태로 다량 존재하였다. 이러한 현상은 리그닌이 셀룰로오스 및 헤미셀룰로오스와 공고히 결합되어 있기 때문이라 판단된다.19)
4. 결 론
국내산 소나무를 원료로 하여 LAS 펄프화법으로 미세 잔류물을 제조한 후, 아염소산을 이용하여 미세 잔류물내 잔존 리그닌의 함량을 인위적으로 조절하였다. 13%의 잔존 리그닌 함유량을 가진 잔류물을 3.0%, 6.5%, 9.0%로 제조하여 용해용제에 대한 용해도를 평가하였다. 아염소산 처리 시간이 증가함에 따라 잔류물에 존재하는 잔존 리그닌 함유량이 감소하였지만, 잔존 리그닌 함유량 감소 정도에 비해 잔류물의 urea/NaOH/water 용해용제에 대한 용해도 증가는 미미하였다. 이는 잔존 리그닌이 감소함에 따라 잔류물의 중합도가 증가함으로써 용해용제에 대한 반응성이 감소하였기 때문이라고 판단된다. 대조구로 사용된 리그닌이 존재하지 않는 MCC 용해액의 경우, 시간이 경과함에 따라 겔화현상이 일어난 반면 LAS 미세 잔류물 용해액의 경우 시간이 경과함에 따른 겔화현상이 일어나지 않는 것을 확인하였다. 잔류물의 잔존 리그닌 함유량 및 잔류물의 중합도가 용해도에 영향을 미치는 인자라고 판단이 된다.