1. 서 론
목질 바이오매스는 광합성을 통해서 자연적으로 발생하는 순환 자원일 뿐만 아니라 조림을 통해 지속적으로 생산 가능한 천연자원이다.1-3) 최근에는 펄프를 응용하여 고성능 식품 포장 소재를 생산하거나 나노셀룰로오스를 이용해 식품, 화장품, 또는 제약 분야에서 점도 조절제와 같은 특수한 용도로 활용하는 등 펄프 및 제지 산업을 기반으로 목질 바이오매스는 석유 기반의 고분자와 경쟁력을 가질 만큼 다양한 최종제품으로 변환하고 있다.4-6) 전 세계적인 환경 규제와 친환경 소재에 대한 관심이 급증함에 따라 목질 바이오매스를 기존에 사용하지 않던 새로운 신소재로 제조하고자 하는 다양한 시도가 이루어지고 있다.7-9) 그중에서도 셀룰로오스에 대한 용해 및 응용은 일상생활에서 접할 수 있는 석유계 고분자를 대체할 수 있는 획기적인 대안이 될 수 있다.
셀룰로오스를 용해할 수 있는 용제로써 NaOH/urea 수용액은 비독성이며 경제적인 이점으로 많은 연구가 진행되고 있다.10-12) 그중에서도 Cai 등13)은 urea/NaOH/water (12 wt%:7 wt%:81 wt%) 용해 용제를 통해 urea의 최적 비율을 탐색하였고 셀룰로오스의 동결 및 해동이 반복됨에 따라 용해율을 최대로 높일 수 있다고 보고했다. 셀룰로오스 용해에 사용되는 용해 원료는 비목질 원료인 면섬유부터 리그닌을 함유하는 목재 펄프까지 다양하며 목재 펄프의 경우 중합도, 당 조성 혹은 리그닌 함량에 따른 용해 특성을 다양하게 검토하였다.14,15) 하지만 리그닌을 고함량으로 함유하는 목재 펄프가 용해에 영향을 미치는 요인 및 재생 셀룰로오스의 특성에 미치는 영향은 면밀하게 조사된 바 없다.
따라서 목질 바이오매스를 용해 원료로 사용하는 경우, 대량으로 생산되며 경제성이 확립된 원료인 크라프트 펄프를 이용하거나 반응 과정에서의 변수들을 제거하기 위해 리그닌이 제거된 목질 바이오매스를 이용하는 경우가 많다.16-19) 하지만 용해 원료로써 목재의 약 30%를 차지하는 리그닌을 포함한다면 높은 생산 수율을 가질 수 있으므로 경제성 높은 신소재 원료로 주목받을 수 있다. 그럼에도 불구하고 여전히 목재를 생성하는 주성분은 셀룰로오스이며 용해 및 응용과정에서 응용은 셀룰로오스의 재생(regeneration)에 초점이 있기 때문에 셀룰로오스, 헤미셀룰로오스 및 리그닌에 따른 원료의 특성이 용해 및 재생 셀룰로오스 형성에 끼치는 요인을 검토해 볼 필요가 있다.20,21)
Kim 등의 연구22)에서 유기용매 펄프화법을 통해 친환경적으로 제조될 수 있는 펄프에 대한 다양한 연구가 진행된 바 있다. 또한 잔존 리그닌 함량이 높은 유기용매 펄프를 응용한 용해 원료를 제조하고 NaOH/urea, NaOH/PEG 등 NaOH 수용액에 용해해 그 특성을 평가한 바 있다.23) 유기용매 펄프화법을 응용해 Choi 등24)은 목분으로부터 미세화 시료(micronized-residues)를 제조하고 아염소산을 이용해 잔존 리그닌 함량을 3-13%로 조절하여 NaOH/urea 수용액에 대한 용해성을 평가하였다. 그 결과 잔존 리그닌 함량에 상관없이 NaOH/urea 수용액에서 약 50%의 용해율을 나타낸 것을 확인하였다. 또한 Ryu 등25)은 유기용매 펄프의 잔존 리그닌 함량이 26.8%(unbleached organosolv pulp, UBOP) 및 14.2%(delignified organosolv pulp, DOP)인 것을 용해한 결과, UBOP의 용해율은 50% 이상, DOP의 용해율은 70% 이상 나타난 것을 확인하였다. 이처럼 용해 원료의 형태 혹은 잔존 리그닌 함량에 따라 NaOH/urea 수용액에 대한 용해 특성이 상이하게 발현될 수 있다.
따라서 본 연구에서는 유기용매 펄프화법을 응용해 잔존 리그닌 함량이 높은 목질 미세화 시료를 제조하고, 리그닌을 제거할 수 있는 세척 용제에 따른 용해 특성을 알아보고자 하였다. 그리고 세척 방법에 따른 목질 미세화 시료를 NaOH/urea에 용해하여 재생 셀룰로오스 필름으로 제조하고 그 특성을 검토하였다.
2. 재료 및 방법
2.1 공시재료
본 연구에서는 함수율이 7.2%인 국내산 소나무(Pinus densiflora) 목분을 40-80의 메쉬망(Sieve shaker, CG-211-8, Chunggye, Korea)에 분급하여 사용하였다. Klason lignin 함량은 에탄올-벤젠 혼합용액(1:2, v/v)으로 24시간동안 추출하여 탈지된 시료를 이용해 측정하였으며 28.1%이었다. 산 가용성 리그닌 함량은 0.5%였다.
본 연구에 사용된 반응 시약은 유기용매 펄프를 제조하기 위해 고비점 용매인 glycol ether(extra pure, Dae-jung Chemicals & Metals, Korea)를 사용하였으며, 순도 35%인 염산(extra pure, Daejung Chemicals & Metals, Korea)을 사용하였다.
2.2 세척 방법에 따른 미세화 시료 제조
미세화 시료를 제조하기 위해 목질 바이오매스 반응 시약을 제조하였다. Glycol ether를 용매로 이용했으며 반응 촉매로 염산을 반응 시약의 0.48 mol/L가 되도록 혼합하여 반응 시약을 제조하였다.26) 40-80 mesh로 분급된 소나무 목질 바이오매스와 반응 시약은 1:2(w/v)로 Vortex mixer(G-560, Scientific Industries Inc., USA)를 이용해 충분히 교반하였다. 혼합 시료는 110℃의 오일 베스(AG 9230, BUCHI, Switzerland)에서 120분간 반응되었다. 반응이 종료된 시료는 투입된 원료의 20배에 해당하는 증류수, 0.5N NaOH 수용액, 98% 아세톤 또는 50% 아세톤을 이용해 실험실용 균질기(HG-15A, DAIHAN Scientific Co., Ltd., Korea)에 2,500 rpm으로 5분간 균질화해 필터 페이퍼(No.2, Advantec Co., Ltd., Japan)로 감압 여과하였다. 그 후 증류수를 사용해 여액이 맑아질 때까지 세척 해 105±3℃ 건조 오븐에서 8시간 이상 건조하였다. 여기서 증류수만을 이용해 세척된 미세화 시료는 Water-R, 0.5N NaOH 수용액으로 세척된 미세화 시료는 0.5N NaOH-R, 아세톤으로 세척된 미세화 시료는 Acetone-R, 50% 아세톤으로 세척된 미세화 시료는 50% Acetone-R로 명명했다.
2.3 용해 및 재생 셀룰로오스 필름 제조
총 4종류의 세척 방법에 따라 제조된 미세화 시료는 NaOH:urea:water=7 wt%:12 wt%:81 wt%로 제조된 NaOH/urea 수용액에 용해되어 최종적으로 재생 셀룰로오스 필름으로 제조되었다.13) 미세화 시료의 농도를 5%로 하여 Vortex mixer에 가볍게 교반한 후 –15℃ 조건에서 동결 및 해동 과정을 4회 거쳐 반응을 종료하였다. 그 후 20,000 rpm의 원심 분리를 통해 용해되지 않은 미세화 시료를 분리했다. 용해된 시료는 직경 50 mm의 크기의 유리판에 1 mL의 용해된 미세화 시료 용액을 투입한 후 일부 수분을 증발시키고 5%의 황산 수용액에 투입하여 재생 셀룰로오스 필름을 제조하였다.27) 재생된 필름은 증류수에 충분히 세척한 후 Gel dryer(SE1160-230V, Pharmacla Biotech Inc., USA)에서 40℃에서 6시간 건조하였다. 여기서 증류수만을 이용해 세척된 미세화 시료의 재생 셀룰로오스는 Water-RC, 0.5N NaOH 수용액으로 세척된 미세화 시료의 재생 셀룰로오스는 0.5N NaOH-RC, 아세톤으로 세척된 미세화 시료의 재생 셀룰로오스는 Acetone-RC, 50% 아세톤으로 세척된 미세화 시료의 재생 셀룰로오스는 50% Acetone-RC로 명명했다.
미세화 시료로부터 제조된 재생 셀룰로오스 필름의 인장강도 특성을 비교하기 위해 대조군으로 microcrystalline cellulose(MCC)로 동일하게 재생 셀룰로오스 필름을 제조하였다. NaOH/urea에 대한 MCC의 용해율은 97.5%이었다.
2.4 측정
2.4.1 미세화 시료의 특성
미세화 시료의 특성을 알아보기 위해 세척 방법에 따라 건조된 시료의 무게를 통해 수율을 계산하였다. 세척을 통해 제거된 미세화 시료의 잔존 리그닌 함량은 Klason lignin(TAPPI T 222 om-02) 및 산 가용성 리그닌(TAPPI UM 250)로 측정하였다. 미세화 시료의 당 조성은 alditol-acetate법으로 분석하였다.28,29) 미세화 시료의 점도 평균 중합도(degree of polymerization, DPv)는 TAPPI T 254에 의거하여 Mark–Houwink–Sakurada식인 [η]=0.57×DPv에 의해 계산되었으며 0.57은 CED 용제와 셀룰로오스 사이의 상수이다.
2.4.2 미세화 시료의 용해 특성
세척 방법에 따른 미세화 시료의 용해 특성은 용해율, 재생 셀룰로오스 필름의 인장강도 및 중합도를 통해 분석하였다. 용해율은 용해되지 않은 미세화 시료의 중량을 이용해 측정되었으며 불용해 잔사는 원심분리되었다. 용해 용제 및 증류수를 이용해 불용해 잔사의 pH가 중성이 될 때까지 세척 및 건조하여 중량을 측정하고 원료의 무게를 이용해 계산하였다. 재생 셀룰로오스 필름의 인장 지수는 다음과 같이 수행되었다. 먼저 Caliper (Daeil Machinery CO., Ltd., Korea)를 사용해 필름의 두께를 10회 이상 측정해 평균값을 사용하였다. 시편의 크기는 1×3 cm2로 제조했으며 만능 인장강도 시험기(Hounsfield H500M, England) 측정기 사이의 간격을 1 cm으로 두고 10 mm/min의 속도로 측정하였다. 필름의 인장 강도에 따른 인장 지수는 재생 셀룰로오스의 밀도를 고려해 필름의 인장강도(N)에서 필름의 밀도(g/m3)로 나누어 계산하였다. 재생 셀룰로오스 필름의 중합도는 미세화 시료의 중합도 측정 방법과 동일하다.
3. 결과 및 고찰
3.1 미세화 시료의 특성
미세화 시료의 세척 방법에 따른 수율 및 잔존 리그닌 함량을 Fig. 1에 나타냈다. 증류수만을 이용해 세척된 경우(Water-R) 78.3%의 수율을 나타내며 네 가지 세척 방법 중 가장 높았다. 다음으로 50% 아세톤으로 세척된 미세화 시료(50% Acetone-R)의 수율이 52.4%로 높았고 아세톤으로 세척한 경우(Acetone-R) 42.6%, 0.5N NaOH 수용액으로 세척한 경우(0.5N NaOH-R) 39.3%의 가장 낮은 수율을 나타낸 것을 확인하였다. 0.5N NaOH-R에서 가장 낮은 수율을 나타내는 이유는 세척을 통해 미세화 시료의 리그닌이 제거되었기 때문이다. NaOH 수용액의 경우 리그닌을 용해할 수 있으며 일반적인 크라프트 펄프화 공정에서 리그닌의 추출을 위해 알칼리 수용액을 사용한다고 보고되고 있다.30,31) 또한 아세톤은 리그닌을 용해할 수 있는 용제로 증류수와의 희석 비율에 따라 리그닌을 용해시킬 수 있는 정도가 달라질 수 있다고 보고된 바 있다.32) 이에 따라 50% 아세톤으로 세척된 미세화 시료의 수율은 순도 98%의 아세톤으로 세척된 것보다 약 9.8% 높은 수율을 나타내는 것을 확인하였다.
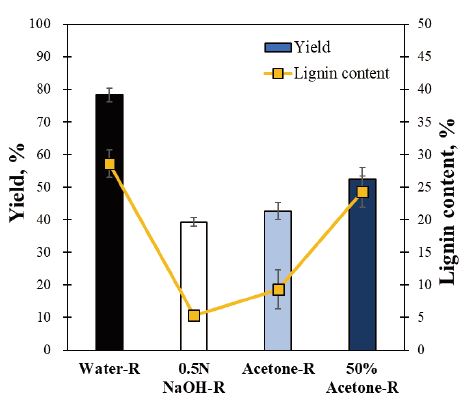
Fig. 1.
Organosolv pulping yield and residual lignin content by final washing treatment (left) bar graph; yield, right) dotted graph; lignin content).
세척 방법에 따른 미세화 시료의 잔존 리그닌 함량은 다음과 같다(Fig. 1 right, Table 1). Water-R은 28.6%로 가장 높으며 0.5N NaOH-R은 약 5.3%로 가장 낮았다. 다음으로 Acetone-R에서는 9.3%의 잔존 리그닌 함량을 나타냈으며 50% Acetone-R은 24.3%로 증류수로 세척된 시료와 유사하게 나타났다. 이와 같은 결과는 전반적인 수율 감소폭과 유사했다. Table 1의 Klason lignin은 세척 방법에 따라 차이가 발생하는 한편, 산 가용성 리그닌의 함량은 전반적으로 큰 차이가 없었다. 이와 같은 결과는 미세화 시료의 산 가용성 리그닌이 Klason lignin과 더불어 정량적으로 증감하는 것이 아니며 세척의 종류에 영향을 받지 않음을 의미한다.
Table 1.
Lignin contents of samples
(Unit: %)
| Water-R | 0.5N NaOH-R | Acetone-R | 50% Acetone-R | |
|---|---|---|---|---|
| Klason lignin | 27.5 | 4.0 | 7.9 | 23.0 |
| Acid-soluble lignin | 1.1 | 1.4 | 1.4 | 1.3 |
| Total lignin | 28.6 | 5.3 | 9.3 | 24.3 |
Table 2는 세척 방법에 따른 미세화 시료의 당 조성 분석 결과이다. Water-R를 기준으로 보았을 때, 0.5N NaOH-R은 글루코만난 및 자일란에서 유래하는 헤미셀룰로오스가 현저히 감소한 것을 확인할 수 있다. 이는 세척되는 과정에서 리그닌에 존재하는 리그닌-탄수화물 복합체(LCC)가 함께 다량으로 추출되었기 때문이다. Fig. 1 및 Table 1의 결과에서도 확인할 수 있듯이 NaOH 수용액으로 세척할 때 가장 많은 리그닌이 제거된 것을 확인할 수 있다. 반면 Acetone-R에서 헤미셀룰로오스가 소폭 감소한 것을 확인하였고 50% Acetone-R에서도 유사한 결과를 나타냈다. 이 역시 아세톤이 리그닌을 용해하면서 일부 당 성분이 빠져나온 것으로 판단되며 Vishtal 등33)에 따르면 아세톤으로 리그닌을 추출하였을 때 알칼리가 첨가된 추출보다 상대적으로 리그닌의 순도가 높다고 보고된 바 있다.
Table 2.
Neutral sugar analysis of samples
(Unit: %)
세척 방법에 따라 추출되는 리그닌의 함량에 차이가 있겠지만 0.5N NaOH 수용액을 사용하면 리그닌이 상당량 제거되는 반면 시료의 당 조성에 변동을 줄 수 있고, 아세톤을 사용하는 경우는 리그닌을 제거하면서도 전체적인 시료의 당 조성을 변화시키지 않는 것을 확인하였다.
3.2 미세화 시료의 용해 특성
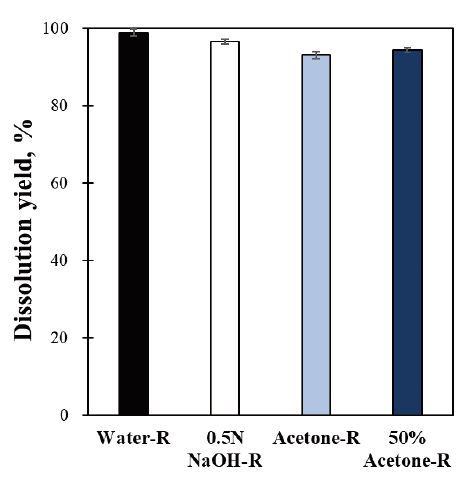
Fig. 2는 세척 방법에 따라 제조된 미세화 시료의 NaOH/urea 수용액 용해 특성을 나타낸 것이다. Water-R의 경우 용해율이 98.9%로 가장 높은 용해율을 나타내었다. Fig. 1 및 Table 1을 통해 알칼리 세척만으로 제거 가능한 리그닌이 존재함을 확인하였다. 따라서 Water-R은 셀룰로오스 용해 용제인 NaOH/urea 수용액에 의해 증류수에 세척되지 않았던 리그닌이 추출되어 높은 용해율을 나타낸 것으로 추측된다. 0.5N NaOH-R 또한 96.5%의 높은 용해율을 나타내며 증류수 세척된 미세화 시료의 용해율 다음으로 가장 높은 용해율을 나타내었다. Acetone-R의 경우에도 93.1%, 50% Acetone-R의 용해율은 91.4%로 전반적으로 90% 이상의 높은 용해율을 나타냈다. Acetone-R의 잔존 리그닌 함량은 9.3%, 그리고 50% Acetone-R의 잔존 리그닌 함량은 24.3%이었다. 따라서 알칼리 수용액 또는 아세톤에 의해 세척되는 리그닌은 NaOH/urea 수용액에 의해 용해될 수 있다고 판단하였다.
Fig. 3은 용해 원료 물질인 미세화 시료(raw materials, R)와 이를 용해해 제조된 재생 셀룰로오스 필름(regenerated cellulose, RC)의 고분자 특성을 알아보기 위해 점도 평균 중합도를 측정한 결과이다(Fig. 3). 먼저 세척 방법에 따른 미세화 시료의 차이는 다음과 같다. Water-R의 점도 평균 중합도는 972.3으로 잔존 리그닌 함량이 7%인 크라프트 펄프의 평균 중합도가 1,300인 것에 비해 높은 잔존 리그닌 함량을 가지면서도 낮은 중합도를 나타냈다.34) 0.5N NaOH-R의 중합도는 667.2로 다른 세척 방법에 비해 크게 감소한 것을 확인하였다. 이와 같은 결과는 리그닌 제거에 따른 결과로 이 과정에서 LCC까지 함께 제거된 것이 용해 원료의 전체 분자량이 감소하는 데에 원인이 될 수 있다고 판단하였다.35) Acetone-R 및 50% Acetone은 모두 약 890으로 증류수 세척 미세화 시료보다는 낮은 수준이지만 0.5N NaOH-R보다는 높아 리그닌 제거에 따른 중합도 차이를 한 번 더 확인하였다.
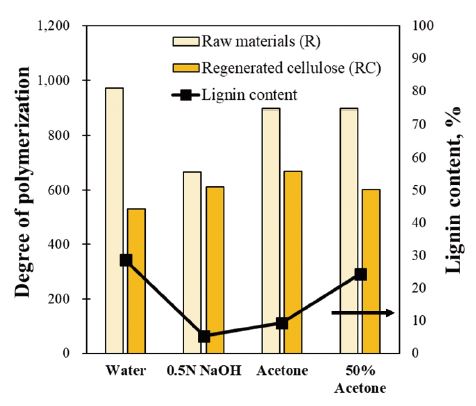
Fig. 3.
Degree of polymerization (DPv) of samples organosolv and its regenerated cellulose film (left) bar graph; degree of polymerization, right) dotted graph; lignin content).
다음은 재생 셀룰로오스 필름의 점도 평균 중합도에 대한 결과이다. 전체적으로 원료의 중합도에 비해 감소하는 경향을 나타냈으며 용해 원료의 중합도와 가장 차이가 많이 나타나는 것은 Water-RC로 용해 원료와 442.8만큼 차이가 나타났다. 반면 용해 원료와 가장 적게 차이가 나타나는 것은 0.5N NaOH-RC로 56.2의 차이로 611.0이 측정되었다. 이와 같은 결과는 용해 원료 중합도의 결과와 비례하여 나타나지 않은 것으로 용해 원료를 구성하는 성분 중에서 용해될 수 있는 것과 재생될 수 있는 것에 차이가 있음을 의미한다. Shi 등34)에 따르면 용해 원료의 잔존 리그닌 함량이 증가하더라도 재생 셀룰로오스의 중합도에는 크게 영향을 주지 않는다고 보고하였다.
Acetone-RC의 중합도는 670.2로 601.6인 50% Acetone-RC보다 높은 중합도의 재생 셀룰로오스 필름을 얻었고 전체 세척 방법 중에서 가장 높게 나타났다. 이때 원료의 잔존 리그닌 함량은 9.3%로 원료의 잔존 리그닌이 중합도 상승에 영향을 끼친 것으로 판단하였고 50%의 아세톤 세척된 시료는 잔존 리그닌 함량이 24.3%로 용해된 리그닌 일부만 재생되었다고 판단하였다. 따라서 용해 및 재생 셀룰로오스를 형성하는 과정에서 재생될 수 있는 리그닌의 분자량이 한정될 수 있다고 판단하였다.16)
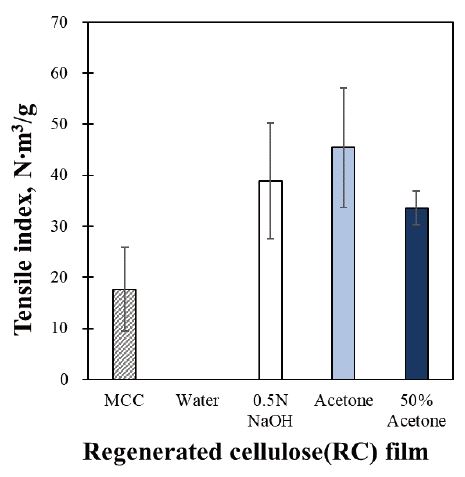
Fig. 4는 세척 방법에 따른 미세화 시료의 재생 셀룰로오스(RC) 필름 인장 지수 특성으로 MCC로부터 제조된 재생 셀룰로오스 필름과 비교하였다. Water-RC 필름은 건조 과정에서 수축으로 인해 인장 지수를 측정하기 위한 시편이 형성되지 않았다. 중합도가 약 100인 MCC로부터 제조된 MCC-RC 필름의 인장 지수는 17.7 N·m3/g이었다. 미세화 시료의 세척 방법 중 Acetone-RC 필름에서 45.4 N·m3/g으로 가장 높은 인장 지수를 나타냈다. Qi 등36)에 따르면 분자량이 증가함에 따라 한계치가 있지만 재생된 필름의 인장강도가 증가한다고 보고하였다. 재생된 미세화 시료의 중합도는 최소 600 이상으로 중합도가 최대 100인 MCC-RC 필름보다 높은 인장 지수를 나타내는 것을 확인하였다. 뿐만 아니라 미세화 시료로부터 제조된 재생 셀룰로오스 필름 내에서도 중합도와 인장 지수에 대해 유사한 경향성을 나타냈다. 따라서 미세화 시료의 세척 방법에 따라 발생하는 재생 셀룰로오스(RC) 중합도 차이가 필름의 인장 지수에 영향을 끼치는 것을 확인하였다.
4. 결 론
유기용매 펄프화법을 응용해 제조된 목질 미세화 시료의 세척 방법에 따른 용해 특성은 다음과 같다. 우선 세척 방법에 따른 목질 미세화 시료의 특성은 다음과 같다. 수율은 Water-R에서 78.3%, 50% Acetone-R에서 52.4%, Acetone-R는 42.6%, 그리고 0.5N NaOH-R에서 39.3% 순으로 나타났고 잔존 리그닌 함량도 유사한 경향성을 나타낸 것을 확인하였다. 미세화 시료의 당 조성 분석 결과, Water-R를 기준으로 0.5N NaOH-R은 리그닌이 제거됨에 따라 헤미셀룰로오스를 포함하는 LCC 역시 함께 제거됨을 확인했으며 Acetone-R 및 50% Acetone-R에서는 헤미셀룰로오스의 함량이 줄어들었지만 비교적 Water-R와 유사한 당 조성이었다.
세척 방법에 따라 제조된 미세화 시료의 NaOH/urea 수용액 용해 특성을 알아보기 위해 재생 셀룰로오스 필름(RC)의 특성을 알아보았다. 점도 평균 중합도를 측정한 결과 원료의 중합도에 비해 감소하는 경향을 나타냈으며 용해 원료 중합도의 결과와 비례하여 나타나지 않았다. 미세화 시료의 재생 셀룰로오스 인장 지수 측정 결과 Acetone-RC 필름에서 가장 높은 인장 지수를 나타냈으며 전반적으로 중합도와 인장 지수에 대해 유사한 경향성을 나타냈다.
따라서 최종적으로 미세화 시료의 세척 방법에 따라 수율, 잔존 리그닌, 당 조성 및 중합도가 변할 수 있음을 확인했으며 최종 생산물인 재생 셀룰로오스 필름의 인장 지수는 원료의 중합도가 아닌 재생된 셀룰로오스의 중합도를 따라 적용되는 것을 확인하였다. 따라서 미세화 시료의 잔존 리그닌 함량을 9.3%까지 낮출 수 있고 높은 중합도를 나타내었던 아세톤 세척 방법을 사용하는 것이 가장 효과적이라고 판단하였다.