1. 서 론
2. 재료 및 방법
2.1 재료
2.2 화학적 미분화
2.3 특성 및 성분분석 방법
3. 결과 및 고찰
3.1 LCMFs의 형태학적 특성
3.2 분획된 리그닌의 화학적 특성
3.3 분획 리그닌의 알칼리성 니트로벤젠 산화물
3.4 분획 리그닌 내 존재하는 중성당 분석
4. 결 론
1. 서 론
석유와 같은 화석 탄소원은 에너지로 사용될 뿐만 아니라 플라스틱과 같은 산업 재료로 소비되고 있다. 지속 가능한 산업 사회를 구축하기 위해서는 석유 화합물을 대체할 수 있는 재생 가능한 친환경 소재를 개발해야 한다는 것에는 모두 동의할 것이다. 이러한 친환경 소재 개발에 있어서 가장 핵심이 되는 원료라 할 수 있는 바이오매스에 주성분 중 하나인 셀룰로오스는 식물 광합성의 결과로 지구상에서 가장 풍부한 천연 고분자이며 재생 가능한 소재로 주목받고 있다.
Zhang 등(2012)1)은 에틸렌 글리콜, 글리세롤, 황산 혼합 용매를 사용하여 유칼립투스 목분의 액화를 시도하였다. 액화 반응 시간과 촉매의 농도에 따라 액화 목재 잔류물의 수율이 달라졌으며 이 때 생성되는 반응물의 주성분 함량을 측정하였다. 그러나 액화 조건은 반응 온도가 매우 높고 반응 시간이 길다는 단점이 있다.
이전의 연구에서는 글리콜 에테르와 산 촉매를 사용하여 저온에서 유칼립투스 목재의 펄프화 가능성을 평가한 바 있다.2) 이 용매를 사용하여 소나무 목분을 마이크로파 조사 하에 단시간 반응시켰을 때, 산 함량이 증가함에 따라 목분의 평균 입자 크기가 작아지는 것을 확인했으며 이를 화학적 미분화라고 보고한 바 있다.3) 또한, 최근 발표한 논문에서는 글리콜 에테르 유기용매 공정에 있어서 반응 조건을 조절하여 제조한 LCMFs(lignocellulosic microfines)의 물리‧화학적 특성을 분석하고 제조된 반응물로부터 알칼리 용해특성을 분석함으로써 용해용 펄프로써의 가능성을 보고한 바 있다.4)
이렇듯 비교적 간단한 방법으로 목재에서 리그닌을 제거하고 목재 세포벽을 동시에 정제할 수 있다면 나노셀룰로오스의 생산이나 셀룰로오스의 가용화를 보다 쉽게 수행할 수 있어 목질계 바이오매스로부터 기능성 소재를 경제적으로 생산할 수 있을 것으로 기대된다.
글리콜 에테르를 이용하여 마이크로파 혹은 autoclave 장비로 화학적 미분화를 통해 LCMFs의 특성을 연구하였던 이전의 연구3,4)와 달리 본 연구에서는 가열 맨틀을 이용하여 동일 반응에 의해 생성된 유칼립투스 LCMFs의 제조 수율을 간단히 비교하고 이 반응에서 회수된 리그닌을 분리하여 그 특성을 분석함으로써 신소재 제조에 적합한 원천 소재로써의 가능성을 탐색하고자 하였다.
2. 재료 및 방법
2.1 재료
본 연구에 사용된 유칼립투스 목재 칩은 성냥개비 모양으로 분쇄되어 있는 것으로써 실험을 실시하기 전에 에탄올-벤젠 혼합용액으로 칩 내에 존재하는 가용성 물질, 유지, 정유 등을 제거하였다. 이후 세척 및 건조된 목재 칩을 실험용 분쇄기(IKA MF 10.1, IKA-Werke GmbH & Co., Germany)를 이용하여 20-60 mesh 크기로 분급하여 본 연구에 사용하였다. Table 1에는 유칼립투스 목분의 기본 정보를 나타내었다.
Table 1.
Basic information of wood meals
| Wood meals | Eucalyptus globulus |
| Size | 20-60 mesh |
| Moisture content | 7.3% |
| Klason lignin | 24.6% |
| Solvent(Et-OH-benzene) soluble | 1.7% |
화학적 미분화를 위해 사용된 고비점 용매인 글리콜 에테르(Pure grade, Sigma-Aldrich Co.)는 이전의 연구5,6)에 사용되었던 것과 동일한 것으로 녹는점은 –80℃이고, 끓는점이 197℃이며 밀도는 0.99이다. 반응 촉매로는 95% 황산(Daejung Chemicals & Metals, Korea)을 사용하였으며 세척 및 리그닌 추출을 위한 에탄올과 아세톤은 Sigma-Aldrich사의 Pure grade 시약을 사용하였다.
2.2 화학적 미분화
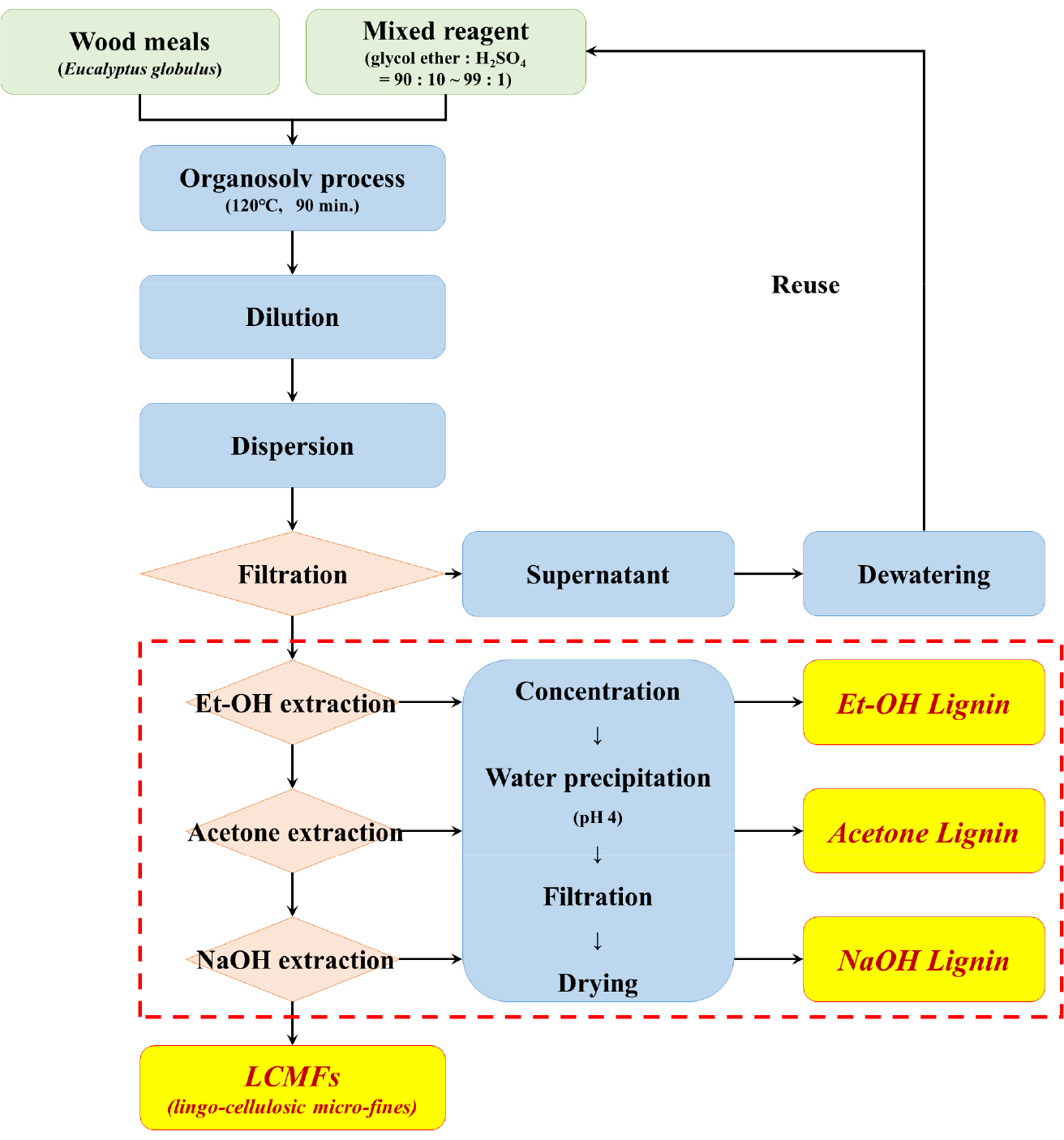
유칼립투스 목분의 화학적 미분화는 Fig. 1과 같이 수행되었다. 5 g의 목분 시료를 1 : 2(w/v)의 비율로 글리콜 에테르 혼합용액(glycol ether : H2SO4 = 90-99 : 1-10, w/w)과 혼합하였다. 글리콜 에테르 혼합물을 가열 맨틀(MS-DMB603, M TOPS®, Korea)에서 120℃로 가열하면서 90분동안 교반하였다. 반응이 완료된 시료들은 300 mL의 증류수를 첨가하여 호모게나이저(WiseTis homogenizer, HG-15A, DAIHAN Scientific Co. Ltd., Korea)로 2700 rpm에서 2분간 분산시킨 후 여과하였다. 이때 여과액은 회수하여 다음 실험을 위해 재사용하였으며 여과 잔류물은 에탄올, 아세톤, 및 0.5N NaOH로 순차 추출을 실시하여 리그닌을 추출하였다. 추출된 리그닌들은 농축과정을 거친 후 500 mL의 증류수에 분산시키고 초산을 이용하여 pH를 4로 조절한 다음 24시간동안 정치시켰다. 이후 침전물들을 여과하여 원심분리 후 최종적으로 리그닌 시료를 획득하였다. 순차 추출 과정에서 잔류물로 얻어진 시료들은 증류수로 충분히 세척하고 건조하여 LCMFs를 얻을 수 있었다.
2.3 특성 및 성분분석 방법
2.3.1 LCMFs의 형태학적 특성 및 입도
LCMFs의 형태학적 특성을 관찰하기 위해 광학 현미경(BX 50, Olympus Optical Co. Ltd., Japan)을 사용하여 60배율 및 150배율로 관찰하였다. 1-10% 촉매를 사용한 organosolv 공정에 의해 제조된 LCMFs의 입도는 이미지 분석기(i-Solution, IMT I-Solution Inc, Canada)를 사용하여 측정하였다.
2.3.2 LCMFs의 수율과 잔존 리그닌 함량
LCMFs의 수율을 측정하고 72% 황산법(Klason lignin method, KL)을 사용하는 TAPPI T 222 om-02에 의거하여 LCMFs의 리그닌 함량을 정량하였다.
2.3.3 IR 분석
용제별로 분획된 리그닌의 IR 스펙트럼은 ATR-IR 분광기(Alpha-P model, Bruker Optics, Germany)로 측정하였다. IR 스펙트럼 범위는 4,000 - 400 cm-1이며 4 cm-1 간격으로 측정되었다. 또한 각 시료당 24회의 반복 스캔을 통해 평균값을 계산하였다.
2.3.4 GPC(gel permeation chromatography) 분석
리그닌의 분자량 분포를 측정하기 위해 RI detector가 장착된 GPC system(Alliance e2695, Waters, USA)을 사용하였다. GPC에 사용된 column은 Waters Styragel HR3, Waters Styragel HR4 및 Waters Styragel HR5E이다. 리그닌을 THF(tetahydrofuran)에 충분히 용해시키고 35℃에서 40분 동안 1 mL/min.의 유속으로 측정하였다. 표준물질은 폴리스티렌(Mw 1060, 1220, 2980, 6940, 18300, 51200, 124000, 326000, 661000)을 사용하였다.
2.3.5 중성당 및 알칼리성 니트로벤젠 산화물 분석
상기의 실험조건에 따라 얻어진 LCMFs와 분획된 리그닌에 대하여 각각 중성당 분석 및 알칼리성 니트로벤젠 산화물 분석을 실시하였다. 중성당 분석의 경우, 알디톨-아세테이트 분석법을 사용하여 GC 분석을 수행하였다.7,8) 알칼리성 니트로벤젠 산화물 분석은 Billa 등(1996)9) 및 Huang 등(2012)10)의 방법에 따라 수행하였다. Table 2는 각 시료의 중성당 분석 및 알칼리성 니트로벤젠 산화물 분석을 위한 가스 크로마토그래피의 조건을 나타내었다.
Table 2.
GC conditions for lignin structure and neutral sugar analysis
3. 결과 및 고찰
3.1 LCMFs의 형태학적 특성
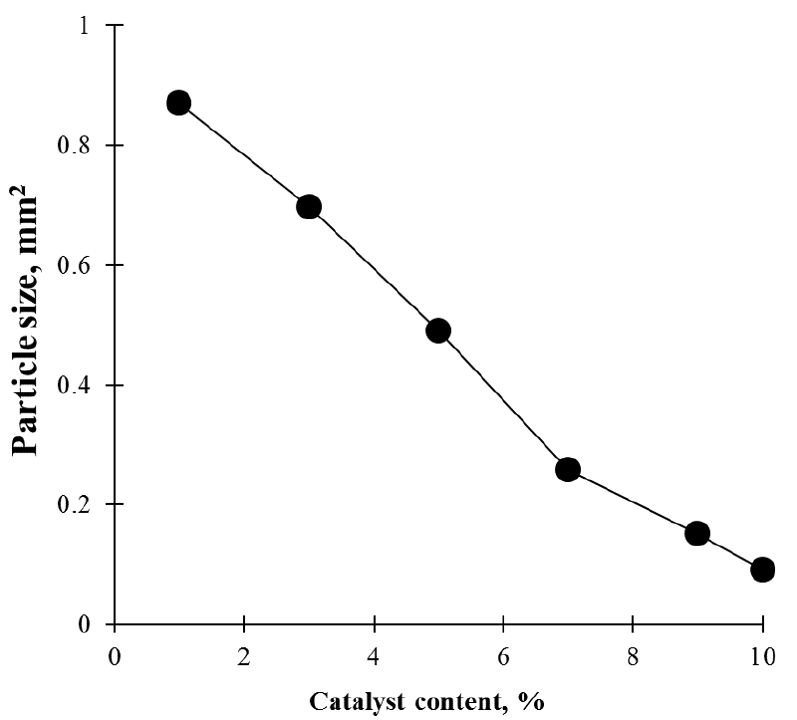
Fig. 2는 120℃에서 90분 동안 다양한 농도의 황산을 함유한 글리콜 에테르와 반응시킨 후 분산된 유칼립투스 목분(LCMFs)의 현미경 사진를 이용하여 이미지 분석으로 측정한 평균 입도를 나타낸 것이다. 이전의 연구3,5,6)에서는 마이크로파 조사 하에서 촉매의 농도와 시간을 달리하여 반응시킨 반응 잔류물의 입도를 측정한 바 있다. 그 결과 촉매 농도와 마이크로파 반응 시간이 증가할수록 입자 크기가 감소하는 것이 확인되었다. 본 연구 결과에서도 산성 촉매의 농도가 증가함에 따라 유칼립투스 목분의 입도가 점차 감소하는 것을 확인할 수 있었다. 또한, Nah 등(2017)의 연구3)에서 20-60 mesh의 소나무 목분을 단시간 동안 마이크로파 반응시킨 후 알칼리로 세척하였을 때 목재 세포벽에서 리그닌이 용출되고 섬유화 되는 결과가 나타났다. 특히, 이 공정은 저온에서 리그닌 제거와 함께 목분의 유기용해가 동시에 이루어지기 때문에 4차산업 신소재로 각광받고 있는 나노셀룰로오스(CNF 또는 CNC) 생산의 원료로 적용할 수 있을 것으로 판단된다.
3.2 분획된 리그닌의 화학적 특성
본 연구의 글리콜 에테르를 이용한 유기용매 반응에서 1 : 2(w/v)의 액비로 인해 반응 초기(10분 경과)에는 목분에 글리콜 에테르 혼합용액의 고른 흡수가 이루어지지 못하였다. 그러나 20-30분이 지나면서 반응물이 검게 변하고 유동성이 증가하게 되었는데 이는 반응물의 색이 검은색으로 변하면서 목분 내의 리그닌이 분해되어 용매로 용출되었기 때문으로 보인다. 진한 검은색의 페이스트(목분 50g)를 약 300 mL의 물에 분산시켜 침전물을 형성하도록 방치한 후, 높은 상등액을 분리하였다. 이를 여과하여 짙은 회색의 침전물(유칼립투스 목분 반응물)을 회수하고 여과액을 농축하여 반응 용액으로 재사용하였다. 이러한 방법을 적용하면 반응에 사용되는 용매와 촉매를 지속적으로 순환시킬 수 있기 때문에 원가 경쟁력이 매우 높다고 할 수 있다. 회색의 침전물을 에탄올로 추출하여 19.3%의 에탄올 리그닌을 획득하였으며, 여기에는 75.6%의 KL을 함유하고 있었다(Table 3). 이후 에탄올 추출 잔류물에서 아세톤으로 추출을 계속 진행하였다. 아세톤으로 추출한 리그닌은 3.7%였으며, 70.3%의 KL을 함유하고 있었다. 즉, 에탄올과 아세톤으로 분리한 리그닌 분획물에는 탄수화물 또는 기타 화합물의 25-30%가 함유되어 있었다고 볼 수 있다. 에탄올과 아세톤으로 추출한 후 잔류물을 다시 0.5 N NaOH로 추출하였다. NaOH 추출 분획의 수율은 5.1%, KL 함량은 57.1%로 측정되었다. 이는 비리그닌 화합물의 약 40%가 리그닌과 함께 추출되었다는 것을 의미한다.
Table 3.
Yield and KL content of solvent extracted residues and LCMFs
나머지 잔류물은 목분의 47.5%, KL 함량은 3.3%로 대부분의 리그닌이 에탄올, 아세톤 및 0.5 N NaOH에서 용출되었음을 시사한다. 글리콜 에테르 유기용매 공정 후 순차적으로 추출하지 않고 0.5 N NaOH로 직접 추출한 후에도 동일한 리그닌 함량의 LCMFs를 얻을 수 있는지에 대한 추가 실험이 필요할 것으로 보인다. 극성이 다른 용매에 의해 용출된 분획물의 화학적 특성은 글리콜 에테르 유기용매 반응의 탈리그닌화 메커니즘을 이해하는 데 도움이 될 것으로 사료된다.
이하의 분석에서는 촉매 농도 3%에서 글리콜 에테르 유기용매 반응에 의해 얻어진 시료들을 대상을 실험을 진행하였다.
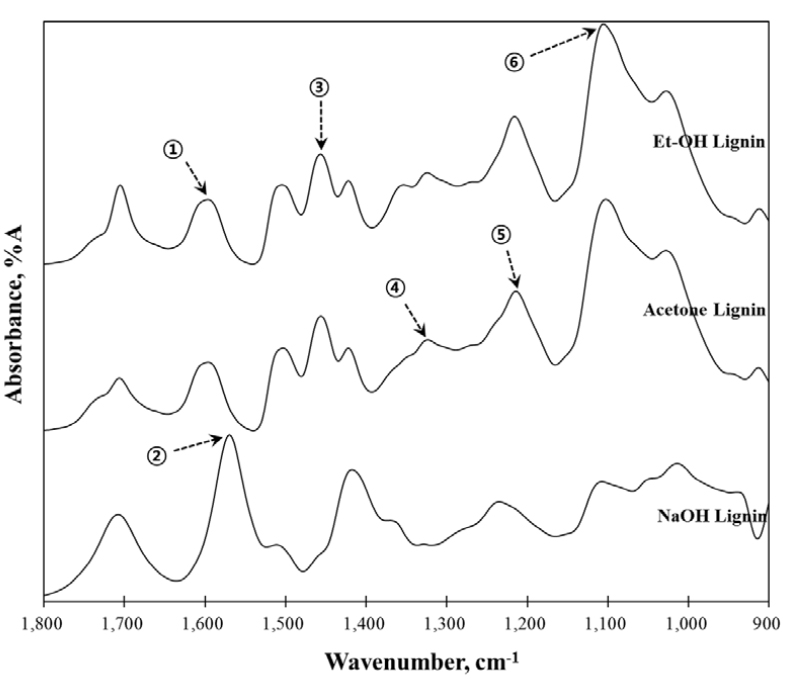
Fig. 3은 다양한 용매로 회수한 리그닌 시료의 IR 스펙트럼을 보여준다. 회수된 리그닌 시료에는 7개의 특징적인 피크가 확인되었다. 이들 IR 피크를 통해 추출 공정별 성분 분리 과정을 추적해 보았다. Table 4는 추출 용매에 따른 리그닌 유래 잔류물의 7가지 피크에 해당하는 성분을 요약한 것이다.
Table 4.
Peak wavenumber of IR absorption bands and their assignments
| Peak number | Wavenumber | Assignment |
| ① | 1,598 cm-1 | Carbohydrates : C=O stretch |
| ② | 1,568 cm-1 | Carbohydrates : C=O stretch (shifted from 1,598 cm-1) |
| ③ | 1,452 cm-1 | Lignin : Asymmetric C-H bending from methoxyl group |
| ④ | 1,324 cm-1 | Lignin : Phenolic OH, S* ring + G** ring condensed |
| ⑤ | 1,208 cm-1 | Lignin : C-O of G ring |
| ⑥ | 1,102 cm-1 | Lignin : G and S, C-H |
1,598 cm-1의 피크는 주로 탄수화물의 C=O 결합에서 유래하며, 시료에 셀룰로오스와 헤미셀룰로오스가 존재함을 확인할 수 있다.11) 또한, 1,568 cm-1의 피크는 1,598 cm-1의 피크와 같이 탄수화물에서 파생된 C=O 결합을 나타내는 것이다.11,12) 즉, 1,568 cm-1의 피크는 NaOH 추출에 의해 1,598 cm-1의 피크로 약간 이동했다고 볼 수 있을 것으로 사료된다. 이러한 결과는 Schwanninger 등(2004)11)과 Široký 등(2010)12)의 연구에서도 언급한 바 있다. 1,452 cm-1 및 1,324 cm-1의 피크는 각각 리그닌의 메톡실기와 페놀성 수산기의 C-H 굽힘진동에 해당하는 피크들이다.13) NaOH 리그닌에서 이 피크의 세기는 에탄올 리그닌 및 아세톤 리그닌의 피크보다 약하게 관찰되었다. 이는 NaOH 리그닌이 에탄올 리그닌이나 아세톤 리그닌에 비해 탄수화물 유래 물질을 다량 함유하고 있음을 시사한다. 또한, 이 결과는 Table 3의 KL 분획 분석 결과와 일치하였다. 1,208 cm-1 및 1,102 cm-1의 피크는 리그닌에서 구아이아실 고리의 C-O 결합과 구아이아실 및 시린길 고리의 C-H 결합을 각각 나타낸다.14,15) NaOH 리그닌의 1,208 cm-1 피크는 에탄올 리그닌 및 아세톤 리그닌보다 약하며, 이는 리그닌의 β-O-4 결합이 상대적으로 감소한 것으로 해석할 수 있다.
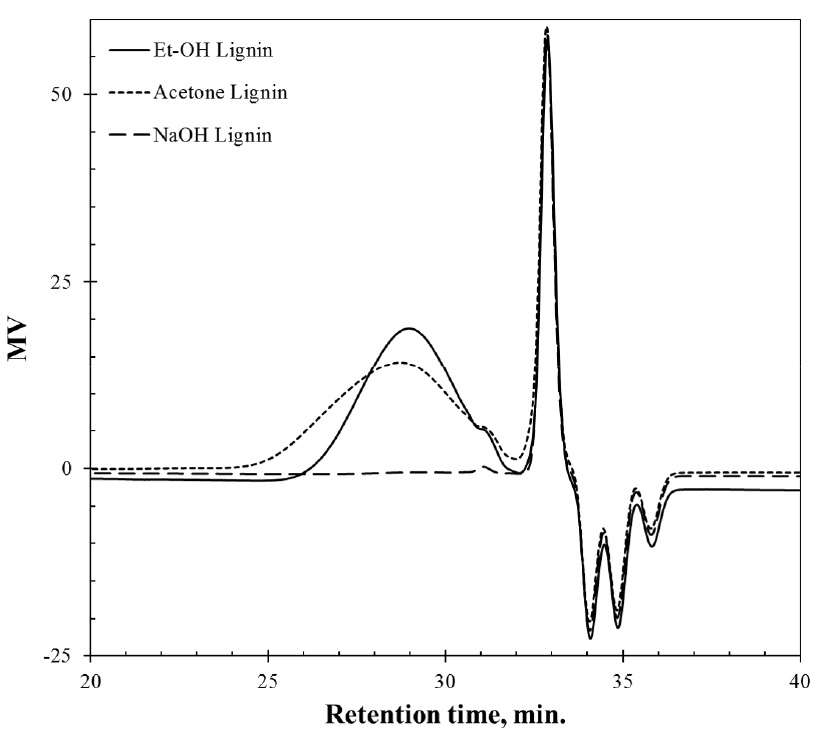
Fig. 4는 용제별로 분획된 리그닌의 GPC 결과를 나타낸 것이다. NaOH 가용분은 리그닌 함량이 약 50%로 다량의 다당류와 리그닌이 매우 밀접하게 존재하고 있음을 알 수 있었다. 따라서, GPC 용매에 충분히 용해되지 않아 GPC에 의한 분자량 분포 곡선이 잘 나타나지 않는 것으로 판단된다. Table 5에서와 같이 아세톤 리그닌의 Mn과 Mw가 에탄올 리그닌에 비해 높게 나타났다. 글리콜 에테르 유기용매 공정에 의해 세포벽에서 용매로 용출된 대부분의 리그닌은 에탄올에 쉽게 용해되어 회수되었다. 그러나 화학적으로 분해되었지만 에탄올에 용해되지 않은 소량의 고분자 리그닌들이 목재의 세포벽에 남아있었다. 이 리그닌들은 다음 용제인 아세톤에 의해 용해되어 회수된 것으로 추정할 수 있다.
Table 5.
GPC results of extracted precipitates (including lignin) according to various solvent
| Sample | Mn | Mw | Polydispersity |
| Et-OH lignin | 2,216 | 2,903 | 1.31 |
| Acetone lignin | 2,692 | 4,064 | 1.51 |
| NaOH lignin | - | - | - |
3.3 분획 리그닌의 알칼리성 니트로벤젠 산화물
유칼립투스 목분과 리그닌 시료의 알칼리성 니트로벤젠 산화 분해 생성물 분석 결과를 Table 6에 나타내었다. 유칼립투스 목분의 알데히드 수율은 KL 기준 50.1%이며 syringaldehyde/vanillin의 몰비는 5.7이었다. 이와 비교하여 용제별 분획 리그닌과 LCMFs의 알칼리성 니트로벤젠 산화 분해 생성물은 매우 낮은 알데히드 수율과 S/V 몰비를 보였다. 이는 아마도 리그닌의 변성, 글리콜 에테르 유기용매 반응에서 황산 촉매에 의한 리그닌의 산화 분해 및 용출과 함께 생성된 라디칼이 수반되는 축합 때문일 것이다.16) 특히, 시린길 핵(syringyl nucleus)에서 β-O-4 결합의 절단 및 축합이 구아이아실 핵(guaiacyl nucleus)의 결합보다 우선하기 때문에 S/V 몰비가 더 낮다는 결론을 내릴 수 있다. 상대적으로 강한 산을 반응 촉매로 사용하기 때문에 리그닌 변성이 심해지는 것으로 예상된다. 따라서, 이 방법으로 얻은 리그닌의 적절한 사용은 축합 정도를 고려하여 결정해야 할 것으로 생각된다. 용매의 극성에 따라 리그닌을 순차적으로 추출하였음에도 불구하고, 알칼리성 니트로벤젠 산화에 의한 분해 생성물의 특성이 잔류 리그닌의 경우와 유사하다는 사실을 자세히 살펴볼 필요가 있다.
Table 6.
Aromatic nucleus of extracted lignins and LCMFs
3.4 분획 리그닌 내 존재하는 중성당 분석
Table 7은 유칼립투스 목분, 분획된 리그닌 및 LCMFs에 포함된 중성당의 함량과 구성 단당류의 상대적 조성 비율을 측정한 결과이다. 목분의 단당류 조성은 유칼립투스 목분의 일반적인 당 조성을 보였으며, 헤미셀룰로오스의 주성분으로 자일란이 확인되었다. 에탄올과 아세톤 리그닌의 KL 함량이 약 70%인 것을 고려하면 총 중성당의 정량값이 다소 낮게 측정되었는데, 이는 글리콜 에테르 유기용매 과정에서 당류가 변성되기 때문으로 추정할 수 있다. 에탄올 리그닌의 자일로스 함량은 아세톤 리그닌의 거의 두 배에 달하는데, 이는 목재 세포벽에서 용출된 자일란이 리그닌보다 에탄올에 우선적으로 용출되었기 때문이다. 다음으로 글루코만난 등과 함께 남아있는 자일란이 아세톤에 의해 용출된 것으로 볼 수 있었다. NaOH 리그닌의 단당류 조성 비율은 아세톤 리그닌의 단당류 조성 비율과 매우 유사하다고 볼 수 있다. NaOH 리그닌의 KL 함량은 약 50%에 불과하지만, NaOH 리그닌에는 변성이 높은 당이 많이 포함되어 있기 때문에 중성당 함량이 매우 낮게 분석되었을 것으로 생각한다. 글리콜 에테르 유기용해 공정을 거친 LCMFs는 대부분이 glucose이며 3.3%의 KL, 세포벽에서 용출되기 어려운 소량의 헤미셀룰로오스로 구성되어 있었다. 따라서, LCMFs는 용해용 셀룰로오스의 제조를 위한 용해특성이 우수한 셀룰로오스 원료가 될 수 있을 것으로 판단되었다.
Table 7.
Total and relative neutral sugar content in lignins and LCMFs
4. 결 론
글리콜 에테르 유기용매 공정에서 목재 성분의 거동을 이해하기 위해 LCMFs와 회수된 리그닌의 화학적 특성을 조사한 결과는 다음과 같다.
동일한 조건에서 산 촉매의 농도가 증가함에 따라 20-60 mesh 크기의 목분이 점점 작아지고 10%의 촉매에서 가장 작은 입도를 보였다. 나머지 잔류물은 목분의 47.5%, KL 함량은 3.3%이었으며, 대부분의 리그닌은 에탄올, 아세톤 및 0.5 N NaOH에서 용출되었다. 리그닌은 황산에 의한 글리콜 에테르 유기용매 반응으로 변성되고 축합되었다. 한편, 글리콜 에테르 유기용매 공정에 의해 제조된 LCMFs는 글루코오스 위주의 단당류가 주로 구성되어 있어 용해용 셀룰로오스 혹은 CNC로써의 적용 가능성이 높을 것으로 보인다.