1. 서 론
식물은 주어진 환경으로부터 어떠한 경우에도 스스로 이동할 수가 없다. 그래서 식물은 환경에 적응하여 생존하거나 생태계로부터 도태되어 사멸한다. 보통 식물은 환경에 잘 적응하며 이러한 능력을 조절하는 유전인자의 실체를 분석하여 파악하는 것은 식물에 관한 이해도를 높이는 측면에서 뿐만 아니라 펄프·제지 산업으로의 이용 측면에서도 중요한 과제이다.1)
우리나라의 펄프·제지 산업은 국제 펄프가 및 국제 유가의 등락폭에 따라 큰 영향을 받고 있다. 이에 전 세계적으로도 목재펄프 대체재로 비 목재펄프의 사용을 많이 시도하고 있다. 비 목재펄프의 이용도 좋지만 국내에서 이용가치가 불분명하여 제대로 사용하지 못하는 생장응력(growth stress) 목재의 이용도 중요하다. 이러한 생장응력 목재는 염분의 노출이 많은 해안가에서 자란 수종, 어떠한 힘에 의해 변형이 되어버린 인장응력 수종 그리고 다른 수목에 가려 태양광을 제대로 받지 못하고 자란 수종 등 다양하다.2,3) 따라서 이러한 생장응력 수목을 활용한 연구의 필요성이 요구되며 이에 섬유 자원으로의 이용 가능성을 확인하기 위한 방법으로 생장응력 수목의 세포벽 성상을 확인할 필요가 있다.
식물이 환경에 적응하여 분화 발달하고 있다는 증거는 식물체 자체인 세포벽이라는 생육의 결과물로서 인식되고 있다. 식물이 환경에 적응하려고 할 때 발현되는 어떤 유전적 형질이라도 그 결과는 세포벽 중에 남게 마련이다. 따라서 특별히 통제된 환경에 적응하여 분화 발달된 세포벽의 이화학적 성상은 식물의 환경 적응 메커니즘을 이해하는데 결정적인 정보를 제공할 수가 있다.3,4)
하지만 식물의 환경 적응에 관련하여 유전자 수준에서의 연구가 과거부터 매우 활발하게 진행되고 있음에 비하여 염 스트레스 등과 같은 비 생물학적 스트레스 환경5-9) 중에서 분화되어 발달된 세포벽의 화학적 성상에 관해서는 2005년 이후에서야 관련 연구가 조금씩 진행되고 있다.
Louis 등(1997)은 식물이 비 생물학적 스트레스인 염에 노출되게 되면 세포내 삼투압의 불균형을 가져오며 이러한 환경에 적응하기 위해 외부의 삼투압 변화에 반응하여 이면성 용질(compatible solute)이라고 하는 삼투물질을 세포내에 축적하게 된다고 보고하였다.10) 이런 삼투물질의 종류에는 Hasegawa 등(2000)의 연구에서 당류(saccharose, polysaccharide), 당 알코올류(glycerol, methylated inositol), 복합 당류(trehalose, raffinose, fructans) 그리고 전하 대사산물(glycine betaine, dimethyl sulfonium propionate, proline, ectoine) 등이 있는 것으로 밝혀졌다.11) 그 중에서도 삼투물질인 D-chiro-inositol과 D-chiro-inositol의 메틸화 형태인 D-pinitol은 식물에서 비 생물학적 스트레스에 의해 생성되고 축적되어 식물에서 스트레스에 대한 저항성을 부여하는 것으로 보고되어 있다.12)
본 연구에서는 비 생물학적 스트레스를 받고 생장한 수목의 섬유 자원화를 위한 기초 연구의 일환으로 고염분의 조건 하에서 생장한 해송 세포벽의 화학적 성상을 비교·분석하였다.
2. 재료 및 방법
2.1 공시재료
본 연구를 위해 Jiang 등(2006)의 연구7)와 같이 무처리(0 mM), 75 mM, 150 mM 및 300 mM의 NaCl을 처리한 상태로 성장한 2년생과 3년생 해송(Pinus thunbergii Parl.)의 줄기를 mixer를 이용하여 60 mesh 이하가 되도록 모두 분쇄하였다.
2.2 실험방법
2.2.1 유기용매 추출 및 리그닌 정량
분쇄한 해송 시료 1 g을 500 mL 삼각플라스크에 넣고 ethanol-benzene 용액(1:2)으로 실온에서 24시간동안 교반한 후 잔사의 중량을 칭량하여 유기용매 추출물을 정량하였고 Klason lignin법에 의하여 불용성 리그닌을 정량하였다.
2.2.2 원소 및 당 조성 분석
해송 시료의 원소조성은 원소분석기(Flash 2000, ThermoFisher, Italy)를 이용하여 C, H, N의 함량을 분석하였으며 alditol-acetate법으로 전처리한 해송 시료의 중성당 조성을 분석하기 위하여 GC-FID(GC-14A, Shimadzu, Japan)를 사용하였다. 중성당 조성 분석을 위해 사용된 GC의 분석 조건은 Table 1과 같다.
3. 결과 및 고찰
3.1 염 처리분 해송의 화학 조성
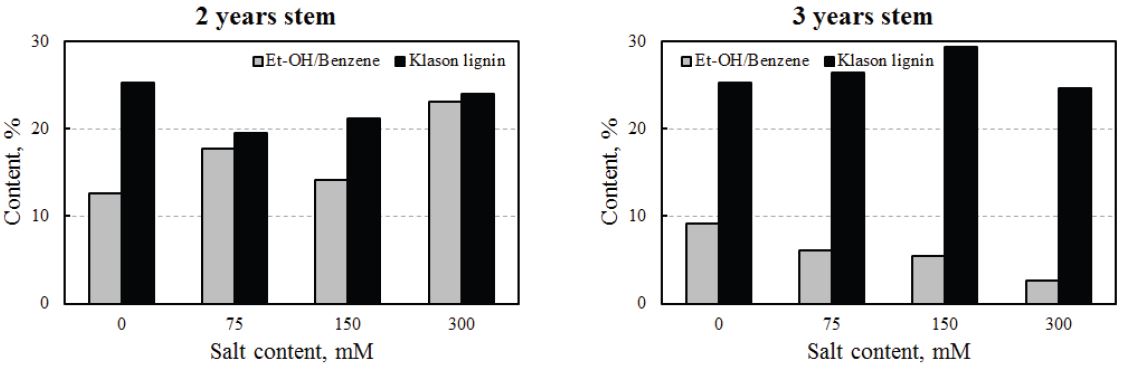
Fig. 1은 2년생과 3년생 염분 처리 해송의 유기용매 및 Klason 리그닌 함량을 측정한 결과이다. 2년생 해송의 유기용매 추출물(가용성 화합물)은 대조구(0 mM)에 비해 전체적으로 상승하는 결과를 가져왔다. 그리고 Klason 리그닌의 양은 대조구에 비하여 높은 하락폭을 보였으며 이는 염분의 농도가 증가함에 따라 상승하였다. 한편, 3년생의 해송은 2년생의 시료와는 달리 유기용매의 양이 대조구보다 감소하였다. 그리고 유기용매의 양이 2년생 해송보다 전체적으로 적게 나타났다. 3년생의 해송에서 Klason 리그닌의 양은 대조구에 비해 염분 처리된 해송이 오히려 더 높게 나타났다. 염분 처리된 2년생 해송은 3년생에 비해 어린 줄기이며 생장이 활발히 일어나고 있어 가용성 화합물(활성 유기물)의 양이 많은 것이며 반대로 3년생의 해송은 2년생의 것보다 어느 정도 성장이 이루어져 유기물보단 리그닌의 변화에 많은 변화가 나타난 것이다. 따라서 고염분으로 생장한 해송을 섬유로 자원화하기 위해서는 기존의 해송보다는 비교적 많은 양의 리그닌을 함유하고 있어 액비, 활성 알칼리 등 펄프화 조건을 신중히 설정할 필요가 있다.
3.2 염 처리분 해송의 원소 및 당 조성
염분 처리를 한 2년생과 3년생 해송의 원소 조성을 나타낸 그래프를 Table 2과 3에 나타내었다. Table 2에서 보면 관수의 염분 농도가 높아짐에 따라 wood meals 내 질소 함량이 낮아지는 것은 매우 흥미로운 결과로서 동시에 탄소함량이 감소하고 수소함량이 증가하는 것으로 Jiang 등7)과 Ashraf 등13)이 연구한 결과와 유사하였다. 한편, Klason lignin 중의 질소 함량이 그다지 변화를 보이지 않거나 wood meals에 비하여 오히려 감소하는 것은 wood meals 내 단백질 유래의 성분이 리그닌과 함께 거동하지 않기 때문으로 생각된다. 통상적으로 목재 내의 단백질이 리그닌과 함께 거동하는 것에 비하여 흥미로운 결과를 보이고 있다. 그리고 wood meals의 탄소 함량과는 달리 Klason lignin 중의 탄소 함량이 증가한 것을 알 수 있는데 이것은 수산기를 많이 갖고 있는 탄수화물이 가수분해 되어 제거되기 때문이다. 질소나 수소의 농도는 미량의 차이가 있으나 주목할 정도는 아닌 것으로 생각된다.
Table 2.
Elemental composition of wood meals and Klason lignins in Pinus thunbergii Parl. of 2 years (%)
| 150 mM | Nitrogen | Carbon | Hydrogen | |
|---|---|---|---|---|
| Wood meals | 0 mM | 0.9 | 45.1 | 3.4 |
| 75 mM | 0.5 | 44.6 | 5.0 | |
| 150 mM | 0.2 | 43.4 | 6.0 | |
| 300 mM | - | - | - | |
| Klason lignin | 0 mM | 0.3 | 60.8 | 5.2 |
| 75 mM | 0.3 | 62.0 | 5.6 | |
| 150 mM | 0.2 | 62.1 | 5.3 | |
| 300 mM | 0.2 | 62.3 | 5.6 | |
Table 3에서도 Table 2의 결과와 마찬가지로 wood meals 내 질소와 수소의 농도변화는 거의 없으나 Klason lignin 중의 탄소는 탄수화물의 가수분해로 인해 농도가 증가한 것을 알 수 있다.
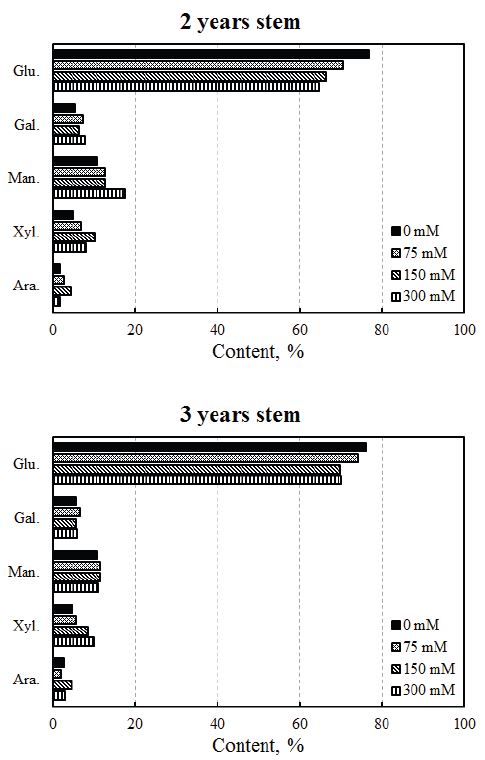
Table 4과 Fig. 2는 NaCl을 농도별로 처리한 2년생과 3년생 해송의 총 중성당의 함량 및 중성당 상대 조성비를 나타낸 결과이다. 2년생 해송 시료는 중성당의 비율이 대조구(0 mM)에 비해 염 처리 목분에서 더 높게 나타났지만 glucose의 경우는 염분의 농도가 높아질수록 감소하는 경향이 나타났으며 이는 Prado 등14)과 Parida 등15)의 결과와 유사하였다. 반면에 xylose와 mannose 경우는 다른 당들에 비해 많이 증가하였다. 3년생의 해송 시료도 2년생의 시료와 마찬가지로 arabinose, xylose, mannose 및 galactose의 함량은 증가하였고 glucose는 염 처리의 농도가 높을수록 감소하는 경향이 나타났다. 2년생 해송의 시료와 같이 xylose의 양이 가장 많이 증가하였다. 이상의 결과에서 알 수 있듯이 염처리의 농도가 높아질수록 셀룰로오스보다 헤미셀룰로오스의 양이 늘어난다는 것을 알 수 있다. 특히, 염분 처리에 의해 xylan 유래의 헤미셀룰로오스의 세포벽 퇴적이 증가하는 것은 흥미 있는 결과이며 염분 처리 해송을 펄프화 재료로 사용할 때 헤미셀룰로오스의 잔존이 펄프 수율 및 이에 따른 경제성 측면에서 중요하다고 볼 수 있다.
3.3 염 처리분 해송의 작용기 분석
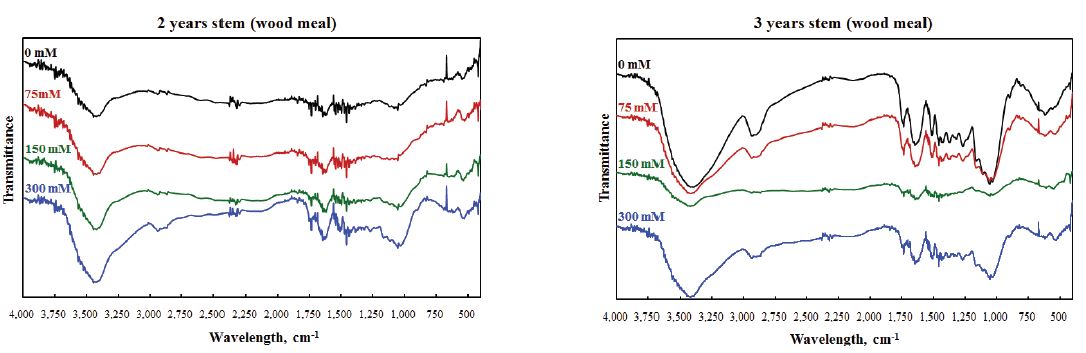
Fig. 3은 2년생과 3년생 NaCl 처리 해송의 FT-IR spectra를 나타내었다. 무처리(0 mM)와 75 mM, 150 mM 및 300 mM NaCl 처리한 시료의 FT-IR spectra는 그 패턴에 있어서 거의 유사하게 나타났으며 대조구(0 mM)에 비해 염분 처리가 된 해송의 1,600 cm-1 부근 흡수가 상대적으로 강해지는 것으로 나타나지만 이것으로 리그닌의 결합구조 변화 등을 유추 해석할 수 없다.
Table 3.
Elemental composition of wood meals and Klason lignins in Pinus thunbergii Parl. of 3 years (%)
| 3 years stem | Nitrogen | Carbon | Hydrogen | |
|---|---|---|---|---|
| Wood meals | 0 mM | 0.4 | 45.3 | 6.4 |
| 75 mM | 0.4 | 44.9 | 6.4 | |
| 150 mM | 0.3 | 44.5 | 6.2 | |
| 300 mM | 0.2 | 44.6 | 6.1 | |
| Klason lignin | 0 mM | 0.3 | 60.6 | 5.3 |
| 75 mM | 0.2 | 61.9 | 5.4 | |
| 150 mM | 0.2 | 61.8 | 5.4 | |
| 300 mM | 0.2 | 61.9 | 5.5 | |
Table 4.
Sugar composition of Pinus thunbergii Parl. of 2 and 3 years (%)
| 2 years stem | Total neutral sugar | 3 years stem | Total neutral sugar |
|---|---|---|---|
| 0 mM | 37.6 | 0 mM | 41.3 |
| 75 mM | 39.0 | 75 mM | 36.6 |
| 150 mM | 39.3 | 150 mM | 41.0 |
| 300 mM | 42.1 | 300 mM | 37.1 |
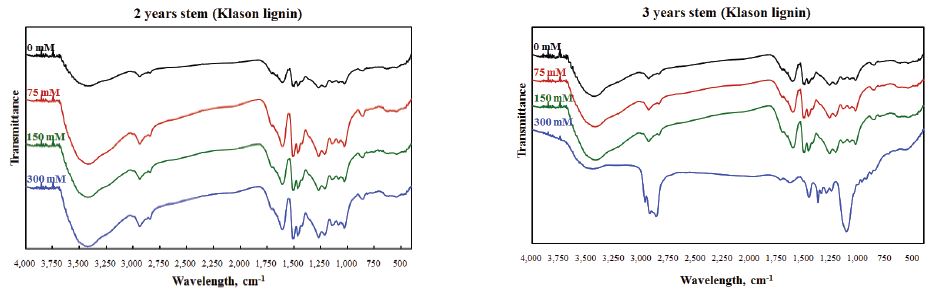
Fig. 4는 2년생 및 3년생 해송을 Klason lignin법에 의해 정량한 후 얻어진 리그닌 시료의 FT-IR spectra를 나타낸 것이다. 목분 시료의 IR spectra와 마찬가지로 무처리 시료(0 mM)와 염 처리 시료의 차이점을 발견할 수가 없다. 그러나 3년생 300 mM 처리 해송 시료에서 1,000–1,250 cm-1 대의 C-O 결합과 2,750–3,000 cm-1 대의 C-H 결합에 유래하는 피크의 흡수가 강하게 나타나고 3,500 cm-1 부근의 O-H 결합에 유래하는 흡수가 감소하는 특이한 결과가 나타났다.
4. 결 론
무 처리, 75 mM, 150 mM, 300 mM의 NaCl 용액을 관수하여 성장시킨 2년생 및 3년생 해송 세포벽의 화학성상을 분석한 결과는 다음과 같다.
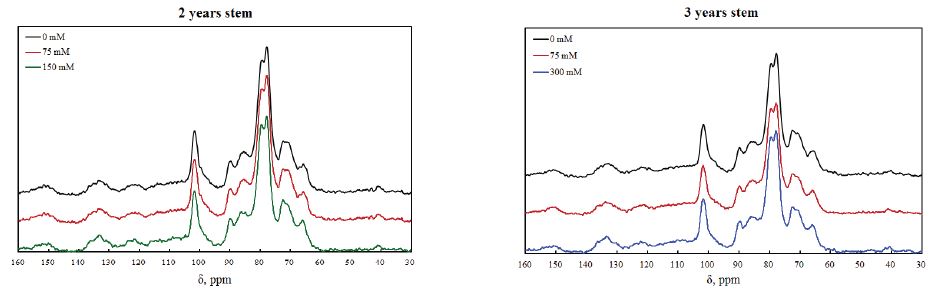
2년생 해송은 유기용매 추출에 의한 가용성 화합물을 많이 함유하고 있으나 3년생은 상대적으로 화합물의 함량이 감소하였으며 리그닌의 함량에는 큰 변화를 보이지 않고 있다. 그리고 2년생과 3년생 해송을 리그닌 정량하면 질소와 수소의 변화는 크게 나타나지 않았지만 탄수화물의 가수분해로 인해 탄소 농도가 증가하는 결과를 보였다. 또한 염분 처리된 해송에서 xylan의 퇴적이 눈에 띄게 증가하였으며 IR spectra에서는 거의 변화가 없었고 NMR spectra에서도 무처리(0 mM) 시료와 Klason lignin 사이에 별다른 차이가 나타나지 않았다. 따라서 염분에 의한 생장응력 수목의 섬유 자원화를 위해서는 액비, 활성 알칼리 등과 같은 펄프화 조건을 재설정할 필요가 있으며 상대적으로 많은 양의 헤미셀룰로오스를 잔존시켜야 경제적인 측면에서 이용 가치가 있을 것으로 보인다.