1. 서 론
최근 급속한 도시화와 산업화에 따라 강, 호수, 바다 등에 배출되는 유기염료로 인한 수질 오염이 심각한 수준이라고 보고되었다.1,2) 유기염료는 섬유, 피혁, 제지, 플라스틱 등의 산업에서 연간 70 만톤이 생산되고 있으며, 그 중 10-15% 가 폐수로 배출되고 있다.1.3) 이렇게 배출된 유기염료는 미생물 분해와 같은 자연 부패과정에서 화학적으로 내성이 강하고 독성이 강한 특성을 가진다.2.4) 본 연구에서 사용한 Brilliant Green (BG)은 다양한 목적으로 사용되는 일반적으로 알려진 양이온성 유기염료 중 하나이고 섬유 염색 및 종이 인쇄뿐만 아니라 생물학적 착색, 피부과학, 수의학, 그리고 곰팡이나 균류, 장에 기생하는 기생충의 번식을 억제하는 첨가제 등 다양한 용도로 사용되고 있다.4,5) 그러나 BG는 독성을 가지고 있고, 피부 접촉 및 섭취의 경우 설사와 구토, 메스꺼움 같은 증상을 일으킨다.3,4) 특히 흡입의 경우 폐에 유독하여 기도 이상을 일으킨다.3,5) 게다가 BG는 열분해가 된다면, 이산화탄소, 일산화탄소, 황산화물 및 질소산화물 등을 생성할 수 있기 때문에 제거 기술을 필요로 한다.5) 따라서 최근에 이러한 유기염료를 효과적으로 제거하는 기술이 전 세계적으로 주목받고 있으며, 많은 과학자들이 폐수에서 유해물질을 효율적으로 제거하기 위해 친환경 소재를 이용하는 저가의 바이오 흡착제를 개발하고 있다.5)
리그닌은 식물의 주요 성분 중 하나이며, 기본적으로 페닐프로판(C6-C3) 기반의 천연 방향족 고분자이다. 리그닌은 지구상 유기 물질의 약 30%를 차지하고, 친환경적이고, 지속가능한 자원으로 연구가 활발하게 진행되고 있다.6) 또한 리그닌은 페놀, 하이드록실, 카복실, 벤질 알코올, 메톡실, 알데하이드와 같은 다양한 작용기를 가지고 있고,6-8) 랜덤한 가교된 리그닌으로 3차원 구조를 가지고 있기 때문에 잠재적인 저가 흡착제로 사용될 가능성이 충분하다. 그러나 개질되지 않은 리그닌은 다른 흡착제에 비하여 흡착 능력이 뛰어나지 않은 것으로 나타났다.9,10) 따라서 리그닌의 화학적 개질, 즉 효과적인 작용기를 도입하는 것은 흡착능력을 증가시키는 유망한 기술로 간주된다.8,11) 특히 아민기는 전기음성도가 높은 원자인 질소를 함유하고, 비공유 전자쌍을 가지므로 양성자화가 되기 쉽고, 수소결합을 유도할 수 있는 작용기로써 pH에 따라 염료와의 다양한 상호작용이 이루어지기 때문에 흡착제 개발에 있어서 중요한 작용기로 알려져있다.12,13) 따라서 리그닌에 아민기를 도입하고 염료 흡착 효율 및 흡착제로서의 활용 가능성을 알아보고자 하였다.
이 연구에서 amino-silane modified lignin (AL)은 amino-silane을 이용하여 amine-silanization 반응에 의해 제조되었고, AL의 화학 구조는 gel permeation chromatography (GPC), fourier-transform infrared (FT-IR) spectroscopy, X-ray photoelectron spectroscopy (XPS)을 통해 분석되었고, 물리적 특성은 열중량 분석, 입자크기 분석 및 표면전하를 측정하여 확인하였다. 또한 BG에 대한 AL의 흡착 거동을 조사하였고, 그리고 흡착제 투여량, 침전시간 및 pH 조건들을 달리하여 염료의 제거 효율에 미치는 영향을 평가하였다. 추가적으로 Langmuir, Freundlich, 및 Temkin model을 사용하여 흡착 등온선 분석을 하였고, 흡착 동역학 분석 및 열역학적 분석을 수행하였다.
2. 재료 및 방법
2.1 공시재료
본 연구에서 사용한 리그닌은 kraft lignin으로 국내 M 사로부터 제공받았고, kraft lignin으로부터 methanol에 용해되는 methanol lignin (ML)을 분리하여 사용하였다.8) AL을 합성하기 위해서 (3-aminopropyl)trimethoxysilane (APTMS, 97%)을 Sigma-Aldrich (USA)에서 구입하였고, 용매로 사용된 anhydrous toluene (99.8%)은 Daejung Chemicals & Metals Co. Ltd. (Korea)에서 구매하여 사용하였다. 염료 흡착에 사용되는 염료는 Sigma-Aldrich (USA)의 Brilliant green (BG, dye content: ~90%)을 사용하였다. GPC 용매로 사용된 N,N-dimethylformamide (DMF, 99.5%), lithium bromide anhydrous (LiBr, 98%)은 Daejung Chemicals & Metals Co. Ltd. (Korea)에서 구매하여 사용하였다. 또한 3차 증류수기(Human RO-180, Human, Korea)로 제조한 탈 이온수(deionized water)를 실험에서 사용하였다. 구매한 모든 화학 물질은 추가 정제 없이 사용되었다.
2.2 실험방법
2.2.1 Amino-silane modified lignin (AL) 제조
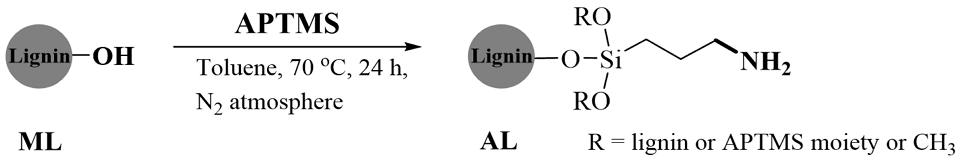
AL 제조는 Scheme 1과 같이 한 단계 반응으로 수행하였다.8) 250 mL 둥근 플라스크에 2 g의 ML을 anhydrous toluene (100 mL)과 혼합하고, 초음파 세척기(JAC-5020, KODO, Korea)를 통하여 500 W의 초음파 출력과 40 kHZ의 주파수에서 약 15분간 ML을 충분히 분산시켰다. 이후 질소가스 치환을 실시하고 APTMS를 제각각 8 mmol, 12 mmol, 18 mmol을 서서히 첨가하였다. 이후 70℃에서 24 h 동안 350 rpm의 속도로 자석 교반을 유지하며 환류 장치를 이용하여 환류하였다. 반응 종료 후, 반응물을 ice-bath를 이용하여 냉각시키고, filter paper (F2040, CHMLAB®, φ 90 mm)를 이용하여 여과시켰다. 미반응 APTMS을 제거하기 위하여 toluene으로 여러 번의 세척 과정을 거치고, 이때 형성된 고형분(amino-silane modified lignin)을 72 h 동안 40℃의 진공 오븐에서 건조시켰다. 이때 8 mmol의 APTMS와 반응이 진행된 리그닌을 AL-1, 12 mmol의 APTMS와 반응이 진행된 리그닌을 AL-2, 18 mmol의 APTMS와 반응이 진행된 리그닌을 AL-3이라고 명칭하였다.
2.2.2 Amino-silane modified lignin (AL) 화학적·물리적 특성 분석
모든 리그닌 샘플은 화학적 작용기 및 구조 분석을 하기 위하여 attenuated total reflectance attachment (ATR)가 장착된 FT-IR spectroscopy (Nicolet Summit, Thermo Fisher Scientific, USA)를 이용하였다. 모든 리그닌 샘플은 완전하게 건조하여 파우더 형태로 측정을 진행하였으며, 조건은 4000~500 cm-1 범위의 wavenumber에서 64회 스캔을 진행하였다.13,15)
추가적으로 다양한 리그닌 샘플의 표면 원소 함량 및 다양한 공유 결합들을 분석하기 위하여 XPS (K Alpha+, Thermo Scientific, U.K.)을 분석하였고, dwell time 30 ms, 50 eV의 pass energy와 시료당 30회 스캔하여 측정하였다.
리그닌 샘플의 분자량 분석은 1 mg의 리그닌과 1 mL을 0.1% DMF-LiBr에 용해 후 GPC (Shimadzu-20A, Japan)으로 분석하였다. 분자량 분석에서 PLgel 5-μm mixed-C and -D, PLgel 3-μm mixed-E이 장착된 GPC column을 사용하였고, UV detector 파장은 280 nm, Injection volume은 100 μL로 설정하였으며 flow rate 100 mL·min-1의 조건 하에 DMF/LiBr를 이동상으로 사용하였다.13,14) 분자량의 범위가 1,480∼1,233,000 g·mol-1인 polystyrene으로 calibration 검량선을 작성한 후 분자량 분석을 수행하였다.
열 안정성을 분석하기 위하여 열중량 분석기(Thermogravimetric analyzer, SDT Q600, USA)를 사용하였고, 질소 분위기하에서 측정을 수행하였다. 측정 조건은 질소 유속을 100 mL·min-1으로 하였고, heating rate 10℃·min-1으로 진행하였으며, 25℃부터 700℃까지 열을 가하였다.16)
모든 리그닌 샘플의 입자 크기분포는 레이저 회절 입도 분석기(Mastersizer 3000, Marvern Panalytical Ltd., Netherlands & UK)를 사용하여 분석하였다. 리그닌 샘플의 표면전하를 측정하기 위하여 Zetasizer Nano S (Malvern Instruments, UK)을 사용하였다. 리그닌을 0.001 M NaCl 수용액에 0.025%, w/w으로 분산시켰고, pH를 0.1 M HCl 및 0.1 M NaOH 수용액으로 적정을 하여 pH 3-10 범위에서 제타 전위를 측정하였다.13,17)
2.2.3 BG 염료의 흡착 특성 분석
AL-3의 BG 흡착 성능을 알아보기 위하여 흡착량을 평가하였다. 속도와 온도를 고정할 수 있는 shaking incubator (IST-4075, JEIO TECH, Korea)에서 실험을 수행하였고, 25℃ 에서 200 rpm의 속도로 반응을 진행하였다. 또한 pH에 따른 흡착 능력을 관찰하기 위하여 0.1 N HCl 수용액와 0.1 N NaOH 수용액을 이용하여 pH를 조절하였다. 반응 후에 원심분리용 튜브에 용액을 옮긴 후 원심분리기(Hanil, MF550, Korea)를 이용하여 10000 rpm, 5 min 조건에서 원심분리를 진행하였다. 이때 형성된 상등액을 샘플링하고, UV-Vis spectrometer(UV-2550, Shimadzu, Japan)를 이용하여 최대 흡수 파장 624 nm에서 흡광도를 측정하였고 다음 Eq (1-2)에 따라 염료 제거 효율을 결정하였다.
여기서 Q는 흡착량 (mg·g-1)이며, E는 흡착 효율(%)을 나타내고, Ci와 Cf는 BG의 초기 농도와 흡착 후 농도를 의미한다. V는 BG 용액의 부피(L), M은 흡착제의 무게(g)를 의미한다.
2.2.4 흡착 등온선, 흡착 동역학 및 열역학적 분석
흡착 등온선, 흡착 동역학, 및 열역학적 분석은 최대 BG 흡착량, 흡착 반응 속도식, 흡착공정의 과정을 탐색할 수 있는 분석이며, 흡착 메커니즘을 조사하는 데 효과적인 방법이다. 흡착 등온선 분석은 Langmuir, Temkin, 및 Freundlich 등온선을 사용하여 분석하였다. 선형 Langmuir, Temkin, 및 Freundlich 흡착 등온선은 Eq (3-5)에 따라 계산되었다.
여기서 qe는 평형 흡착 용량(mg·g-1)이고, Ce는 평형상태에서의 흡착물 농도(mg·L-1), qm은 최대 흡착용량(mg·g-1), KL은 Langmuir 상수, KF와 n은 Freundlich 상수를 나타낸다. Temkin 등온식의 B=RT·bt-1, bt (kJ·mol-1)이고, KT (L·mg-1)는 흡착열 및 평형 결합 상수와 관련된 Temkin 상수이다. R (8.314 J·mol-1·K-1) 및 T (K)는 각각 기체 상수 및 절대 온도를 나타낸다.
흡착 동역학 분석은 pseudo-first-order kinetic (PFO) 및 pseudo-second-order kinetic (PSO)을 사용하였다. 흡착 동역학 분석은 반응 시간에 따른 BG 흡착량 분석을 통해 얻은 데이터 기반으로 분석하였다. 선형 PFO 및 PSO는 Eq (6-7)에 따라 분석되었다.
여기서 qe는 평형 흡착 용량(mg·g-1), qt는 시간 t (min)에서의 흡착 용량(mg·g-1), k1 및 k2 (g·mg-1min-1)는 각 PFO 및 PSO의 동역학 속도 상수를 나타낸다.
열역학적 분석은 흡착과정에서 온도의 영향을 나타낸다. 이는 100-200 mg·L-1의 BG 용액과 AL-3를 혼합하고 각 다른 온도인 298.15-333.15K에서 열역학적 흡착 실험을 수행하였다. 표준 자유 에너지(ΔG°), 엔탈피(ΔH°), 엔트로피(ΔS°)의 변화와 같은 열역학적 매개변수는 다양한 온도에서 측정된 데이터로부터 Eq. (8-10)을 이용하여서 분석되었다.
여기서 Kd는 서로 다른 온도에서 ln(qe/Ce) 흡착 분포 계수이며, ΔH° (kJ·mol-1)는 표준 엔탈피 변화, ΔS° (J·mol-1·K-1)은 표준 엔트로피 변화, ΔG° (kJ·mol-1)는 표준 자유 에너지 변화, R (8.314 J·mol-1·K-1)은 기체 상수, T (K)는 각각 절대 온도를 의미한다.
3. 결과 및 고찰
3.1 Amino-silane modified lignin의 화학적 물리적 특성 분석
3.1.1 Amino-silane modified lignin의 원소 함량 및 분자량 분석
제조된 AL의 수율, 원소 함량 및 분자량 분석은 Table 1에 나타내었다. 수율은 AL-1, AL-2 그리고 AL-3은 각 2.44, 2.48, 및 2.54 g으로 나타났고, APTMS의 첨가량이 증가함에 따라 수율이 증가하는 것으로 나타났다. 아민화-실란화 반응 후 원소 함량의 변화가 나타났고, 각 AL-1, AL-2 및 AL-3의 질소 원소 함량이 3.3, 8.8, 10.2%으로 나타났으며, 이는 APTMS의 첨가량이 증가함에 따라 질소 원소 함량이 비교적 증가하는 경향이 확인되었다. 추가적으로 Si의 원소 함량을 분석해본 결과, AL-3의 Si의 표면 원소 함량은 11.83%으로 상당히 높은 함량으로 나타났다. 리그닌의 분자량은 수 평균 분자량(Mn) 및 중량 평균 분자량(Mw)으로 계산되었다. ML의 수평균 분자량은 5,000 g·mol-1, 중량 평균 분자량은 7,500 g·mol-1으로 나타났다. Amine-silanization 후의 AL은 모두 수평균 분자량과 중량 평균 분자량이 증가하였고, AL-1 < AL-2 < AL-3 순으로 큰 분자량을 가지는 것으로 확인되었다. 따라서 APTMS의 첨가량에 따라 수율 증가, 질소 원소 함량의 증가 및 분자량의 증가를 통해서 ML과 APTMS 분자 간의 반응이 성공적으로 이루어졌다고 생각되었다.
Table 1.
Yields, surface elemental atomic ratio, and molecular weight of ML and ALs
| Entry | Yield (g) | Surface elemental content | Molecular weight | |||||
|---|---|---|---|---|---|---|---|---|
| C (%) | N (%) | Si (%) | Mn (g·mol-1) | Mw (g·mol-1) | PDI | |||
| ML | NA | 76.30 | 0.76 | NA* | 5,000 | 7,500 | 1.50 | |
| AL-1 | 2.44 | 70.14 | 3.34 | 3.43 | 6,100 | 9,900 | 1.62 | |
| AL-2 | 2.48 | 57.16 | 8.80 | 10.49 | 6,400 | 9,900 | 1.54 | |
| AL-3 | 2.54 | 53.55 | 10.21 | 12.38 | 6,500 | 10,000 | 1.54 | |
3.1.2 Amino-silane modified lignin의 화학적 특성 분석
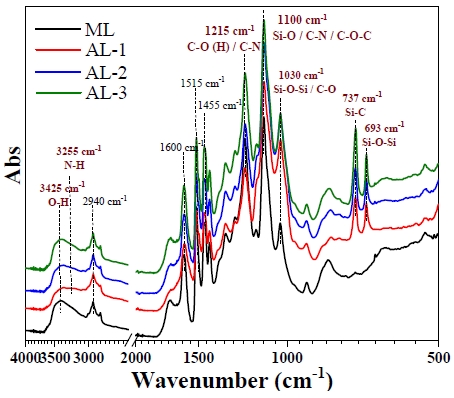
모든 리그닌 샘플들의 작용기를 분석하기 위하여 FT-IR spectra를 Fig. 1에 나타내었다. ML은 약 3,400 cm-1 부근에서 특징적인 -OH의 피크가 관찰되었고,18) 약 1,600 cm-1에서 benzene ring (C=C)에 해당하는 피크가 나타났다. 추가적으로 강한 세기로 나타나는 약 1,100-1,030 cm-1의 피크는 C-O-C와 C-O 결합에 기인되는 것으로 사료되었다.18,19)
아민화-실란화 반응 후 AL의 경우 ML과 비교하였을 때, 특징적으로 -OH의 피크 세기의 감소가 관찰되었고, 새로운 약 3,255 cm-1의 피크가 확인되었다. 약 3,255 cm-1의 피크는 리그닌의 -OH과 APTMS의 축합반응으로 인해 도입된 amino-silane에 해당되는 -NH2으로 판단된다.20,21) 추가적으로 특징적인 피크는 약 1,100과 1,030 cm-1부근에 피크의 세기가 강해진 것으로 확인되었고, 이는 C-O-C, C-O 결합뿐만 아니라, amino-silane에 존재하는 Si-O, C-N, 및 Si-O-Si 결합에 기인된 것으로 사료된다.20,21) 약 737, 693 cm-1에서 뚜렷한 새로운 두 피크가 확인되었고, 이는 Si-C와 Si-O-Si 결합에 기인된 것으로 확인되었다.12) 결과적으로 감소된 -OH 피크, 새롭게 관찰된 -NH2, Si-C, 및 Si-O-Si 피크는 ML의 -OH에 APTMS가 성공적으로 도입되었다고 판단된다.
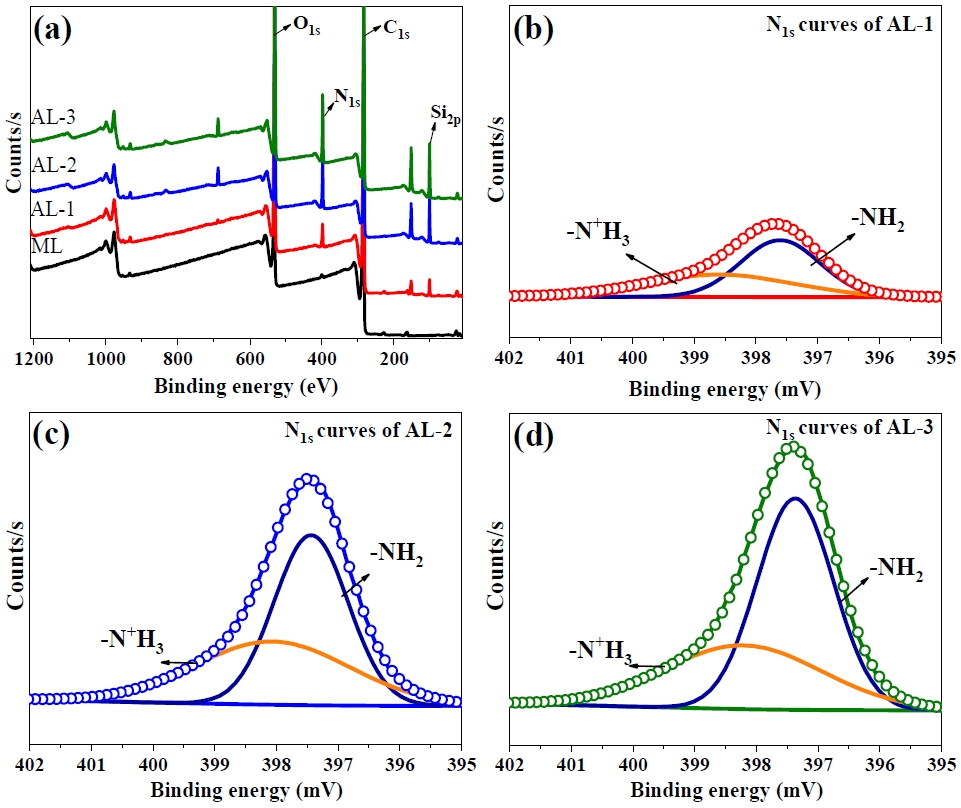
리그닌 샘플의 XPS spectra를 Fig. 2에 나타내었다. Fig. 2(a)는 각각 ML, AL-1, AL-2 및 AL-3의 XPS survey scan spectra를 나타내었다. 모든 리그닌 샘플에서 C1s(285eV) 및 O1s(531eV)에 해당하는 두 개의 주요 피크가 관찰되었고,22) amine-silanization 후, 400 eV 및 101 eV에서 두 개의 새로운 피크가 AL의 스펙트럼에 나타났으며, 각각 N1s 및 Si2p에 할당되었다.13) XPS 스펙트럼에서 N1s 와 Si2p의 피크 세기는 AL-3가 가장 강하게 나타나는 것을 확인하였고, 이는 APTMS의 도입이 상대적 많음을 나타내고, 리그닌과 amino-silane의 결합이 상대적으로 많다는 것을 의미한다. 또한, 얻어진 N1s core level spectra는 두 개의 피크로 분리할 수 있고, 그 결과는 Fig. 2(b)-2(d)에 나타내었다. 두 개의 피크 분리는 약 398.7 eV 및 400.0 eV으로 각각 아민기(-NH2) 및 양성자화된 아민기(-NH3+)에 할당되었다.13,23) 결과적으로 FT-IR 분석 및 XPS 분석을 통하여 AL의 합성은 성공적인 것으로 사료되었다.
3.1.3 Amino-silane modified lignin의 물리적 특성 분석
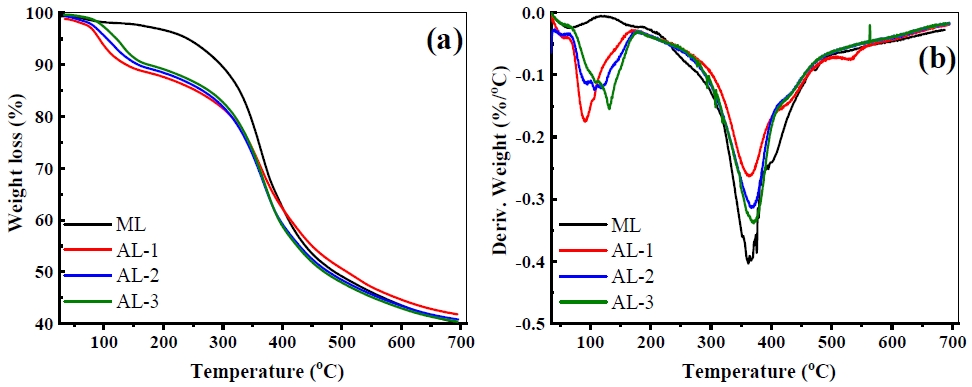
리그닌 샘플의 열분해 거동을 파악하기 위해 열중량 분석을 수행하였다. Fig. 3(a)-3(b)에는 thermogravimetric analysis (TGA) 및 derivative thermogravimetric analysis (DTG) 그래프를 나타내었고, Table 2에 최대분해온도(Tmax)를 나타내었다. Fig. 3(b)에 해당하는 DTG 그래프에서, 0∼100℃의 분해는 물의 증발로 인한 열 중량 손실이고, ML의 경우 열분해가 주로 300∼450℃에서 진행되었다. AL의 열분해는 주로 두 단계로 나타났고, AL의 열분해의 첫 단계는 100∼200℃ 사이에서 확인되었다. 이는 ML에서 없는 열분해임으로써 amino-silane unit의 열분해에 기인하는 것으로 판단되었다. 또한 두 번째 단계는 300∼450℃에서 일어난 것으로 lignin이 주로 분해되는 것으로 나타났다.40) 결과적으로 AL은 ML에 비하여 최대 열분해 온도(Tmax)가 증가한 것으로 확인되었다. 이는 amino-silane은 cross-linking 및 coupling reagent로 거대한 리그닌 축합 구조를 형성에 기여함으로써 열안정성이 증가하는 것으로 사료되었다.40)
Table 2.
Thermal properties and surface charge properties of ML, AL-1, AL-2, and AL-3
| Samples | Thermal properties | Properties of surface charge | ||
|---|---|---|---|---|
| Tmax (℃) | pHIEC | Zeta potential (mV) | ||
| ML | 359.3 | NA | -54.5 | |
| AL-1 | 362.4 | 7.5 | 13.7 | |
| AL-2 | 364.5 | 8.8 | 20.0 | |
| AL-3 | 365.6 | 9.4 | 36.4 | |
Fig. 4(a)에 입자 크기 분포도를 나타내었다. 입자 크기 분포도를 보면, ML은 상대적으로 좁은 분포를 보였고, AL은 입자 크기 분포가 넓어지는 것으로 나타났다. Amine-silanization 반응 후 랜덤한 축합반응을 통하여 크기 분포가 넓어진 것으로 판단되고, APTMS 첨가량이 커질수록 리그닌의 큰 입자들의 비율이 증가하고 입자 크기 분포가 넓은 것으로 확인되었다.
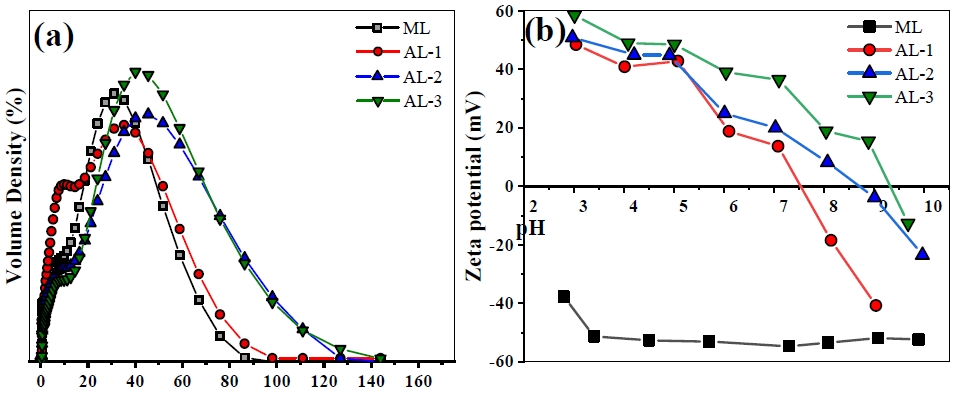
Fig. 4.
(a) Particle size distribution and (b) zeta-potential of ML, AL-1, AL-2, and AL-3 according to pH.
Fig. 4(b)는 pH에 따른 제타 전위의 그래프를 나타냈고, pH 7에서의 제타 전위 값을 Table 2에 나타내었다. ML은 풍부한 지방족 수산기와 방향족 수산기를 포함하기 때문에 pH 2-11 범위에서 음전하의 표면전하를 띠는 것으로 확인되었다. Amine-silanization 반응 후 전 pH 범위에서 표면전하가 전체적으로 크게 증가하였다. 각 AL의 제타 전위는 산성(pH 2-5)에서 아민기의 양성자화로 인해 양의 표면전하를 띠는 것으로 사료되었다.8) 또한 AL-1, AL-2, 및 AL-3의 등전점(pHIEC)은 7.5, 8.8, 및 9.4으로 확인되었고, 이때 APTMS의 첨가량이 가장 많았던 AL-3의 pHIEC이 높은 pH인 것은 -OH의 함량은 줄어들고, 아민기의 함량이 증가되었기 때문인 것으로 판단된다.13,24) 이에 따라 약 pH 7에서 제타 전위는 AL-3이 36.4 mV으로 상대적으로 가장 큰 양의 표면전하를 나타난 것으로 확인되었다. 또한 APTMS의 첨가량을 달리한다면 리그닌의 표면전하를 제어할 수 있는 것으로 사료되었다.
표면전하는 염료 흡착 공정에서 중요한 요인으로 작용한다. 특히 아민기는 산성 조건에서 양성자화를 통하여 양의 표면전하를 띠게 될 수 있고, 염기성 조건에서 음의 표면전하를 갖도록 할 수 있는 작용기이다. 따라서 pH 범위에 따라 표면전하를 달리 할 수 있는 아민기는 유리한 흡착 및 선택적인 흡착을 수행할 수 있는 능력을 제공할 수 있을 것이라 판단된다.
3.2 BG 염료 흡착 특성 분석
3.2.1 흡착제 투여량에 따른 BG 염료 흡착 특성 분석
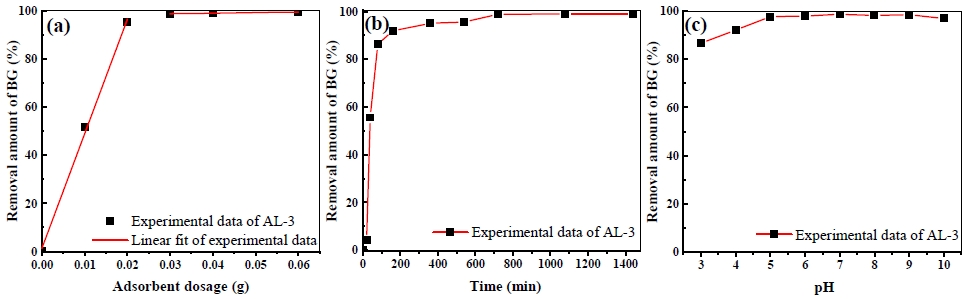
흡착제의 투여량은 BG의 제거 능력을 직접적으로 결정하기에 중요한 매개변수로 알려져 있다.7,25,26)Fig. 5(a)는 AL의 투여량에 따른 BG의 제거 효율을 나타냈다. 흡착제의 투여량이 0.01 g일 경우 BG의 제거량은 50% 이상인 것으로 나타났고, 흡착제 투여량이 0.02 g으로 증가할 경우 약 90%의 BG 제거량으로 급증한 것을 확인하였다. 이후 흡착제 투여량이 0.03 g 이상에서는 BG가 95% 이상 제거되는 것으로 나타났다. 결론적으로 AL의 투여량이 증가함에 따라 제거 효율이 증가하고, AL 입자의 증가로 인해 표면적 및 활성 부위가 제거 효율증가에 영향을 준 것으로 판단되었다.25) 추후 진행된 실험에서는 0.03 g의 AL로 흡착 실험을 수행하였다.
3.2.2 시간에 따른 BG 염료 흡착 특성 분석
흡착제의 투여량을 고정하고 일정 간격의 시간별(0-1440분)로 측정했을 때의 BG의 제거효율에 변화가 생기는지 알아보기 위해 진행한 실험의 결과를 Fig. 5(b)에 나타내었다. Fig. 5(b)를 보면 10분에서 5% 미만의 BG의 제거 효율이 나타났고, 40분에서 50% 이상의 제거효율이 나타났다. 이후 80분 이상부터는 90% 이상의 제거 효율을 나타냈고 720분 이후부터는 제거 효율이 100%로 모두 제거되는 것으로 나타났다. 이는 반응 시간이 지남에 따라 흡착제와 BG의 접촉시간도 증가하면서 제거 효율증가에 기여하였다고 판단된다.
3.2.3 pH에 따른 BG 염료 흡착 특성 분석
pH에 따라 AL이 BG의 흡착에 어떤 영향을 미치는지 알아보기 위해 pH 3∼10 범위에서 측정한 결과를 Fig. 5(c)에 나타냈다. Fig. 5(c)를 보면 pH가 2에서 5까지는 BG의 제거 효율이 증가하고 그 이후 pH에서는 BG의 높은 제거 효율을 유지하다가 pH 10에서 약간의 감소되는 경향을 나타냈다. 앞서 Fig. 4(b)에 도시된 제타 전위 그래프에 의하면, 산성 조건(pH 3∼4)에서는 표면전하가 약 60 mV의 높은 양의 표면전하를 띄는 것에 기인하여 AL의 아민기가 양성자화되어 표면이 양전하 상태로 하전 된 것으로 판단되었다. 이로 인해 산성 조건에서는 양이온성 암모늄기가 양이온성 BG 간의 정전기적 반발로 인해 흡착량이 낮은 것으로 나타났다. pH 5 이상 조건에서는 제타 전위 값이 점차 줄어드는 것이 확인되었다. 그로 인해 AL은 pH가 증가할수록 BG 정전기적 반발력이 점차 감소되어 제거 효율이 증가한 것으로 판단된다.13,27)
3.3 BG 흡착 동역학, 흡착 등온선, 및 열역학적 분석
3.3.1 흡착 동역학 분석(Kinetic isotherms)
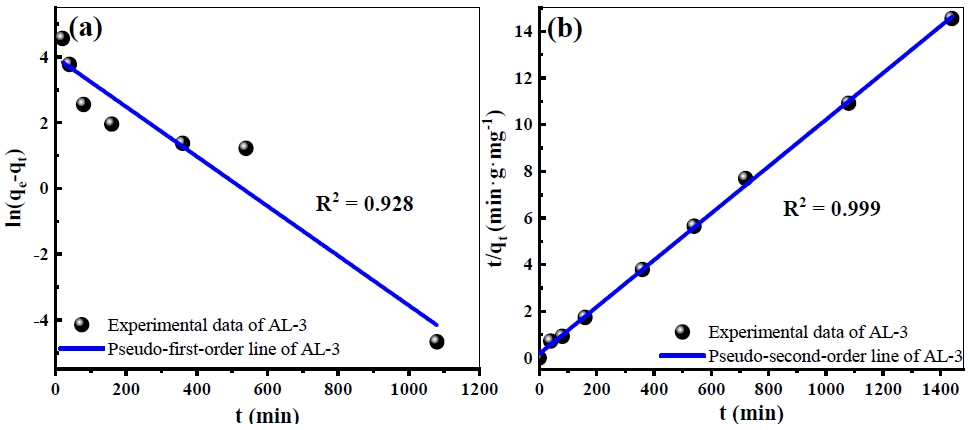
흡착 동역학 분석은 반응 시간에 따른 BG 흡착량 분석을 통해 얻은 데이터를 기반으로 수행하였다. Fig. 5(b)에 나타낸 결과를 기반하여 PFO과 PSO에 적용하였고,7,13) 그 결과를 각각 Fig. 6과 Table 3에 나타내었다.
Table 3.
Characteristic parameters of Pseudo-first-order kinetics and Pseudo-second-order-kinetics for the adsorption of BG onto AL-3
| Samples | Pseudo-first-order kinetics | Pseudo-second-order kinetics | ||||||
|---|---|---|---|---|---|---|---|---|
| R2 | K1 | qe.(cal) | R2 | K2 | qe.(cal) | qe.(exp) | ||
| (min-1) | (mg·g-1) | (g·mg-1·min-1) | (mg·g-1) | (mg·g-1) | ||||
| AL-3 | 0.928 | 7.6·10-3 | 54.21 | 0.999 | 5.5·10-4 | 99.70 | 98.99 | |
Table 3을 보면 식에 대한 상관계수인 R2값이 PSO (R2=0.999)가 PFO (R2=0.928)보다 1에 가까운 것으로 나타났고,7,28) 실험적 값인 qe.(exp)가 PSO의 qe.(cal) 값과 유사한 것을 확인하였고 PFO보다 PSO이 더욱 적합한 모델이라고 판단된다.7) PFO은 물리적 흡착을, PSO은 화학적 흡착을 판단할 수 있는 근거로 알려져 있다.29) 결론적으로 AL을 이용한 BG의 흡착 실험은 물리적 흡착보다 화학적 흡착이 지배적인 것으로 판단된다.
3.3.2 흡착 등온선 분석 (Adsorption isotherms)
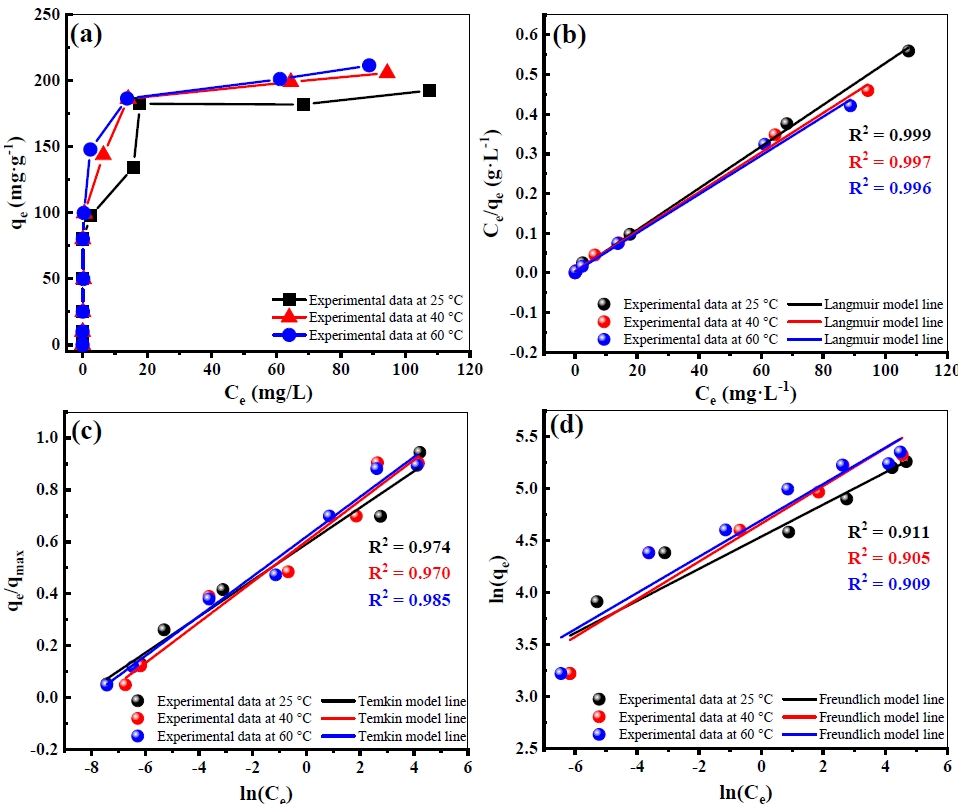
다양한 농도(10-300 mg·L-1)에서 흡착 실험을 진행하여 Fig. 7(a)에 나타내었고, 이 실험데이터를 기반으로 흡착 등온선 분석을 진행하였다. 흡착 등온식에는 여러 종류가 있지만, 앞서 전술한 Eq. (3-5)에 의거하여 Langmuir, Freundlich, Temkin 흡착 등온선 분석을 수행하였다. 다양한 모델에 피팅한 결과와 매개변수 값을 Fig. 7(b)-7(d) 및 Table 4에 나타내었다. AL의 BG 흡착공정은 상관계수 R2를 기반으로 Langmuir > Temkin > Freundlich 순서로 모델에 적합하고, 특히 Langmuir와 Temkin model이 적합한 모델이라고 판단되었다.13,27,30)
Table 4.
Characteristic parameters of Langmuir, Temkin, and Freundlich isotherms for the BG adsorption onto AL-3
Langmuir model은 흡착제의 표면에 한정된 흡착 부위에 흡착질이 단일 흡착으로 이루어진다고 알려져 있다.30,31)Table 4을 보면 온도가 각 298.15, 313.15, 333.15 K으로 증가하면, 최대 흡착량 qm(cal)은 각 190.48, 200.40, 204.92 mg·g-1로 증가한 것으로 나타났다.31)
Langmuir model은 무차원 분리 계수 (RL)을 통하여 흡착의 적합성 여부를 판단할 수 있다.32,33)RL의 식은 RL=1/(1+CeRL) 으로 계산되어졌다. 이 RL 값은 각각 비가역(RL=0), 적합(0 < RL < 1), 선형(RL=1), 부적합(RL>1)으로 알려져 있다.30,34) 그 결과 AL-3에 대한 BG 흡착의 RL 값은 각 온도 298.15, 313.15, 333.15 K에서 0.005406-0.1937, 0.008129-0.60412, 0.006419-0.9553으로 나타났다. 따라서 AL에 대한 BG의 흡착공정은 적합한 공정이며 다층 흡착보다는 단층 흡착이 지배적인 것으로 사료되었다.13,35)
Temkin model은 흡착제와 흡착물의 상호작용을 고려할 수 있는 매개변수를 포함한다.26,30) Temkin model의 bt 상수는 흡착에너지의 변화와 관련이 있고,26) 물리적·화학적 흡착인지를 판별하는데 사용되는 것으로 알려져 있다.27) bt는 298.15, 313.15, 333.15 K에서 35.40, 33.22, 36.08 kJ·mol-1이었다. bt>0.020 kJ·mol-1은 화학적 흡착임을 의미하기 때문에 AL와 BG의 흡착공정이 화학적 흡착이고 주로 정전기적 인력으로 이루어진다고 사료된다.36) 결과적으로 이 흡착 공정은 흡착 등온선에 따르면 BG가 AL에 단층 흡착 및 화학적 흡착이 지배적으로 진행되었다고 판단되었다.
3.3.3 흡착 열역학적 분석(Thermodynamic studies)
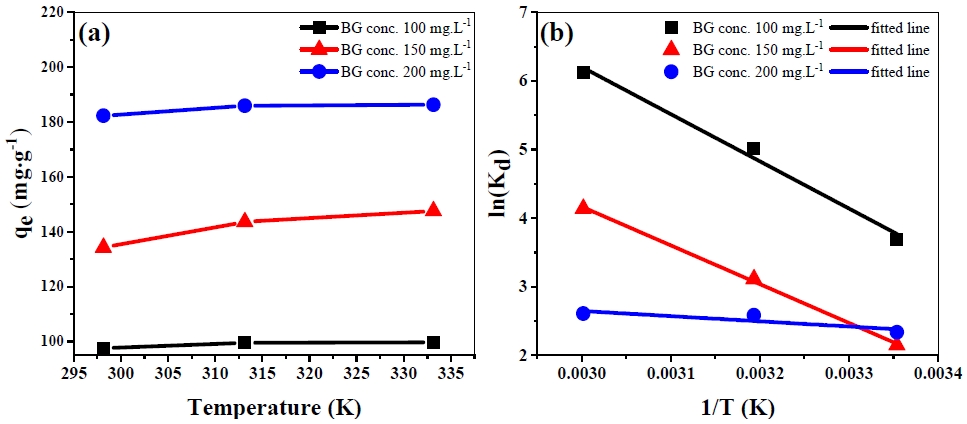
Fig. 8(a)는 다른 농도의 BG에서 AL의 흡착 용량에 대한 온도의 영향을 나타내었다. 온도 및 흡착 메커니즘의 영향을 평가하기 위하여 Eq. (8-10)을 사용하여, ln(Kd)와 1/T 간의 관계를 Fig. 8(b)에 나타내었고, 이를 기반으로 열역학적 매개변수 값을 Table 5에 요약하였다. 일반적으로 AL-3의 모든 ΔG° 값은 음의 값으로 온도가 증가함에 따라 더욱 음의 값을 갖는 경향을 나타내었다.30,37) 이는 BG 흡착 공정은 자발적인 흡착 공정이며, 온도가 증가함에 따라 더욱 자발적인 흡착 공정으로 이루어진다고 사료된다. 또한 모든 흡착과정의 ΔH° 값은 양수를 나타냈고, 이는 흡열 과정이며 흡착물과 흡착제 사이의 강한 상호작용을 의미한다.37,38) 양수의 ΔS° 값은 전체 흡착계의 무질서도가 증가한 것으로, 이는 AL의 표면에 BG가 흡착되면서 고체 액체 계면에서 BG 주위에 고정된 물 분자가 용액으로 방출되었기 때문이다.39) 따라서 열역학적 분석에 따르면 AL과 BG와의 친화력이 우수하고, 온도가 증가할수록 흡착을 유도할 수 있다고 판단된다.
Table 5.
Characteristic parameters of thermodynamic analysis
3.4 형태학적 분석
Fig. 9는 리그닌 샘플들의 SEM image를 나타냈다. AL-1, AL-2, AL-3을 비교하면, AL-3 이 가장 큰 공극을 갖는 것으로 관찰되었다. 이는 APTMS의 첨가량이 증가할수록 중축합반응에 의해서 리그닌의 공극이 막히거나 좁아질 수 있기 때문에 AL-3은 상대적으로 공극은 크지만, 밀도가 높은 구조를 갖는 것으로 판단된다.40)Fig. 9(d)를 보면, BG 흡착 후 AL-3으로 표면에 많은 양의 BG 입자가 흡착된 것을 알 수 있다. 따라서 AL-3의 BG 흡착은 성공적으로 이루어졌다고 사료되었다.
4. 결 론
본 연구는 저가의 친환경 소재인 리그닌을 이용한 화학적 개질을 통해 양이온성 염료 흡착제로서의 활용 가능성을 검토하였다. AL은 화학적 및 물리적 분석을 통하여 성공적으로 제조되었다는 것을 확인하였고, APTMS의 첨가량이 증가할수록 많은 아민기를 도입할 수 있고, 표면전하가 전체적으로 증가하는 경향을 확인하였다. 염료 흡착 실험에서 AL은 양이온성 염료를 중성 및 염기성 조건에서 뛰어난 제거할 수 있음을 나타냈으며, 산성 조건에서 양이온성 암모늄기를 포함하기에 양이온성 염료와 정전기적 반발력이 작용할 수 있음으로써 상대적 낮은 제거 효율로 나타났고, 염기성 조건에서 비공유 전자쌍을 갖는 아민기는 양이온성 염료와 정전기적 인력으로 접근성이 우수한 것으로 확인되었다. 흡착 등온선 및 동역학 분석을 통하여, 염료 흡착 공정은 Langmuir와 Temkin model이 적합하였고, Langmuir model에 기반한 BG의 최대 흡착량은 197.44 mg·g-1에 도달하였다. 열역학적 분석 결과, 전반적인 흡착 실험은 모두 자발적인 흡착과정임을 나타냈고, 흡착 공정의 온도가 증가함에 따라 더욱 자발적인 흡착으로 확인되었다. 따라서 본 연구를 통해 아미노-실란이 도입된 리그닌 기반 흡착제의 활용 가능성을 확인하였고, 다양한 오염물질의 제거에 적용할 수 있는 지속가능한 바이오 흡착제의 응용을 기대할 수 있다.