1. 서 론
2. 재료 및 방법
2.1 공시재료
2.2 실험방법
3. 결과 및 고찰
3.1 OL의 물리·화학적 특성 분석
3.2 OLH의 화학적 특성 분석
3.3 OLH의 형태학적 및 기계적 특성 분석
4. 결 론
1. 서 론
하이드로겔은 3차원 고분자 네트워크가 다량의 물을 함유하는 재료로서, 높은 수분 함량과 조절 가능한 미세구조를 기반으로 환경 정화, 생체재료, 코팅 및 소프트 디바이스 등 다양한 분야에서 활용 가능성이 확대되어 왔다[1,2,3]. 하이드로겔은 용액 상태에서 성형이 가능하고, 내부 네트워크가 물질 전달(확산)과 기계적 변형을 동시에 허용한다는 점에서 기능성 플랫폼 소재로 주목받았다[3,4]. 그러나 일반적인 하이드로겔은 높은 수분 함량으로 인해 네트워크 밀도가 낮고, 외부 하중이나 반복 변형에 의해 네트워크가 쉽게 손상되거나 구조적 이완이 발생하는 경향이 있다[5,6]. 그 결과, 강도 및 내구성 부족은 실제 공정·현장 적용에서 하이드로겔의 장기 안정성을 제한하는 주요 요인으로 지적되어 왔으며, 특히 압축·인장·전단 조건에서의 형태 안정성 확보와 파괴 저항성 향상은 여전히 중요한 연구 과제로 남아 있다[6,7,8]. 따라서 지속가능한 원료를 기반으로 하면서도 기계적 성능과 네트워크 안정성이 우수한 하이드로겔을 구현하기 위한 분자 설계와 네트워크 제어 전략이 요구된다.
최근에는 친환경 소재 수요 증가와 함께 바이오매스 유래 고분자를 활용한 하이드로겔 연구가 활발히 수행되어 왔다[9,10,11]. 셀룰로오스, 키토산, 알지네이트 등 다당류 기반 소재는 생체적합성과 친수성을 바탕으로 폭넓게 적용되었으나, 강도 및 장기 안정성 확보를 위해서는 가교 구조의 정교한 설계나 보강재 도입이 필수적인 경우가 많았다[12]. 이와 같은 배경에서 리그닌은 펄핑 및 바이오리파이너리 공정에서 대량으로 발생하는 방향족 바이오매스 부산물로, 자원 순환성과 경제성 측면에서 고부가가치 소재로의 전환 가능성이 높은 원료로 평가되어 왔다[11,13]. 리그닌은 방향족 골격과 페놀성 구조를 기반으로 자외선 흡수, 항산화, 항균 등 다양한 기능성을 내재하며, 동시에 다수의 수산기 및 반응성 작용기를 포함할 수 있어 고분자 네트워크 소재로의 확장 가능성을 제공한다[14]. 그럼에도 불구하고 리그닌은 원료(수종) 및 공정(kraft, soda, organosolv 등)에 따라 구조적 이질성이 크고, 분자량 분포가 넓으며, 분자 간 π–π 상호작용 및 수소결합에 의해 강한 응집을 나타내기 때문에 균일한 용해·분산과 네트워크 형성이 어렵다는 한계가 존재해 왔다[15,16,17]. 또한 리그닌의 반응성 작용기는 존재하더라도 접근성과 반응성이 제한되거나, 네트워크 형성 과정에서 구조 제어가 어려운 경우가 많아 단순 혼합이나 제한적 가교만으로는 고강도 하이드로겔 구현에 한계가 있었다[18,19,20].
리그닌 기반 하이드로겔의 제조 효율성 및 성능을 향상시키기 위해서는 리그닌을 하이드로겔용 빌딩블록으로 기능화하여, 네트워크 내에서 실제로 기여할 수 있는 결합점과 상호작용을 동시에 확보하는 전략이 필요하다[21,22,23]. 즉, 가교 반응에 참여할 수 있는 반응성 결합점의 도입 또는 증가, 친수성/유연성/상용성 조절을 통한 균일한 네트워크 형성, 변형 시 에너지 소산이 가능한 물리적 결합 또는 동적 상호작용의 설계가 함께 고려될 필요가 있다. 특히 아민기는 수소결합과 이온성 상호작용을 통해 네트워크 내 물리적 결합을 형성할 수 있을 뿐만 아니라, 다양한 화학적 가교 반응에 참여할 수 있어 네트워크 강화에 유리한 기능기로 알려져 있다[23,24]. 또한 아민기의 도입은 리그닌의 표면 전하 및 친수성을 변화시켜 분산성 향상과 네트워크 내 상호작용 조절에도 기여할 수 있다[25]. 한편 옥시프로필화(oxypropylation)은 리그닌의 수산기에 프로필렌 옥사이드 유래 사슬을 도입하여 분자 사슬의 유연성을 부여하고, 상용성 및 가공성을 향상시키는 개질로 활용되어 왔다[26,27]. 이러한 유연한 곁사슬은 네트워크 형성 과정에서 분자 이동성을 증가시켜 보다 균일한 겔화를 유도할 수 있으며, 변형 시에는 사슬의 재배열을 통해 에너지 소산에 기여함으로써 강도와 내구성 향상에 유리하게 작용할 수 있다[26,28].
본 연구에서는 리그닌을 아민화한 후 옥시프로필화를 적용하여 이중 기능화 리그닌을 제조하고, 이를 대상으로 다양한 화학·물리적 분석을 수행하여 개질 성공 여부와 구조적 변화를 체계적으로 규명하였다. 또한 이중 개질 리그닌을 기반으로 하이드로겔을 제조하여 네트워크 형성 거동과 기계적 특성을 평가하였다. 그 결과, 이중 기능화 리그닌 기반 하이드로겔의 네트워크 안정성 향상 가능성을 검토하고, 특히 기계적 강도 특성의 변화를 확인하고자 하였다.
2. 재료 및 방법
2.1 공시재료
크라프트 리그닌(kraft lignin, KL)은 침엽수 목재(Pinus Massoniana)의 크라프트 펄핑 공정을 통해 얻어졌으며, 중국 T사에서 제공받았다. KL은 흑액에 20 wt% 황산 수용액을 첨가하여 pH 2로 산성화한 후, 탈이온수로 여러 차례 세척하고 감압 여과를 통해 정제하였다. 이후, 자연 건조하여 파우더 형태로 얻어 사용하였다. 31P NMR 분석 결과, KL의 총 수산기 함량은 4.2 mmol/g으로 계산되었고, 2.2.3항에서 제시한 GPC 분석을 통해 중량 평균 분자량(Mw)이 11,800 g/mol로 확인되었다[29]. 2-chloroethylaminue hydrochloride (CEH, 99.0%), polypropylene oxide (PO, 99.0%) 및 poly(ethylene glycol) diglycidyl ether (PEGDGE, Mn = 500 g/mol)는 Sigma Aldrich (USA)를 통해 구매하였다. N,N-dimethylformamide (DMF, 95.0%), potassium carbonate (K2CO3, 98.0%), sodium hydroxide (NaOH, 98.0%), hydrochloric acid (HCl, 35%) 및 potassium hydroxide (KOH, 98.0%)는 Daejung Chemicals & Metals Co. Ltd. (Korea)를 통해 구매하였다. 또한, 실험에서는 3차 증류수기(HIQ II, Human Science, Korea)를 이용해 제조한 탈이온수(distilled water, DW)를 사용하였으며, 모든 시약은 추가 정제 없이 그대로 사용하였다.
2.2 실험방법
2.2.1 아민화 및 옥시프로필화 리그닌 제조
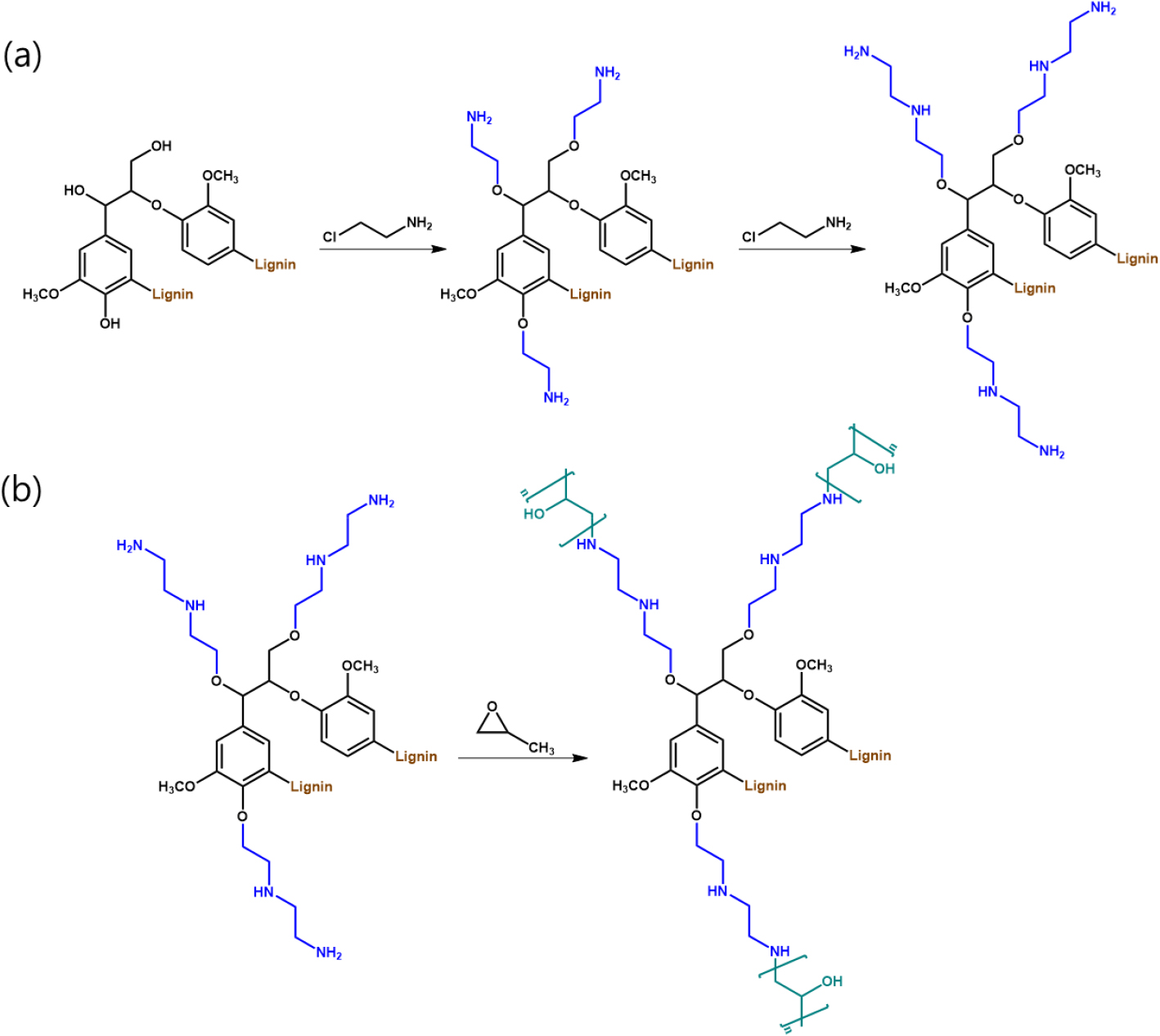
CEH를 이용한 KL의 아미노화 반응은 환류 응축기와 자석 교반기가 장착된 250 mL 둥근 바닥 플라스크에서 수행되었다. 구체적으로, KL (3 g)을 DMF 용액(100 mL)에 용해시켰다. 그 후, 반응 혼합물에 CEH 5.8 g과 K2CO3 2 g을 첨가하였다. 혼합물을 80°C로 가열하고 24시간 동안 교반을 진행하였다. 반응 후, 혼합물을 2 M HCl 수용액 200 mL에 첨가하여 고형화를 진행하고, 원심분리를 이용하여 미반응물을 제거하고 얻어진 고형분을 DW에 분산시킨 후 필터페이퍼(F2040 grade ashless quantitative filter paper, φ 90 mm, chm lab group, Spain)를 통해 세척을 진행하였다. 최종적으로, 세척된 고형분을 동결건조를 통해 아민화 리그닌을 얻었다. 초기 KL 질량을 기준으로 한 수율은 약 93%였다. 이와 같은 방법을 반복하여 2차 아민화 샘플을 얻었다. 얻어진 샘플들은 AL-1과 AL-2라고 명명하였다(Fig. 1a).
옥시프로필화 리그닌은 AL-2 2 g을 1 M NaOH 50 mL가 담겨있는 250 mL 둥근 바닥 플라스크에 첨가하여 충분히 용해를 진행하였다. PO 3 mL를 첨가하고 40°C 조건에서 24시간동안 반응을 진행하였다. 반응이 끝나고 2 M HCl과 많은 양의 DW를 이용하여 필터를 통해 세척을 진행하였다. 세척이 끝난 반응물은 동결건조를 통해 옥시프로필화 리그닌을 얻었다. 초기 AL-2 질량을 기준으로 한 수율은 약 90%였다. 이렇게 최종적으로 얻어진 리그닌을 옥시프로필화 리그닌(oxypropylated lignin, OL)이라고 명명하였다(Fig. 1b).
2.2.2 아민화 및 옥시프로필화 리그닌 기반 하이드로겔 제조
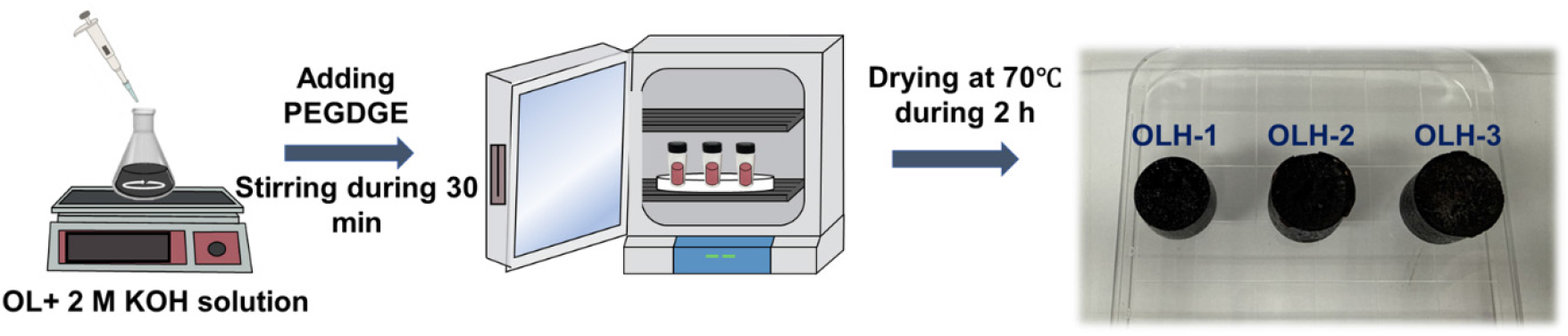
옥시프로필화 리그닌 기반 하이드로겔은 OL 1 g을 2 M KOH 5 mL가 담긴 비커에 첨가하고, 자석교반을 이용하여 충분히 용해시켰다. 이후 가교제인 PEGDGE의 첨가량을 기준으로, 각각 3 g, 4 g, 5 g의 PEGDGE를 첨가한 시료를 OLH-1, OLH-2, OLH-3으로 명명하였다. 혼합물은 추가 교반을 거친 후, 70°C 조건에서 2시간동안 열처리하여 PEGDGE와 OL간의 가교 반응을 유도함으로써 겔화를 진행하였다. 그 후 DW와 2 M HCl를 이용하여 미반응물 제거 및 세척하였다(Fig. 2). 동결건조를 통해 에어로겔로 변환 후 압축강도를 제외한 모든 특성 분석에는 에어로겔을 사용하여 분석을 진행하였다.
2.2.3 물리·화학적 특성 분석
리그닌의 화학적 구조 분석을 위해 감쇠 전반사(attenuated total reflectance, ATR) 부착 장치가 장착된 Fourier transform infrared (FT-IR) 분광기(IRTracer-100, Shimadzu, Japan)를 사용하였다. FT-IR 스펙트럼은 4,000–500 cm-1 범위에서 64회 스캔하여 획득하였다. 표면 원소 조성 및 결합 상태를 분석하기 위해 X-ray photoelectron spectroscopy (XPS; K-Alpha+, Thermo Scientific, UK)를 사용하였으며, dwell time 30 ms, pass energy 50 eV 조건에서 시료당 30회 스캔하여 측정하였다. 리그닌의 분자량 및 분자량 분포는 0.1% DMF-LiBr 용매 시스템에서 gel permeation chromatography (GPC; Shimadzu-20A, Shimadzu, Japan)로 분석하였다. GPC 컬럼은 PLgel 5-µm MIXED-C 및 MIXED-D, PLgel 3-µm MIXED-E로 구성하였고, 검출기는 UV (λ = 280 nm)를 사용하였다. 주입량은 100 µL, 유속은 1.0 mL/min으로 설정하였다. 분자량 보정은 분자량 범위 1,480–1,233,000 g/mol의 폴리스타이렌 표준물질을 이용하여 검량선을 작성한 후 수행하였다. 열적 안정성은 열중량분석기(thermogravimetric analyzer; SDT Q600, USA)를 이용하여 질소 분위기에서 평가하였다. 질소 유량은 100 mL/min으로 유지하였고, 승온 속도는 10 °C/min으로 설정하여 25–1,000°C 범위에서 측정하였다. 형태학적 특성은 전계방출 주사전자현미경(field-emission scanning electron microscope, FE-SEM; JSM-7900F, JEOL, Japan)을 이용하여 관찰하였다. 분석 전 시료는 백금(Pt) 코팅을 수행하였다. 분석은 가속 전압은 5 kV 조건에서 수행하였다. 지내 또한 표면 원소 분포 및 조성 분석을 위해 에너지 분산형 X선 분광(energy-dispersive X-ray spectroscopy, EDS) 분석을 함께 수행하였다. 하이드로겔의 기초적인 형태는 디지털 카메라(iPhone 16 pro max, Apple, USA)를 이용하여 기록하였다. 리그닌 기반 하이드로겔의 기계적 특성은 CTX 텍스처 분석기(CTX Texture Analyzer; AMETEK Brookfield, USA)를 이용하여 압축 강도를 측정하였다. 하이드로겔의 압축 강도 시험은 원통형 시편(직경 25 mm, 높이 20 mm)을 사용하여 수행하였다. 측정은 압축 속도 20 mm/s 조건에서 진행하였으며, 최대 하중 5 kgf까지 적용하였다. 시험 중 압축 거동은 시험기의 크로스헤드 이동에 따른 변위(distance)로 기록되었으며, 본 연구에서는 변형 거동을 distance 기준으로 평가하였다.
3. 결과 및 고찰
3.1 OL의 물리·화학적 특성 분석
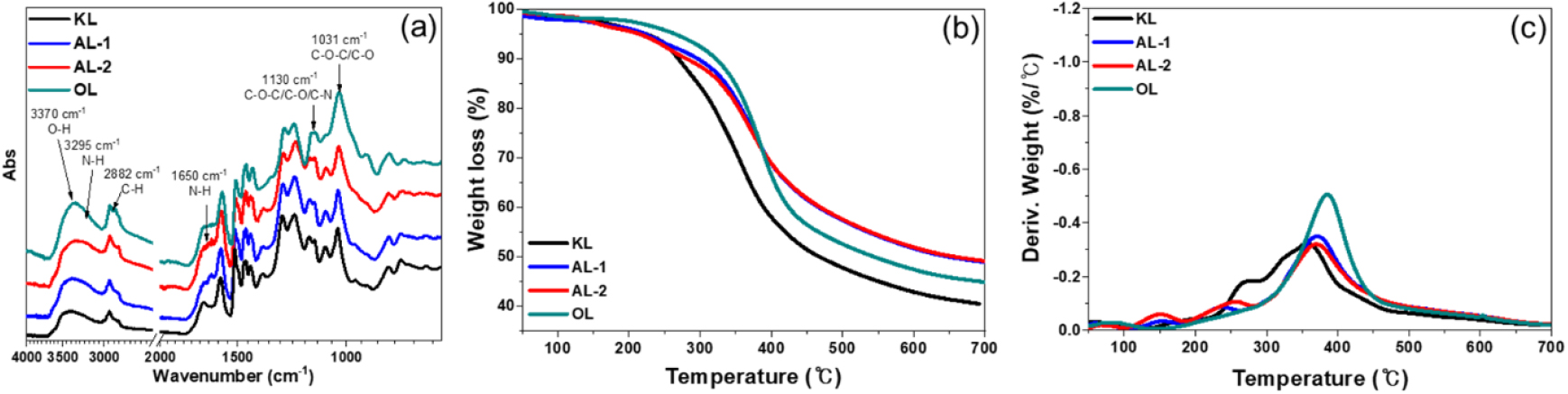
본 연구는 아민화 리그닌 및 옥시프로필화 리그닌의 화학적 구조 및 열적 특성을 확인하기 위해 FTIR 및 TGA 분석한 결과를 Fig. 3을 도시하였다. 먼저 Fig. 3a를 보면 KL 대비 AL-1 및 AL-2 시료에서는 3,300 cm-1 부근의 수산기 흡수 피크가 유지되었으며, 3,200–3,500 cm-1 범위에서 N-H 신축 진동에 해당하는 피크가 뚜렷하게 관찰되었다. 약 1,650 cm-1 부근에서는 아민화 반응에 따른 N-H bending 진동 피크가 확인되었으며, 1,030–1,130 cm-1 영역에서 C–N 결합에 기인한 특성 피크가 추가적으로 관찰되었다. AL-1과 AL-2를 비교했을 때 AL-2가 전반적으로 특성 피크들이 증가하는 경향이 확인되었으며, 이는 CEH를 이용한 반복적인 아민화 반응이 성공적으로 진행되었음을 시사한다[30,31,32]. OL의 경우는 2,880–2,970 cm-1 영역에서 알킬 사슬에 해당하는 신축 진동 피크가 새롭게 관찰되었으며, 이는 옥시프로필기 도입에 따른 구조적 변화를 명확히 보여준다[26,27].
TGA 결과 KL에 비해 AL 샘플들의 최대 열분해 온도가 상승한 경향이 확인되었다(Fig. 3b). AL-1과 AL-2의 경우는 AL-2가 다소 높은 최대 열분해 온도를 나타냈으며. 이는 반복적인 아민화 반응으로 인해 분자간 상호작용 증가 및 구조적 안정화에 기인한 것으로 판단된다[25,33]. 또한 OL의 경우 가장 높은 최대 열분해 온도를 나타냈는데, 이는 PO의 도입에 따른 유연한 알킬 사슬 구조 및 부분적인 가교 효과가 열안정성 향상에 기여했음을 의미한다[26,34]. DTG 분석 결과, 모든 시료는 리그닌 특유의 단계적 열분해 거동을 보였다(Fig. 3c). 일반적으로 100–200°C 구간에서는 수분 및 저분자 성분의 제거에 의한 약간의 질량 감소가 관찰되며, 200–350°C 구간에서 1차적인 분해가 진행되는 양상이 확인되었다. 해당 구간의 분해는 주로 측쇄 및 산소 함유 작용기의 절단 및 저분자 휘발성 성분의 방출로 인한 것을 해석된다. 약 350–450°C 구간에서 주요 열분해가 일어난 것을 확인하였고, 이는 리그닌의 방향족 골격에 대한 분해 및 재배열이 진행되는 구간에 해당한다[25]. KL은 해당 구간에서 비교적 넓고 완만한 형태의 DTG 피크를 나타내어 다양한 결합 환경이 동시에 분해되는 비균일한 열분해 특성을 보였다. 반면, AL-1과 AL-2는 KL에 비해 보다 높은 온도에서 열분해가 일어난 경향을 나타냈다. 아민화 반응으로 도입된 작용기들로 인해 열분해 지연에 기여했기 때문에로 판단된다. OL의 경우 350–450°C 구간에서 가장 높은 온도에서 뚜렷한 피크가 확인되었으며, 이는 옥시프로필화에 의해 형성된 탄소 사슬 구조가 분자 구조를 부분적으로 안정화 하여 분해가 지연되었을 가능성을 시사한다[26].
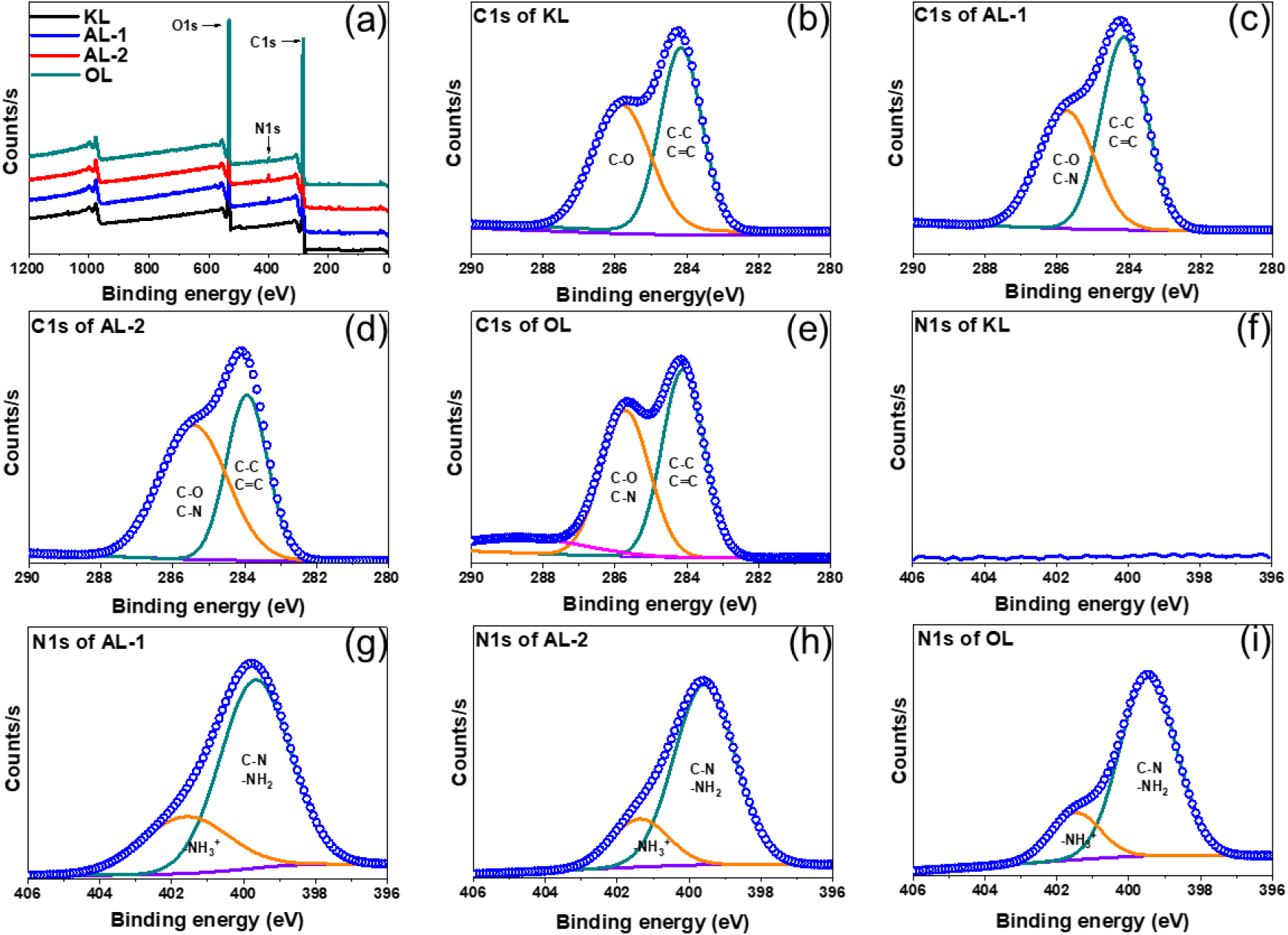
추가적으로 화학적 구조를 파악하기 위해 분석된 XPS 결과를 Fig. 4에 나타내었다. XPS survey scan 결과, 모든 샘플에서 공통적으로 C1s (285 eV)와 O1s (531 eV)에 해당하는 피크가 확인되었고, AL 및 OL의 경우에는 N1s (400 eV)에 해당하는 피크가 새롭게 확인되었다(Fig. 4a)[35]. 아민화 및 옥시프로필화의 영향을 알아보기 위해 C1s 및 N1s의 코어레벨 스펙트럼을 분석한 결과를 Fig. 4b–i에 도시하였다. 모든 샘플들은 C–C/C=C (284.5 eV) 및 C–O (286 eV) 두 피크로 디콘볼루션(deconvolution)되었다. AL의 경우에는 C-N 피크가 추가적으로 중첩되어 증가하는 경향이 관찰되었다. 이는 아민화 반응으로 형성된 C-N 결합으로 인한 것으로 판단된다[21]. OL의 경우 옥시프로필화로 인해 C–O의 결합이 증가하면서 상대적으로 C–O/C–N 피크의 비율이 증가하는 경향이 확인되었다. N1ss 코어레벨 스펙트럼에서는 KL은 유의한 피크가 나타나지 않았지만 AL 및 OL은 C–N/-NH2 (400 eV)과 -NH3 (401 eV) 두 개의 피크로 디콘볼루션되었다. 이를 통해 아민화 반응이 성공적으로 진행되었으며, OL에서도 아민기가 안정적으로 잔존하고 있음을 확인하였다[35].
추가적으로 분자량 및 원소 분석을 수행하였으며, 그 결과를 Table 1에 나타내었다. GPC 분석 결과 KL 대비 AL 시료들의 분자량은 점진적으로 증가하는 경향을 나타냈다. 이는 반복적인 아민화 반응에 의해 치환기 도입 및 분자 구조 변화가 누적되었기 때문으로 판단된다. 또한 OL은 AL-2 대비 분자량이 크게 증가하였는데, 이는 옥시프로필화 과정에서 알킬사슬이 형성됨으로써 분자량이 증가한 결과로 해석된다. 원소 분석한 결과 KL은 상대적으로 낮은 질소 함량을 나타냈다. 반면 AL-1과 AL-2는 질소 함량이 각각 1.37%와 1.51%로 KL에 비해 크게 증가하였고, 이는 CEH를 이용한 아민화 반응을 통해 질소 함유 작용기가 성공적으로 도입되었음을 의미한다. OL의 질소 함량이 AL-2에 비해 감소하였으나, 이는 질소 작용기의 소실보다는 옥시프로필화로 인한 알킬 사슬의 형성으로 인해 탄소의 비율이 증가하면서 상대적으로 낮아진 결과로 판단된다.
Table 1.
Molecular weight and elemental atomic ratio of lignin samples
3.2 OLH의 화학적 특성 분석
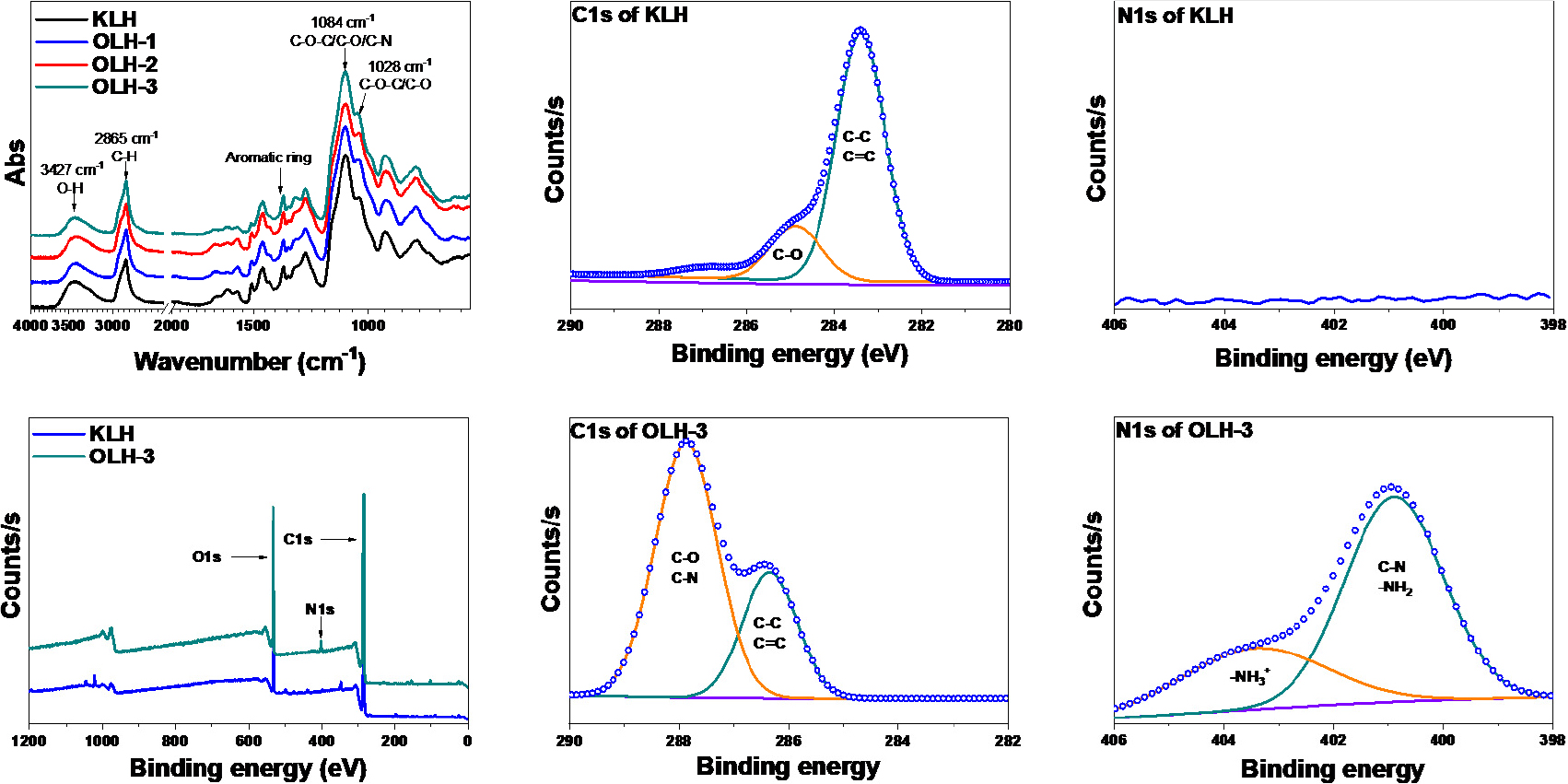
OLH의 화학적 구조 분석을 위해 FT-IR 및 XPS 결과를 Fig. 5에 도시하였다. 먼저 Fig. 5a에 도시한 FT-IR 분석 결과를 보면 모든 시료에서 약 2,865 cm-1 피크에서 C-H 신축 진동 피크가 공통적으로 관찰되었으며, 이는 가교제로 사용된 PEGDGE로 인해 형성된 피크인 것으로 사료된다[36]. OLH 샘플의 경우1,084 cm-1 부근의 피크들이 점진적으로 증가하는 경향을 나타냈다. 이는 PEGDGE 첨가량 증가에 따라 C-O-C/C-O 결합 기여가 증가했음을 시사한다. 이러한 결과는 PEGDGE의 에폭시기가 OL의 수산기 및 아민기와 반응하여 가교 구조가 형성되었음을 뒷받침한다[37]. 한편 겔화 과정 이후에도 리그닌의 방향족 골격에 해당하는 피크가 유지되어, 리그닌 구조가 안정적으로 보존됨을 확인하였다.
Fig. 5b에 나타낸 XPS survey scan 결과, KLH와 OLH-3 모두 공통적으로 C1s (285 eV)와 O1s (531 eV)에 해당하는 피크가 확인되었으며, OLH-3에서는 N1s (400 eV)에 해당하는 피크가 새롭게 관찰되었다. Fig. 5c와 d에 도시한 C1s 코어레벨 스펙트럼 분석 결과, KLH는 C–C/C=C (284.5 eV) 및 C–O (286 eV) 두 피크로 디콘볼루션되었다[36]. 그러나 OLH-3의 경우 C–N/C–O (286 eV) 피크의 비율이 상대적으로 크게 증가한 결과를 나타냈다. 이는 PEGDGE를 이용해 가교반응을 진행함으로써 C–O 결합의 증가로 인한 결과인 것으로 사료된다[21]. Fig. 5e와 f에 나타낸 N1s 코어레벨 스펙트럼에서는 KLH의 경우 아민 피크가 나타나지 않았고, OLH-3에서는 398 eV와 401 eV에서 두 개의 피크가 디콘볼루션된 것을 확인하였다.
3.3 OLH의 형태학적 및 기계적 특성 분석
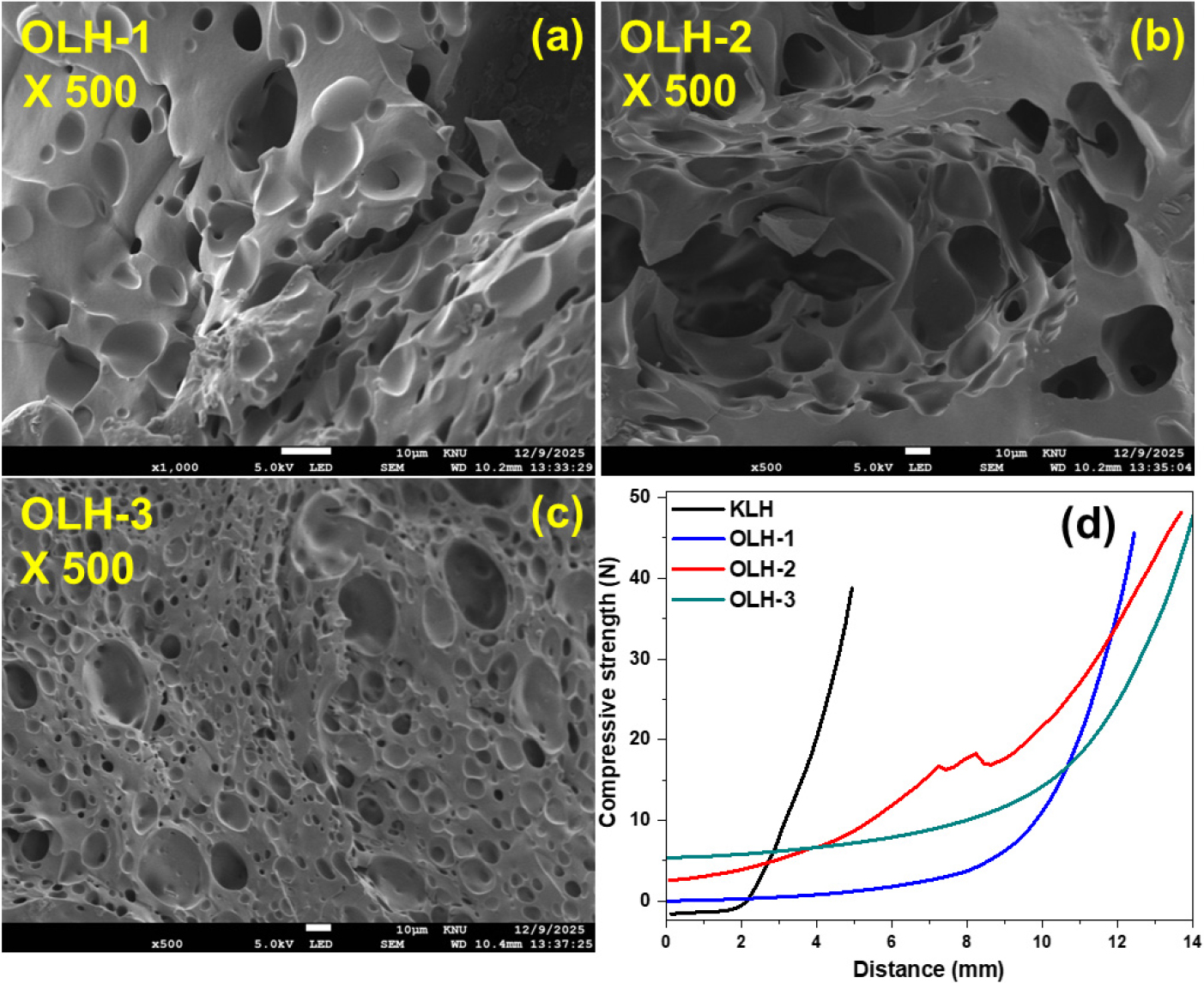
OLH의 형태학적 분석과 기계적 특성 분석을 위한 SEM이미지와 압축강도 시험을 수행하였으며, 그 결과를 Fig. 6에 도시하였다. SEM 분석 결과, 모든 시료에서 개방형 다공성 구조를 확인하였고, 기공의 크기 및 분포에서 차이가 관찰되었다(Fig. 6a–c). OLH-1은 비교적 큰 기공과 불균일한 기공 분포가 동시에 나타났으나, OLH-2에서는 기공이 보다 연속적인 네트워크 형태로 발달하는 경향을 보였다. 한편 OLH-3에서는 미세 기공이 고밀도로 분포하면서 상대적으로 균일한 기공 구조가 형성되었으며, 이는 PEGDGE 첨가량 증가에 따라 겔 네트워크가 점차 치밀화되고 가교 구조가 발달했음을 시사한다[19,38]. 압축강도 시험 결과, KLH는 낮은 변형 구간에서도 급격한 응력 증가와 함께 파괴가 발생하여 외부 하중에 대한 구조적 안정성이 제한적인 것으로 나타났다(Fig. 6d). 반면 OLH 시료들은 변형이 증가함에 따라 응력이 점진적으로 상승하는 거동을 보였고, 상대적으로 큰 변형에서도 구조를 유지하는 압축 안정성을 나타냈다[39]. 특히 OLH 계열은 KLH 대비 전반적으로 높은 압축 응력을 나타냈으며, PEGDGE 첨가량이 증가한 시료일수록 최대 압축 응력과 변형 허용 범위가 함께 증가하는 경향을 보였다. 이러한 결과는 PEGDGE 기반 가교 반응을 통해 형성된 3차원 네트워크가 하중 전달을 효과적으로 분산시키고, 압축 과정에서 다공성 구조가 단계적으로 변형·붕괴되며 에너지를 흡수함으로써 파괴 저항성이 향상되었기 때문으로 해석된다[40].
4. 결 론
본 연구에서는 리그닌을 아민화한 후 옥시프로필화를 연속적으로 적용하여 이중 기능화 리그닌을 제조하였고, 이를 기반으로 고강도 하이드로겔을 성공적으로 구현하였다. 다양한 화학·물리적 분석을 통해 아민 기능기의 도입과 옥시프로필 곁사슬의 형성이 확인되었으며, 기능화가 이루어졌음을 검증하였다. 특히 분자량 분석 결과, KL 대비 OL에서 분자량이 유의하게 증가하는 경향이 관찰되었는데, 이는 옥시프로필 곁사슬 도입 및 구조적 확장이 이루어졌음을 시사한다. 제조된 리그닌 기반 하이드로겔은 내부에 다양한 형태의 공극 구조를 형성하였고, 고리 열림 반응에 기반한 가교가 효과적으로 진행된 것으로 나타났다. 또한 이중 기능화 리그닌을 적용한 하이드로겔은 기존 시스템 대비 네트워크 안정성이 향상되었으며, 기계적 성능 측면에서 강도 및 내구성이 유의하게 개선되었다. 이러한 성능 향상은 이중 기능화 리그닌이 네트워크 내에서 결합점 제공과 동시에 유연한 곁사슬에 의한 재배열 및 에너지 소산을 유도함으로써, 3차원 네트워크의 구조 조직화와 기계적 강화에 기여한 결과로 해석된다. 본 연구는 리그닌의 연속 기능화(아민화–옥시프로필화)를 통해 리그닌을 하이드로겔용 빌딩블록으로 전환하고, 네트워크 구조 제어를 기반으로 고강도 하이드로겔을 구현할 수 있음을 제시하였다. 본 연구는 리그닌 기반 하이드로겔의 구조–물성 상관성을 확립하는 데 기여하며, 향후 지속가능 고분자 네트워크 소재 개발 및 다양한 응용(환경 정화, 기능성 코팅, 소프트 소재 등)으로 확장 가능한 기반 기술로 활용될 수 있을 것으로 기대된다.