1. 서 론
석탄, 석유, 천연가스 등과 같은 화석연료는 과거 서식했던 동·식물의 유해가 지하부에 매장되어 오랜 시간 동안 높은 압력과 열을 받아 형성된 연료이다. 화석연료는 값이 저렴하고, 연소시킬 경우 단위 질량 당 발생하는 에너지의 양이 큰 장점 때문에 에너지자원으로 광범위하게 사용되고 있다. 그러나 에너지를 얻기 위해 화석연료를 연소시키면 질소산화물, 황산화물 등과 같은 대기오염물질들이 발생하며 이들은 지구온난화, 엘니뇨 등과 같은 이상기온 현상 등의 다양한 환경문제를 유발한다. 이뿐만 아니라 화석연료는 매장량이 한정된 유한자원이며 자원의 편중이 심하므로 시장의 흐름에 민감하여 가격과 공급이 불안정한 단점이 있다.
따라서 최근 세계 각국은 G8, APEC 정상회담 등을 통해 화석연료 사용의 의존도를 줄이고, 태양열, 지력, 풍력, 조력 및 바이오에너지 등과 같은 신재생 에너지 개발을 통한 친환경 성장을 실현하기 위하여 노력하고 있다.1,2) 이 중 바이오에너지는 바이오매스를 연료로 하여 얻어지는 에너지를 의미하는데 바이오매스는 연간생산량이 석유 전체 매장량과 비등하며 질소산화물, 황산화물 등과 같은 대기오염물질 발생시키지 않는 청정에너지원이다.3,4) 또한, 바이오매스는 열분해, 가스화, 효소 당화 및 발효 등과 같은 물리적, 생화학적 열화학적 공정 등 어떤 변환공정을 거치냐에 따라서 다양한 형태의 에너지로 변환 가능한 장점이 있다.5)
이중 급속열분해 공정은 산소가 없는 비활성 조건 하에서 450-550°C 온도에서 짧은 시간(1-2초) 동안 열분해하여 생성되는 휘발성 유기화합물을 냉각장치, 전기집진 장치를 이용하여 짙은 갈색의 바이오오일을 얻는 대표적인 열화학적 변환공정이다. 급속열분해 공정은 원료의 제한이 적으며 공정이 간단하고, 생산되는 바이오오일의 수율이 높은 장점이 있다. 생산된 바이오오일은 일반 목질칩과 비교하여 3배 정도 높은 에너지밀도를 갖는 장점이 있다.6) 급속열분해 공정을 통해 생산되는 주요 생산물인 바이오오일의 수율 및 물리화학적 특성은 바이오매스의 종류, 시료의 입자크기, 반응기 형태, 열분해 온도, 열분해 기체의 체류시간에 영향은 받는다고 보고된 바 있다.7) 다양한 열분해 영향 인자 중에서 열분해 온도는 바이오오일 수율에 가장 큰 영향을 미치는 열분해 영향인자로 알려져 있으며 이에 대한 바이오매스 급속열분해 공정에 관한 연구가 많이 진행되고 있다.8,9)
본 연구에서는 유동형반응기를 이용하여 국내에서 발생하는 소경목 자원 중 침엽수와 활엽수종인 낙엽송과 신갈나무를 다양한 온도조건에서 급속 열분해하여 바이오오일을 생산하였다. 각 온도조건에서 생산된 바이오오일의 수율 변화를 관찰하고, 바이오오일의 물리, 화학적 특성을 분석하여 열분해 온도가 바이오오일의 수율 및 물성에 미치는 영향을 규명하였다.
2. 재료 및 방법
2.1 공시재료
본 연구에서는 수피와 가지가 포함된 낙엽송(Larix Kaempferi)과 신갈나무(Quercus mongolica) 소경목을 공시재료로 사용하였다. 열분해를 수행하기 전 각 시료는 분쇄기(PULVERISETTE 19, Fritsch, Germany)를 사용하여 입자크기 0.5 mm이하로 분쇄하여 목분 형태로 사용하였으며 평균 함수율은 8%를 유지하였다. 낙엽송과 신갈나무를 구성하는 탄소, 수소, 질소, 산소의 함량은 원소분석기(CHNS 932, USA)를 이용하여 측정하였으며 산소의 함량은 백분율을 기준으로 탄소, 수소, 질소 함량의 차를 이용하여 계산하였다. 각 시료의 화학조성을 측정하기 위하여 홀로셀룰로오스와 리그닌의 함량을 각각 Wise 법(1946)10) 과 72% 황산가수분해법(TAPPI method (T222 om-88))에 의거하여 정량하였다.
2.2 열중량 분석
급속열분해 공정을 실시하기 전 공시재료인 낙엽송과 신갈나무의 열분해 특성을 관찰하기 위해서 열중량 분석을 실시하였다. 열중량 분석은 비활성 가스인 질소 조건에서 승온속도 10 °C/min로 설정하였으며 측정범위는 40-800°C내에서 분석하였다. 분석 기기로는 서울대학교 농생명과학공동기기원의 Q-5000 IR(TA instruments, USA)을 이용하였다.
2.3 급속열분해 공정
본 연구에서는 유동형 반응기를 이용하여 낙엽송과 신갈나무 소경목의 급속열분해 공정을 실시하였다. 각 시료는 시간당 150 g의 속도로 스크류형 공급기를 통해 반응기 내부로 공급되었다. 반응기 내 균일한 열전달을 위해 200 g의 모래를 반응기에 투입하였으며 모래의 효율적인 분산과 반응기 내 비활성 상태 유지를 위해 질소가스를 공급하였다. 체류시간은 반응기 부피를 단위시간 당 반응기 내부로 유입되는 질소의 부피로 나누어 계산하였으며 흘려주는 질소가스 유량을 조절하여 1.3초로 고정하였다. 급속열분해 공정 후 생성된 휘발성 유기화합물은 사이클론 장치를 거치면서 바이오탄으로 분리되고, 냉각장치 및 전기집진 장치를 거치면서 액상의 바이오오일로 응축되었다. 열분해 생성물인 바이오탄, 바이오오일, 가스의 수율은 다음식에 따라 계산하였다.
2.4 바이오오일의 물리, 화학적 특성 분석
각 온도조건별로 생성된 바이오오일의 물리, 화학적 특성을 분석하기 위해 수분함량, 점도, 화학적 성분을 분석하였다. 바이오오일의 수분함량은 870 KF Titrino plus(Radiometer, Switzerland)를 이용하여 측정하였으며 Hydranal Compostie 5(Riedel de Haen 34805)를 적정용 시약으로 사용하였다. 점도는 모세관식 점도계를 사용하여 온도조건 40°C에서 측정하였다. 바이오오일에 존재하는 주요 화학물의 성분을 분석하기 위해서 불꽃 이온화 검출기(flame ionization detector, FID)와 질량 선택성 검출기(mass selective detector, Agilent Technology 5975C)가 장착된 Agilent 7890A 가스 크로마토그래피를 이용하여 분석하였다(분석 칼럼 DB 5(30 m × 0.25 mm × 0.25 μm)). 불꽃 이온화 검출기는 300°C, injector는 250°C 조건에서 분석하였으며 오븐온도는 50°C에서 5분간 유지한 후 3 °C/min 승온속도로 280°C까지 승온 후 10분간 유지하였다. 또한, 바이오오일에 존재하는 화합물의 정성 및 정량 분석을 위해 NIST (National Institute of Standards and Technology) spectral mass library와 내부표준물질로는 플로란센(Sigma) 용액(25 mg fluoranthene/ml acetone)을 사용하였다.
3. 결과 및 고찰
3.1 원소조성 및 화학조성
낙엽송과 신갈나무의 원소조성과 화학조성을 분석하여 Table 1에 나타냈다. 원소조성 결과 신갈나무는 낙엽송과 비교하면 탄소함량은 높으나 산소함량은 낮은 것으로 나타났다. 반면 수소와 질소의 함량은 낙엽송과 신갈나무두 수종 모두 비슷한 수준을 나타냈다. 공시재료의 화학조성을 살펴보면 침엽수종인 낙엽송이 활엽수종인 신갈나무에 비해 홀로셀룰로오스 함량은 2.5% 낮은 반면 리그닌함량은 3.8% 높은 것으로 확인되었다. 일반적으로 침엽수는 활엽수에 보다 홀로셀룰로오스 함량이 적고, 리그닌 함량이 많다고 알려졌으며 본 연구에서 사용한 공시재료에서도 유사한 결과를 확인하였다.
Table 1.
Elemental composition and chemical content of feedstock
| Elemental analysis (%) | Components analysis (% dry basis) | ||||||
|---|---|---|---|---|---|---|---|
| C | H | O* | N | Holocellulose | Lignin | Ash | |
| Larix | 45.2 | 6.7 | 47.7 | 0.4 | 72.4 | 29.9 | 0.16 |
| Quercus | 47.8 | 6.6 | 45.4 | 0.2 | 74.9 | 26.1 | 0.42 |
3.2 열중량 분석
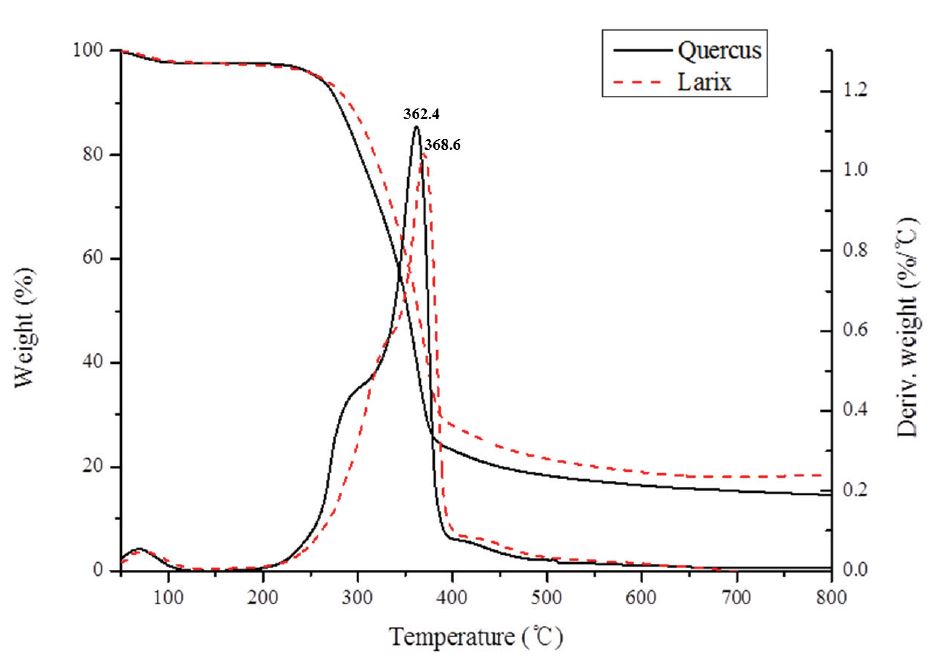
급속열분해 공정에 앞서 낙엽송과 신갈나무의 열적 특성을 분석하기 위하여 열중량 분석을 시행하였으며 분석결과를 Fig. 1과 Table 2에 나타냈다. 낙엽송과 신갈나무는 측정 범위 내 최종 온도인 800°C까지 꾸준히 분해되는 경향을 나타냈다. 초기 100°C에서 소량의 중량감소가 관찰되었으며 이는 시료 내 존재하던 수분 손실로 나타나는 것으로 사료된다.11) 이후 각 시료는 200-400°C 범위온도에서 중량감소가 관찰되었으며 300°C 부근에서의 변곡점과 360-370°C 부근의 극점을 관찰하였다. 300°C 부근의 변곡점은 일반적으로 헤미셀룰로오스 분해로 발생하며 360-370°C 부근의 극점은 셀룰로오스 내 글루코사이드 결합이 끊어지면서 셀룰로오스 올리고머가 저분자량 화합물로 분해되어 나타나는 중량변화이다.12) Fig. 1에서 확인할 수 있듯이 신갈나무는 낙엽송에 비해 300°C부근의 변곡점이 더 크고 넓게 관찰되었다. 이는 활엽수종인 신갈나무가 침엽수종인 낙엽송에 비해 상대적으로 높은 헤미셀룰로오스 함량을 나타내어 열중량 분석과정에서 상대적으로 많은 헤미셀룰로오스가 분해되어 관찰되는 변곡점의 크기가 큰 것으로 사료된다. 리그닌의 경우 열분해 초기 온도부터 최종 온도까지 광범위한 온도조건에서 서서히 분해되는 특성이 있으며 최대분해온도(temperature at maximum degradation rate = TM, °C) 이후 시료의 중량이 감소하는 것은 리그닌 분해에 의한 것으로 분석된다. 휘발성 가스는 급속열분해 과정에서 바이오오일로 회수될 수 있는 휘발성 유기화합물과 비응축성가스(CO, CO2, H2, CH4 등)를 의미하며 낙엽송에서 81.6%, 신갈나무에서 85.5%로 나타났다. 최종 온도인 800°C에서 낙엽송과 신갈나무 시료의 탄 수율을 살펴보면 18.4%(낙엽송), 14.5%(신갈나무)로 침엽수인 낙엽송에서 높게 나타났다. 이러한 결과는 앞서 언급한 각 시료의 화학조성 차이인 것으로 사료된다. 리그닌은 넓은 온도범위에서 분해가 서서히 진행되기 때문에 최종온도는 800°C에서 미처 분해되지 못한 리그닌이 탄으로 전환된 것으로 추측된다. 낙엽송은 신갈나무에 비해 리그닌 함량이 높기 때문에 상대적으로 최종온도 800°C에서 열분해 되지 못한 리그닌 비율이 높아 낙엽송에서 더 높은 탄수율을 나타낸 것으로 분석된다.
최대분해온도는 시료가 최대 속도로 분해되는 온도를 의미하며 낙엽송과 신갈나무에서 각각 368.6°C, 362.4°C로 큰 차이가 나타나지 않았으며, 최대분해율(maximum degradation rate at TM = VM, wt%/°C) 또한 낙엽송에서 1.0 wt%/°C, 신갈나무 1.1 wt%/°C로 큰 차이가 없음을 확인하였다.
3.3 급속열분해 공정
3.3.1 바이오오일의 수율
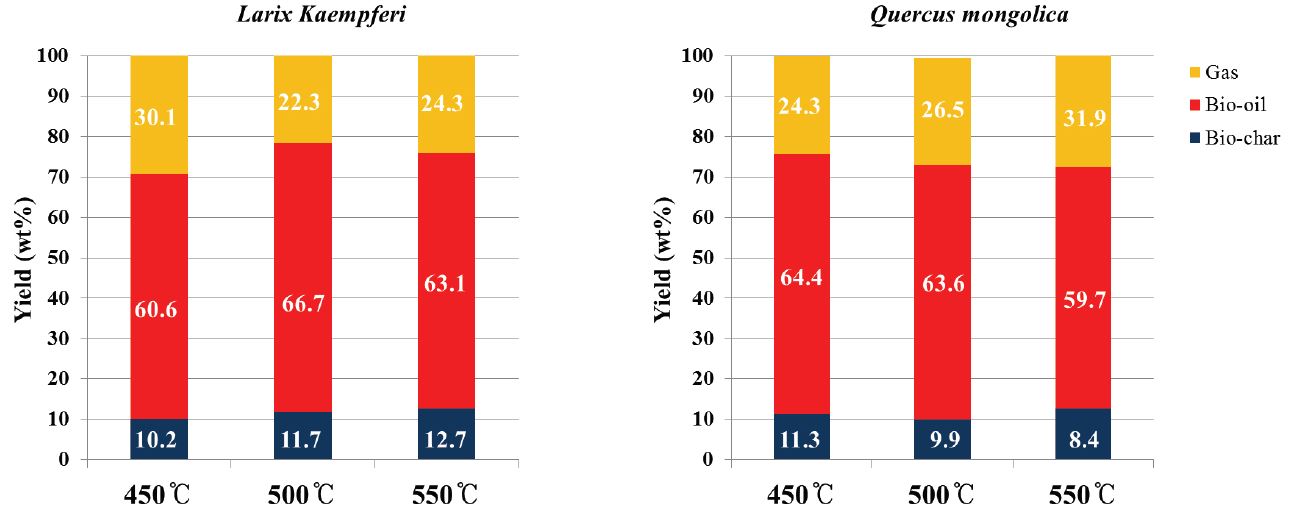
본 연구에서는 급속 열분해 공정 중 열분해 온도가 열분해 산물(바이오오일, 바이오탄, 비응축성 가스)의 수율에 미치는 영향을 살펴보기 위하여 다음 온도조건 450°C, 500°C, 550°C에서 급속열분해 공정 실시하였다. 생성된 급속열분해 산물의 수율을 Fig. 2에 나타냈으며 생성된 바이오오일의 수율은 두 수종에서 59.7-66.7 wt% 수준으로 나타났다. 낙엽송의 경우 500°C(66.7 wt%)에서, 신갈나무는 450°C(64.4 wt%)에서 가장 높은 바이오오일의 수율을 나타냈다. 선행연구에 의하면 다양한 바이오매스에서 유래한 바이오오일의 수율은 약 500°C에서 최고 수율을 나타낸다고 보고된바 있다.8,13) 한편 본 연구에서는 낙엽송 급속열분해는 500°C에서 바이오오일의 최대 수율을 나타냈으나 신갈나무 급속열분해는 450°C에서 최대수율을 나타냈다. 이러한 결과는 신갈나무는 낙엽송에 비해 열적으로 불안정한 홀로셀룰로오스 함량이 높고, 열적으로 안정한 리그닌 함량이 낮기 때문으로 판단된다. 온도 조건 550°C에서는 낙엽송과 신갈나무 두 시료 모두에서 가장 낮은 바이오오일의 수율(낙엽송 63.1 wt%, 신갈나무 59.7 wt%)을 나타냈다. 이는 열분해 온도 550°C에서는 과도한 열분해로 인해 1차 열분해 산물의 2차 분해가 유발되어 휘발성유기화합물로부터 전환되는 바이오오일의 수율이 낮기 때문인 것으로 사료된다.
급속열분해 후 생성된 고형성분인 바이오 탄 수율은 8.4-12.7 wt%로 나타났다. 낙엽송 바이오탄은 550°C에서 12.4 wt% 신갈나무 바이오탄은 450°C에서 11.3 wt%로 최대 수율을 나타냈다.
3.3.2 바이오오일의 물리, 화학적 특성
각 온도 조건별로 생산된 낙엽송 및 신갈나무 바이오오일의 물리, 화학적 특성을 분석하기 위하여 수분함량, 점도를 측정하였으며 그 결과는 Table 3에 나타냈다. 바이오 오일의 수분함량은 낙엽송의 경우 450°C에서 26.0%, 500°C에서 25.3% 그리고 550°C에서 28.2%를 나타냈으며 신갈나무 경우 450°C에서 25.6%, 500°C에서 24.5%, 550°C에서 25.9%를 나타냈다. 낙엽송과 신갈나무 바이오매스의 초기 수분함량을 고려해볼 때(낙엽송 8.1 wt%, 신갈나무 8.5 wt%) 바이오오일의 수분은 초기 시료보다 소폭 상승한 것으로 나타나며 이는 시료 내에 존재하던 자유수와 결합수로부터 유래했을 뿐만 아니라 셀룰로오스와 리그닌의 열분해과정에서 발생하는 탈수반응에 의한 것으로 사료된다.14,15) Bridgewater(2004)에 의하면 바이오오일에 존재하는 수분은 증발잠열로 인하여 바이오오일의 발열량을 낮추고, 연소율을 감소시키는 등 부정적인 영향을 미치기도 하지만 바이오오일의 점도를 낮춰 유동성을 좋게 하기도 한다고 보고된바 있다.7) 본 연구에서 생산된 바이오오일은 낙엽송과 신갈나무 시료에서 500°C에서 가장 낮은 수분함량을 나타내어 500°C에서 생산된 바이오오일의 발열량이 가장 높을 것으로 추측된다. 낙엽송과 신갈나무에서 생산한 바이오오일의 점도는 13-17.7 cSt 범위로 측정되었으며 열분해 온도에는 크게 영향을 받지 않는 것으로 나타났다.
Table 3.
Physicochemical properties of bio-oil
| Larix | Quercus | |||||
|---|---|---|---|---|---|---|
| 450°C | 500°C | 550°C | 450°C | 500°C | 550°C | |
| Water content (%) | 26.0 | 25.3 | 28.2 | 25.6 | 24.5 | 25.9 |
| Viscosity (cSt) | 13 | 17.7 | 17.1 | 16.2 | 15.1 | 13.4 |
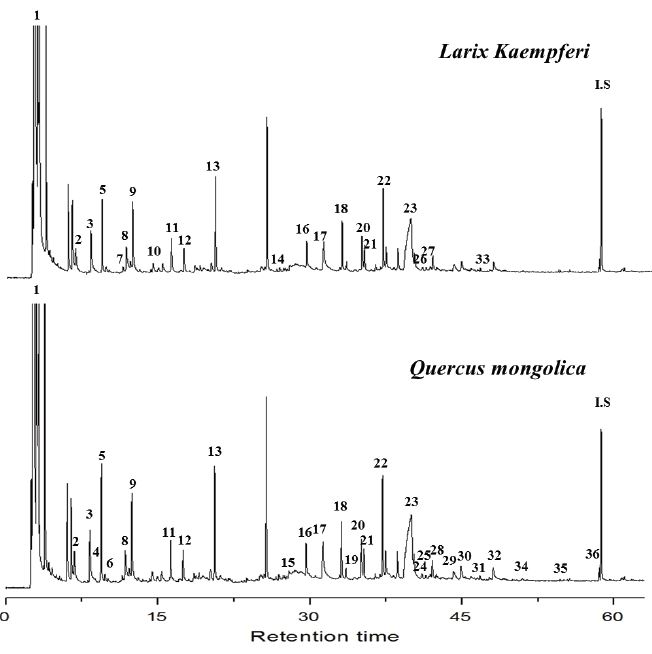
각 온도조건 별로 생산된 바이오오일의 수율, 수분 함량들을 미루어 볼 때 낙엽송 및 신갈나무 소경목으로부터 바이오오일 생산의 최적 온도조건은 500°C이며 최적조건인 500°C에서 생산된 바이오오일 내에 존재하는 화합물을 분석하기 위해 GC-MS 분석을 실시하였다. 낙엽송과 신갈나무로부터 생산된 바이오오일의 크로마토그램은 Fig. 3과 같으며 각 화합물의 상대적인 양을 측정하여 Table 4에 나타냈다.
Table 4.
Concentration of chemical compounds in bio-oil from Larix Kaempferi and Quercus mongolica
약 36개의 화합물이 검출되었으며 낙엽송 유래 바이오오일에서는 총 22개의 화합물이, 신갈나무 유래 바이오오일에서는 총 31개의 화합물이 검출되었다. 생성된 주요 화합물로는 셀룰로오스와 헤미셀룰로오스의 C-C와 C-O 결합의 절단(bond-cleavage), 탈수(dehydration), 아세틸기 이탈(elimination), 가수분해(hydrolysis)등에 의해 생성되는 acetic acid, levoglucosan, ketone류 화합물 및 aldehyde류 화합물이 있다. Butanedial과 고리형 화합물인 2-furaldehyde, 1-pentene-3-one의 수율은 낙엽송과 신갈나무에서 큰 차이가 나타나지 않았다. 그러나 acetic acid의 함량은 신갈나무가 더 높게 나타났으며 이는 신갈나무가 낙엽송에 비해 헤미셀룰로오스 함량이 높아 열분해 과정에서 상대적으로 많은 acetyl group이 이탈하였기 때문으로 사료된다.16) 따라서 신갈나무로부터 생산된 바이오오일이 상대적으로 낙엽송으로부터 생산된 바이오오일에 비해 낮은 pH를 나타낼 것으로 추측된다. 리그닌 유래 물질로는 phenol, guaiacol류, syringols류가 있으며 이들은 리그닌 구조내부의 ether 결합의 가수분해가 촉진되어 생성된 것으로 판단된다. 침엽수인 낙엽송에는 G단위로 이루어진 리그닌으로 구성되어 있기 때문에 guaiacol류 화합물이 검출되었으며 활엽수인 신갈나무 리그닌은 주로 G, S 단위체로 이루어져 있으므로 guaiacol류 화합물과 syringol류 화합물이 검출되었다.
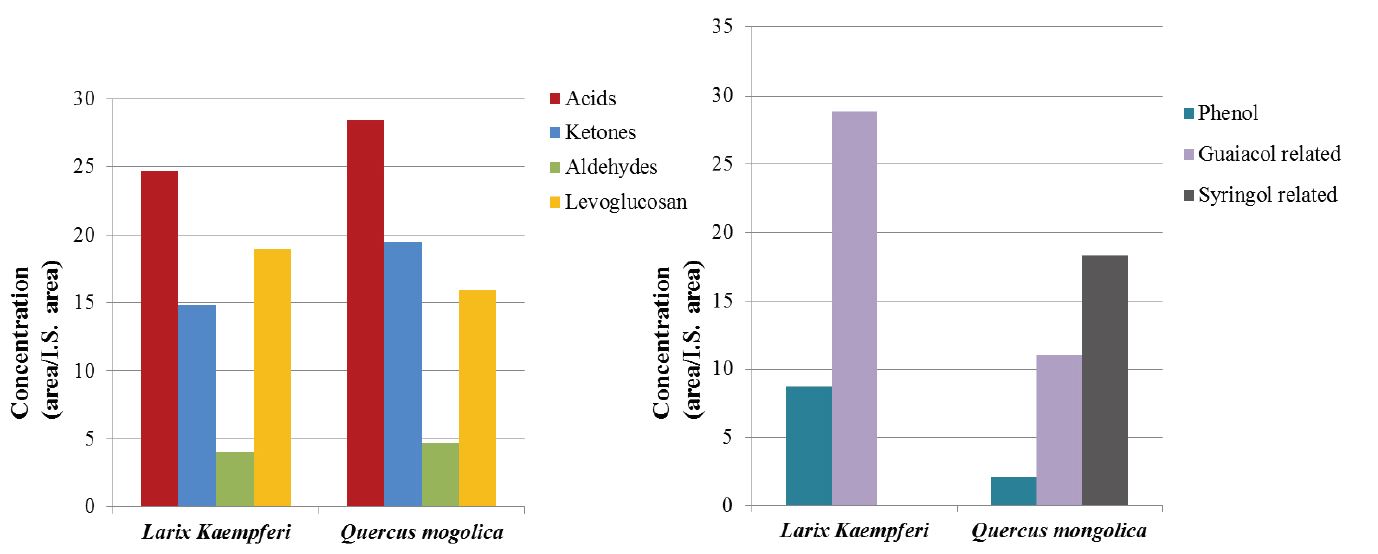
바이오오일에 함유된 화합물들을 화학 구조에 따라 acids, ketones, aldehydes, phenols, guaiacol류, syringol류로 그룹을 분류하여 Fig. 4에 나타냈다. 신갈나무 유래 바이오오일에서 acids, ketones, aldehydes 함량이 더 높은 것으로 나타났는데 이는 활엽수인 신갈나무의 홀로셀룰로오스 함량이 높고, 리그닌 함량이 낮아 셀룰로오스 열분해 시 생성되는 위 화합물의 수율이 높은 것으로 사료된다.
4. 결 론
낙엽송과 신갈나무 소경목의 급속열분해 공정 중 열분해 온도가 열분해 산물의 수율 및 물성에 미치는 영향을 구명하기 위해 유동형 반응기를 이용하여 온도조건 450°C, 500°C, 550°C에서 급속열분해 공정을 실시하였다. 각 시료의 화학 조성분석결과 낙엽송은 신갈나무에 비해 홀로셀룰로오스 함량이 낮고, 리그닌 함량이 높은 것으로 나타났다. 열중량 분석결과 휘발성 유기화합물은 81.56 wt%(낙엽송), 85.47 wt%(신갈나무)로 나타났으며 탄의 수율 18.44 wt%(낙엽송), 14.57 wt%(신갈나무)로 나타났다. 급속열분해 공정 후 생산된 바이오오일 수율은 낙엽송은 500°C에서 66.7 wt%로 최대수율을 나타냈으며 신갈나무는 온도조건 450°C에서 64.4 wt%의 최대수율을 나타냈다. 두 시료 모두 550°C에서 가장 낮은 수율을 나타냈으며 이는 과도한 열분해로 인해 1차 열분해 산물의 2차 분해가 유발된 것으로 추측된다. 생산된 바이오오일의 물성분석에 의하면 바이오오일에 함유된 수분함량은 24.5-26% 수준으로 나타났으며 두 시료 모두 500°C에서 생산된 바이오오일이 가장 낮은 수분함량을 나타냈다. 바이오오일에는 약 36종 이상의 화합물이 존재하는 것으로 확인되었으며, 주요 화합물로는 acetic acid, ketone류, aldehyde류 화합물, levoglucosan 등이 검출되었고, 이들의 농도는 신갈나무에서 생산된 바이오오일에서 상대적으로 높게 나타났다.