1. 서 론
목질계 바이오매스 기반으로 하는 에너지 원료의 개발은 지속적인 발전과 재생에너지 자원이라는 측면에서 각광을 받고 있다. 무분별한 수확이 아닌 계획적인 재배와 수확에 의하여 지속적인 개발이 가능하며 이런 개발을 통하여 재생에너지 자원 생산이 가능하다.
목질계 바이오매스를 원료로 바이오 알코올을 생산하기 위해서는 다당류를 단당으로 전환 시키는 공정과 전환된 단당을 알코올로 발효 시키는 공정을 거쳐야 된다. 목질계 바이오매스 내 존재하는 다당류로는 셀룰로오스와 헤미셀룰로오스가 대표적이며 이와 더불어 리그닌이라는 성분과 함께 3가지 주요 성분이 복잡한 구조를 이루고 있다.
이러한 복잡한 구조는 셀룰라아제나 헤미셀룰라아제와 같은 효소가 선택적으로 다당류에 흡착하여 단당화하는 것을 방해한다. 이 문제를 해결하기 위해서 목질계 바이오매스의 복잡한 구조를 파괴함으로써 효소가 쉽게 접근할 수 있도록 하는 전처리 공정이 필수적이다.1) 전처리 공정은 리그닌을 제거하는 공정2), 자이란을 제거하는 공정3), 셀룰로오스의 결정 구조4)를 파괴 시키는 공정으로 대별되며, 공정에 따라 이 세 가지 개념들 중 두 가지 이상 함께 사용되기도 한다.
산 가수분해 공정은 산 촉매 조건에서 가수분해 반응에 의하여 다당류에서 단당류로 전환시키는 공정이다.5) 산의 농도나 반응온도에 따라 진한 산 가수분해 공정과 묽은 산 가수분해 공정으로 대별되며 목질계 바이오매스 자원의 대부분을 효과적으로 당화 시킬 수 있지만 사용한 산의 처리 문제와 장비의 부식성과 같은 문제점을 가지고 있다. 산 가수분해 공정을 사용하여 셀룰로오스나 헤미셀룰로오스 다당류가 단당으로 전환되는 과정에서 공정에서 사용하는 약품에 따라 양이온 염이 생성 된다. 공정 과정에서 생성된 양이온 염은 발효 과정에서 균주의 성장과 활동을 저하시킨다.6,8)
에탄올 발효 공정에서 사용되는 발효 균주로는 Sac-charomyces cerevisiae가 가장 대표적으로 사용되고 있다. 에탄올에 대한 내성이 커서 에탄올 농도 15%까지 견디고 있으며 아세트산과 같은 유기산에 의한 발효 저해가 일어나지도 않는다.9) 단점으로는 일반적으로 유전자 조작을 하지 않는 한 xylose나 arabinose 같은 오탄당 발효를 하지 못하며 발효에 적합한 최적온도가 30-33℃이며 37℃이상에서 균주의 번식력과 생명력이 떨어지기 시작한다.10,11)
Kluyveromyces marxianus는 내열성을 가진 균주로 발효 조건이 높은 온도를 필요로 할 때 사용되는 균주로, 발효에 최적 온도는 35~45℃이기 때문에 높은 온도를 필요로 하는 동시 당화 발효 공정 등에 사용되고 있다.12,14) 본 연구에서는 발효 균주 중 K. marxianus가 양이온 염이 첨가된 배양액에서 염의 종류, 농도에 따른 에탄올 발효 특성을 확인 하고자 하였다.
2. 재료 및 방법
2.1 공시재료
2.1.1 공시 배지
표준 당 수용액에 사용한 시약은 glucose (OCI Co., Ltd., Korea), peptone (ventech bio Co., Ltd,. Ko-rea), malt extract (Bacto laboratories Pty., Ltd., Australian), yeast extract (Bacto laboratories Pty Ltd., Australian), KH2PO4 (Ducksan pure chemi-cal Co., Ltd., Korea), MgSO4·7H2O (Shinyo Pure Chemical Co., Ltd., Japan)를 사용했으며, 첨가한 염은 Na2SO4 (Deajung chemical & metals Co., Ltd., Korea), K2SO4 (Deajung chemical & metals Co., Ltd., Korea)으로 순도 99% 이상의 제품을 사용하였다.
2.1.2 공시 균주
사용 균주는 Kluyveromyces marxianus KCCM 32422(이후 K. marxianus로 약칭)을 한국미생물보존협회에서 분양받아 사용하였으며, K. marxianus의 발효 특성을 비교하기위한 비교군으로 Saccharomyces cerevisiae를 사용하였다.15)
2.2 실험방법
2.2.1 표준 당 수용액 제조
발효에 사용한 표준 당 수용액의 조성은 포도당 60.0 g/L, peptone 5.0 g/L, yeast extract 5.0 g/L, KH-2PO4 1.0 g/L, MgSO4·7H2O 2.0 g/L을 넣어 제조 하였다. 표준 당 수용액에 첨가한 염의 수준은 20.0℃ 용해도(Na2SO4 202 g/mL, K2SO4 120 g/mL)를 기준으로 3개의 농도로 나누어 첨가 하였다.
2.2.2 K. marxianus 배양
YM배지(glucose 10.0 g/L, yeast extract 3.0 g/L, malt extract 3.0 g/L, peptone 5.0 g/L) 20.0 mL에 K. marxianus 한 개의 colony를 넣고 18시간 이상 43.0℃ , 200 rpm 조건으로 진탕 배양기에서 배양 하였다. 18시간 이상 배양한 K. marxianus 배양액을 YM배지에 1%(v/v)비율로 넣은 후 43.0℃, 200 rpm 조건으로 진탕 배양기에서 배양하였다. 3시간 이후 1시간 간격으로 샘플을 채취하여 UV-visible spectrophotometer (UV-1601, Shimadzu, Japan)로 600 nm에서 흡광도를 측정하여 이후 에탄올 발효과정에서 효모 첨가 수준에 반영하였다.
3. 결과 및 고찰
3.1 K. marxianus와 S. cerevisiae의 발효 특성 비교
고온 발효 균주의 발효 특성을 확인하기 위하여 같은 배양액을 만들어서 에탄올 발효를 실시하였다. 각 효모의 최적 발효 온도에서 발효를 실시하였다. K. marxianus균주는 10시간이내에 포도당을 모두 소비하여 발효가 완료되었지만 S cerevisiae균주는 10시간 발효 후 배양액 분석 결과 30% 정도의 포도당이 아직 잔류하였다(Fig. 1). 이것은 K. marxianus가 S. cerevisiae보다 포도당을 에탄올로 더 신속하게 발효 시킨다는 것이다. 완전 발효 후 에탄올 농도는 12시간 발효 후 S. cerevi-siae에서 24.5 g/L로 K. marxianus의 23.4 g/L보다 더 많은 에탄올을 생산하였다.
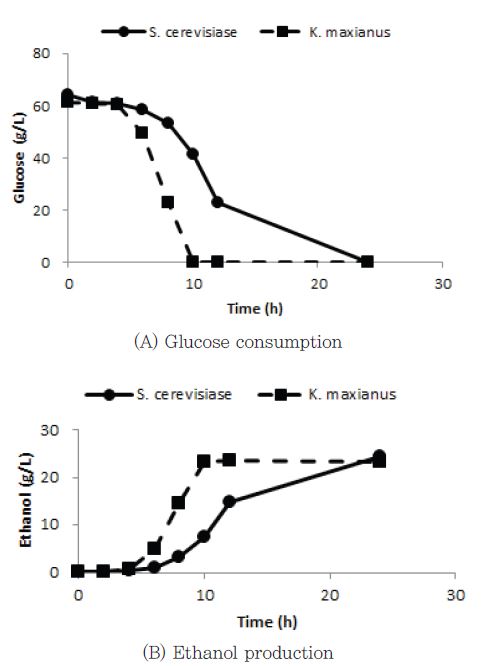
Fig. 1.
Time course profile for the glucose consumption and ethanol production by S. cerevisiae15) and K. marxianus.
3.2 칼륨 양이온이 K. maxianus발효에 미치는 영향
K. marxianus의 칼륨 양이온에 대한 발효 특성을 확인 하고자 배양액에 각각 황산칼륨을 최대 용해도 기준으로 1/3(0.46 M), 2/3(0.92 M), 3/3(1.38 M)을 첨가하여 확인 하고자 하였다.
발효 종료 후 최대 에탄올 농도는 칼륨 최대 용해도의 1/3에 해당하는 황산칼륨을 배양액에 첨가한 경우 23.4 g/L, 칼륨 최대 용해의 2/3에 해당하는 황산칼륨을 첨가한 배양액에서 22.9 g/L, 황산칼륨의 최대용해도에 해당하는 염을 첨가한 배양액의 발효에서 22.8 g/L를 보였다. 황산칼륨 용해도 값의 1/3에 해당하는 황산칼륨 첨가 배양액과 2/3에 해당하는 황산칼륨 첨가 배양액은 12시간이내에 포도당을 완전하게 소비하였지만, 황산칼륨 용해도 값에 해당하는 황산칼륨 첨가 배양액은 24시간에서 시료를 채취에서 포도당의 완전한 소비가 관찰되었다(Fig. 2).
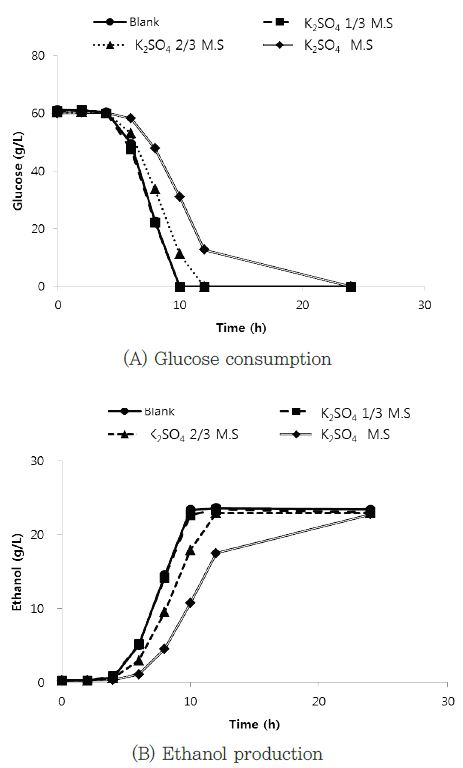
Fig. 2.
Time course profile for the glucose consumption and ethanol production by K. marxinus in the present of different concentration of potassium sulfate.
칼륨 양이온이 존재하는 조건에서 K. maxianus와 S. cerevisiae의 발효 특성을 비교하였다. 황산칼륨 최대 용해도의 2/3에 해당하는 황산칼륨을 첨가하였을 때 K. maxianus는 12시간 발효에서 포도당이 소진된 것을 확인하였지만 S. cerevisaie에서는 41.1 g/L의 포도당이 잔류 하는 것이 관찰되었다. 24시간 발효 후 시료에서는 S. cerevisiae에서도 포도당의 소진을 확인하였다(Fig . 3).
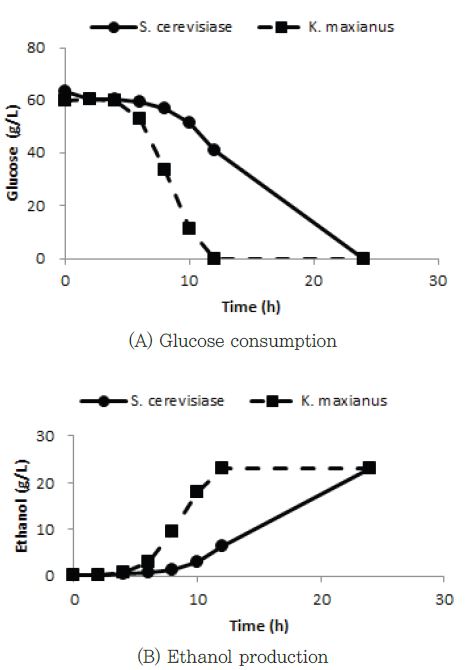
Fig. 3.
Time course profile for the glucose consumption and ethanol production by S. cerevisiae15) and K. marxianus. in the 2/3 maximum solubility sodium sulfate.
3.3 나트륨 양이온이 K. maxianus발효에 미치는 영향
K. marxianus의 나트륨 양이온에 대한 발효 특성을 확인 하고자 당 수용액에 각각 황산나트륨을 최대 용해도 기준으로 1/3(0.95 M), 2/3(1.90 M), 3/3(2.84 M)을 첨가하여 확인 하고자 하였다(Fig. 4).
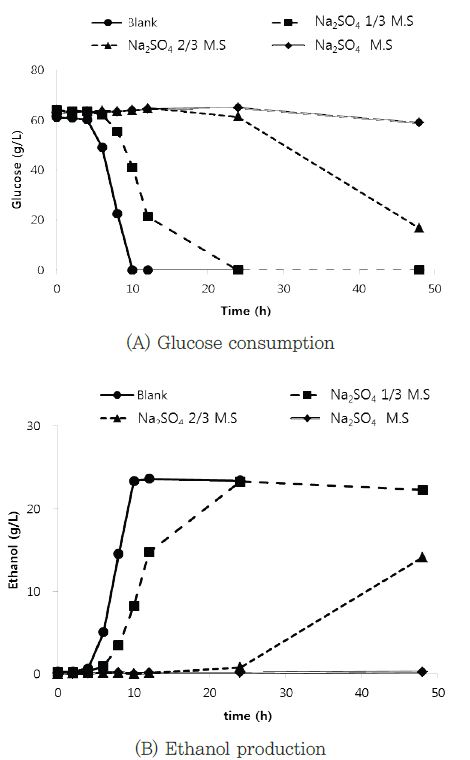
Fig. 4.
Time course profile for the glucose consumption and ethanol production by K. marxinus in the present of different concentration of sodium sulfate.
발효 종료 후 최대 에탄올 농도는 최대 용해도의 1/3에 해당하는 황산나트륨을 당 수용액에 첨가한 경우 22.3 g/L, 최대 용해의 2/3에 해당하는 황산나트륨을 첨가한 당 수용액에서 14.1 g/L, 황산나트륨의 최대용해도에 해당하는 염을 첨가한 배양액 발효에서 0.2 g/L를 보였다. 황산나트륨을 첨가한 배양액은 황산칼륨을 첨가한 배양액은 48 h 이후 1/3농도의 황산나트륨을 첨가한 배양액만 발효가 완료 된 것을 확인 하였다. 2/3농도의 황산나트륨을 첨가한 배양액은 48 h에서 14.1 g/L의 에탄올이 생성되었고, 포도당은 16.8 g/L가 남아 있는 것을 확인 하였다. 최대 용해도 값의 1/3에 해당하는 황산나트륨 첨가 당 수용액은 24 h에서 포도당이 전부 소비된 것을 확인 할 수 있었다. 하지만 2/3농도의 황산나트륨이 첨가된 당 수용액은 48 h에서 16.8 g/L의 포도당이 남아 있었고, 최대 용해도의 황산나트륨이 첨가된 당 수용액은 59.0 g/L가 남아 48 h이후에도 발효가 종료되지 않은 것을 확인 할 수 있었다.
나트륨 양이온이 존재하는 조건에서 K. maxianus와 S. cerevisiae의 발효 특성을 비교하였다(Fig. 5). 황산칼륨 최대 용해도의 2/3에 해당하는 황산나트륨을 첨가하였을 때 K. maxianus와 S. cerevisaie에 모두 48 h까지 발효가 종료되는 것을 확인 할 수 없었다. 하지만 남아있는 포도당량이 K. marxianus는 16.8 g/L, S. cerevisiae는 51.5 g/L로 K. marxianus가 같은 시간에서 S. cerevisiae보다 많은 양의 포도당을 소모한 것을 확인 할 수 있었다. 에탄올 농도에서도 K. marxianus는 14.1 g/L가 만들어 졌고, S. cerevisiae는 2.7 g/L로 에탄올 생상량에서도 K. marxianus가 높은 것을 확인 할 수 있었다.
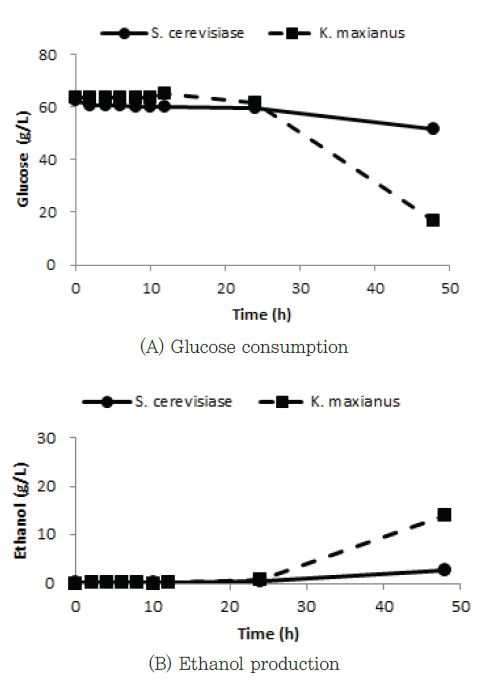
Fig. 5.
Time course profile for the glucose consumption and ethanol production by S. cerevisiae15) and K. marxianus. in the 2/3 maximum solubility sodium sulfate.
4. 결 론
본 연구에서는 당 수용액에 황산칼륨과 황산나트륨을 첨가하여 수용액 내 존재하는 수용성 염이 K. marxianus의 에탄올 발효과정에서 미치는 영향을 확인 하고자 하였다. 염이 첨가되지 않은 당 수용액보다 염이 첨가된 당 수용액으로 발효에 사용했을 경우 K. marxianus의 에탄올 발효 속도를 저하시키는 것을 확인 할 수 있었다. 또한 당 수용액에 첨가한 수용성 염의 수준이 높아질수록 발효 속도가 더 느려지는 것이 확인되었다. 또한 S. cerevisiae와 비교 했을 때 K. marxianus의 에탄올 발효 속도가 빠르게 진행 되었으며, 염이 첨가 된 당 수용액을 발효 했을 때 S. cerevisiae보다 발효 속도가 더 빠른 것을 확인하였다.
본 연구를 통해 수용성 염이 첨가된 당 수용액을 발효 할 경우 K. marxianus의 발효 속도가 늦는 것을 확인 했지만, 다른 에탄올 발효 균주인 S. cerevisiae보다 발효 속도가 빠른 것을 확인 할 수 있었다. 또한 수용성 염으로 인한 발효 저하효과는 S. cerevisiae보다 K. marxianus가 더 적게 받는 것을 확인 하였다.




