1. 서 론
바이오매스 주 구성성분인 리그닌은 셀룰로오스 다음으로 세계에서 가장 풍부한 재생가능한 소재이며 실제 많은 양의 리그닌이 펄프제지산업 뿐만 아니라 바이오에너지를 위한 셀룰로오스 당화공정 등 다양한 관련 산업으로부터 부산물 또는 폐기물로 발생되고 있다. 이러한 리그닌의 가치증대 및 활용은 석유기반 경제구조를 대체하는 바이오매스의 자원화와 에너지화 산업구조의 효용성을 높이는 데 있어서 매우 중요한 역할을 할 수 있을 것으로 판단되고 있으나 리그닌 고유의 복잡한 구조와 구성요소의 다양성 및 불규칙성 때문에 표준화된 자원 또는 소재로서 상업적 활용은 충분히 이루어지지 못하고 있는 실정이다.1,2)
리그닌은 무정형 3차원의 매우 복잡한 구조를 가지고 있으며 그 구조를 이루는 단위체의 다양성과 불규칙성으로 정확한 구조 및 특징을 정의하는 것은 매우 어렵기 때문에 이러한 리그닌의 추출 및 분리, 석출 과정 등을 통해 최종 제조되는 리그닌의 구조나 특징의 균일성을 확보하기 위한 연구개발이 필요한 상황이라고 할 수 있다. 리그닌은 식물의 종류와 생장환경, 존재하는 부위 및 실제 리그닌을 분리, 정제하는 공정 등에 따라 다양하게 나타나지만, C6-C3 페닐프로파노이드를 지닌 p-coumaryl alchol(H), guaiacyl alchol(G), sinapyl alcohol(S) 세 가지 종류의 단위체를 기반으로 이루어진 3차원의 비정질 중합체로 되어있다.3,4) 이러한 리그닌은 분리되는 방식에 따라 그 구조적 특성과 성질이 상이하게 나타나는 데 현재 이러한 리그닌의 대량 발생원으로 제지산업의 주요 원료인 펄프를 생산하는 펄프산업이 대표적이라고 할 수 있다. 목재칩 또는 비목질 바이오매스 내 리그닌을 용해, 제거하여 셀룰로오스 섬유를 제조하는 화학펄프화 공정은 부산물로서 다량의 리그닌을 발생시키고 있다. 특히, 다양한 펄프화 과정 중에서 전 세계적으로 가장 많이 활용되고 있는 방식으로 탈리그닌화율이 높을 뿐만 아니라 강도가 우수한 섬유를 얻을 수 있는 크라프트 펄핑방식을 들 수 있다.5,6)
크라프트 리그닌은 크라프트 펄핑 중에 발생되는 흑액으로부터 만들어진 리그닌으로서 실제 전 세계 리그닌 생산량 중 약 85%를 차지하는 대표적인 리그닌이라고 할 수 있다.6,7) 크라프트 증해 시 목재는 대체로 170°C 내외의 온도조건에서 약 2시간 동안 수산화나트륨과 황화나트륨 수용액에서 처리되는데, 이 과정 중 목재 리그닌의 약 90-95%가 용해되어 흑액으로 배출된다.8) 크라프트 리그닌은 크라프트 펄핑 흑액을 주로 무기산 또는 이산화탄소 등으로 중화 및 산성화하여 석출시키고 이후 산세척 등을 통해 정제하여 제조되게 된다.9) 이렇게 크라프트 펄핑 흑액으로부터 만들어지는 리그닌의 활용은 현재 많은 관심의 대상이 되고 있는데, 석유화학에서 유래된 다양한 페놀성 고분자물질들을 대체할 수 있는 정밀화학 소재로서 바닐린, 분산제, 우레탄 등 다양한 소재와 용도로써 활용하기 위한 기술개발이 활발히 이루어지고 있다.10)
리그닌의 상업적 활용을 위한 연구개발에서 어떤 리그닌을 활용하고 사용할 것인가는 매우 중요한데 리그닌의 구조나 특징이 획득되는 과정과 조건에 따라 크게 달라질 수 있게 때문이다. 따라서 본 연구는 국내산 소나무의 크라프트 흑액으로부터 리그닌의 석출하여 획득할 때 다양한 석출조건에 따른 영향과 석출된 리그닌의 특성변화 등을 알아보았다. 이러한 연구결과들을 토대로 향후 표준화된 리그닌의 획득을 통한 리그닌 활용성 증대기술개발의 기반을 확보하고자 하였다.
2. 재료 및 방법
2.1 공시 재료
크라프트 리그닌의 제조를 위하여 10-30 mm 크기의 국내산 소나무 칩을 P 업체에서 분양받았으며 TAPPI standard T264 cm-97에 의거하여 함수율을 측정한 결과 펄핑 전 함수율은 35.1%였다.
2.2 크라프트 펄핑
실험실용 다이제스터를 이용하여 국내산 소나무 칩을 Table 1에서 정리한 바와 같이 활성알칼리 20%, 황화도 25%, 액비 5:1 조건으로 펄핑하였다. 증해 온도인 170°C까지 최고온도 도달시간은 50분이었고 이후 90분 동안 증해를 실시하였다. 펄핑 후 흑액을 채취하고 얻어진 펄프는 흑액이 나오지 않을 때까지 충분히 깨끗이 세척하여 TAPPI standard T204 cm-97에 의거하여 펄프내의 잔존 리그닌을 측정하였다.
Table 1.
Pulping conditions of korean pine chips Kraft pulping
| Pulping conditions |
|---|
| Active alkali (%) | 20 |
| Sulfidity (%) | 25 |
| Max. temp. (°C) | 170 |
| Time to max. temp. (min) | 50 |
| Time at max. temp. (min) | 90 |
| Liquor to wood ratio | 5:1 |
2.3 크라프트 리그닌 석출
크라프트 펄프흑액 시료 각 20 mL에 황산(98%, w/w)을 일정량 첨가하여 리그닌을 침전시켰는데, pH에 따른 리그닌의 침전효율을 평가하기 위해 황산의 첨가량을 달리하여 pH 3.5-10의 범위로 조절하였다. 이 후 원심분리기로 3,000 rpm으로 15분 동안 원심분리하여 침전물을 분리하여 석출리그닌을 획득하였으며 얻어진 석출리그닌은 pH 2의 황산 수용액으로 2회 세척하여 잔존 알칼리염 및 불순물 등을 제거하였다. 이후 60°C 오븐에서 항량에 달할 때까지 건조한 후 리그닌의 특성을 분석하였다. Fig. 1은 리그닌의 석출과 석출리그닌 특성분석을 위한 단계별 분석체계를 나타낸 모식도이다.
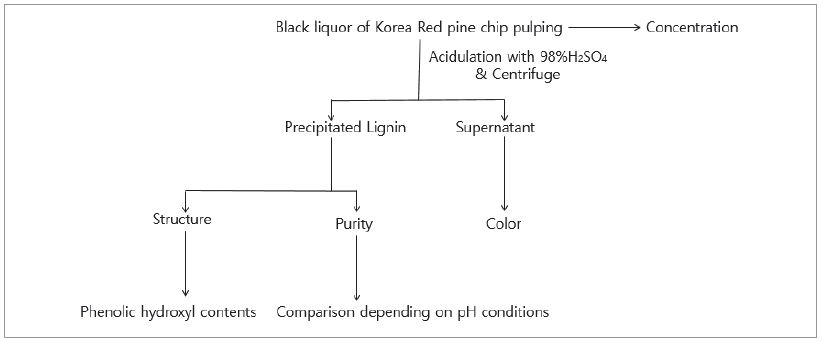
Fig. 1.
Schematic diagram of the precipitation process of kraft lignin.
2.4 석출리그닌의 특성 평가
석출된 크라프트 리그닌의 pH조건에 따른 특성을 비교하기 위하여 UV-VIS분석(UV/Vis spectrophotometer, SHIMADZU UV-1800)을 실시하였다. 리그닌의 분광법에 적합한 스펙트럼의 자외선 범위는 200-380 nm이며 이 범위에서 흡수된 에너지는 전자의 π-π* 전이를 나타내는 것으로 보고된 바 있다.11,12) 특히, 크라프트 리그닌의 경우 일반적으로 약 280 nm에서 나타나는 피크로 분석하는데, 이는 이 파장에서 guaiacyl과 syringyl에 기초한 구조화합물이 최대 흡광률을 보이며13) 탄수화물 분해물로부터 가장 간섭을 적게 받기 때문이다. 또한, 리그닌이 가지고 있는 천연적인 방향족 구조는 특정 파장에서 강한 자외선을 흡수하며 그 리그닌의 타입과 화학적 개질, 녹인 용매에 따라 UV 흡광도의 세기와 최대 파장이 달라지는 특성이 있기 때문에,14,15) 크라프트 리그닌의 UV 분광 분석에 용이한 것으로 알려져 있다.16) 실제 Joyce 와 Patterson 등은 아황산염에서 UV-VIS 분석을 통해 용액 내 리그닌의 농도를 측정하였고, Kleinert와 Alėn 등은 Kraft 펄핑액과 폐수에서의 리그닌 농도를 자외선 분광법을 통하여 평가한 바 있다.11)
석출된 크라프트 리그닌은 UV 분광분석을 실시하였을 때 280 nm에서 최대 흡광도를 나타냈으며, 따라서 이 파장에서 흡광도가 크게 나타나는 것은 리그닌 단위물질의 존재량에 비례적으로 영향을 받는 것으로 유추되는데,17) 이를 이용해 같은 농도의 각 조건별로 석출된 리그닌 시료를 채취하고 이러한 리그닌의 흡광도를 측정하여 비교 평가하였다.
조건별 리그닌의 흡광도를 정확히 비교하기 위하여 흡광도는 흡수율로 나타내었으며, 리그닌의 정확한 몰 질량과 구조를 정확히 알기 힘들기 때문에 특정 흡수율(D, Lg-1cm-1)로 Eq. 1과 같이 환산하여 평가하였다:11,18)
A: absorbance,
c: concentration in g/L,
b: path length through the sample (cm).
리그닌의 유리 페놀 수산기는 알칼리 용액에서 이온화되어 적색이동(bathochromic shift) 및 농색효과(hyperchromic effect)가 일어나며 이 이온화된 리그닌의 스펙트럼과 중성용액에 녹인 리그닌의 스펙트럼을 뺀 차 스펙트럼(Δ 스펙트럼, UV Difference spectrum)으로 타나낼 수 있다. 기준이 되는 참조 셀(Reference cell)에 중성용액을 넣고 샘플 셀에 이온화된 리그닌을 넣고 측정함으로써 리그닌의 차 스펙트럼을 측정할 수 있고, 이를 이용하여 리그닌의 유리 페놀성 수산기의 양을 정량하였다.11)
본 실험에서는 슬릿폭 1 nm, 200-400 nm의 파장 범위에서 리그닌의 스펙트럼을 폭 10 mm의 큐벳을 이용하여 측정하였다. 리그닌의 흡광도 측정을 위해 석출된 0.005-0.01 g의 리그닌을 2:1 dioxane:water(w/w) 30 mL에 완전히 녹인 후 폭 10 mm의 큐벳에 0.3 mL를 옮겨 다시 dioxane-water 용액으로 3 mL가 될 때까지 큐벳에 가해 최종 농도가 약 0.01-0.05 g/L가 되도록 한 후 pH에 따른 리그닌의 흡광도를 비교하였다. 이 때, 참조 셀에는 2:1 dioxane-water 용액을 사용하였다.
리그닌의 차 스펙트럼 측정은 상기의 농도 0.01-0.05 g/L의 리그닌이 용해된 dioxane-water 용액 5 mL에 pH 7 Buffer 용액 1 mL를 참조 셀에 넣은 후, buffer를 첨가하지 않은 상기 리그닌 용액에 NaOH 0.2 M 수용액을 첨가하여 이온화 후 샘플 셀에 넣어 차 스펙트럼을 측정하였다.
3. 결과 및 고찰
3.1 석출 조건에 따른 석출 리그닌의 특성 평가
침엽수 칩의 크라프트 펄핑 후 채취한 흑액의 특성을 평가한 결과를 Table 2에 나타내었다. TAPPI T264 cm-97에 의거하여 흑액 내 고형분 함량 및 고형분 내 무기질 함량을 분석한 결과 흑액의 고형분 함량은 16.8%이었고 이중 금속염 등의 무기물 함량이 70.3%인 것으로 나타났다. Garcia 등19)은 바이오매스의 소다펄핑 후 흑액에서 소다리그닌을 추출하는 연구를 실시한 바 있는데 본 연구 결과와 유사하게 총고형분 함량에서 무기물의 함량비가 67.9% 정도인 것으로 보고하였다.
Table 2.
The Characterization of the kraft black liquor
| pH | Density
(g/mL) | Total dissolved solids (%)a) | Total dissolved solids |
|---|
| Inorganic contents (%) | Organic contents (%) |
|---|
| Kraft black liquor | 13 | 1.14 | 16.8 | 70.3 | 29.7 |
리그닌 석출 시 황산 첨가량 즉, pH 조건에 따른 리그닌 석출량을 분석한 결과를 Table 3에 나타내었다. 리그닌의 석출결과 pH의 감소에 따라 리그닌의 석출량은 증가하는 것으로 나타났다. 리그닌 석출량을 총 고형분함량에 대한 수율(%)로 나타내어 보면 Table 3에서 보는 바와 같이 리그닌의 석출량이 pH 7 이상에서는 약 15% 이하로 미미하였으며 이 후 석출량이 점점 증가하여 특히 pH 4.7보다 낮은 pH에서 리그닌의 석출이 두드러지게 증가하였다. 이는 Garcia 등19)의 연구에서 pH 6.5에서 석출된 리그닌의 양과 pH 4.7에서 석출된 리그닌양이 약 20%에서 41%로 급격히 증가하는 유사한 결과가 보고된 바 있다.
Table 3.
Yield of kraft lignin obtained by the precipitation depending on the pH conditions
| pH | 10.0 | 8.5 | 6.5 | 4.7 | 3.5 |
|---|
| Precipitated kraft lignin (g/mL) | 0.0112 | 0.0266 | 0.0393 | 0.0654 | 0.0731 |
| Precipitated kraft lignin (%) | 5.84 | 13.87 | 20.49 | 34.1 | 38.11 |
리그닌 석출 후 상등액의 색상을 비교한 Fig. 2를 확인해보면 pH 10.0의 조건에서는 매우 어두운 갈색을 나타내었으며 이 후 리그닌 석출 pH가 내려갈수록 색상이 점점 밝은 노란색으로 변하는 것을 확인할 수 있었다. 이는 흑액 내 색을 나타내는 리그닌 물질들이 석출되어 침전되면서 상대적으로 상등액의 색상이 밝아지는 것으로 판단되었다.

Fig. 2.
Color changes of the supernatant depending on the pH of black liquor.
3.2 pH에 따른 리그닌의 흡광도 비교
측정결과 Fig. 3과 Table 4에서 나타낸 바와 같이 pH가 높을수록 리그닌의 흡광도는 증가하는 추세를 보였고, 상대적으로 낮은 pH조건에서 리그닌의 흡광도가 낮은 특성을 나타내어 리그닌의 순도가 상대적으로 낮은 것으로 판단되었다. 이는 흑액의 pH가 낮아질수록 금속염 또는 헤미셀룰로오스 등의 탄수화물 분해물이 리그닌과 같이 석출되기 때문인 것으로 판단되었다.17)
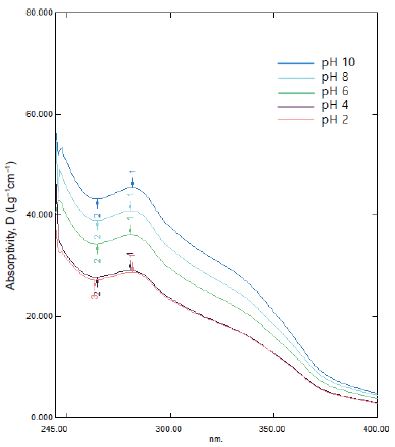
Fig. 3.
UV absorbance spectrum absorbance of precipitated lignin depending on the pH.
Table 4.
Absobance at 280nm of precipitated lignin depending on the pH
| pH | 10.0 | 8.5 | 6.5 | 4.7 | 3.5 |
|---|
| Absorptivity (Lg-1cm-1) | 45.412 | 40.891 | 36.107 | 29.081 | 28.755 |
3.3 추출리그닌 내 유리 페놀 수산기 정량평가
리그닌의 방향족 고리는 π-π* 전이를 나타내며 UV 분광분석 시 약 300-380 nm 파장에서 유리 페놀 수산기에 의한 흡광도가 매우 강하게 나타나게 된다. 이러한 특징을 통해 Fig. 4에서 나타난 것과 같은 리그닌의 유리 페놀 수산기 그룹의 양을 평가할 수 있다.11) 본 연구에서는 리그닌의 알칼리 스펙트럼과 중성 스펙트럼의 차 스펙트럼을 통해 크라프트 리그닌의 유리 페놀 수산기의 양적인 특징을 간접적으로 측정하였다.20,21)
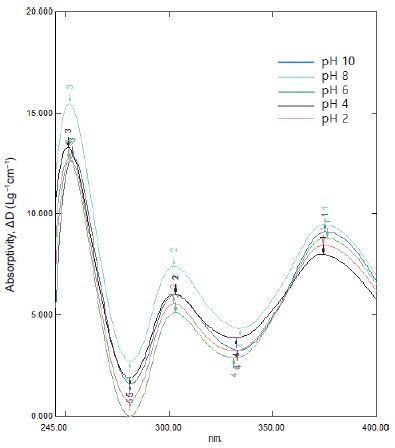
Fig. 4.
The UV spectrum of the precipitated kraft lignin depending on pH conditions.
Fig. 4에서와 같이 이온화한 리그닌의 차 스펙트럼을 측정한 결과 300 nm 및 375 nm의 파장조건에서 흡광도의 최댓값이 측정되었다. 이에 따라 Fig. 5에서 나타난 것과 같은 Type I, unconjugated 리그닌(298-300 nm)과 Type IV, p,p’-stilbene 구조의 conjugated 리그닌(370-375 nm)에 의한 최대 흡광도를 나타내는 파장과 같은 정도로 나타나는 것을 확인할 수 있었다. 이러한 결과들을 활용하여 다음과 같은 식으로 두 타입의 유리 페놀 수산기를 정량하였으며 몰 당 흡수율은 문헌을 참고하여 수치를 대입하였다(Eq. 2).11)
where ΔDMax(Lg-1cm-1) = Maximum absorbance at difference spectrum,
ΔDε(Lmol-1cm-1) = Difference of molar absorptivity.
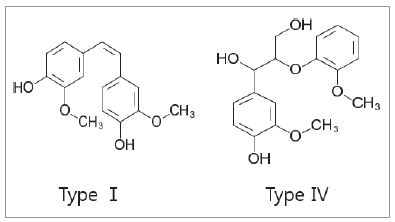
Fig. 5.
Possible phenolic structures of lignin.
측정된 흡광도를 이용하여 계산한 각각의 차 스펙트럼을 Table 5에 정리하였는데 실제 pH 조건별로 석출된 리그닌별로 유의한 경향이 나타나지 않는 것을 확인할 수 있었다.
Table 5.
The specific absorptivity of the precipitated kraft lignin depending on pH conditions
| pH | 10.0 | 8.5 | 6.5 | 4.7 | 3.5 |
|---|
| 375 nm ΔD | 9.131 | 9.482 | 8.821 | 7.996 | 8.455 |
| 300 nm ΔD | 6.002 | 7.416 | 5.125 | 6.042 | 5.564 |
Eq. 2를 기반으로 계산된 리그닌 페놀 type 별 추정량을 Table 6에 나타내었는데 석출조건에 따라 리그닌내의 유리 페놀 수산기 함량에는 유의한 차이는 발견되지 않았다. 이러한 결과를 통해 흑액에서 리그닌의 석출시 석출 pH 조건은 석출된 리그닌의 전체 구조적 특징의 변화를 간접적으로 평가해주는 페놀 수산기 함량비의 변화를 가져오지 않는 것으로 판단되었다.
Table 6.
The contents of the phenolic hydroxyl group in the precipitated kraft lignin depending on pH conditions
(unit: meq/g)
| pH | 10.0 | 8.5 | 6.5 | 4.7 | 3.5 |
|---|
| Type I Phenolic OH | 1.46 | 1.25 | 1.27 | 1.47 | 1.36 |
| Type 4 Phenolic OH | 0.25 | 0.25 | 0.24 | 0.21 | 0.23 |
4. 결 론
바이오매스 활용공정 등에서 다량으로 발생되는 폐기성 리그닌의 고도 활용을 위한 방안을 모색해보고자 국내산 소나무 크라프트 펄핑 흑액으로부터 리그닌을 추출하기 위한 기반 연구를 실시하였다. 펄핑흑액을 황산으로 적정하면서 각각의 pH 조건에서 석출되는 리그닌의 발생량과 특징을 평가하였다. 리그닌 석출시 pH가 낮아질수록 리그닌의 석출량은 증가하는 것을 볼 수 있었고 특히, pH 4-5 사이에서 상대적으로 석출효율이 높게 나타나는 것을 확인할 수 있었다.
석출된 리그닌의 특성을 평가하기 위하여 UV 분광분석을 실시하였는데 리그닌의 존재를 나타내는 특정 파장에서의 흡광도는 석출 pH 조건이 낮을수록 낮게 나타났으며 이는 석출 pH가 낮아질수록 리그닌 이외의 물질의 석출이 동시에 발생되어 리그닌의 순도가 낮아지는 것을 보여주는 것으로 판단되었다. 이러한 석출 pH 조건에 따라 석출되는 리그닌의 구조의 변화를 간접적으로 평가하고자 리그닌 구조를 이루는 페놀 수산기 함량 변화를 UV 분광법을 통해 평가하였다. 각각의 조건별 석출 리그닌에서 페놀 수산기의 함량비는 유의한 차이를 나타내지 않았는데 이를 통해 리그닌의 구조적 특징은 석출 pH 조건에 의해 크게 달라지지 않는 것으로 판단되었다. 본 연구를 통해 펄프 흑액으로부터 리그닌의 석출을 위한 pH 조절 조건별 영향을 알아보았는데, 순도와 수율 및 리그닌의 활용방안을 고려하여 최적의 석출조건을 도출하고 이를 통해 균일성을 가지는 리그닌 획득을 기반으로 상업적 가치를 가지는 리그닌 소재화 등의 연구가 지속적으로 이루어져야 할 것으로 판단되었다.
Acknowledgements
본 연구는 한국연구재단 과제번호 NRF-2016R1D1A1B03936220의 지원으로 이루어졌습니다.
Literature Cited
C. Mai, O. Milstein and A. Hüttermann, Journal of Biotechnology,
Chemoenzymatical grafting of acrylamide onto lignin,
79(2); 173-183 (2000)
Mai, C., Milstein, O., and Hüttermann, A., Chemoenzymatical grafting of acrylamide onto lignin, Journal of Biotechnology 79(2):173-183 (2000).
10.1016/s0168-1656(00)00230-3A. Vishtal and A. Kraslawski, BioResources,
Challenges in industrial applications of technical lignins,
6(3); 3547-3568 (2011)
Vishtal, A. and Kraslawski, A., Challenges in industrial applications of technical lignins, BioResources 6(3):3547-3568 (2011).
F. G. Calvo-Flores, J. A. Dobado, J. Isac-Garcia and F. J. Martin-MartÍnez, Lignin and lignans as renewable raw materials: Chemistry, technology and applications; 12-18, Chichester. John Wiley & Sons. (2015)
Calvo-Flores, F. G., Dobado, J. A., Isac-Garcia, J., and Martin-MartÍnez, F. J., Lignin and lignans as renewable raw materials: Chemistry, technology and applications, John Wiley & Sons, Chichester, pp. 12-18 (2015).
S. Laurichesse and L. Avérous, Progress in Polymer Science,
Chemical modification of lignins: Towards biobased polymers,
39(7); 1266-1290 (2014)
Laurichesse, S. and Avérous, L., Chemical modification of lignins: Towards biobased polymers, Progress in Polymer Science 39(7): 1266-1290 (2014).
10.1016/j.progpolymsci.2013.11.004F. S. Chakar and A. J. Ragauskas, Industrial Crops and Products,
Review of current and future softwood kraft lignin process chemistry,
20(2); 131-141 (2004)
Chakar, F. S. and Ragauskas, A. J., Review of current and future softwood kraft lignin process chemistry, Industrial Crops and Products 20(2):131-141 (2004).
10.1016/j.indcrop.2004.04.016D. Mohan, C. U. Pittermann Jr. and P. H. Steele, Journal of Colloid and Interface Science,
Single, binary and multi-component adsorption of copper and cadmium from aqueous solutions on Kraft lignin — A biosorbent,
297(2); 489-504 (2006)
Mohan, D., Pittermann Jr., C. U., and Steele, P. H., Single, binary and multi-component adsorption of copper and cadmium from aqueous solutions on Kraft lignin — A biosorbent, Journal of Colloid and Interface Science 297 (2):489-504 (2006).
10.1016/j.jcis.2005.11.023A. Tejado, C. Peña, J. Labidi, J. M. Echeverria and I. Mondragonm, Bioresource Technology,
Physico-chemical characterization of lignins from different sources for use in phenol-formaldehyde resin synthesis,
98(8); 1655-1663 (2007)
Tejado, A., Peña, C., Labidi, J., Echeverria, J. M., and Mondragonm, I., Physico-chemical characterization of lignins from different sources for use in phenol-formaldehyde resin synthesis, Bioresource Technology 98(8): 1655-1663 (2007).
10.1016/j.biortech.2006.05.042H. Loutfi, B. Blackwell and V. Uloth, Tappi Journal,
Lignin recovery from kraft black liquor: Preliminary process design,
74(1); 203-210 (1991)
Loutfi, H., Blackwell, B., and Uloth, V., Lignin recovery from kraft black liquor: Preliminary process design, Tappi Journal 74(1):203- 210 (1991).
B. M. Upton and A. M. Sasko, Chem. Rev,
Strategies for the conversion of lignin to high-value polymeric materials: Review and rerspective,
116(4); 2275-2306 (2016)
Upton, B. M. and Sasko, A. M., Strategies for the conversion of lignin to high-value polymeric materials: Review and rerspective, Chem. Rev., 116(4):2275-2306 (2016).
10.1021/acs.chemrev.5b00345J. D. Gargulak and S. E. Lebo, Commercial use of lignin-based materials, Lignin: Historical, Biological, and Materials Perspectives, Chapter 15; 304-320, Washington, DC. American Chemical Society. (2000)
Gargulak, J. D. and Lebo, S. E., Commercial use of lignin-based materials, Lignin: Historical, Biological, and Materials Perspectives, Chapter 15, American Chemical Society, Washington, DC, pp. 304-320 (2000).
S. Y. Lin and C. W. Dence, Methods in lignin chemistry, New York. Springer-Verlag. (1992)
Lin, S. Y. and Dence, C. W., Methods in lignin chemistry, Springer-Verlag, New York, pp. 42-44, 217-228 (1992).
L. A. M. Nevárez, L. B. Casarrubias, A. Celzard, V. Fierro, V. T. Muñoz, A. J. Davila, J. R. T. Lubianm and G. G. Sánchez, Sci. Technol. Adv. Mater,
Biopolymer-based nanocomposites: Effect of lignin acetylation in cellulose triacetate films,
12(4); 16 (2011)
Nevárez, L. A. M., Casarrubias, L. B., Celzard, A., Fierro, V., Muñoz, V. T., Davila, A. J., Lubianm, J. R. T., and Sánchez, G. G., Biopolymer-based nanocomposites: Effect of lignin acetylation in cellulose triacetate films, Sci. Technol. Adv. Mater. 12(4):16 (2011).
R. Hatfield and R. S. Fukushima, Crop Sci,
Can lignin be accurately measured?,
45(3); 832-839 (2005)
Hatfield, R. and Fukushima, R. S., Can lignin be accurately measured?, Crop Sci. 45(3):832-839 (2005).
10.2135/cropsci2004.0238D. Dengel and G. Wegener, Wood, Chemistry, Ultrastructure, Reactions; 157-160, Berlin. Walter de Gruyter. (1984)
Dengel, D. and Wegener, G., Wood, Chemistry, Ultrastructure, Reactions, Walter de Gruyter, Berlin, pp. 157-160 (1984).
O. Goldschmid, K. V. Sarkanen and C. H. Ludwig (eds), Ultraviolet spectra, In Lignin: Occurrence, formation structure and reactions; 241-266, New York. Wiley-Interscience. (1971)
Goldschmid, O., Ultraviolet spectra, In Lignin: Occurrence, formation structure and reactions, Sarkanen, K. V. and Ludwig, C. H. (eds), Wiley-Interscience, New York, pp. 241-266 (1971).
R. Alén and T. Hartus, Cellul. Chem. Technol,
UV spectrophotometric determination of lignin from alkaline pulping liquors,
22(6); 612-618 (1988)
Alén, R. and Hartus, T., UV spectrophotometric determination of lignin from alkaline pulping liquors, Cellul. Chem. Technol. 22(6):612-618 (1988).
R. C. Sun, J. Tomkinson and J. Bolton, Polymer Degradation and Stability,
Effects of precipitation pH on the physicochemical properties of the lignins isolated from the black liquor of oil palm empty fruit bunch fibre pulping,
63(2); 195-200 (1999)
Sun, R. C., Tomkinson, J., and Bolton, J., Effects of precipitation pH on the physicochemical properties of the lignins isolated from the black liquor of oil palm empty fruit bunch fibre pulping, Polymer Degradation and Stability 63(2):195-200 (1999).
10.1016/s0141-3910(98)00091-3B. L. Browning, Methods of wood chemistry,
Vol. 1.; 179-180, New York. Interscience. (1967)
Browning, B. L., Methods of wood chemistry, Vol. 1., Interscience, New York, pp. 179-180 (1967).
A. GarcÍa, A. Toledano, L. Serrano, I. Egüés, M. González, F. Marín and J. Labidi, Separation and Purification Technology,
Characterization of lignins obtained by selective precipitation,
68(2); 193-198 (2009)
GarcÍa, A., Toledano, A., Serrano, L., Egüés, I., González, M., Marín, F., and Labidi, J., Characterization of lignins obtained by selective precipitation, Separation and Purification Technology 68(2):193-198 (2009).
O. Goldschmid, Anal. Chem,
Determination of phenolic content of lignin preparations by Ultraviolet spectrophotometry,
26(9); 1421-1423 (1954)
Goldschmid, O., Determination of phenolic content of lignin preparations by Ultraviolet spectrophotometry, Anal. Chem. 26(9):1421- 1423 (1954).
W. M. Goldmann, J. Ahola, O. Mankinenm, A. M. Kantola, S. Komulainen, V. Telkki and J. Tanskanen, Period. Polytech. Chem. Eng,
Determination of phenolic hydroxyl groups in technical lignins by ionization difference ultraviolet spectrophotometry (Δε-IDUS method),
61(2); 93-101 (2017)
Goldmann, W. M., Ahola, J., Mankinenm, O., Kantola, A. M., Komulainen, S., Telkki, V., and Tanskanen, J., Determination of phenolic hydroxyl groups in technical lignins by ionization difference ultraviolet spectrophotometry (Δε-IDUS method), Period. Polytech. Chem. Eng. 61(2):93-101 (2017).









