1. 서 론
나노셀룰로오스는 셀룰로오스를 물리, 화학적 처리 등의 방법을 통해 수-수십 나노미터의 폭과 수백-수천 나노미터의 길이로 갖도록 가공한 셀룰로오스이다. 그 종류는 제조 방법으로부터 나누어지며 셀룰로오스 나노피브릴(CNF), 화학적 산 가수분해에 의한 셀룰로오스 나노크리스탈(CNC)로 분류되며, 전기방사법이나 박테리아 셀룰로오스(BC)로 만들어지기도 한다.1,2) 셀룰로오스가 나노셀룰로오스로 가공되면 비표면적과 종횡비가 크며, 150-250 GPa의 고탄성률과 5 GPa 이상의 고강도를 갖는 것으로 알려져 있다.3-5) 또한 탄소, 유리섬유의 물성보다 우수하며, 그 외에 낮은 열팽창계수와 경량성, 치수안정성, 친환경성 등의 장점을 가지고 있어, 전자 소재, 흡착제, 강화 필러 등에 적용하려는 연구가 진행되고 있다.6-9)
나노셀룰로오스의 원료인 셀룰로오스를 정제하는 방법은 펄프화 법과 표백법이 있다. 펄프화 법은 일반적으로 화학펄프화법을 사용하고 있으며, 화학약품을 사용하여 고온, 고압에서 제조되므로 목재조직 중의 리그닌이 분해, 용출 되어 섬유소를 얻게 된다. 리그닌 분해, 용출은 효과적이나 셀룰로오스 및 헤미셀룰로오스의 손실이 생겨 기계 펄프화법보다 펄프의 수율이 낮다. 표백법은 화학펄프화법과 마찬가지로 화학약품을 사용하여 목재의 리그닌을 제거하는 방법으로 화학펄프와 다르게 셀룰로오스 및 헤미셀룰로오스의 손실이 적다. 이러한 장점에 불구하고 표백법은 약품 가격이 화학 펄프화에 사용하는 약품가격에 비해 높기 때문에 실제 공정에서는 두 가지 방법을 병행하여 셀룰로오스를 정제하고 있다.
비목질계 원료는 목질계 원료의 공급 제한에 따른 대처방안으로 연구되어왔다. 두 원료 모두 셀룰로오스와 헤미셀룰로오스, 리그닌 그리고 추출물로 구성되어 있는 공통점이 있으며, 세포 구성에서도 섬유와 유세포가 존재하는 등 두 원료는 매우 유사하다. 하지만 두 원료의 가장 큰 차이는 비목질계 원료의 경우 유세포가 목질계 원료에 비해 높은 비율을 차지하고 있다.10,11) 유세포는 펄프 제지산업에서 많은 단점으로 작용하는데, 유세포는 추출물 함량이 높아 펄프 수율이 떨어지며, 펄프내 존재하는 많은 유세포는 제지 공정에서 미세분으로 작용하여 탈수악화 문제를 발생시킨다. 이러한 문제를 해결하기 위해 비목재 원료를 이용하기 전 수(pith)를 제거하는 공정 등의 유세포를 제거하는 방법을 사용하고 있다.12)
비목질계 원료 중 대나무는 전 세계적으로 생육하고 있으며, 1,100에서 1,500여 종의 대나무가 약 2천 2백만 헥타르 이상 분포하고 있다.13) 지구상에서 빠르게 자라는 식물자원중 하나로 단자엽 식물이며 나이테가 없고, 비대생장을 하지 않는 특징이 있다.14) 또한 열대지역과 산악지역까지 다양한 지역에서 서식하며, 섬유길이가 길어 침엽수 펄프와 비견되는 섬유 특성을 가지고 있다.15) 그 외 대나무를 화학 펄프로 만들 때 리그닌 제거가 용이하고 목재 섬유에 비해 가는 섬유를 가지고 있기 때문에 펄프제지 산업에서 목재를 대체하는 원료로 사용하고 있다.16)
본 연구에서는 리그닌 제거 방법에 따라 나노피브릴 제조 특성의 변화를 확인하고자 하였으며, 원료로는 국내에서 가장 많이 자생하는 대나무 중 맹종죽을 원료로 하였다. 이산화염소 표백법과 소다-안트라퀴논 펄프화 후 표백 방법을 사용하여 홀로셀룰로오스와 표백 소다-안트라퀴논 펄프를 제조하여 리그닌 제거 방법에 따라 나노피브릴화 특성을 확인하고자 하였다.
2. 재료 및 방법
2.2 실험 방법
2.2.1 홀로셀룰로오스 제조
대나무로 홀로셀룰로오스로 제조하기 위해 이산화염소를 사용하여 리그닌을 제거하였다. 대나무는 디스크 그라인더로 기계펄프로 제조하여 사용하였으며, 대나무 기계펄프 50.0 g을 증류수를 이용하여 10%(w/w)희석한 후 17.2 g 차아염소산나트륨과 아세트산을 pH가 3-4가 되도록 가하여 이산화염소가 발생하도록 하였다. 반응 조건은 75°C에서 한 시간 동안 반응시켜 리그닌을 제거하였다. 반응이 끝난 후 증류수를 사용하여 흡인여과 방법으로 세척하였다. 리그닌이 충분히 제거될수록 위 과정을 총 4회 반복하여 홀로셀룰로오스를 제조하였다.
2.2.2 소다-안트라퀴논 펄프 제조
대나무를 펄핑에 적합한 크기(0.2×0.2×3 cm)로 제조한 뒤 활성알칼리 20%(as Na2O), 안트라퀴논 0.1%(as wood chip), 액비 1:4로 약액을 제조하여 170°C에서 90분 유지하여 증해 하였다. 증해가 끝난 펄프는 세척 후 이산화염소로 표백하였다. 이산화염소 표백조건은 펄프 50.0 g(oven dry)를 증류수를 사용하여 10%(w/w)로 희석한 후 1.7 g 차이염소산나트륨과 아세트산을 pH가 3-4가 되도록 가하여 이산화염소가 발생하도록 하였다. 반응 조건은 75°C에서 한 시간 동안 반응시켜 펄프를 표백하였다. 표백이 끝난 펄프는 증류수를 사용하여 흡인여과방법으로 세척하였으며, 세척된 표백 펄프는 충분히 탈수하여 냉장 상태로 보관하였다.
2.2.3 카르복시메틸화 전처리
제조된 대나무 소다-안트라퀴논 펄프를 나노피브릴로 제조하기 위한 전처리로 카르복시메틸화 전처리를 실시하였다. 대나무 펄프 20.0 g을 수산화나트륨 12.3 g이 용해된 에탄올 400 mL에 상온에서 2시간 침지시켜 방치하였다. 상온에 방치된 펄프에 각각 염화아세트산 1.4 g (carboxymethylated soda-AQ pulp 1, CMP 1), 2.8 g (CMP 2)이 용해된 에탄올 100 mL을 혼합하여 70°C에서 2시간 반응시켜 카르복시메틸화를 실시하였다. 반응이 끝난 각 펄프는 흡인여과방법으로 세척한 후 나노피브릴 제조에 사용하였다.
2.2.4 나노피브릴 제조
대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 소다-안트라퀴논 펄프에 증류수를 사용하여 1%(w/w) 현탁액으로 만든 후 고압 균질기를 사용하여 나노피브릴을 제조하였다. 사용한 고압균질기(PANDA PLUS, GBH, Germany)로 최초 압력을 150-200 bar에서 1회 통과시킨 후 2회 통과부터는 700-800 bar로 압력을 조절하였다. 모든 펄프의 통과 횟수는 최소 통과 횟수를 포함하여 9회 통과시켜 나노피브릴을 제조하였다.
2.2.5 리그닌 분석 및 핵자기공명 분석
대나무와 대나무로 제조된 기계 펄프, 홀로셀룰로오스, 소다-안트라퀴논 펄프의 리그닌을 측정하기 위하여 Klason 리그닌 분석을 실시하였다. 샘플 0.275 g에 72% (w/w) 황산 4.5 mL을 가하여 한 시간 동안 30°C에서 일차 가수분해 시킨 후 증류수 145 mL을 가하여 121°C에서 한 시간 동안 이차가수분해를 실시하였다. 가수분해가 끝난 샘플을 유리여과기를 사용하여 여과한 후 잔유물을 측정하여 리그닌 함량을 측정하였다.
대나무와 대나무로 제조된 기계 펄프, 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 소다-안트라퀴논 펄프의 핵자기공명 분석을 위하여 시료 40.0 mg에 0.8 mL의 72% 황산을 넣고 30°C로 한 시간 동안 반응하여 일차 가수분해를 실시하였다. 이차 가수분해 반응은 2.0 mL의 중수로 일차 가수분해 산물을 희석 후 100°C에서 한 시간 동안 반응시켰다. 가수분해 후 여과하여 가수분해 액을 수집하여 1H-NMR 분석을 하였다. 핵자기공명분광기-500MHz(AVACE 500MHz, Bruker, USA)와 Topspin program으로 NMR스팩트럼 상에서 anomeric hydrogen peak에서 탄수화물을 확인하였으며, 카르복실기 피크와 아세트산에 존재하는 수소 피크를 적분하여 카르복실기와 아세트산 함량을 계산하였다.17)
2.2.6 투과전자현미경 분석
대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 소다-안트라퀴논 펄프로 제조된 나노피브릴의 크기를 분석하기 위하여 투과전자현미경 분석을 실시하였다. 분석하기 위한 그리드 제조 방법은 나노피브릴을 0.01%(w/w)로 희석 한 후 300 mesh 카본그리드에 위치시킨 후 아세트산 우라늄으로 음영염색을 하여 관찰용 샘플을 제조하였다. 투과전자현미경(Libra 120, Carl zeiss, Germany) 관찰 조건은 가속전압 120 kV에서 관찰하였으며, 나노피브릴 섬유 50개의 크기를 측정하여 분석하였다.
3. 결과 및 고찰
3.1 대나무 원료, 기계펄프, 홀로셀룰로오스, 소다-안트라퀴논의 화학 조성 분석
대나무와 대나무로부터 제조된 기계펄프, 홀로셀룰로오스, 소다-안트라퀴논 펄프의 화학 조성 분석 결과를 Table 1에 나타내었다. 화학 조성 분석결과 대나무와 대나무로 제조한 기계펄프의 화학 조성은 차이가 없었다. 홀로셀룰로오스와 소다-안트라퀴논 펄프는 리그닌 제거 공정에서 대부분의 리그닌이 제거되었고, 홀로셀룰로오스의 경우 자일란의 일부가 제거 되었으며, 소다-안트라퀴논 펄프는 글루칸 일부와 자일란 의 대부분이 제거된 것이 확인 되었으며, 이 때문에 소다-안트라퀴논 펄프의 경우 수율이 매우 떨어진 것이 확인되었다.
Table 1.
Chemical composition of moso bamboo, mechnical pulp from moso bamboo, holocellulose (bleached mechanical pulp from moso bamboo), and soda-AQ pulp from moso bamboo
| Yield | Lignin | Glucan | Xylan | Mannan | Arabinan | Galactan | |
|---|---|---|---|---|---|---|---|
| Moso bamboo20) | 100 | 30.4 | 36.3 | 31.0 | 0.2 | 0.7 | 1.4 |
| Mechanical pulp | 100 | 31.2 | 35.8 | 30.6 | 0.2 | 0.7 | 1.4 |
| Holo cellulose | 64.1 | 0.9 | 37.1 | 26.1 | - | - | - |
| Soda-AQ pulp20) | 31.7 | 0.3 | 26 | 5.1 | - | - | - |
홀로셀룰로오스의 경우 산화반응에 의해 리그닌이 대부분 제거되었지만, 헤미셀룰로오스는 일부 제거되었지만, 소다-안트라퀴논에 비해 자일란 함량이 크게 감소하지 않았다. 이는 소다-안트라퀴논 펄프와 다르게 홀로셀룰로오스는 자일란의 측쇄에 존재하는 성분이 잔류할 것으로 판단되며, 특히 자일란에 존재하는 4-O-Me-글루쿠론산의 카르복실기가 홀로셀룰로오스에 잔류했을 것으로 생각되었다.
나노피브릴의 원료의 카르복실기의 존재가 중요한 이유는 이전 연구를 참고 하였을 때, 일반적으로 나노피브릴을 제조할 때, 음이온을 띄는 카르복실기 함량이 높을수록 나노피브릴화 공정에서 유리하다. 기존 연구에서 TEMPO-oxidation를 사용하여 카르복실기를 도입한 후 나노피브릴화 공정을 실시한 경우 폭이 8-9 nm의 나노피브릴이 제조되었으며, 카르복시 메틸화 전처리를 통해 카르복시메틸기를 도입한 경우 폭이 10 nm 이하인 나노피브릴이 제조된다는 보고가 있다.18,19) 이러한 기존연구를 홀로셀룰로오스에 존재하는 글루쿠론산에 의해 전처리 없이 비슷한 효과를 얻을 수 있을 것으로 예상하였다.
3.2 대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 전처리 소다-안트라 퀴논 펄프의 핵자기 공명 분석
대나무로 제조횐 홀로셀룰로오스와 소다-안트라퀴논 펄프의 화학 조성 분석 결과 홀로셀룰로오스의 경우 Table 1에서와 같이 글루칸과 자일란이 대부분 잔류한 것으로 확인 되었으며, 소다-안트라퀴논 펄프의 경우 셀룰로오스 일부와 자일란 대부분이 제거된 것이 확인 되었다. 때문에 홀로셀룰로오스에는 글루쿠론산에 의한 카르복실기가 존재할 것으로 예상되지만 소다-안트라퀴논 펄프에는 거의 존재하지 않을 것으로 판단되어 카르복시메틸화 처리를 하여 소다-안트라퀴논 펄프에 카르복실기를 도입하였다.
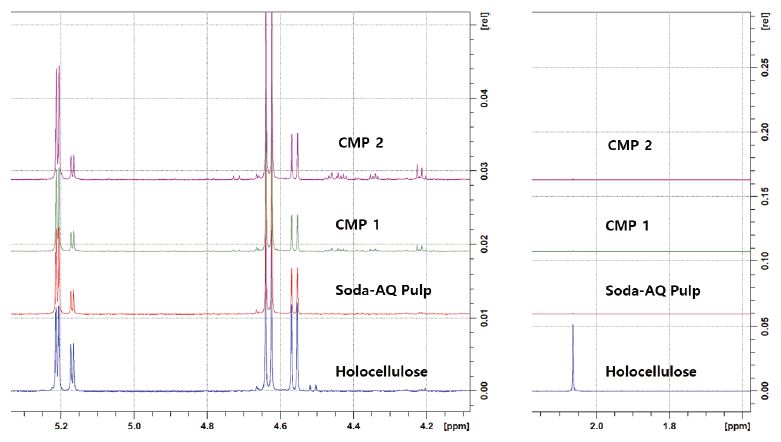
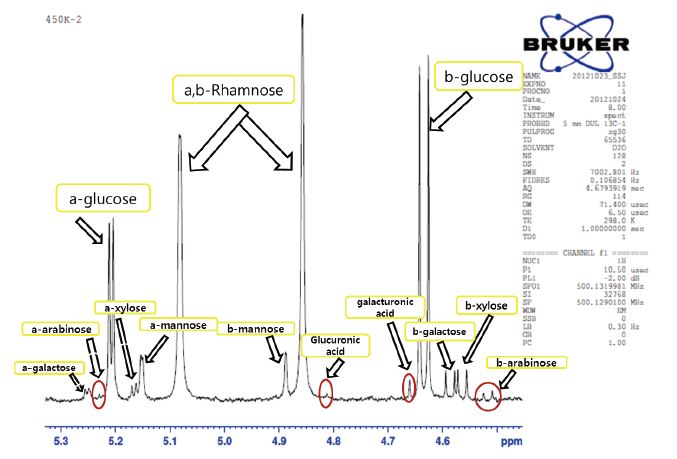
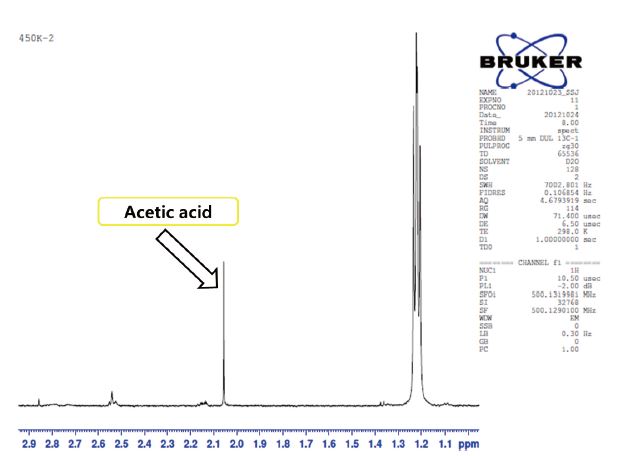
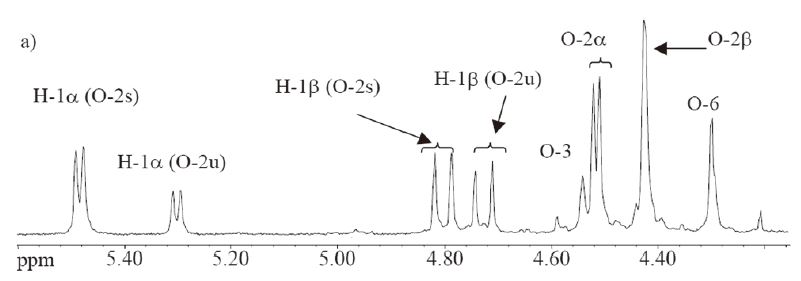
나노피브릴의 제조 공정에서 카르복실기의 함량과 자일란에 측쇄로 존재하는 아세틸기를 측정하기 위해 핵자기 공명 분석을 실시하였다. Fig. 1에서와 같이 스펙트럼상의 피크를 적분하고 해석하여 목재에 존재하는 아노머성 수소 부분을 분석하여 탄수화물(Fig. 2) 조성을 계산하고 아세트산(Fig. 3) 피크 영역을 해석하였으며, 카르복실기의 위치는 Fig. 4를 해석하여 탄수화물, 아세트산, 카르복실기 피크를 적분한 값을 Table 2에 나타내었다.
Table 2.
Carboxyl group contents in polysaacharides by NMR peak comparison among different nanofibril raw materials
| Glucose | Xylose | Acetic acid | Carboxyl group | Carboxyl group/cabohydrate | |
|---|---|---|---|---|---|
| Holo cellulose | 2.52 | 1.37 | 1.65 | 0.04 | 0.01 |
| Soda-AQ pulp | 2.57 | 0.68 | 0.02 | 0.03 | 0.01 |
| CMC1 | 2.58 | 0.57 | 0.02 | 0.21 | 0.07 |
| CMC2 | 2.59 | 0.52 | 0.06 | 0.36 | 0.12 |
핵자기공명 분광 분석 결과 홀로셀룰로오스는 셀룰로오스의 주 성분인 글루코스와 자일란의 주성분인 자일로스의 비율은 2.5:1.4로 존재하였지만 소다-안트라퀴논 펄프와 카르복시메틸화 소다-안트라퀴논 펄프의 경우 2.5:0.5-0.7로 소다-안트라퀴논 펄프에서 유래한 원료는 셀룰로오스 대비 자일란 비율이 매우 떨어지는 것이 확인 되었다. 때문에 자일란에 측쇄로 존재하는 아세트산의 함량을 확인 하였을 때, 홀로셀룰로오스에는 대부분 잔류하는 것이 확인 되었지만, 소다-안트라퀴논 펄프와 카르복시메틸화 소다-안트라퀴논 펄프의 경우 대부분 제거된 것이 확인 되었다.
Table 2에서 확인된 핵자기공명 분석결과 holocellul-soe에는 자이란 유래 카르복실기의 함량이 매우 낮았으며,22) 이런 경향은 Soda-AQ 펄프에서도 나타났다. 전처리에 의한 카르복시메틸화 처리 시료는 당량적으로 카르복시메틸화가 진행되었음을 확인할 수 있었다.
핵자기 공명 분광분석 결과 홀로셀룰로오스와 소다-안트라퀴논 펄프 모두 카르복실기가 적은양이 존재함이 확인 되었으며, 이러한 화학적 조성분의 차이는 나노피브릴 제조에 영향을 미칠 것으로 생각된다.
3.3 대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 전처리 소다-안트라 퀴논 펄프를 원료로 제조한 나노피브릴의 투과전자현미경 분석
대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸처리된 소다-안트라퀴논 펄프로 제조된 나노피브릴의 크기를 측정하기 위해 투과전자현미경 분석결과를 Fig. 5에 나타내었다. 투과전자현미경을 통해 확인한 결과 나노피브릴의 폭 크기는 홀로셀룰로오스의 경우 5.8-38.6 nm(평균 11.6 nm), 카르복시메틸화 처리된 소다-안트라퀴논 펄프로 제조된 경우 CMP 1은 5.3-250 nm(평균 42.4 nm)의 폭크기를 가지고 CMP 2의 나노피브릴의 폭 크기는 7.3-99.1 nm(평균 25.3 nm)로 같은 전처리와 통과횟수를 동일하게 했을 경우 대나무 홀로셀룰로오스로 제조된 나노피브릴의 폭이 좁게 확인되었다. 대나무 소다-안트라퀴논 펄프의 경우 5.5-8.4 μm(평균 7.3 μm)의 크기를 가진 섬유만 확인 되어 나노피브릴화 되지 않았다.

Fig. 5.
Transmission electron microscopy image of nanofibrils (A: Holocellulose, B: soda-AQ pulp, C: CMP 1, D: CMP 2).
핵자기공명 분석 결과와 비교했을 때, 대나무 홀로셀룰로오스의 경우 카르복실기의 함량이 거의 확인되지 않아 폭이 큰 나노피브릴이 제조될 것으로 판단하였지만, 실제 결과 가장 좁은 폭을 가진 나노피브릴이 제조되었다. 이는 다른 재료에 비해 높은 헤미셀룰로오스와 아세틸기에 의해 셀룰로오스간 결합을 방해 받은 것으로 판단된다. 이러한 이유로 대나무 소다-안트라퀴논 펄프의 경우 헤미셀룰로오스 함량이 적고, 카르복실기와 아세틸기가 전혀 없어 나노단위의 셀룰로오스가 아닌 마이크로 단위의 셀룰로오스가 제조 되었다. 카르복시메틸화 처리한 소다-안트라퀴논 펄프의 경우 나노단위로 제조된 셀룰로오스와 마이크로 단위로 제조된 셀룰로오스가 혼재하는 것이 확인되었다.
3.4 나노피브릴의 점도 및 보습력 비교
셀룰로오스를 나노단위로 가공하게 되면 표면적이 증가하게 된다. 이때, 셀룰로오스가 가지고 있는 수산기의 노출이 증가되며, 수산기 노출이 증가할수록 셀룰로오스가 물과 상호작용하는 면적이 넓어져 겔과 같은 상태로 변화하며 점도가 증가한다.
대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 된 소다-안트라퀴논 펄프로 제조한 나노피브릴의 점도를 측정한 결과를 Fig. 6에 나타내었다. 대나무 홀로셀룰로오스로 제조된 나노피브릴의 경우 투과전자현미경으로 분석한 결과 소다-안트라퀴논 펄프, 카르복시메틸화 전처리 소다-안트라퀴논 펄프에 비해 폭이 좁은 나노피브릴이 제조되었다. 점도는 물과 상호작용하는 면적이 클수록 증가하기 때문에 홀로셀룰로오스로 제조된 나노피브릴의 점도가 가장 큰 것으로 판단된다.
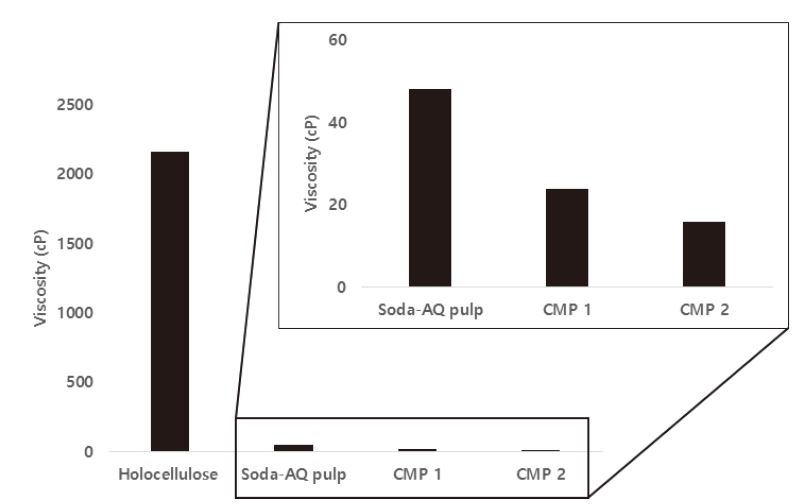
Fig. 6.
Viscosity comparison of nanfibrils from different origin of bamboo holocellulose, soda-AQ pulp, carboxymethylated pulp.
소다-안트라퀴논 펄프로 제조된 셀룰로오스 마이크로피브릴의 경우 표면적이 나노피브릴보다 낮기 때문에 점도가 낮은 것으로 판단된다. 하지만 카르복시메틸화 전처리 소다-안트라퀴논 펄프로 제조된 나노피브릴의 경우 소다-안트라퀴논 펄프로 제조된 셀룰로오스 마이크로피브릴에 비해 점도가 낮은 것이 확인 되었다.
셀룰로오스의 보습성은 셀룰로오스가 나노단위로 작아지게 되면 표면적이 증가하게 되고, 셀룰로오스 표면의 수산기 노출이 많아진다. 수산기 노출이 많아질수록 셀룰로오스가 가지는 물과의 친화력은 증가하고, 이러한 특성은 셀룰로오스가 나노피브릴화 될수록 즉 표면적이 넓어질수록 증가한다. 높은 표면적으로 인한 셀룰로오스의 높은 친화력은 나노피브릴을 건조하는데 비용이 나노피브릴화 되지 않은 셀룰로오스를 건조할 때에 비해 높은 비용이 요구되며, 이러한 특성을 이용하면 나노피브릴을 수분을 유지시켜주는 물질로 사용할 수 있다.
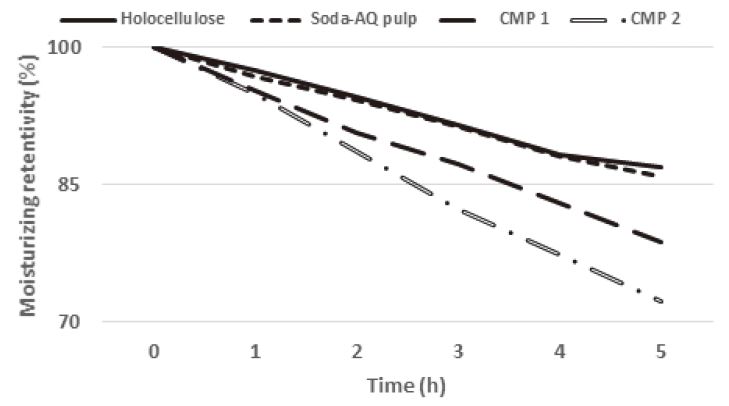
대나무 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 된 소다-안트라퀴논 펄프로 제조한 나노피브릴의 보습력을 측정한 결과를 Fig. 7에 나타내었다. 보습력을 측정한 결과 홀로셀룰로오스로 제조한 나노피브릴과 대나무 소다-안트라퀴논 펄프로 제조된 셀룰로오스 마이크로피브릴의 보습력이 가장 우수하게 확인되었다. 카르복시메틸화 전처리 소다-안트라퀴논 펄프로 제조된 나노피브릴의 경우 카르복실기가 증가할수록 보습력이 감소되었다.
4. 결 론
본 연구에서는 대나무를 원료로 각각 홀로셀룰로오스, 소다-안트라퀴논 펄프, 카르복시메틸화 전처리 소다-안트라퀴논 펄프를 제조한 후 이를 원료로 나노피브릴을 제조하여 그 특성을 확인하였다. 핵자기공명 분석결과 홀로셀룰로오스에서는 카르복실기가 적었으며, 헤미셀룰로오스의 주 성분인 자일로스와 아세틸기에서 유래한 아세트산이 높게 확인되었다. 하지만 낮은 카르복실기 함량으로 인해 카르복시메틸화 전처리 소다-안트라퀴논 펄프에 비해 나노피브릴 제조에 적합하지 않을 것으로 판단하였다.
실제 나노피브릴을 제조한 결과 홀로셀룰로오스를 이용하여 제조한 나노피브릴의 폭이 좁은 나노피브릴이 제조되었으며, 카르복시메틸화 전처리 소다-안트라퀴논 펄프의 경우 나노피브릴과 셀룰로오스 마이크로피브릴이 혼재하고 있는 것이 확인 되었다. 또한 보습력과 점도를 측정한 결과 홀로셀룰로오스가 높은 점도와 보습력을 가지고 있는 것이 확인 되었다. 이러한 결과의 원인은 홀로셀룰로오스에 카르복실기가 적게 있지만 헤미셀룰로오스와 아세틸기가 셀룰로오스간의 결합을 방해하여 나노피브릴화가 쉽게 일어나도록 역할을 한 것으로 판단된다. 이러한 결과를 통해 홀로셀룰로오스법으로 리그닌을 제거하여 나노피브릴 원료를 제조할 경우 전처리 없이 작업성이 높고, 폭이 좁은 나노피브릴 제조가 가능한 것으로 판단된다.