1. 서 론
패키징산업은 기술집약형 미래지식산업임과 동시에 고부가가치의 브랜드 산업으로서 패키징산업의 부가가치율은 38%로 반도체의 24.9% 보다 약 13.1% 높은 것으로 보고되었다. 또한 세계 패키징 시장의 규모는 약 6,700억 달러에 달하고 향후 2016년까지 연간 3% 성장률로 8,200억 달러의 규모를 형성할 것으로 추산된다. 반면 국내 패키징산업은 약 3.8조원의 시장규모를 형성, 2015년 까지 5.2조원의 규모로 성장이 예상되고 있으며 국내를 비롯한 세계 패키징 소재별 사용률은 2016년 플라스틱 44%, 제지 30%, 금속유리등의 기타 소재가 26%의 시장을 형성할 것으로 보인다. 1, 2) 그러나 최근 환경폐기물의 관리와 처리문제, 이에 따른 지속가능한 환경 친화적 소재 및 시스템 개발을 요하는 사회적 관심이 증대되면서 난분해성 플라스틱 포장재의 사용 억제와 함께 재활용, 재사용 그리고 재생 가능한 친환경 소재인 제지를 활용한 기능성 포장소재의 개발과 응용에 관심이 높다. 이에 따라 수분 및 가스차단성과 기계적 강도 등의 개선 및 항균 항산화 등의 기능성을 부여한 포장용 종이 소재의 개발이 활발하다. 3)
최근 과일 채소류 등을 열처리 등의 별도의 가공 없이 샐러드 등의 형태로 직접 섭취하는 경우가 급격히 증가하면서 농산물의 오염에 의한 식중독 사고의 예방과 농산물 안전성에 대한 관심이 증대하고 있다. 이에 따라 농산물과 화훼류 포장에 가장 보편적으로 사용되고 있는 종이 포장재로부터 농산물의 신선도를 연장하고 오염균과 미생물로부터의 변패를 방지하는 기능성 항균 포장지의 개발을 위한 연구가 활발하다. 4) 화훼류의 선도유지를 위하여 자몽종자 추출물을 골판지용 라이너에 처리하거나 황을 종이 포장지 표면에 코팅하는 방법 또는 은(Ag), 금(Au), 구리(Cu), 식물오일, 에센스오일 등의 항균물질을 포장 원지에 코팅 또는 침지하는 방법으로 종이포장재에 항균성을 부여하는 연구결과 등이 보고되고 있다. 5- 8)
특히 은은 인체에 해가 없고 독성이 없으며, 미생물 체내의 신진대사 기능을 억제하여 650여 종류의 유해 세균을 효과적으로 죽이는 것으로 알려져 있으며 9) 최근 나노기술의 발전과 함께 그 제조 및 응용이 급속히 증가하고 있는 은나노는 필름 내 분산성 및 안정성 등이 우수하고 높은 비표면적으로 인한 미생물의 세포벽과의 접촉 기회가 증가함에 따라 세포벽의 파괴를 가속화하여 항균력을 극대화시킴으로써 매우 효율적인 항균 나노물질로 알려져 있다. 10) 이러한 은나노의 합성에 최근 녹색합성법(green synthesis)이 새로운 친환경 제조공정으로서 높은 관심을 받고 있으며 이에 관한 연구사례가 활발히 보고되고 있다. 11) 녹색화학(green chemistry)의 영향을 받은 녹색합성은 환경위해성을 갖는 화학물질의 사용을 적극적으로 배제하고 자연유래 천연물질을 활용하는 합성법으로 정의되며 12) 일반적으로 친환경성, 가격효율성, 생체적합성 등을 갖춘 다당류, 꿀, 해초, 허브잎 추출물, 키토산 등을 환원제 및 안정제로 사용하고 이러한 물질들을 이용하여 금속나노물질을 합성한다. 13)
게, 가재, 새우 등 갑각류의 껍질로부터 얻는 키틴은 셀롤로오스 다음으로 풍부한 천연고분자로 셀롤로오스 C-2위치의 –OH가 CH3CONH-로 치환된 구조이며 셀롤로오스와 매우 비슷한 구조를 가진 불용성 물질이다. 키틴의 CH3CONH-의 탈아세틸화를 통해 얻어지는 키토산은 생분해성과 생체적합성이 탁월하고 인체에 무독하다고 알려진 천연고분자로 천연고분자 중 유일한 양이온성을 갖는 물질로 필름형성력이 우수하다고 알려져 있다. 14- 17) 이러한 키토산의 뛰어난 생체적합성과 친환경성 그리고 물리적 특성을 활용하여 기능성종이를 연구한 사례들이 발표되고 있으며 F. Ham- Pichavant 등 18)은 기름차단성을 부여하기 위하여 종이에 키토산을 코팅하였고, 키토산과 비즈왁스 또는 카제인(caseinate)의 이중층으로 코팅하여 종이의 수분차단성을 향상시킨 연구결과가 발표되었다. 1920) Yunzhi ling 등은 키토산/montmorillonite (MMT)/은나노 입자를 이용한 항균성제지에 대한 연구를 수행하였으며 합성물질을 종이의 첨가제로 넣는 것보다 종이의 표면에 코팅하였을 때 항균효과가 더 크다고 발표하였다. 21)
본 연구에서는 친환경 천연고분자인 키토산의 활성 아미노기와 히드록시기를 이용하여 은나노 입자의 녹색합성을 수행하고 이를 통해 얻어진 키토산-은나노 복합물질을 활용한 항균코팅 종이를 제조, 그 표면특성과 항균성을 평가하였다. 키토산 및 은나노 합성의 전구체로 사용되는 질산은의 농도 그리고 반응시간에 따른 은나노의 녹색합성 영향을 파악하였으며 코팅지의 표면분석과 항균성 평가를 통해 향후 녹색합성법을 응용한 새로운 형태의 친환경 키토산-은나노 항균 포장종이로써 응용가능성을 검토하였다.
2. 재료 및 방법
2.1 공시재료
키토산-은나노 합성을 위해 순도 90% 이상의 80% 디아세틸화 된 키토산 (CB0660, Bio Basic Inc., Markham, Canada)과 은나노 입자 합성의 전구체로써 질산은 (Silver nitrate,, Alfa Aesar, Ward Hill, USA)을 사용하였고, 키토산 용해를 위한 용매로서 1%(v/v) acetic acid (Alfa Aesar, Ward Hill, USA)를 사용하였다. 키토산-은나노 녹색합성 복합물질 코팅 지의 항균성 평가를 위해 MacConkey Agar (211380, BD Difco, Sparks, USA)와 Nutrient Broth (234000, BD Difco, Sparks, USA)를 사용하였다.
2.2 실험방법
2.2.1 키토산-은나노 녹색합성
1%(v/v) acetic acid 용액에 0.5~2%(w/w) 농도의 키토산을 12시간 동안 상온에서 용해시킨 후 용해된 키토산용액 10 g과 질산은 용액(3~100 mM) 1 mL를 혼합하였다. 키토산-질산은 혼합용액을 일정시간 골고루 교반한 뒤 오토클레이브 (HST-506-6, Hanbaek, Korea)에 15 psi, 121 ℃ 조건에서 15-120 초 동안 반응시킨 후 상온에서 자연냉각 시켜 키토산-은나노 녹색합성 복합물질을 제조하였다. 얻어진 키토산-은나노 용액은 반응에 참여한 키토산과 질산은의 농도에 따라 연한 자줏빛에서 진한 노란색을 띄었다.
2.2.2 키토산-은나노 복합물질의 코팅
녹색합성된 키토산-은나노 코팅지는 Meyer Bar No. 7 (Kipae E&T, Suwon, Korea)를 사용하여 편면 코팅하였으며 코팅 원지는 100 ℃ 오븐(JSOF-100, JSR, Korea)에서 1 시간 동안 건조시킨 마닐라 보드(Mead West Vaco, 110 g/m2, 두께 0.25 mm)를 사용하였다. 2%(w/w)의 키토산과 각기 다른 농도의 질산은(27 mM, 60 mM, 100 mM)용액을 반응시킨 키토산-은나노 합성용액을 5회, 10회, 15회 코팅하였으며 1회 코팅에 적용된 키토산-은나노 합성용액은 2 mL이었다. 코팅층 두께는 디지털 마이크로미터 (QUICKmini, Mitutoyo, Tokyo, Japan)를 이용하여 측정하였으며 코팅지는 23±1℃, 50±2%의 항온항습기에서 48시간 동안 조습처리한 후 항균성 평가 등을 수행하였다.
2.2.3 키토산-은나노 복합물질 및 코팅지의 특성 분석
키토산 내 은나노 합성 유무의 확인을 위해 UV-Vis spectroscopy (OPTIZEN 2120UV, Mecasys, Daejeon, Korea)와 FTIR spectroscopy (Spectrum 65, Perkin Elmer, Waltham, USA)분석을 수행하였다. UV-Vis 흡수 스펙트럼은 300-800 nm 파장 범위에서 측정하였으며 FTIR의 경우 ATR(attenuated total reflectance) mode를 사용하여 4000-400 cm-1의 파수 범위에서 16회 스캔 후 평균치를 택하였다. 합성된 은나노의 형태 및 크기 분석을 위해 TEM (JEM-2010, JEOL Ltd., Tokyo, Japan) 분석을 수행하였으며 이를 위한 시편은 제조된 키토산-은나노 복합용액 한 방울을 TEM 전용 copper grid (Ted Pella, Redding, USA) 위에 떨어뜨린 후 이를 상온에서 건조하여 준비하였다. 키토산-은나노 복합물질 코팅지 표면은 field emission scanning electron microscopy (FESEM, Quanta FEG 250, FEI, USA)를 이용하여 500배의 배율에서 분석하였으며 코팅층 표면에 존재하는 은의 정확한 농도 측정을 위하여 energy dispersive spectroscopy (EDS, AMETEK Inc., Berwyn, USA) 분석을 수행하였다. EDS의 정확한 결과값을 얻기 위해 동일한 시편에서 5회 이상 측정하여 평균값을 취하였다.
2.2.4 항균성 평가 (Halo Test)
제조된 키토산-은나노 코팅지의 항균성 평가를 위해 ASTM E 2149-10 22)에 따른 항균 정성분석을 수행하였다. 그람양성균의 하나인 E. coli DH5a (ATCC PTA 1977)를 사용하였으며 제조된 키토산-은나노 코팅지 시편을 균이 접종된 영양배지를 굳힌 plate 상에 접촉시킨 후 샘플 주위에 형성되는 halo를 비교하여 공시 균주의 생육저해 정도를 측정하였다. 먼저 증류수 100 mL에 nutrient broth 0.8 g과 MacConkey agar 5 g를 넣어 121℃, 오토클레이브에서 15분 동안 가열하여 멸균시킨 후 균을 접종할 영양배지를 준비하였다. 멸균된 영양배지 15 mL와 3 x 106 CFU/mL로 희석된 균 용액 0.5 mL를 혼합하고 이를 petri dish (90 x 15 mm)에 담아 1시간 동안 상온에서 건조시켜 균이 접종된 agar plate를 준비하였다. 준비된 agar plate 위에 항균코팅 종이 시편 (2 cm x 2 cm)을 올리고 38℃의 incubator에서 24시간 동안 균을 배양한 후 시편 주위에 형성된 halo의 유무로써 항균성을 확인하였으며 모든 실험은 3회 반복하여 재현성을 확인하였다.
3. 결과 및 고찰
3.1 키토산-은나노 녹색합성 복합물질의 특성 분석
키토산과 질산은의 농도 및 반응시간에 따른 키토산 내 은나노의 녹색합성 유무를 확인하기위해 UV-Vis 흡수 spectrum을 조사하였다. 일반적으로 은나노 입자는 그 모양과 크기에 따라 410~430 nm 영역에서 고유흡수밴드가 나타나는 것으로 알려져 있다. 2324)Fig. 1은 키토산의 농도에 따른 은나노 합성 결과로 키토산과 반응하는 질산은의 농도와 반응시간을 동일하게 유지하고 키토산의 농도만을 증가시키는 경우 은나노 흡수밴드의 세기는 키토산의 농도에 비례하여 증가하는 것을 확인할 수 있다. 이는 키토산의 농도가 증가할수록 은나노의 환원제로 작용하는 아미노기의 수 또한 증가하기 때문인 것으로 판단된다. Fig. 2는 오토클레이브 30초의 조건에서 2.0%(w/w) 키토산과 질산은 용액의 농도별 합성 반응에 따른 UV-Vis spectrum이다. 질산은을 혼합하지 않은 순수 키토산의 경우 고유흡수밴드가 전혀 나타나지 않은 반면 질산은 27 mM 이상의 농도에서는 은나노에 의한 410~430 nm 영역의 고유흡수밴드를 관찰할 수 있다. Fig. 3은 2%(w/w) 키토산과 질산은 60 mM의 오토클레이브 반응시간에 따른 UV-Vis spectrum 비교 결과이다. 반응시간을 15, 30, 60, 120초로 두었을 때 키토산 내 은나노 합성에 필요한 최적의 반응시간이 존재함을 확인할 수 있었으며 반응시간 30초가 본 연구에서 수행하는 실험조건에서 가장 적합한 은나노 합성조건임을 알 수 있었다. 오토클레이브 반응을 시도한 Maragoni Ven. 등 23)의 연구에 따르면 반응시간이 길어질수록 흡수밴드의 높이 또한 증가하였으나 본 연구에서는 30초 이상의 시간에서는 오히려 은나노에 의한 UV-Vis 흡수 세기가 감소하는 상반된 결과를 보였으며 이는 고온, 고압에서 합성된 키토산 내 은나노 입자의 밀도, 크기와 모양 등의 변화를 유도하는 추가적인 반응이 일어나는 것으로 판단되며 이에 대한 보다 심도 깊은 연구가 필요한 것으로 보인다.
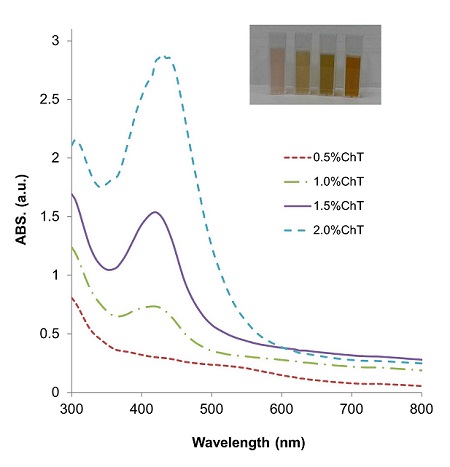
Fig. 1.
Effect of chitosan concentration on the green synthesis of Ananoparticles; chitosan: 0.5-2.0%(w/w), AgNO3: 60 mM, Reaction time in an autoclave : 15 sec.
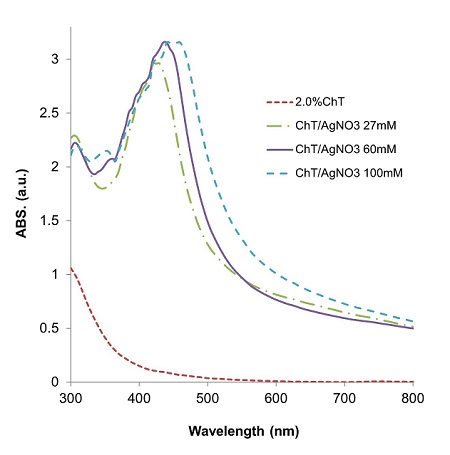
Fig. 2.
Effect of AgNO3 concentration on the green synthesis of Ag nanoparticles in chitosan; chitosan: 2.0%(w/w), AgNO3: 27, 60, 100 mM, Reaction time in an autoclave : 30 sec.
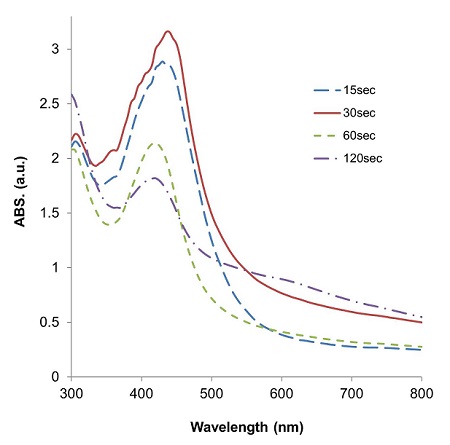
Fig. 3.
Effect of reaction time on the green synthesis of Ag nanoparticles in chitosan; chitosan: 2.0%(w/w), AgNO3: 60 mM, Reaction time in an autoclave : 15 – 120 sec.
Fig. 4는 1%(w/w)키토산과 30 mM 질산은 혼합액으로부터 녹색합성된 은나노 입자의 대표적 TEM 분석 사진으로서 20 nm 이하의 분포를 보이는 구형의 은나노 입자가 키토산 내에 성공적으로 합성되었음을 관찰할 수 있다. 이와 유사하게 Dong Wei 등은 95℃ 열합성 조건에서 키토산 내 은나노를 합성하였으며 10 nm 이하의 입자 분포를 보이는 TEM 결과를 보고하였다. 24)
3.2 키토산-은나노 코팅지의 표면분석
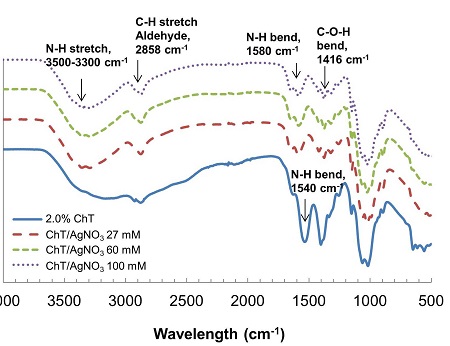
키토산 내 은나노 입자의 생성에 따른 키토산의 화학적 결합구조 분석을 위해 FTIR spectrum을 측정하였다. Fig. 5는 오토클레이브 30초 조건에서 2%(w/w) 키토산과 반응한 질산은 27, 60, 100 mM의 키토산-은나노 코팅 필름의 스펙트럼을 나타낸 것으로 키토산의 경우 3500-3300 cm-1 파수영역의 –NH stretch, 1540 cm-1의 –NH bend, 1440-1200 cm-1 영역의 –OH 및 1375 cm-1의 메틸(CH3) 그룹의 고유흡수 밴드를 보인다.23) 반면 키토산-은나노 합성 복합필름의 경우 순수 키토산필름과 비교했을 때 3500-3300 cm-1, 1540 cm-1, 1416 cm-1 파수에서 은나노 합성에 따른 현저한 변화를 관찰할 수 있다. 3500-3300 cm-1와 1540 cm-1 파수영역은 아미노그룹에 해당하는 것으로 24) 아미노그룹의 흡수밴드의 감소는 키토산 분자 내 아미노그룹이 은나노 합성을 위한 환원반응에 참여한 결과에 기인한 것으로 판단되며 1540 cm-1 피크의 1580 cm-1 파수로의 이동 또한 새로이 생성된 은입자의 결합에 따른 영향으로 해석된다. 이는 DongWei 등 25)이 보고한 은나노 합성과정과 유사한 결과로서 키토산 내 은나노의 녹색합성은 크게 은이온과 아미노기와의 결합 및 결합된 은이온의 환원과정을 거치는 것으로 판단된다. 뿐만 아니라 주환원제로 작용하는 키토산의 아미노그룹과 함께 흡수된 은 이온 주변에 인접한 –OH 그룹이 환원반응을 촉진하고 상호작용하면서 알데히드와 산으로 산화되고 은 이온은 은나노 입자로 환원되어 합성이 종결되는 것으로 예상된다. 이는 Fig. 5의 키토산-은나노 필름 시편에서 알데히드의 C-H 그룹에 해당하는 2858 cm-1 파수의 강한 흡수밴드가 관찰됨으로서 –OH 그룹의 환원제 역할에 대한 부분적인 설명은 가능하나 1740-1720 cm-1 영역의 카르보닐기에 해당하는 흡수피크가 관찰되지 않아 반응메커니즘을 증명할 추가적 연구가 필요하다.
녹색합성된 키토산-은나노 복합물질을 적용한 코팅지의 코팅 표면과 코팅층 내 존재하는 은의 농도를 측정하였다. 오토클레이브 30초 조건에서 합성된 2% (w/w) 키토산-은나노 용액을 Meyer Bar를 사용하여 0.25 mm 두께의 마닐라 보드에 코팅하였으며 코팅 횟수에 따른 코팅층의 두께는 10-30 ㎛이었다. Fig. 6은 키토산-은나노 녹색합성 복합물질 코팅지의 FESEM (x500) 사진과 표면 내 은의 농도에 대한 EDS 측정값이다. FESEM 분석 결과 코팅 횟수의 증가에 따라 섬유 및 섬유 간 결합의 표면형상은 키토산-은나노 코팅층에 의해 점차 감소함을 확인 할 수 있으며 코팅층 표면 갈라짐 또는 박리에 의한 들뜸현상은 관찰되지 않았다. 키토산-은나노 코팅층 표면의 EDS 분석 결과 표면 은나노 입자의 농도는 반응에 참여한 질산은 용액의 농도와 코팅 횟수에 따라 1.62-7.14 wt% 범위의 측정값을 보였으며 동일한 코팅 횟수에서 반응에 참여한 질산은의 농도가 증가할수록 생성된 표면 은나노 입자의 질량비 값도 증가하는 경향을 보였다.
3.3 키토산-은나노 코팅지의 항균성
녹색합성법을 이용한 키토산-은나노 합성 복합물질을 적용한 코팅지의 항균성 포장소재로서 응용가능성을 검토하기 위해 제조된 녹색합성 키토산-은나노 코팅 제지의 E. coli균에 대한 항균성을 평가하였다. 다양한 농도의 은나노 입자가 코팅 된 키토산-은나노 코팅제지와 이들의 halo 항균정성 평가법에 의한 항균력 시험 결과 Fig. 7과 같다. 본 실험의 대조군으로 코팅되지 않은 마닐라보드와 2%(w/w) 키토산만을 코팅한 키토산 코팅지를 사용하였으며 각각의 시편들을 E. coli균과 24시간 동안 접촉시킨 후 항균력을 확인하였다. 은나노가 포함되지 않은 대조군의 경우 E. coli균에 대한 halo가 발견되지 않아 키토산 물질 자체의 항균성은 관찰되지 않았으며 이는 Mehdi Abdollaki 등의 25) 연구와 동일한 결과로 키토산이 agar와 같은 매개체 안에서 분산력이 약하고 이로 인해 대상 병원균과의 접촉이 용이하지 않기 때문인 것으로 판단된다. 26) 반면 키토산-은나노 복합물질이 코팅된 마닐라보드는 코팅횟수가 증가할수록 선명한 halo가 발견되어 코팅된 마닐라보드가 E. coli균의 생장을 효과적으로 억제함을 알 수 있으며 합성된 은나노의 농도가 증가할수록 항균력 또한 강화되는 경향을 보였다.
4. 결 론
본 연구에서는 키토산 바이오폴리머를 활용한 은나노 입자의 친환경 녹색합성을 수행하였으며 제조된 키토산-은나노 합성용액을 마닐라보드에 코팅, 이들의 물리화학적 특성 및 항균성을 평가하였다. UV-Vis 흡수 spectrum과 TEM 분석을 통해 키토산 내 은나노 입자가 안정적으로 생성, 분포하고 있음을 확인하였으며 FTIR 분석에 의해 은나노 합성과정에서 키토산의 활성아미노기와 소량의 히드록시기가 은나노 환원반응에 참여함으로써 키토산이 은나노 입자의 합성을 위한 환원제 및 안정제로 작용하였음을 확인할 수 있었다. 은나노 녹색합성의 최적조건에서 합성된 다양한 농도의 키토산-은나노 복합물질을 마닐라보드에 코팅하고 이를 FESEM과 EDS분석을 통해 표면의 형상, 코팅의 균일도 및 은나노의 함유량을 조사하였다. 그 결과 키토산-은나노 녹색합성 복합물질이 섬유상에 적절한 친화력과 함께 섬유 간 결합을 향상시키고 종이 표면에 균일한 코팅을 이루고 있으며 제조된 코팅지의 코팅층 표면 내에 1~7 wt%의 은이 존재하는 것을 확인하였다. 또한 키토산-은나노 녹색합성 복합물질 코팅지의 항균 정성평가 결과 시험된 코팅지 시편 모두에서 항균성을 보였으며 함유된 은의 농도가 증가함에 따라 항균력 또한 증가하여 코팅층 표면 내에 3% 이상의 은이 존재하는 경우 매우 우수한 항균성이 관찰되었다. 본 연구를 통해 녹색합성법에 기인한 키토산-은나노 코팅지가 새로운 형태의 친환경 항균소재로서 적합함을 확인하였으며 향후 나노 복합물질 코팅 기능성 종이로서 식품, 의료, 화장품 포장 등의 폭넓은 적용을 위해서 수분, 오일 및 가스차단성, 물리적 강도, 화학적 특성, 항균내구성 등 포장소재로서 요구되는 다양한 요소의 체계적 연구가 수행될 것이다.