1. 서 론
2. 재료 및 방법
2.1 재료
2.2 산 가수분해에 의한 선택적인 헤미셀룰로오스 제거
2.3 화학 분석
3. 결과 및 고찰
3.1 케나프 속대의 화학적 조성
3.2 반응 온도가 헤미셀룰로오스 제거 효율에 미치는 영향
3.3 반응 시간이 케나프 속대 산 가수분해에 미치는 영향
4. 결 론
1. 서 론
케나프 섬유(Kenaf)는 초본류 중 바이오매스 생산량이 많아서 미래 바이오리파이너리 산업에서 지속 생산이 가능한 원료 후보로 주목받고 있어, 전 세계적으로 널리 재배되는 초본류이다.1,2,3,4,5,6) 케나프의 장점은 생장 속도가 빠르고, 환경에 대한 적응성이 높고, 재배 비용이 저렴하다는 점이다. 케나프 줄기는 외부 인피섬유, 내부 속대로 구별되며, 외부 인피섬유에는 외피, 내피로 분류된다.3) 케냐프 줄기는 주로 두 가지 구성 요소인 외부 인피섬유(25-40%)와 내부 속대(60-75%)로 분리할 수 있다. 인피섬유는 섬유가 길어 종이나 복합체에서 우수한 강도적 성질을 부여한다. 속대는 짧은 섬유로 구성되어 있어 응용 분야에 제한이 있다.4,5,6)
셀룰로오스, 헤미셀룰로오스, 리그닌 성분뿐만 아니라 추출물 성분까지 각 용도에 맞게 활용하는 것이 바이오 리파이너리 산업이며 이를 위해서 원료의 안정적 공급이 중요하다.7,8,9,10,11) 케냐프 속대의 화학성분은 홀로셀룰로오스(87.2%) 중 셀룰로오스(49.0%), 헤미셀룰로오스(38.2%)와, 리그닌(19.2%), 추출물(4.7%), 회분(1.9%)으로 구성되어 있다.4) 케나프의 속대는 인피섬유보다 셀룰로오스 함량이 낮고 헤미셀룰로오스와 리그닌 함량이 높다.4) 케나프의 펄프화 특성 연구는 대부분 인피섬유를 이용하였지만 속대를 이용한 고 순도 셀룰로오스 제조 관련 연구가 필요하다.9,10)
셀룰로오스는 지구상에서 가장 풍부한 천연 고분자 자원이다.12) 이와 같은 셀룰로오스는 에스테르화 및 에틸화 처리 등 다양한 개질 처리에 의해 메틸 셀룰로오스, 에틸 셀룰로오스, 카복시메틸 셀룰로오스, 하이드록시프로필셀룰로오스, 하이드록시 에틸 셀룰로오스 등 고품질의 제품 생산이 가능한데, 이들 개질 셀룰로오스 제조를 위해서는 순도가 높은 셀룰로오스가 필요하다.13,14) 셀룰로오스는 부분적인 산 가수분해 반응으로 미세결정 셀룰로오스를 제조할 수 있으며 뛰어난 결합력과 제형능력으로 제약 산업에서 부형제로 널리 사용된다.15)
이런 용도에 적합한 순도가 높은 셀룰로오스가 필요하며 주로 고순도의 면 셀룰로오스가 이용된다. 하지만 목질계 바이오매스도 용해용 펄프 제조 공정을 통하여 고순도 셀룰로오스 제조가 가능기 때문에 이를 원료로 사용하기도 한다.12,15)
정밀화학 원료로 사용하는 용해용 펄프 등급의 셀룰로오스는 순도 90.0% 이상을 요구한다.7) 고순도 셀룰로오스를 생산하기 위하여 효과적으로 리그닌과 헤미셀룰로오스를 제거해야 한다.17,18) 화학 펄핑과 표백으로 리그닌을 제거하고 헤미셀룰로오스 제거 공정이 필요하다.3) 헤미셀룰로오스 제거 공정으로 적절한 농도의 염기를 사용하여 헤미셀룰로오스를 용해시키는 염기성 조건의 처리와 산성 조건에서 셀룰로오스 보다 헤미셀룰로오스의 가수분해 속도가 빠른 점을 이용한 산 가수분해 처리로 크게 나뉜다.19,20)
황산이나 염산을 사용하여 선택적으로 헤미셀룰로오스를 제거하는 공정은 용해용 펄프 생산 뿐만 아니라 효소당화 이전 단계의 전처리 공정으로 많은 연구가 진행 되어 왔다.21,22,23) 리그노셀룰로오스 성분들의 산 가수분해 특성을 연구한 결과에 의하면, 산 가수분해 반응에서 자일란의 분해속도가 가장 빠르다.24) 글루코만난도 셀룰로오스 보다 분해속도가 빠르다.25) 이런 분해속도의 차이를 이용하면 대부분의 셀룰로오스를 잔류시키면서 헤미셀룰로오스의 제거가 가능하다. 따라서 본 연구에서는 리그닌을 제거한 케나프 속대를 이용하여 정밀화학 원료인 고 순도 셀룰로오스를 제조하기 위하여 묽은 산 가수분해 조건에서 헤미셀룰로오스의 선택적 제거 가능성을 탐색하였다.
2. 재료 및 방법
2.1 재료
케나프 원료는 전북 농업 기술원에서 공급한 2021년에 재배된 원료를 사용하였다. 속대 부분을 회수하기 위하여 인피섬유를 제거하였다. 속대를 분쇄한 후 스크린닝을 통하여 0.80-0.91 mm 크기의 입자로 선별하였다. 인피섬유가 제거된 속대를 차아염소산 표백을 통하여 잔류 리그닌 0.6%의 홀로셀룰로오스를 제조한 후 이것을 본 실험의 시료로 사용하였다.
산 가수분해 처리를 위해 황산(95.0%, 순도, 삼전화학), 아세톤(99.7%, 순도, 삼전화학)의 제품을 사용하였고 휴먼 사이언스사의 2차 증류수 제조 장비를 사용하여 제조된 증류수를 사용하였다. 당 분석 과정에서 사용한 중수(D2O)는 미국 Sigma-Aldrich 사의 제품을, 당 표준 물질인 α-L(+)-rhamnose monohydrate는 일본 Wako Pure Chemical Industries Ltd. 사의 제품을 사용하였다.
2.2 산 가수분해에 의한 선택적인 헤미셀룰로오스 제거
선택적으로 헤미셀룰로오스를 제거하기 위하여 황산 촉매로 가수분해 반응을 실시하였다. 산 농도 0.25, 0.50, 1.00 N, 반응 온도 110, 120, 130℃, 반응 시간 60, 90, 120분에서 각각 산 가수분해를 하였다. 모든 반응은 2.0 g의 홀로셀룰로오스에 20 mL의 묽은 황산을 넣은 후 튜브 반응기에서 수행되었다. 반응 종료 후 반응 시료를 냉각시키고, P4(10-16 µm) 유리 필터를 사용하여 여과하고, 증류수로 잔류 산을 제거한 후 건조하여 잔류량과 화학조성 분석에 필요한 시료를 준비하였다.
2.3 화학 분석
2.3.1 추출물 분석
케냐프 속대 내 추출물 함량을 분석하기 위하여 아세톤을 이용한 소수성 추출(TAPPI T 204 cm-97)과 끓는 물을 이용한 친수성 추출(TAPPI T 207 cm-99)을 실시하였다.
2.3.2 잔류 리그닌 분석
산 불용성 리그닌 함량을 측정하기 위하여, TAPPI 222 om-21 방법에 의거하여 잔존 리그닌(Klason lignin) 함량을 측정하였다.
2.3.3 탄수화물 조성 분석
홀로셀룰로오스의 탄수화물 조성 분석을 위하여, 시료(20.0 mg)에 72% 황산(0.6 mL)을 이용하여 30℃에서 1시간 동안 1차 가수분해 후, 희석용매로 중수(D2O, 3.0 mL)를 사용하여 100℃에서 1시간 동안 2차 가수분해 반응을 실시하였다. 상온으로 냉각시키고 단당이 포함된 용액을 여과하여 NMR 튜브에 옮겨 담은 후 Bruker사의 AVANCE NMR spectrophotometer(400 MHz) 장비를 사용하여 분석을 실시하였다. 분석 후 NMR 스펙트럼 상에서 아노머성 수소 피크를 적분하여 탄수화물을 정량분석 하였다.26)
3. 결과 및 고찰
3.1 케나프 속대의 화학적 조성
케나프 속대의 화학적 조성을 Table 1에 나타내었다. 홀로셀룰로오스 및 리그닌 등의 주성분 이외에도 소수성 추출물이나 친수성 추출물을 포함하고 있었다. 특히 소수성 추출물보다 친수성 추출물 함량이 월등하게 높게 나타났다. 소수성 추출물 성분은 지방산, 탄화수소 알코올, 스테로이드 성분 등이 있으며, 친수성 추출물에는 리그난, 플라보노이드, 페놀성 추출물 등이 있다. 소수성 추출물보다 친수성 추출물에서 다양한 종류의 추출물들이 확인되었다.27)
Table 1.
Materials balance of raw kenaf core fiber
|
Chemical Compositions
|
Raw Samples (%)
|
|
Carbohydrates
| |
|
Cellulose
|
52.8±0.2
|
|
Hemicellulose
|
21.9±0.2
|
|
Xylan
|
19.5±0.0
|
|
Others Sugar
|
2.4±0.2
|
|
Lignin
|
15.2±0.2
|
|
Extractives
| |
|
Hydrophobica |
0.4±0.2
|
|
Hydrophilicb |
9.7±0.1
|
추출물을 제거한 탈지 시료 내 각 주성분의 조성을 분석한 결과 리그닌 함량이 15.2%로 인피 섬유 리그닌 함량 8.4%보다 더 많은 리그닌을 함유하였다. 다른 보고의 18.5%보다 리그닌이 함량이 낮은데 이것은 지역적 차이나 재배 연도의 차이에 의한 것으로 추정된다.28,29,30)
다당류 분석을 위하여 1H-NMR 분광 분석을 사용하였다. 분석 대상 물질은 황산 가수분해하여 단당류로 전환 시킨 후 분광 분석을 실시하였다. 단당류의 아노머성 수소의 화학 이동 값이 단당 종류별 다른 점을 이용하여 다른 화학 이동 값 피크 영역에서 피크 면적을 적분하여 정량 분석하였다. Fig. 1에서 볼 수 있듯이 화학 이동 값별 다른 단당 영역을 보여주었으며, 이러한 차이를 이용하여 각 단당류들을 정량 분석하였다.
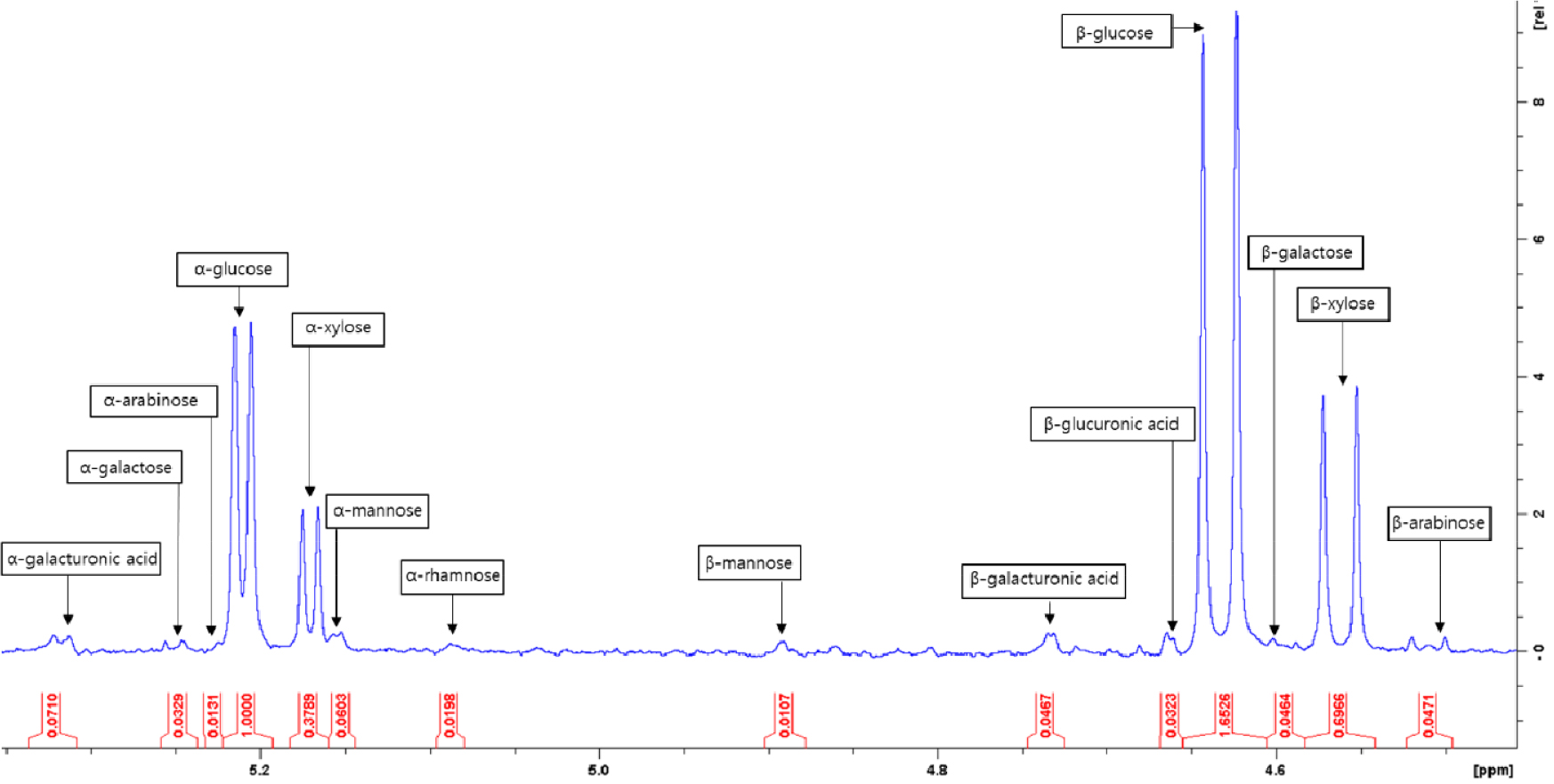
Fig. 1.
The anomeric hydrogen of acid hydrolyzate from raw kenaf core fiber.
분석 결과, 셀룰로오스의 함량은 52.8%이고 헤미셀룰로오스의 함량은 21.9%였다. 헤미셀룰로오스의 대부분은 자일란(19.5%)이었으며 이외 성분은 글루코만난(2.4%)이 주로 함유되어 있음이 확인되었다.
3.2 반응 온도가 헤미셀룰로오스 제거 효율에 미치는 영향
황산은 산 가수분해 반응에서 촉매로 작용하여 다당을 단당으로 분해한다.16) 이런 산 가수분해 반응에서 반응 온도는 매우 중요하다. 헤미셀룰로오스와 셀룰로오스의 가수분해 반응에 미치는 영향을 파악하기 위하여 110, 120, 130℃의 반응 온도를 달리하여 케나프 속대의 산 가수분해 반응을 수행한 후, 각 산 가수분해 반응 산물을 회수하여 다당류 조성을 분석하였다. 산 가수분해 전후 대표적인 헤미셀룰로오스 단당류인 자일로스의 변화를 살펴본 결과, Fig. 2에서 보는 바와 같이 산 가수분해 후 자일란 고분자의 가수분해 산물인 자일로스 피크 영역이 뚜렷하게 감소하는 것을 확인하였다. 다당류 조성분석 결과는 Table 2에 나타내었다. Table 2에서 보는 바와 같이 반응 온도가 증가함에 따라 헤미셀룰로오스의 제거율이 증가하였다. 셀룰로오스의 일부도 제거되었지만 헤미셀룰로오스 보다는 제거율이 낮아 반응 온도를 달리하여 선택적인 헤미셀룰로오스의 제거가 가능함을 확인하였다. 실제로 반응 온도에 따른 산 가수분해 후 각 시료의 헤미셀룰로오스는 대부분 제거되었으며 110℃는 4.7%, 120℃는 1.5%, 130℃는 0.9%로 잔류량이 남아있다. 셀룰로오스 순도를 비교분석하면 110℃는 91.13%, 120℃는 94.59%, 130℃는 97.64%로 반응온도가 증가할수록 고순도의 셀룰로오스 섬유가 제조되었다.
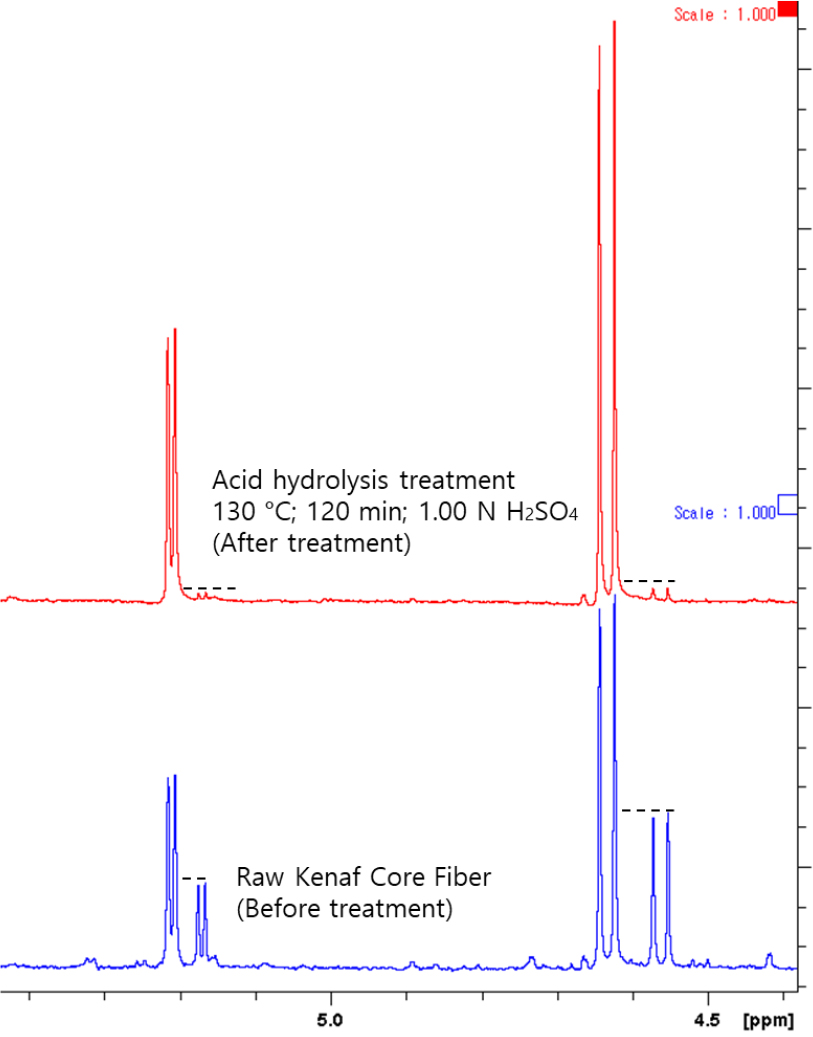
Fig. 2.
Anomeric hydrogens of acid hydrolyzates from kenaf core fiber before and after sulfuric acid hemicelluloses removal.
Table 2.
Chemical composition of kenaf core fiber with different reaction temperature (90 min reaction time)
Temperature
(℃)
|
Yield
(%)
|
Chemical Composition
|
Cellulose
purity (%)
|
|
Cellulose (%)
|
Hemicellulose (%)
|
Lignin (%)
|
|
110
|
56.4±0.3
|
51.4±0.3
|
4.7±0.3
|
0.3±0.6
|
91.1±0.3
|
|
120
|
51.8±0.3
|
49.5±0.1
|
1.5±0.1
|
0.3±0.5
|
96.5±0.1
|
|
130
|
50.9±0.1
|
49.7±0.3
|
0.9±0.3
|
0.3±0.1
|
97.6±0.3
|
Table 3.
Chemical composition of kenaf core fiber with different reaction time hydrolysis at 130°C
Time
(min)
|
Yield
(%)
|
Chemical Composition
|
Cellulose
purity (%)
|
|
Cellulose (%)
|
Hemicellulose (%)
|
Lignin (%)
|
|
60
|
51.5±0.1
|
50.0±0.6
|
1.2±0.6
|
0.3±0.1
|
97.1±0.6
|
|
90
|
50.9±0.1
|
49.7±0.3
|
0.9±0.3
|
0.3±0.1
|
97.6±0.3
|
|
120
|
50.1±0.1
|
49.4±0.1
|
0.4±0.1
|
0.3±0.1
|
98.6±0.1
|
3.3 반응 시간이 케나프 속대 산 가수분해에 미치는 영향
황산 1.0 N, 반응온도 130℃에서 반응 시간을 60분, 90분, 120분으로 달리하여 셀룰로오스와 헤미셀를로오스의 가수분해 정도를 비교하였다. Table 3에서와 같이 반응 시간이 증가함에 따라 수율이 감소하였고 이것은 셀룰로오스와 헤미셀룰로오스의 가수분해 때문이다. 가수분해 반응은 헤미셀룰로오스에서 더욱 뚜렷하게 진행되었는데 120분 가수분해 반응으로 대부분의 자일란이 19.5%에서 0.4%로 19.1% 포인트 만큼 제거되었지만 셀룰로오스의 제거량은 첨가한 케냐프 속대 2.0 g 당 52.9%에서 50.1%로 2.8% 포인트가 감소하였다.
반응 시간에 따른 산 가수분해 후 각 시료의 셀룰로오스 순도를 비교 분석하면 60분 97.09%, 90분 97.64%, 120분은 98.60%로 반응 시간이 증가함에 따라 셀룰로오스 순도가 소폭 증가되었다. 반응시간을 60분에서 120분으로 증가 시킴에 따라 셀룰로오스 수율은 0.6% 포인트 감소하였고, 헤미셀룰로오스의 잔류량도 0.8% 포인트 감소하여 반응 시간을 증가시키면 셀룰로오스의 순도가 증가하지만 반응의 선택성이 온도보다 떨어진다.
산 가수분해 시 반응온도 및 시간에 따른 셀룰로오스 순도 변화를 살펴보면 결과, 반응온도가 주요한 반응인자임을 확인되었으며, 반응 시간 증가가 셀룰로오스 순도 증가에 거의 영향을 미치지 않음을 확인하였다. 일례로, Guerra-Rodríguez 등31)은 높은 반응 온도와 짧은 반응 시간이 헤미셀룰로오스 제거에 유리하여 셀룰로오스의 순도를 향상시킨다고 보고한 바 있다.
4. 결 론
본 연구에서는 생장 사이클이 빠르고 단위 면적당 생산성이 타 수목에 비해 높은 케나프의 속대로부터 순도 높은 셀룰로오스로 정제하기 위하여 선택적인 리그닌과 헤미셀룰로오스 제거 방법에 대해 알아보았다. 케나프 속대 황산 가수분해 반응으로 대부분의 헤미셀룰로오스를 제거하고 용해용 펄프 등급의 셀룰로오스 제조가 가능하였다. 특히 반응 온도 및 시간에 따른 셀룰로오스 순도 변화를 살펴본 결과, 황산 1.00 N, 130℃, 60분 반응 조건에서의 셀룰로오스 순도가 가장 높았다. 이 조건에서 셀룰로오스의 순도 97.09%, 수율 51.5%로 제조가 가능하였다. 비목질 섬유인 왕겨와 황마의 고순도 셀룰로오스 제조를 위한 황산 가수분해에서도 반응 온도가 높아질수록 자이란의 가수분해가 촉진되어 헤미셀룰로오스 함량이 낮아지지만 동시에 셀룰로오스의 가수분해가 촉진되어 셀룰로오스의 수율이 감소하였다.
Acknowledgements
본 연구는 행정안전부 및 전라북도의 지역균형 뉴딜사업 재원으로 (재)전북바이오융합산업진흥원의 지원을 통해 수행되었습니다.
References
Alexopoulou, E., Papatheohari, Y., Christou, M., and Monti, A. Origin, description, importance, and cultivation area of kenaf. In Kenaf: A multi-purpose crop for several industrial applications, Monti, A., and Alexopoulou, E., (Eds) Springer, London, UK. pp. 1-15 (2013).
10.1007/978-1-4471-5067-1_1Saba, N., Jawaid, M., Hakeem, K. R., Paridah, M. T., Khalina, A., and Alothman, O. Y., Potential of bioenergy production from industrial kenaf (
Hibiscus cannabinus L.) based on Malaysian perspective, Renewable and Sustainable Energy Reviews 42:446-459 (2015).
10.1016/j.rser.2014.10.029Tye, Y. Y., Lee, K. T., Abdullah, W. N. W., and Leh, C. P., Optimization of various pretreatments condition of kenaf core (
Hibiscus cannabinus) fibre for sugar production: Effect of chemical compositions of pretreated fibre on enzymatic hydrolysability, Renewable Energy 69:205-215 (2016).
10.1016/j.renene.2016.06.040Sreenivas, H. T., Krishnamurthy, N., and Arpitha, G. R., A comprehensive review on light weight kenaf fiber for automobiles, International Journal of Lightweight Materials and Manufacture 3(4):328-337 (2020).
10.1016/j.ijlmm.2020.05.003Kuroda, K., Nakagawa-izumi, A., Mazumder, B. B., Ohtani, Y., and Sameshima, K., Evaluation of chemical composition of the core and bast lignins of variety Chinpi-3 kenaf (
Hibiscus cannabinus L.) by pyrolysis-gas chromatography/mass spectrometry and cupric oxide oxidation, Industrial Crops and Products 22: 223-232 (2005).
10.1016/j.indcrop.2005.01.002Saba, N., Paridah, M. T., and Jawaid, M., Mechanical properties of kenaf fibre reinforced polymer composite: A review, Construction and Building Materials 76:87-89 (2015).
10.1016/j.conbuildmat.2014.11.043Rahmini, R., Zahra, A., Lim, D. Y., and Shin, S. J., Dilute acid hydrolysis of jute bast fiber for selected xylan removal, Journal of Korea TAPPI 53(5):65-73 (2021).
10.7584/JKTAPPI.2021.10.53.5.65Szulczyk, K. R. and Badeeb, R. A., Nontraditional sources for biodiesel production in Malaysia: The economic evaluation of hemp, jatropha, and kenaf biodiesel, Renewable Energy 192:759-768 (2022).
10.1016/j.renene.2022.04.097Zaini, L. H., Jonoobi, M., Tahir, P. M., and Karimi, S., Isolation and characterization of cellulose whiskers from kenaf (
Hibiscus cannabinus L.) bast fibers, Journal of Biomaterials and Nanobiotechnology 4:37-44 (2013).
10.4236/jbnb.2013.41006Song, Y., Jiang, W., Zhang, Y., Ben, H., Han, G., and Ragauskas, A. J., Isolation and characterization of cellulosic fibers from kenaf bast using steam explosion and Fenton oxidation treatment, Cellulose 25(9):4979-4992 (2018).
10.1007/s10570-018-1916-yLi, T., Chen, C., Brozena, A. H., Zhu, J. Y., Xu, L., Driemeier, C., and Hu, L., Developing fibrillated cellulose as a sustainable technological material, Nature 590(7844):47-56 (2021).
10.1038/s41586-020-03167-733536649Nasrollahzadeh, M., Sajjadi, M., Iravani, S., and Varma, R. S., Starch, cellulose, pectin, gum, alginate, chitin and chitosan derived (nano) materials for sustainable water treatment: A review, Carbohydrate polymers 251:116986 (2021).
10.1016/j.carbpol.2020.11698633142558PMC8648070Nasatto, P. L., Pignon, F., Silveira, J. L., Duarte, M. E. R., Noseda, M. D., and Rinaudo, M., Methylcellulose, a cellulose derivative with original physical properties and extended applications, Polymers 7(5):777-803 (2015).
10.3390/polym7050777Ohkawa, K., Hayashi, S., Nishida, A., Yamamoto, H., and Ducreux, J., Preparation of pure cellulose nanofiber via electrospinning, Textile Research Journal 79(15):1396-1401 (2009).
10.1177/0040517508101455Hindi, S. S. Z., Microcrystalline cellulose: the inexhaustible treasure for pharmaceutical industry, Journal of Nanoscience & Nanotechnology Research 4(1):17-24 (2017).
Fitriani, F., Aprilia, S., Arahman, N., Bilad, M. R., Amin, A., Huda, N., and Roslan, J., Isolation and characterization of nanocrystalline cellulose isolated from pineapple crown leaf fiber agricultural wastes using acid hydrolysis, Polymers 13(23):4188 (2021).
10.3390/polym1323418834883691PMC8659882Siqueira, G., Várnai, A., Ferraz, A., and Milagres, A. M., Enhancement of cellulose hydrolysis in sugarcane bagasse by the selective removal of lignin with sodium chlorite, Applied Energy 102:399-402 (2013).
10.1016/j.apenergy.2012.07.029An, S., Li, W., Xue, F., Li, X., Xia, Y., Liu, Q., Chem, L., Jameel, H., and Chang, H. M., Effect of removing hemicellulose and lignin synchronously under mild conditions on enzymatic hydrolysis of corn stover, Fuel Processing Technology 204:106407 (2020).
10.1016/j.fuproc.2020.106407Tuerxun, D., Pulingam, T., Nordin, N. I., Chen, Y. W., Kamaldin, J. B., Julkapli, N. B. M., and Johan, M. R. B., Synthesis, characterization and cytotoxicity studies of nanocrystalline cellulose from the production waste of rubber- wood and kenaf-bast fibers, European Polymer Journal 116:352-360 (2019).
10.1016/j.eurpolymj.2019.04.021Chandel, A. K., Antunes, F. A., Arruda, P. V. D., Milessi, T. S., Silva, S. S. D., and Almeida Felipe, M. D. G. D., Dilute acid hydrolysis of agro-residues for the depolymerization of hemicellulose: state-of-the-art, In D-xylitol, Fermentation production, application and commercialization, da Silva, S.S and Chandel, A.K. (Eds), Springer, London, UK. pp. 39-61 (2012).
10.1007/978-3-642-31887-0_2Tyufekchiev, M., Finzel, J., Zhang, Z., Yao, W., Sontgerath, S., Skangos, C., Duan, P., Schmidt-Rohr, K., and Timko, M.T., A New Method for Solid Acid Catalyst Evaluation for Cellulose Hydrolysis, Sustain Chem 2:645- 669 (2021).
10.3390/suschem2040036Kildegaard, G., Balbi, M. D. P., Salierno, G., Cassanello, M., De Blasio, C., and Galvagno, M., A Cleaner Delignification of Urban Leaf Waste Biomass for Bioethanol Production, Optimised by Experimental Design, Processes 10(5):943 (2022).
10.3390/pr10050943Luo, X., Gong, Z., Shi, J., Chen, L., Zhu, W., Zhou, Y., Huang, L., and Liu, J., Integrating benzenesulfonic acid pretreatment and bio- based lignin-shielding agent for robust enzymatic conversion of cellulose in bamboo, Polymers 12(1):191 (2020).
10.3390/polym1201019131936846PMC7022729Hernández, I. P., Pérez-Pimienta, J. A., Messina, S., and Saldaña Durán, C. E., Dilute sulfuric acid hydrolysis of tropical region biomass, Journal of renewable and sustainable energy 4(2):021201 (2012).
10.1063/1.3663878Yoon, S. Y., Han, S. H. and Shin, S. J., The effect of hemicelluloses and lignin on acid hydrolysis of cellulose, Energy 77:19-24 (2014).
10.1016/j.energy.2014.01.104Merkx, D. W., Westphal, Y., van Velzen, E. J., Thakoer, K. V., de Roo, N., and van Duynhoven, J. P., Quantification of food polysaccharide mixtures by
1H NMR, Carbohydrate polymers 179:379-385 (2018).
10.1016/j.carbpol.2017.09.07429111064Ren, Z., Wang, C., Zuo, Q. I., Yousfani, S. H. S., Anuar, N. S., Zakaria, S., and Liu, X., Effect of alkali treatment on interfacial and mechanical properties of kenaf fibre reinforced epoxy unidirectional composites, Sains Malaysiana 48(1):173-181 (2019).
10.17576/jsm-2019-4801-20Silvy, N., Reza, S., Uddin, N., and Akther, M., Comparison between different components of some available hardwood and softwood in Bangladesh, IOSR Journal of Biotechnology and Biochemistry 4:1-5 (2018).
Jeun, J. P., Lee, B. M., Lee, J. Y., Kang, P. H., and Park, J. K., An irradiation-alkaline pretreatment of kenaf core for improving the sugar yield, Renewable Energy 79:51-55 (2015).
10.1016/j.renene.2014.10.030Saba, N., Jawaid, M., Hakeem, K. R., Paridah, M. T., Khalina, A., and Alothman, O. Y. Potential of bioenergy production from industrial kenaf (
Hibiscus cannabinus L.) based on Malaysian perspective, Renewable and Sustainable Energy Reviews 42:446-459 (2015).
10.1016/j.rser.2014.10.029Guerra-Rodríguez, E., Portilla-Rivera, O. M., Jarquín-Enríquez, L., Ramírez, J. A., and Vázquez, M., Acid hydrolysis of wheat straw: A kinetic study, Biomass and Bioenergy 36: 346-355 (2012).
10.1016/j.biombioe.2011.11.005





